Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombia Médica
On-line version ISSN 1657-9534
Colomb. Med. vol.52 no.2 Cali Apr./June 2021 Epub June 30, 2021
https://doi.org/10.25100/cm.v52i2.4805
Articulo de revisión
Reintervención en cirugía de control de daños
1 Hospital Pablo Tobon Uribe, Department of Surgery, Medellin, Colombia.
2 Universidad de Antioquia, Department of Surgery, Medellin, Colombia.
3 Hospital Pablo Tobón Uribe, Grupo de Soporte Nutricional y Pared Abdominal, Medellin. Colombia
4 Fundación Valle del Lili, Department of Surgery, Division of Trauma and Acute Care Surgery, Cali, Colombia.
5 Universidad del Valle, Facultad de Salud, Escuela de Medicina Department of Surgery, Division of Trauma and Acute Care Surgery, Cali, Colombia.
6 Universidad Icesi, Cali, Colombia.
7 Hospital Universitario del Valle, Department of Surgery, Division of Trauma and Acute Care Surgery, Cali, Colombia.
8 Fundación Valle del Lili, Centro de Investigaciones Clínicas (CIC), Cali, Colombia
9 Centro Médico Imbanaco, Cali, Colombia.
10Broward General Level I Trauma Center, Department of Trauma Critical Care, Fort Lauderdale, FL - USA
El control de daños es uno de los pilares de la cirugía de trauma. Sin embargo, la reintervención aún genera controversias en cuanto a quién, cuándo y cómo debe realizarse. El presente artículo presenta las recomendaciones del grupo de Cirugía de Trauma y Emergencias (CTE) de Cali, Colombia, respecto a las reintervenciones después de una cirugía de control de daños. Se recomienda el empaquetamiento como la estrategia de control de sangrado y se debe desempaquetar en un lapso entre 48 y 72 horas. La anastomosis diferida debe ser la opción de reparo en las lesiones intestinales. La reintervención vascular en los pacientes manejados con shunt vascular debe ser antes de las 24 horas para dar el manejo definitivo. En un lapso de 8 días se debe intentar realizar el cierre de la pared abdominal o torácica. Estas estrategias buscan disminuir la frecuencia de complicaciones y de morbimortalidad.
Keyword: Laparotomía; ostomía; cavidad torácica; anastomosis quirúrgica; período postoperatorio; procedimientos quirúrgicos cardíacos; unidades de cuidados intensivos; infección de la herida quirúrgica; colostomía; pared abdominal; reoperación; hipertensión intraabdominal
Damage control has well-defined steps. However, there are still controversies regarding whom, when, and how re-interventions should be performed. This article summarizes the Trauma and Emergency Surgery Group (CTE) Cali-Colombia recommendations about the specific situations concerning second interventions of patients undergoing damage control surgery. We suggest packing as the preferred bleeding control strategy, followed by unpacking within the next 48-72 hours. In addition, a deferred anastomosis is recommended for correction of intestinal lesions, and patients treated with vascular shunts should be re-intervened within 24 hours for definitive management. Furthermore, abdominal or thoracic wall closure should be attempted within eight days. These strategies aim to decrease complications, morbidity, and mortality.
Keywords: Laparotomy; ostomy; thoracic cavity; anastomosis surgical; postoperative period; cardiac surgical procedures; intensive care units; surgical wound infection; colostomy; abdominal wall; reoperation; intra-abdominal hypertension
Contribución del estudio
| 1) ¿Por qué se realizó este estudio? |
| Se presentan las recomendaciones del grupo de Cirugía de Trauma y Emergencias (CTE) de Cali, Colombia, respecto a las reintervenciones después de una cirugía de control de daños |
| 2) ¿Cuáles fueron los resultados más relevantes del estudio? |
| Se recomienda el empaquetamiento como la estrategia de control de sangrado y se debe desempaquetar en un lapso entre 48 y 72 horas. La anastomosis diferida debe ser la opción de reparo en las lesiones intestinales. La reintervención vascular en los pacientes manejados con shunt vascular debe ser antes de las 24 horas para dar el manejo definitivo. En un lapso de 8 días se debe intentar realizar el cierre de la pared abdominal o torácica. |
| 3¿Qué aportan estos resultados? |
| Estas estrategias buscan disminuir la frecuencia de complicaciones y de morbimortalidad. |
Introducción
La cirugía de control de daños descrita en 1993 por Rotondo y Schwab fue uno de los avances más importantes en la cirugía de trauma con efecto en la morbimortalidad de los pacientes que tienen mayor compromiso fisiológico 1. Esta estrategia se basa en un manejo de laparotomía abreviada y empaquetamiento abdominal que permite diferir el manejo quirúrgico definitivo hasta que se estabilice el paciente 2. La cirugía de control de daños incluye un espectro amplio de procedimientos tales como ligaduras intestinales, empaquetamiento de órgano sólido y/o retroperitoneo, shunts vasculares y abdomen abierto. Todas ellas son medidas temporales que se realizan ante la gravedad de la lesión y la necesidad de una reanimación hemostática agresiva para compensar su deuda metabólica, difiriendo el manejo definitivo hasta lograr un mejor estado fisiológico del paciente 3.
Después de realizar las medidas de contención del daño, la siguiente decisión en el plan del cirujano es establecer en qué momento se debe re intervenir 4. En esta decisión confluyen variables como la evolución del estado fisiológico y la severidad de la lesión. Sin embargo, la norma general es que los procedimientos definitivos de reconstrucción tanto intestinal, vascular o de cierre de pared abdominal / torácica se deben realizar cuando los parámetros del rombo de la muerte como la acidosis metabólica, hipotermia, hipocalcemia o coagulopatía estén corregidas 5,6. El presente artículo presenta una recopilación de las principales controversias en la reintervención quirúrgica durante la cirugía de control de daños como el desempaquetamiento, el tiempo de anastomosis intestinales, la necesidad de ostomías, el tiempo de retiro del shunt, la reconstrucción vascular y la estrategia para el cierre definitivo de la cavidad abdominal.
Este articulo hace parte de un consenso que sintetiza la experiencia lograda durante los últimos 30 años en el manejo del trauma, cirugía general y cuidado crítico del grupo de cirugía de Trauma y Emergencias (CTE) de Cali, Colombia conformado por expertos de Hospital Universitario del Valle “Evaristo García”y el Hospital Universitario Fundación Valle del Lili, con la Universidad del Valle y la Universidad Icesi, en colaboración con la Asociación Colombiana de Cirugía y la Sociedad Panamericana de Trauma, y la asesoría de especialistas nacionales e internacionales.
Empaquetamiento en cirugía de control daños
El empaquetamiento de una cavidad o un órgano es una estrategia ampliamente utilizada para controlar el sangrado en la fase inicial de la cirugía de control de daños. Usualmente se realiza cuando se encuentra un sangrado intracavitario abundante secundario a destrucción masiva de un órgano, donde el tiempo es limitado. Con una eficacia superior al 90%, el empaquetamiento busca detener de manera temporal o definitiva el sangrado por medio de la presión sostenida con gasas o compresas 7. Si bien parece estar claro cuándo realizar un empaquetamiento abdominal, el interrogante de cuándo retirar el material (gasas, compresas o agentes hemostáticos) no está completamente definido; y la mayoría de artículos reportan un rango de tiempo entre 24 y 72 horas 8-11 (Figura 1)
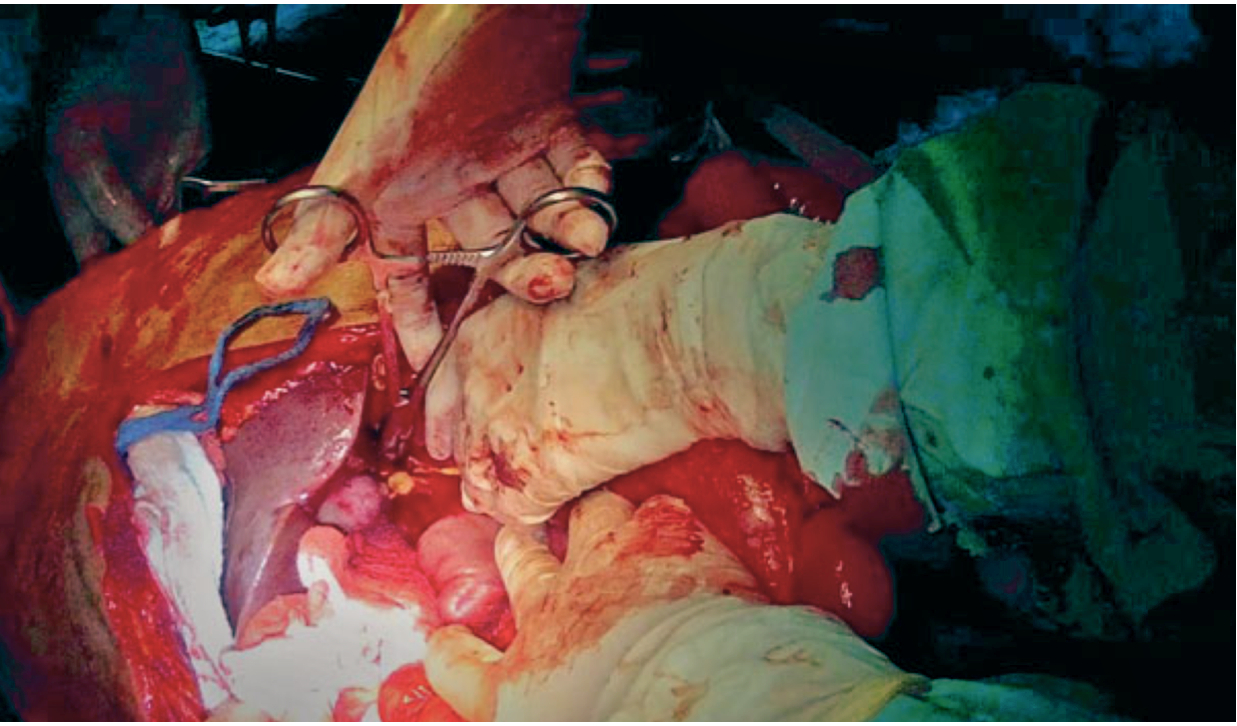
Figura 1 Empaquetamiento Abdominal. Paciente con trauma hepático severo que ha sido controlado mediante empaquetamiento peri hepático para control de la hemorragia.
Aydin et al., describieron el empaquetamiento abdominal en pacientes con trauma hepático severo, encontrando que los pacientes re intervenidos en las primeras 24 horas del trauma fueron aquellos en quienes se había realizado un empaquetamiento inefectivo (mala colocación, exceso o insuficiente número de compresas), y requirieron una estancia más larga en la unidad de cuidados intensivos y una mayor necesidad de transfusión de hemoderivados 12. Nicol et al., demostraron resultados similares al comparar los pacientes que fueron reintervenidos en las primeras 24 horas con aquellos intervenidos en 48 horas, reportando una tasa de re sangrado mayor en el primer grupo pero sin diferencias en la tasa de complicaciones infecciosas 13. Ordóñez et al., argumentan que el retiro prematuro del empaquetamiento (menor a 24 horas) aumenta el riesgo de sangrado, prolongación del abdomen abierto y un mayor número de re empaquetamientos; y que la prolongación de este por más de 72 horas incrementa el riesgo de infección 7. Kang et al., compararon pacientes con trauma hepático de alto grado que fueron desempaquetados antes y después de 48 horas, encontrando una menor tasa de neumonía asociada al ventilador y tiempo de ventilación mecánica cuando este se realizaba en las primeras 48 horas. Sin embargo, este grupo tuvo una mayor tasa de transfusión de hemoderivados y de procedimientos no invasivos como arteriografía / embolización 14.
El empaquetamiento de la cavidad torácica se publicó inicialmente en cirugía cardiaca, resección pulmonar o pleurectomía, como estrategia para el control del sangrado 15-18. El empaquetamiento de la cavidad torácica es una de las medidas más usadas para el control del sangrado por coagulopatía, de superficies cruentas o del área tisular reparada 19. Moriwaki et al., demostraron que el empaquetamiento se ha utilizado con éxito en el sangrado severo proveniente de la pared torácica, el espacio paravertebral, el parénquima pulmonar, y entre la pared torácica y el diafragma. En esta cohorte, solo la mitad de los pacientes presentaron efectos sobre la ventilación o la oxigenación, de carácter reversible. El desempaquetamiento se realizó entre el segundo y tercer día, sin complicaciones infecciosas relacionadas con el procedimiento 20. En el año 2019, García et al., describen una técnica en cuatro pacientes para empaquetar heridas transfixiantes del parénquima pulmonar utilizando una compresa quirúrgica a través de la herida, logrando el control del sangrado de forma segura y rápida en todos los casos) y desempaquetando en las siguientes 24 a 48 horas 21.
El empaquetamiento pélvico se considera una de las estrategias de primera línea en el control del sangrado en pacientes con fracturas pélvicas e inestabilidad hemodinámica, su retiro lo recomiendan entre 24 y 48 horas 22,23.
En conclusión, el empaquetamiento en una cirugía control de daños no debería retirarse antes de 48 horas ni después de 72 horas. En el trauma hepático severo, el desempaquetamiento puede hacerse antes de las 48 horas, siempre y cuando se asocie al uso de técnicas de arteriografía / embolización junto al uso óptimo de hemoderivados 14.
Cuidado postquirúrgico y anastomosis intestinal diferida
Si durante la exploración quirúrgica se identificó contaminación franca del peritoneo por materia fecal, se debe indicar esquema antibiótico con cubrimiento de aerobios y anaerobios. De lo contrario, si la lesión no presenta signos de contaminación tan solo basta con el manejo antibiótico profiláctico prequirúrgico.
Si se ha realizado intervención sobre el intestino, se recomienda dejar una sonda nasogástrica que puede tener un efecto descompresivo del intestino o ser una vía de alimentación enteral en el postquirúrgico, si este lo necesita.
Anastomosis intestinales
Las anastomosis diferidas como medida para disminuir los tiempos quirúrgicos y el riesgo de filtración hacen parte de los procedimientos de la cirugía de control de daños. La finalidad de la ligadura es evitar la contaminación de la cavidad y diferir la reconstrucción del tracto gastrointestinal, una vez se recupere de la deuda fisiológica (Figura 2).
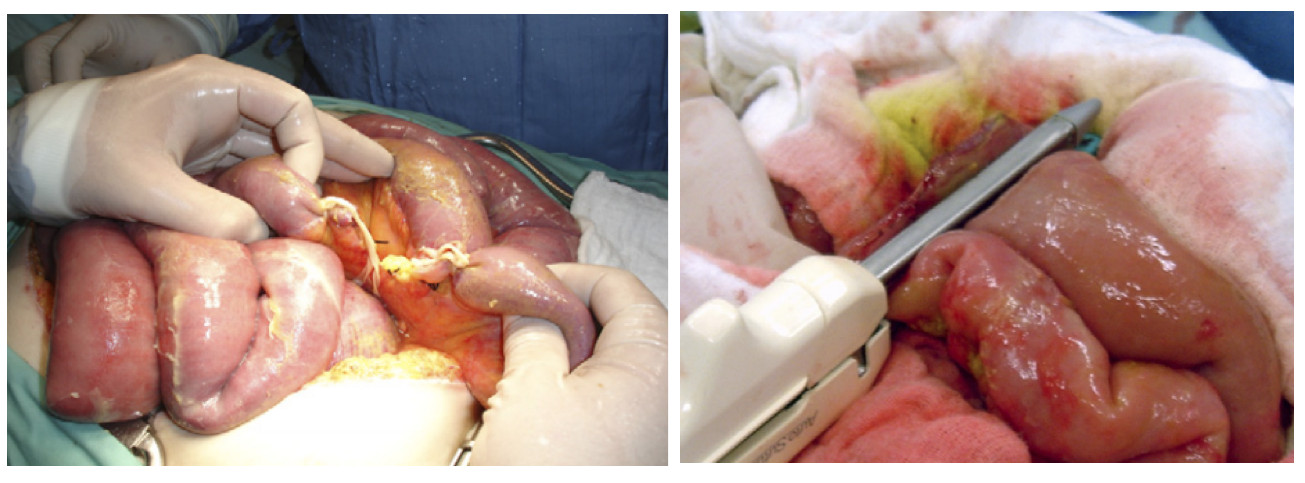
Figura 2 Anastomosis Intestinal Diferida. A. Lesión del intestino delgado manejada a través de cirugía de control de daños dejando en discontinuidad el intestino. B. Reconstrucción intestinal a través de una anastomosis diferida con grapadora
Las preguntas por resolver son: ¿Cuál es el tiempo ideal para realizar el reparo y/o anastomosis intestinales? y ¿Es necesario o no realizar una ostomía? La alteración del tracto gastrointestinal es el potencial mecanismo de translocación bacteriana y sepsis que puede complicar la evolución del paciente a mediano plazo. Esta preocupación se basa en las observaciones de Weinberg y colaboradores, que han encontrado que diferir la anastomosis en pacientes con lesiones destructivas del colon después de una cirugía de control de daños se relaciona con mayor probabilidad de complicaciones (filtración, abscesos, isquemia del estoma), cuando se compara con el manejo definitivo en la primera cirugía (resección-anastomosis o resección-ostomía). Los pacientes sometidos a control de daños tenían una severidad del trauma mayor y que el abdomen abierto solo se manejó con sistema de presión negativa en el 16% de los casos, por lo que recomendaban el manejo por colostomía en el segundo tiempo quirúrgico 24.
No obstante, el manejo diferido de lesiones destructivas o múltiples del intestino pueden ser abordadas en su reparo mediante anastomosis, disminuyendo la necesidad de ostomías, morbilidad y secuelas asociadas 11,25. Otras experiencias han reportado que la frecuencia de complicaciones tales como filtración, fistulas entero cutáneas o infección del sitio operatorio no varía si el paciente es sometido a un manejo intestinal diferido, comparado con aquellos pacientes en que es posible un manejo definitivo 9,26. Igualmente, no hay diferencia en los pacientes sometidos a anastomosis diferida vs ostomías diferida 11,27,28.
Los datos indican que la anastomosis primaria o diferida es segura en comparación con otros procedimientos, además que permite disminuir ostomías innecesarias. Se debe realizar un análisis metódico de las condiciones fisiológicas del paciente y las variables locales al momento de tomar la decisión de realizar una reconstrucción del tracto gastrointestinal, siendo el centro de atención las anastomosis colónicas por considerarlas de alto riesgo y con complicaciones graves. Las estrategias y recomendaciones para otras áreas del intestino (duodeno, yeyuno e íleon) se basan en la estabilidad clínica y paraclínica de los pacientes además de la técnica quirúrgica cuidadosa. Se ha reportado que el duodeno puede repararse de forma primaria o realizar una reconstrucción duodenal temprana. Lo que concuerda con el manejo de las lesiones gastroduodenales en nuestra institución, por lo que asumimos la frase acuñada “menos es más” (menos cirugías, menos reintervención, menor cantidad de procedimientos) podría tener total validez 29,30. El soporte nutricional juega un papel importante en la recuperación y manejo del postoperatorio de la cirugía de control de daños y su inicio debería darse de forma temprana 31.
Las siguientes son las recomendaciones teniendo en cuenta la información disponible:
Realizar la anastomosis lo antes posible, máximo 24-48 horas luego de la ligadura intestinal para evitar las complicaciones sépticas 24,28.
La reconstrucción del duodeno se debe realizar en las primeras 48 horas después de la primera cirugía inicial 29,30.
Se puede diferir la reconstrucción intestinal hasta una segunda o tercera intervención si aún no se ha realizado la adecuada recuperación metabólica o el edema intestinal. De lo contario, será candidato para realizarse una ostomía 9,26.
No hay contraindicación para el uso de la nutrición parenteral total en los pacientes con ligaduras intestinales y su inicio debe ser de forma temprana, en caso de que la nutrición enteral no pueda ser establecida 31.
La nutrición enteral se iniciará una vez se halla reestablecido el tránsito intestinal y no curse con íleo paralítico 31.
Shunt vascular
En el trauma vascular el rápido control de las lesiones tiene como objetivo restaurar el flujo hacia el órgano o extremidad comprometida; cuando no es posible realizar el reparo primario se utilizan los shunts vasculares los cuales pueden ser artesanales o comerciales, sin que se haya encontrado diferencia significativa, incrementado la probabilidad de supervivencia y preservación de la funcionalidad del área afectada. Su uso se popularizó en las guerras con el incremento del trauma vascular en extremidades; y posteriormente, se ha extendió a centros de trauma civil 32 (Figura 3).
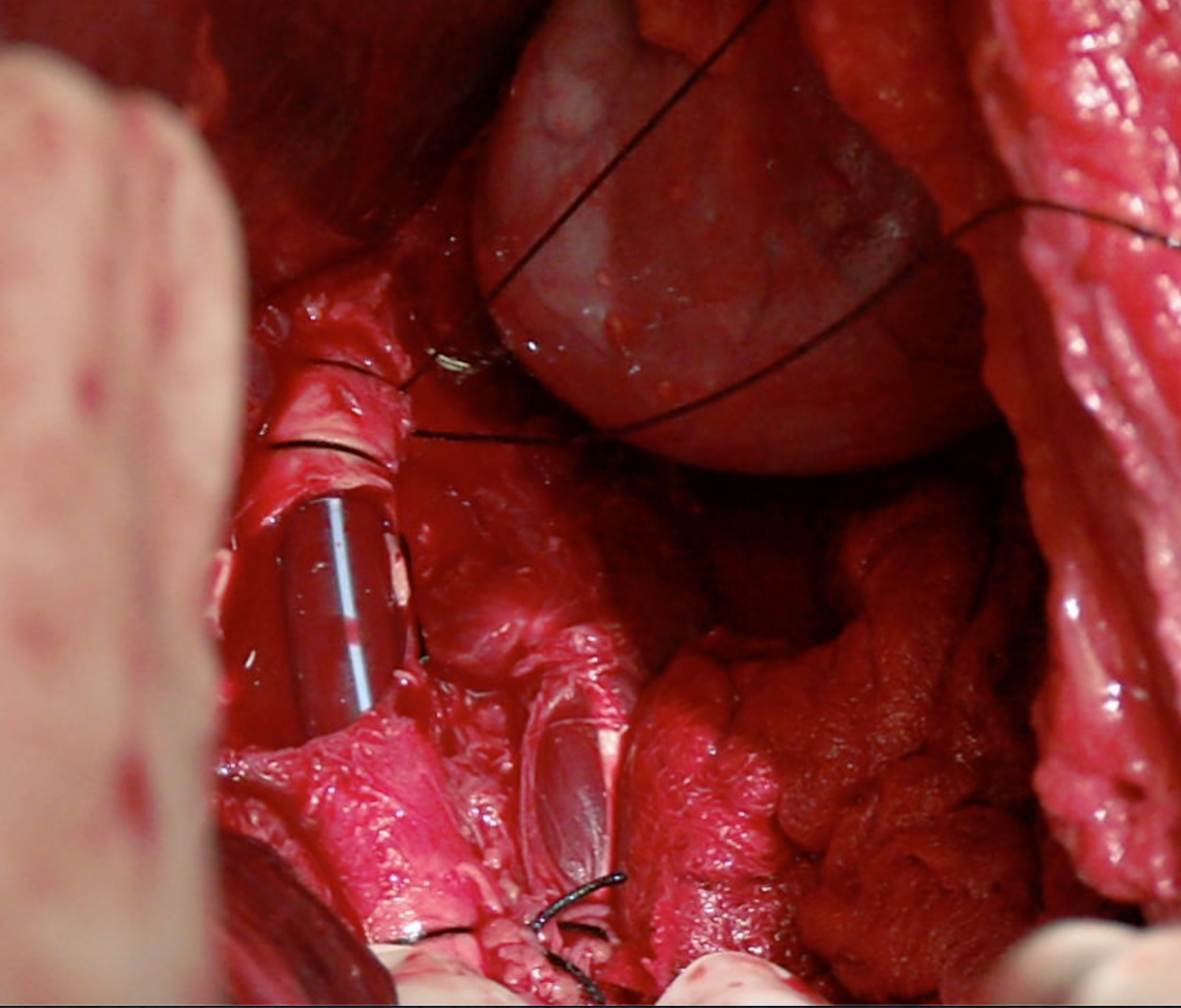
Figura 3 Shunt Vascular en Aorta. Lesión de la Aorta Abdominal Infrarrenal que es manejada temporalmente con la colocación de un shunt vascular (tubo de tórax).
La permeabilidad de un shunt depende de las siguientes variables: el tiempo, la técnica de colocación, el tipo de vaso lesionado y el estado fisiológico del paciente. Inaba et al., demostraron trombosis del shunt en un 5.6%. De estos la mayoría se retiraron en menos de 48 horas sin demostrar complicaciones 33. Ding y colaboradores, con datos obtenidos de un modelo animal, sugirieron que el tiempo ideal de utilización es de 6 horas para mantener la permeabilidad 34. Sin embargo, los rangos de tiempo en varios estudios van desde 2 hasta 52 horas sin usar anticoagulación.
Las conclusiones de la mayoría de los artículos es que los shunts vasculares son una adecuada práctica clínica en el contexto de cirugía de control daños. El uso del shunt vascular debe ser idealmente solo por las primeras 6 horas después de la cirugía índice ya que hacer el manejo definitivo temprano de la lesión vascular debe ser una prioridad.
Cierre de la pared abdominal
En promedio 10% a 15% de las laparotomías son manejadas con cirugía de control de daños con abdomen abierto. Los defectos de la pared abdominal, las fístulas, la desnutrición y la estancia prolongada en la unidad de cuidado intensivo son algunas complicaciones asociadas a esta técnica. La pregunta sería entonces ¿cuándo es el momento adecuado para su cierre? Este tópico se encuentra en debate constante ya que depende de muchos factores: tiempo de reintervención, número de reintervenciones, cantidad de líquidos administrados en la reanimación y la estrategia de cierre temporal utilizada. Si bien en algunas ocasiones no es posible cerrar la cavidad debido al edema de las asas intestinales o al mismo estado hemodinámico, se debe emplear técnicas de cierre temporal para evitar desecación del intestino, trastornos hidroelectrolíticos, inflamación de los tejidos, y la más temida, la pérdida del dominio de la pared abdominal generada por la retracción miofascial y la tensión de los componentes del abdomen. Estos factores dificultan técnicamente la reconstrucción futura 35. Por lo anterior, el cierre se debe realizar lo más pronto posible, una vez el paciente esté completamente reanimado, sin requerimientos de nuevos procedimientos y sin riesgo de síndrome de compartimento abdominal. Algunos autores consideran que el tiempo ideal de cierre son los primeros 9 días 36. Miller et al., en un estudio de 344 laparotomías para control daños, obtuvieron una proporción de cierre primario de la fascia del 65%, y demostraron que el cierre antes de 8 días estaba asociado a mejores desenlaces clínicos 37.
Al realizar la comparación entre los resultados del cierre de la pared abdominal en la primera intervención posterior a la cirugía de control daños versus intervenciones posteriores, algunos estudios han demostrado una tasa menor de abscesos intraabdominales, falla ventilatoria, falla renal y sepsis en los cierres tempranos. Cuando estas variables se ajustaron a la edad, el género masculino y algunos puntajes de trauma, encontraron que las complicaciones infecciosas y no infecciosas son menores en el grupo que es operado de manera temprana.
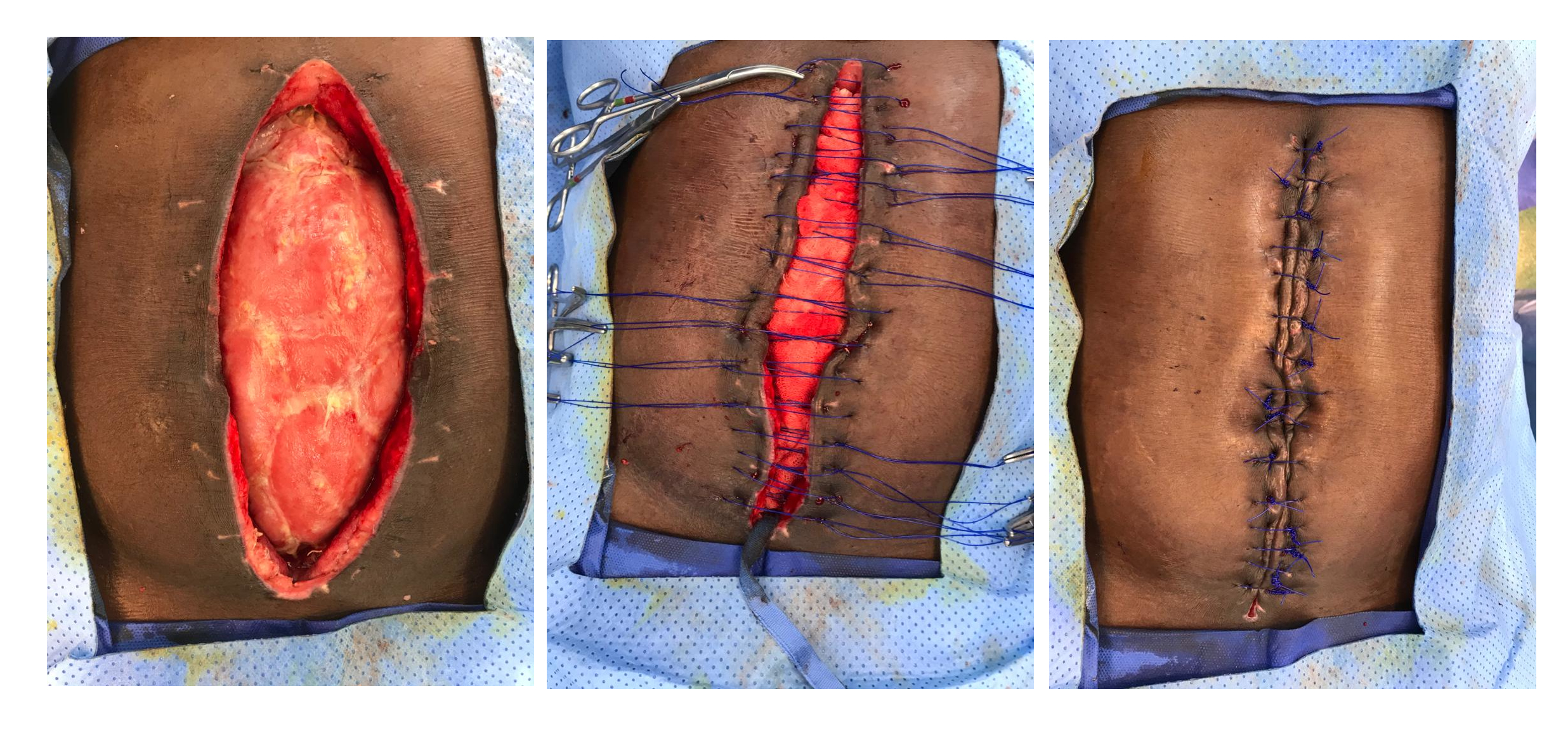
Teniendo en cuenta que la intención debe ser el cierre temprano de la pared abdominal, y que la evisceración es una complicación grave, el uso de mallas es una estrategia para usar en estos pacientes. Se debe estimar los riesgos y beneficios relacionados con su utilización, como la infección del sitio operatorio, los seromas y el rechazo de la prótesis 38. Algunos consensos recomiendan el uso de estrategias como las terapias de presión negativa o las tracciones dinámicas de la fascia para evitar la retracción de los tejidos (Figura 4). En aquellos casos de defectos grandes no se deben descartar técnicas como la separación de componentes de la pared abdominal. Sin embargo, los esfuerzos exagerados para cerrar la pared abdominal podrían traer consecuencias lamentables y es donde aparece la eventración programada como una estrategia aceptable en este grupo, recomendada idealmente después de los 6 meses de la cirugía inicial 39.
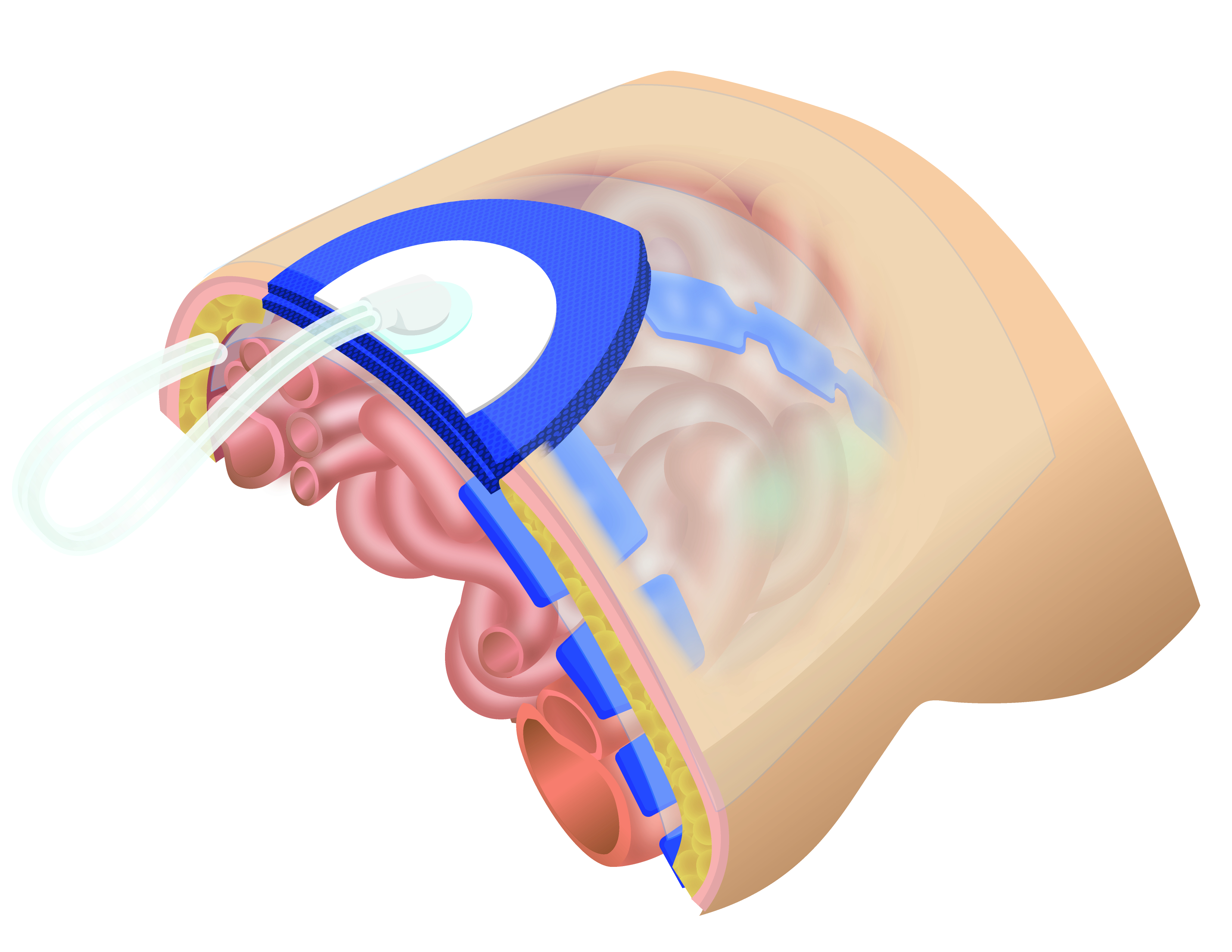
Figura 4 Sistema de presión negativa para el cierre diferido del abdomen. Sistema de Presión Negativa para el cierre diferido abdominal. La interfaz de plástico fenestrado separa los órganos intraabdominales, mientras que las espumas o apósitos se ubican encima y se fijan con una capa doble de plástico adhesivo. El dispositivo de succión se instala sobre el plástico adhesivo recortando un círculo de 3 a 3.5 cm de diámetro.
Por lo tanto, la recomendación es realizar el cierre de la cavidad abdominal en la segunda o tercera reintervención en un tiempo máximo entre el quinto y séptimo día después de la cirugía índice. Si no es posible un cierre del abdomen incluyendo la fascia y el abdomen, se debe optar por cierre únicamente de la piel en la primera semana para evitar complicaciones sobre la pared abdominal (Figura 5).
Conclusión
La decisión de la reintervención es igual de importante que la cirugía de control de daños inicial. Las medidas de control pueden fracasar o tener complicaciones si la reintervención no se define a tiempo y no es tenida en cuenta como una variable critica para el éxito de los esfuerzos de control de daños.
Agradecimientos:
A Linda M. Gallego por sus contribuciones en el desarrollo del artículo.
REFERENCIAS
1. Rotondo MF, Schwab CW, McGonigal MD, Phillips GR, Fruchterman TM, Kauder DR, et al. "Damage control": an approach for improved survival in exsanguinating penetrating abdominal injury. J Trauma. 1993; 35: 375-82; discussion 382-3. [ Links ]
2. Stone HH, Strom PR, Mullins RJ. Management of the major coagulopathy with onset during laparotomy. Ann Surg. 1983; 197: 532-5. Doi: 10.1097/00000658-198305000-00005. [ Links ]
3. Beldowicz BC. The evolution of damage control in concept and practice. Clin Colon Rectal Surg 2018;31:30-5. Doi: 10.1055/s-0037-1602177. [ Links ]
4. Keel M, Trentz O. Pathophysiology of polytrauma. Injury. 2005; 36: 691-709. Doi: 10.1016/j.injury.2004.12.037. [ Links ]
5. Ditzel RM, Anderson JL, Eisenhart WJ, Rankin CJ, DeFeo DR, Oak S, et al. A review of transfusion- And trauma-induced hypocalcemia: Is it time to change the lethal triad to the lethal diamond? J Trauma Acute Care Surg. 2020; 88: 434-9. Doi: 10.1097/TA.0000000000002570. [ Links ]
6. Roberts DJ, Bobrovitz N, Zygun DA, Ball CG, Kirkpatrick AW, Faris PD, et al. Indications for use of damage control surgery in civilian trauma patients. A content analysis and expert appropriateness rating study. Ann Surg. 2016; 263: 1018-27. Doi: 10.1097/SLA.0000000000001347. [ Links ]
7. Ordoñez C, Pino L, Badiel M, Sanchez A, Loaiza J, Ramirez O, et al. The 1-2-3 approach to abdominal packing. World J Surg. 2012; 36: 2761-6. Doi: 10.1007/s00268-012-1745-3. [ Links ]
8. Cullinane DC, Jawa RS, Como JJ, Moore AE, Morris DS, Cheriyan J, et al. management of penetrating intraperitoneal colon injuries: A meta-analysis and practice management guideline from the Eastern Association for the Surgery of Trauma. J Trauma Acute Care Surg. 2019;86:505-15. Doi: 10.1097/TA.0000000000002146. [ Links ]
9. Anjaria DJ, Ullmann TM, Lavery R, Livingston DH. Management of colonic injuries in the setting of damage-control laparotomy: One shot to get it right. J Trauma Acute Care Surg. 2014;76:594-600. Doi: 10.1097/TA.0000000000000132. [ Links ]
10. Hirshberg A, Mattox KL. Planned reoperation for severe trauma. Ann Surg. 1995;222:3-8. Doi: 10.1097/00000658-199507000-00002. [ Links ]
11. Ordoñez CA, Pino LF, Badiel M, Sánchez AI, Loaiza J, Ballestas L, et al. Safety of performing a delayed anastomosis during damage control laparotomy in patients with destructive colon injuries. J. Trauma. 2011; 71: 1512-8. Doi: 10.1097/TA.0b013e31823d0691. [ Links ]
12. Aydin U, Yazici P, Zeytunlu M, Coker A. Is it more dangerous to perform inadequate packing? World J Emerg Surg. 2008;3:1. Doi: 10.1186/1749-7922-3-1. [ Links ]
13. Nicol AJ, Hommes M, Primrose R, Navsaria PH, Krige JEJ. Packing for control of hemorrhage in major liver trauma. World J Surg. 2007;31:569-74. Doi: 10.1007/s00268-006-0070-0. [ Links ]
14. Kang BH, Jung K, Choi D, Kwon J. Early re-laparotomy for patients with high-grade liver injury after damage-control surgery and perihepatic packing. Surg Today. 2021; 51(6): 891-896. Doi: 10.1007/s00595-020-02178-1. [ Links ]
15. Hirshberg A, Wall MJJ, Mattox KL. Planned reoperation for trauma: a two year experience with 124 consecutive patients. J Trauma. 1994;37:365-9. [ Links ]
16. Urschel JD, Bertsch DJ, Takita H. Thoracic packing for postoperative hemorrhage. J Cardiovasc Surg (Torino). 1997;38:673-5. [ Links ]
17. Péterffy Å, Henze A. Haemorrhagic complications during pulmonary resection a retrospective review of 1428 resections with 113 haemorrhagic episodes. Scand Cardiovasc J. 1983;17:283-7. Doi: 10.3109/14017438309099366. [ Links ]
18. Furnary AP, Magovern JA, Simpson KA, Magovern GJ. Prolonged open sternotomy and delayed sternal closure after cardiac operations. Ann Thorac Surg. 1992;54:233-9. Doi: 10.1016/0003-4975(92)91375-J. [ Links ]
19. Manzano-Nunez R, Chica J, Gómez A, Naranjo MP, Chaves H, Muñoz LE, et al. The tenets of intrathoracic packing during damage control thoracic surgery for trauma patients: a systematic review. Eur J Trauma Emerg Surg. 2021; 47(2): 423-434. Doi: 10.1007/s00068-020-01428-8. [ Links ]
20. Moriwaki Y, Toyoda H, Harunari N, Iwashita M, Kosuge T, Arata S, et al. Gauze packing as damage control for uncontrollable haemorrhage in severe thoracic trauma. Ann R Coll Surg Engl. 2013;95:20-5. Doi: 10.1308/003588413X13511609956057. [ Links ]
21. Garcia AF, Manzano-Nunez R, Bayona JG, Millan M, Puyana JC. A clinical series of packing the wound tract for arresting traumatic hemorrhage from injuries of the lung parenchyma as a feasible damage control technique. World J Emerg Surg. 2019; 28; 14: 52. Doi: 10.1186/s13017-019-0273-y. [ Links ]
22. Filiberto DM, Fox AD. Preperitoneal pelvic packing: Technique and outcomes. Int J Surg. 2016;33:222-4. Doi: 10.1016/j.ijsu.2016.05.072. [ Links ]
23. Coccolini F, Stahel PF, Montori G, Biffl W, Horer TM, Catena F, et al. Pelvic trauma: WSES classification and guidelines. World J Emerg Surg. 2017;12:1-18. Doi: 10.1186/s13017-017-0117-6. [ Links ]
24. Weinberg JA, Griffin RL, Vandromme MJ, Melton SM, George RL, Reiff DA, et al. Management of colon wounds in the setting of damage control laparotomy: A cautionary tale. J Trauma. 2009; 67: 929-33. Doi: 10.1097/TA.0b013e3181991ab0. [ Links ]
25. Demetriades D, Murray JA, Chan L, Ordoñez C, Bowley D, Nagy KK, et al. Penetrating colon injuries requiring resection: Diversion or primary anastomosis? An AAST prospective multicenter study. J Trauma. 2001; 50: 765-75. Doi: 10.1097/00005373-200105000-00001. [ Links ]
26. Tatebe LC, Jennings A, Tatebe K, Handy A, Prajapati P, Smith M, et al. Traumatic colon injury in damage control laparotomy - A multicenter trial: Is it safe to do a delayed anastomosis? J. Trauma Acute Care Surg. 2017; 82: 742-9. Doi: 10.1097/TA.0000000000001349. [ Links ]
27. Miller PR, Chang MC, Hoth JJ, Holmes IV JH, Meredith JW. Colonic resection in the setting of damage control laparotomy: Is delayed anastomosis safe? Am Surg. 2007;73:606-9. Doi: 10.1177/000313480707300613. [ Links ]
28. Ordoñez CA, Parra M, Caicedo Y, Padilla N, Angamarca E, Serna JJ, et al. Damage control surgical management of combined small and large bowel injuries in penetrating trauma: Are ostomies still pertinent? Colomb Med (Cali). 2021; 52(2): e4114425. Doi: 10.25100/cm.v52i2.4425. [ Links ]
29. Ordoñez C, García A, Parra MW, Scavo D, Pino LF, Millán M, et al. Complex penetrating duodenal injuries: Less is better. J Trauma Acute Care Surg. 2014;76:1177-83. Doi: 10.1097/TA.0000000000000214. [ Links ]
30. Ordoñez CA, Parra M, Millan M, Caicedo Y, Padilla N, Garcia A, et al. Damage control in penetrating duodenal trauma: less is better. Colomb Med (Cali) 2021; 52(2): e4104509. Doi: 10.25100/cm.v52i2.4509. [ Links ]
31. Fabian TC, Croce MA, Minard G, Bee TK, Cagiannos C, Miller PR, et al. Current issues in trauma. Curr Probl Surg. 2002; 39:1160-244. Doi: 10.1067/msg.2002.128499. [ Links ]
32. Rasmussen TE, Dubose JJ, Asensio JA, Feliciano D V., Fox CJ, Nuñez TC, et al. Tourniquets, vascular shunts, and endovascular technologies: Esoteric or essential? A report from the 2011 AAST Military Liaison Panel. J Trauma Acute Care Surg. 2012;73:282-5. Doi: 10.1097/TA.0b013e3182569df4. [ Links ]
33. Inaba K, Aksoy H, Seamon MJ, Marks JA, Duchesne J, Schroll R, et al. Multicenter evaluation of temporary intravascular shunt use in vascular trauma. J Trauma Acute Care Surg. 2016;80:359-65. Doi: 10.1097/TA.0000000000000949. [ Links ]
34. Ding W, Wu X, Meng Q, Yan M, Fan X, Ji W, et al. Time course study on the use of temporary intravascular shunts as a damage control adjunct in a superior mesenteric artery injury model. J Trauma. 2010; 68: 409-14. Doi: 10.1097/TA.0b013e31819ea416. [ Links ]
35. Demetriades D, Salim A. Management of the Open Abdomen. Surg Clin North Am. 2014;94:131-53. Doi: 10.1016/j.suc.2013.10.010. [ Links ]
36. Coccolini F, Roberts D, Ansaloni L, Ivatury R, Gamberini E, Kluger Y, et al. The open abdomen in trauma and non-trauma patients: WSES guidelines. World J Emerg Surg. 2018; 13: 7. Doi: 10.1186/s13017-018-0167-4. [ Links ]
37. Miller RS, Morris JA, Diaz JJ, Herring MB, May AK, Rotondo MF, et al. Complications after 344 damage-control open celiotomies. J Trauma. 2005; 59: 1365-74. Doi: 10.1097/01.ta.0000196004.49422.af. [ Links ]
38. Lima HVG, Rasslan R, Novo FCF, Lima TMA, Damous SHB, Bernini CO, et al. Prevention of fascial dehiscence with onlay prophylactic mesh in emergency laparotomy: a randomized clinical trial. J Am Coll Surg. 2020; 230: 76-87. Doi: 10.1016/j.jamcollsurg.2019.09.010. [ Links ]
39. Godat L, Kobayashi L, Costantini T, Coimbra R. Abdominal damage control surgery and reconstruction: World society of emergency surgery position paper. World J Emerg Surg. 2013; 8: 53. Doi: 10.1186/1749-7922-8-53. [ Links ]
Recibido: 31 de Marzo de 2021; Revisado: 11 de Junio de 2021; Aprobado: 29 de Junio de 2021











 text in
text in