Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombia Médica
On-line version ISSN 1657-9534
Colomb. Med. vol.54 no.1 Cali Jan./Mar. 2023 Epub Mar 30, 2023
https://doi.org/10.25100/cm.v54i1.4625
Reporte de caso
Síndrome autoinmune / inflamatorio inducido por adyuvantes (ASIA), tratamiento médico de compromiso sistémico severo: reporte de caso
1 Fundación clínica Valle del Lili, Servicio de Reumatología, Cali, Colombia,
2 Universidad ICESI, Facultad de Medicina, Cali, Colombia,
3 Fundación clínica Valle del Lili, Departamento de Patología, Cali, Colombia,
Descripción del caso:
Mujer de 42 años con compromiso inflamatorio pulmonar y mediastinal severo, secundario a infiltración de un material alogénico relacionado con la silicona con migración sistémica.
Hallazgos clínicos:
La paciente desarrolló estenosis esofágica y bronquial, infecciones recurrentes, desnutrición y deterioro respiratorio, imposibilitando la extracción quirúrgica del material alogénico.
Tratamiento y resultado:
Mejoría clínica y radiológica lograda tras un tratamiento con múltiples inmunomoduladores intravenosos y orales.
Relevancia clínica:
El síndrome autoinmune / inflamatorio inducido por adyuvantes (ASIA) es una enfermedad heterogénea que resulta de la exposición a sustancias alógenas en un sujeto con susceptibilidad genética. Estas sustancias inducen fenómenos autoinmunitarios o autoinflamatorios. Desde que ASIA fue descrito hace 10 años, sus criterios diagnósticos continúan en discusión, con un pronóstico incierto. El tratamiento idóneo se basa en eliminar la sustancia causante, pero no siempre es posible, por lo cual se hace necesario iniciar un tratamiento inmunomodulador, empleándose en esta paciente un esquema que no había sido reportado previamente en la literatura.
Palabras clave: ASIA; Autoinmunidad; silicona; materiales biocompatibles; metacrilatos; polímeros; siloxanos; biopolímeros; cuerpos extraños
Case description:
A 42-year-old woman with severe pulmonary and mediastinal inflammatory involvement, secondary to infiltration of a silicone-related allogenic material with systemic migration.
Clinical findings:
The patient developed esophageal and bronchial stenosis, recurrent infections, malnutrition, and respiratory deterioration, making surgical removal of the allogenic material impossible.
Treatment and outcome:
Clinical and radiological improvement was achieved after treatment with multiple intravenous and oral immunomodulators.
Clinical relevance:
Autoimmune/inflammatory syndrome induced by adjuvants (ASIA) is a heterogeneous disease resulting from exposure to allogenic substances in a susceptible subject. These substances cause autoimmune or autoinflammatory phenomena. Since ASIA was described ten years ago, its diagnostic criteria are still under discussion, with an uncertain prognosis. The ideal therapy is based on eliminating the causative substance, but this is not always possible. Therefore, it is necessary to start an immunomodulatory treatment, using it in this patient, a scheme that had not been previously reported in the literature.
Keywords: ASIA; autoimmunity; silicone; biocompatible materials; methacrylates; polymers; siloxanes; biopolymers; foreign bodies
Introducción
Durante varias décadas, se ha reconocido que los adyuvantes, como el silicio o algunos componentes de las vacunas, son factores inductores de una amplia gama de reacciones autoinmunes y autoinflamatorias locales o sistémicas en pacientes genéticamente susceptibles 1. Los adyuvantes pueden unirse a receptores de reconocimiento de patrones, promover cambios en la estructura terciaria de las proteínas e inducir respuestas inflamatorias en linfocitos autorreactivos mediante mimetismo molecular o acumulando sustancias extrañas dentro del citoplasma de los macrófagos 2,3. La reacción tisular producida por la inoculación de estos materiales se describía clásicamente como una reacción granulomatosa a cuerpo extraño. Sin embargo, desde el punto de vista histológico y fisiopatológico, también presentan infiltración de macrófagos, mastocitos y fibroblastos. Otras poblaciones celulares, como las células plasmáticas, células dendríticas y linfocitos reactivos, podrían estar involucradas, además de citoquinas proinflamatorias como IL-1, IL-12 y TNF-α, presentando reacciones sistémicas hasta 15 años después de la inoculación 4,5.
Pueden ocurrir una amplia variedad de manifestaciones relacionadas con sustancias alogénicas, desde condiciones leves como hiperpigmentación de la piel hasta trastornos graves como artritis reumatoide (AR), lupus eritematoso sistémico (LES) y síndrome de Sjögren (SS). Todas estas reacciones caben dentro del síndrome autoinmune/inflamatorio inducido por adyuvantes (ASIA, por sus siglas en inglés). El término ASIA fue propuesto por Shoenfeld et al. (2010) y se ha asociado con el antígeno leucocitario humano (HLA)-DRB1*01, DQA1*0102, DQ2 y DRW53, entre otros. Múltiples expresiones clínicas encajan frecuentemente dentro de los criterios de clasificación de diferentes enfermedades autoinmunes o autoinflamatorias; sin embargo, a menudo son inespecíficas o locales, por lo que Shoenfeld y Agmon-Levin (2011) propusieron un conjunto de criterios diagnósticos 1,2,6, que fueron modificados por Alijotas-Reig (2015) para hacerlos más objetivos, pero aún no han sido validados 7 (Tabla 1).
Tabla 1 Criterios diagnósticos del síndrome autoinmune/inflamatorio inducido por adyuvantes (ASIA). *Modificado de7.
| Criterios mayores | Reporte de caso |
|---|---|
| 1. Exposición a estímulos externos: biomaterialesA, vacunas, anilinas u otros materiales orgánicos/inorgánicos antes de la aparición de manifestaciones clínicas. | X |
| 2. Tiempo mínimo de latencia de días en el caso de vacunas y 1 mes cuando se sospecha que el desencadenante es distinto de las vacunas, es decir, biomaterialesB. | |
| 3. Compromiso clínico: | X |
| ⏺ Local/regional: Nódulos inflamatorios en piel, o edema, o angioedema. Induraciones en piel; pseudo-abscesos; linfadenopatias, paniculitis, morfea, lesiones de tipo sarcoide. | |
| ⏺ Sistemicas: Nódulos inflamatorios a distancia; artritis; sicca o síndrome de SjögrenC; miositisD o debilidad muscularE, paniculitis extendida, compromiso neurológico desmielinizante | |
| ⏺ Evolución hacía enfermedad autoinmune con o sin compromiso de órgano | |
| 4. Biopsia tipo cuerpo extraño del área afectada o ganglios linfáticosF, o hallazgos histológicos consistentes con trastornos autoinmunes/granulomatosos. | X |
| 5. El retiro de los materiales desencadenantes induce la mejoría | |
| 6. Presencia de HLA compatible (por ejemplo, HLA B8, HLA DRB1, HLA DR3, HLA DQB1, o combinación de haplotipos) | |
| Criterios menores | |
| 1. Historia reciente de factores desencadenantes previos al inicio de las manifestaciones clínicasG | |
| 2. Livedo reticularis de gran tamaño de novo y/o eritema en las manos que aparece al inicio de las manifestaciones clínicasH | |
| 3. Presencia de autoanticuerpos y/o hipergammaglobulinemia y/o elevación de ACE y/o elevación de LDH y/o niveles bajos de complemento. | X |
El diagnóstico de ASIA se basa en cumplir con dos criterios mayores o un criterio mayor y dos criterios menores
*HLA: antigeno leucocitario humano; ACE: enzima convertidora de angiotensina; LDH: deshidrogenasa láctica; LES: lupus eritematosos sistémico; MRC: sistema de graduación de fuerza muscular del medical research council
A Parafina, silicona, silicona de uso médico, metacrilato, ácido poli-L-láctico, poliacrilamida, poli-alquil-imida, colágeno, hidroxiapatita, ácido hialurónico, ácido hialurónico estabilizado de origen no animal, alginato.
B Cuando las reacciones adversas ocurren después de un segundo estímulo, se puede aceptar un corto período de tiempo.
C Demostrado a través de pruebas objetivas: flujo salival o centellografía salival; pruebas de Schirmer y Rose Bengala.
D Documentado mediante enzimas musculares elevadas y/o electromiografía y/o biopsia muscular.
E La fuerza muscular debe evaluarse mediante la escala MRC o similar.
F Especificando qué tipo de patrón histopatológico se identificó (por ejemplo, sarcoidal, en palisada, necrobiótico, parafinoma, siliconoma). Se deben considerar y describir patrones histopatológicos específicos de biomateriales y adyuvantes de vacunas.
G Proceso infeccioso, trauma o manipulación de áreas rellenadas/implantadas/vacunadas.
H. Aparición de eritema de novo indoloro, simétrico y bilateral en palmas y a veces en la superficie palmar de los dedos, de coloración rojiza, violácea o azulada, similar a lo observado en LES, hiperestrogenismo o vasculitis.
Una amplia variedad de biomateriales se inyecta de forma subcutánea en tejidos blandos con fines cosméticos para aumentar el volumen. Estas sustancias han sido prohibidas por las leyes de salud de muchos países, especialmente en América Latina, donde se han reportado el mayor número de complicaciones, incluyen metacrilato, petrolato, aceites minerales, polisiloxano y algunas formas de ácido hialurónico 4.
La silicona es un polímero relacionado con el silicón orgánico y es la sustancia más ampliamente utilizada, la cual puede encontrarse en forma líquida o sólida. El componente más estrechamente asociado con el silicón es el polidimetilsiloxano, ampliamente utilizado en implantes médicos, prótesis mamarias o inyecciones directas. El silicón líquido también puede utilizarse para aumentar el volumen de tejidos blandos diferentes a la mama con fines estéticos, para rellenar arrugas o cicatrices, como las de acné. Aunque el silicón se considera biológicamente inerte, se han documentado efectos adversos de origen inflamatorio y autoinmune asociados con la destrucción de tejido.
Aunque aún no hay consenso sobre la relación causal entre el uso de este tipo de materiales 8,9, la presencia de material alógeno se asocia con una mayor prevalencia de enfermedades autoinmunes/autoinflamatorias, con una razón de probabilidades (OR) de 1.22 (1.18-1.26). También se ha descrito la migración local o a distancia de este material, lo que parece aumentar el riesgo de complicaciones 10. La búsqueda constante de tratamientos estéticos de bajo costo, con acceso limitado a servicios de salud de calidad, combinada con la inyección por personal no calificado, ha llevado al manejo indiscriminado de materiales de relleno no autorizados para su uso, con efectos que aún están pobremente documentados, lo que dificulta predecir su progresión con el tiempo y su severidad 5.
El tratamiento de ASIA sugiere la eliminación de la sustancia estimulante; sin embargo, en muchos casos se observa una falta de mejoría a pesar de este manejo, o el material se ha extendido ampliamente en los tejidos volviéndose irresecable, lo que obliga a iniciar una inmunomodulación farmacológica 4,11. Teniendo en cuenta que ASIA es una enfermedad difícil de diagnosticar y clasificar, con un pronóstico incierto y un tratamiento poco definido, especialmente en casos de diseminación del material alógeno con compromiso sistémico severo, es especialmente importante informar este tipo de casos.
Descripción del caso
Paciente de sexo femenino, de 42 años, con antecedente de consumo moderado de tabaco, sin comorbilidades ni antecedentes familiares significativos. Se sometió a una liposucción abdominal, aumento de glúteos con implantes de biopolímeros a los 30 años, y a una mamoplastia de aumento con implantes de silicona en dos ocasiones, la última a los 36 años. La enfermedad actual comenzó a los 37 años cuando presentó disnea moderada, ojo seco, boca seca, tos, artralgia en las manos y fiebre recurrente. En ese momento, la historia clínica previo indicaba que tenía una altura de 165 cm y pesaba 64 kg, con signos vitales de temperatura corporal de 38,8 °C, frecuencia cardíaca de 102 latidos por minuto, frecuencia respiratoria de 22 respiraciones por minuto y presión arterial de 110/78 mmHg. En el examen físico, se registró dolor en las articulaciones metacarpofalángicas e interfalángicas proximales sin sinovitis, y murmullo vesicular normal en el tercio superior de ambos hemitórax, así como crepitaciones finas en los dos tercios inferiores de ambos hemitórax. La tomografía computarizada (TC) de tórax mostró infiltrados reticulonodulares y tractos fibrosos pulmonares bilaterales, descartando fibrosis pulmonar mediante biopsia. Los exámenes inmunohematológicos indicaron anticuerpos antinucleares (ANA) positivos (1:1,280, patrón moteado) y negatividad de anticuerpos anti-Scl-70, anti-ADN, antígenos nucleares extraíbles (ENA) y anticuerpos anticitoplasma de neutrófilos (ANCA), con niveles normales de complemento C3 y C4. Debido a los títulos positivos de ANA y el cuadro clínico, se sospechó un diagnóstico presuntivo de enfermedad del tejido conectivo indiferenciada con compromiso pulmonar. Por lo tanto, se decidió iniciar el tratamiento con prednisolona 25 mg/día y azatioprina 50 mg/día, con control parcial de los síntomas. A los 40 años, la paciente desarrolló disfagia para sólidos, con evidencia endoscópica de estenosis esofágica grave tratada con dilataciones neumáticas y colocación de una prótesis autoexpandible. Después del procedimiento, persistió el dolor precordial y debido a la intolerancia se inició el tratamiento con prednisona 50 mg/día durante un mes, y se intentó sin éxito la extracción de la prótesis esofágica. La resonancia magnética nuclear (RMN) pélvica evidenció infiltración de material en el tejido celular subcutáneo bilateralmente, con inflamación y reacción a cuerpo extraño, principalmente en la región glútea derecha, con participación de las fibras musculares del músculo isquiotibial y glúteo mayor (Figura 1 A, B).
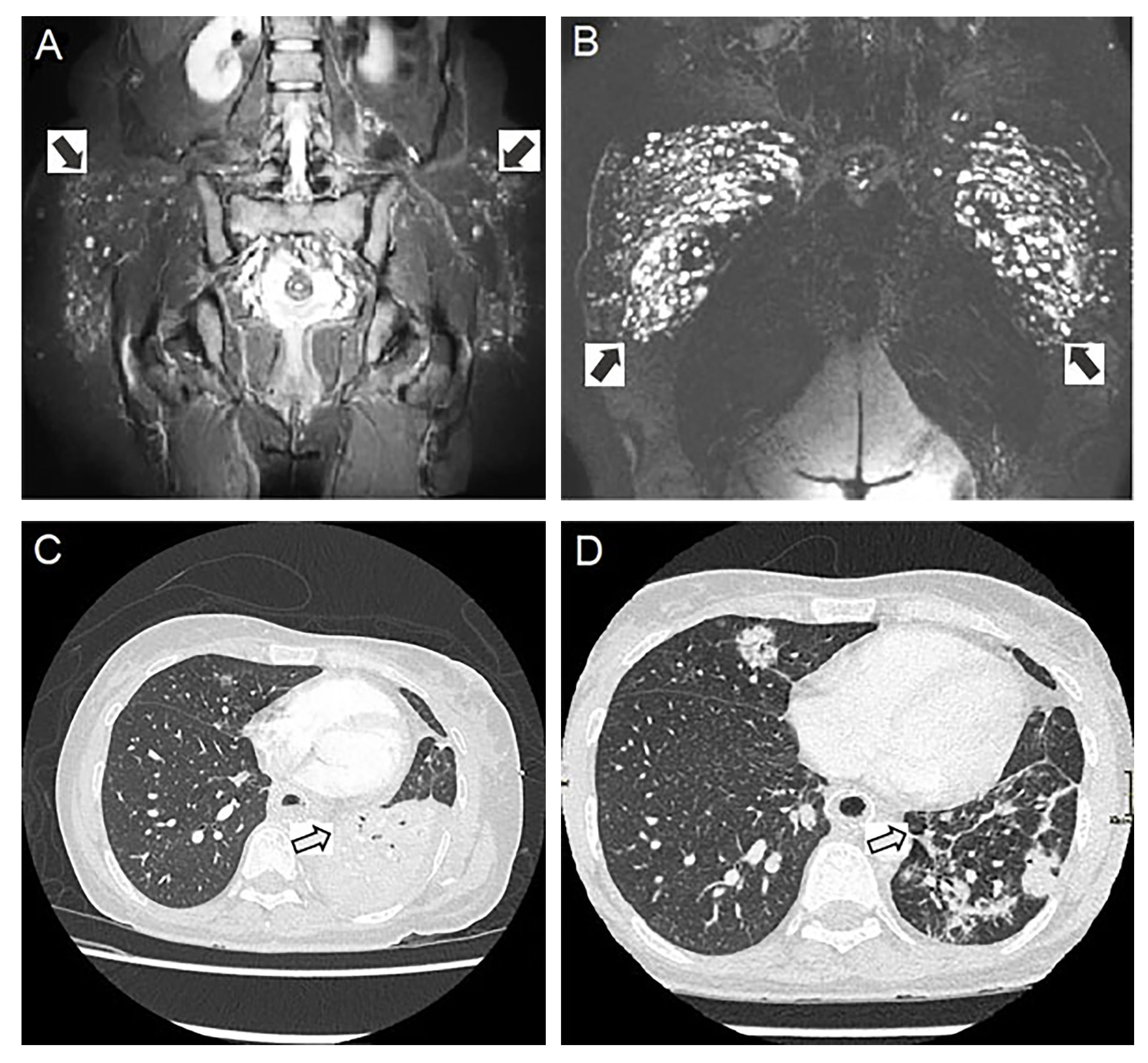
Figura 1 A. RMN de pelvis, vista coronal, secuencia de saturación grasa con densidad de protones que muestra nódulos hiperintensos en el tejido celular subcutáneo. B. Secuencia STIR que muestra realce del material extraño (biopolímero) con inflamación perilesional y reacción a cuerpo extraño. C. Tomografía computarizada de tórax que muestra cambios inflamatorios en el mediastino, ocupación por un material hipodenso en el bronquio fuente izquierdo que se extiende al lóbulo inferior, y neumonía necrotizante. D. Resolución de la obstrucción del bronquio fuente izquierdo, mejora de los cambios intersticiales y de la consolidación en el parénquima pulmonar en comparación con C.
Cuando la paciente tenía 42 años, pesaba 48 kg y fue hospitalizada con signos de desnutrición, taquicardia, tos con expectoración mucopurulenta, empeoramiento de la disnea y dolor torácico, el murmullo vesicular estaba abolido en el hemitórax izquierdo y presentaba roncus gruesos en el hemitórax derecho, con para realizar las actividades básicas de la vida diaria. Los signos vitales de la paciente fueron: 37,2 °C de temperatura corporal, 128 latidos por minuto de frecuencia cardíaca, 24 respiraciones por minuto y una presión arterial de 90 / 60 mmHg. En el examen físico, presentaba induración de la piel de los glúteos con masas palpables en la zona superior con rubor, edema y calor sin dolor superficial en la piel. No se detectaron signos de migración de masas en el examen físico. Además, presentaba elevación de los reactantes de fase aguda (velocidad de sedimentación eritrocitaria de 120 mm/h y proteína C reactiva de 96.4 g/L), trombocitosis reactiva (593,000/μL), sin alteración en la función renal o hepática.
La tomografía de tórax mostró una consolidación en el lóbulo inferior izquierdo, en mediastino; la endoprótesis esofágica con obstrucción parcial severa del esófago por un material hipodenso en la porción superior, y compresión del bronquio fuente izquierdo (Figura 1C). Por lo cual se dio el diagnóstico de neumonía, y se administró vancomicina 1 g/12 horas y meropenem 1 g/8 horas durante 14 días. La broncoscopia reveló oclusión completa del bronquio fuente izquierdo y oclusión del 70% del bronquio fuente derecho, este último ocupado por un material no identificado en ese momento (Figura 2 A, B). Las biopsias obtenidas por broncoscopia mostraron abundantes vasos reactivos e infiltrado inflamatorio mixto, predominantemente neutrofílico, tejido de granulación sin evidencia de células tumorales, y un solo macrófago con escaso material amorfo y refractario en su interior. Además, un examen histopatológico confirmó la presencia de material extraño a nivel bronquial y reacción granulomatosa (Figura 2 C, D, E, F). Por lo tanto, se consideró que la paciente presentaba un compromiso inflamatorio infiltrativo extenso en mediastino y pulmón relacionado con la migración de un material relacionado con silicona tipo biopolímero. Se descartaron diagnósticos diferenciales como esofagitis eosinofílica, enfermedad de Crohn y esclerosis sistémica mediante estudios complementarios, además tuvo niveles elevados de IgG, incluyendo IgG1, IgG2 e IgG3, pero IgG4 normal.
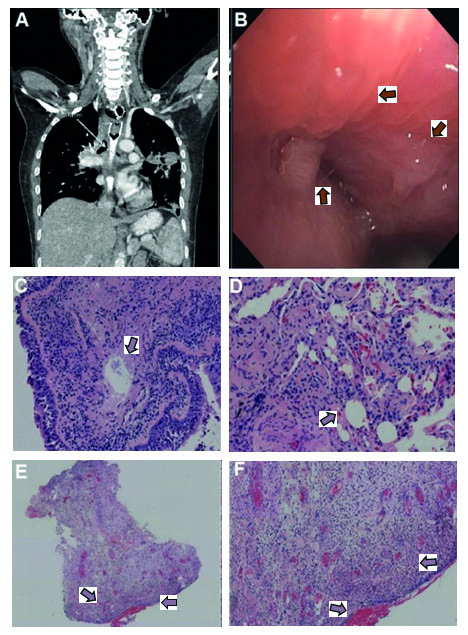
Figura 2 A. TC de tórax, vista coronal, que muestra compromiso con estenosis grave del esófago en el sitio del stent y ocupación de material hiperdenso en el mediastino con afectación de los bronquios fuente y obstrucción total del bronquio fuente izquierdo. B. Vista de broncoscopía fibroóptica endobronquial del bronquio fuente izquierdo colapsado por una obstrucción extrínseca, bronquio fuente derecho con lesión hialina protruyente. C, D. Ampliación de 10x y 20x, respectivamente, tinción con hematoxilina y eosina (H&E) de biopsia transbronquial, mostrando mucosa bronquial del lóbulo superior derecho y parénquima pulmonar y epitelio bronquial respiratorio con inflamación crónica mononuclear en el estroma y presencia de material refractario extraño; a mayor magnificación, se observa distorsión de la arquitectura del parénquima pulmonar debido a la presencia de material refractario redondeado. E, F. Ampliación de 4x y 10x, respectivamente, tinción con H&E de resección de lesión del bronquio fuente derecho, tejido de granulación con neoformación vascular, presencia de infiltrado inflamatorio agudo polimorfonuclear en cantidad moderada, con ulceración del epitelio superficial. No se observa material refractario, granulomas ni microorganismos.
Determinamos que la paciente presentaba ASIA (Síndrome Autoinmune/Inflamatorio Inducido por Adyuvantes) ya que no cumplía con los criterios de otras enfermedades autoinmunes o autoinflamatorias y había tenido exposición a un estímulo externo derivado de silicona (biopolímero), además de presentar compromiso local y sistémico. Esto se debía a induración de la piel en glúteos, nódulos inflamatorios a distancia en el mediastino, debilidad muscular, xerostomía, xeroftalmia, artralgia en las manos, hipergammaglobulinemia, y hallazgos en la biopsia pulmonar de migración de material alogénico con reacción granulomatosa (Tabla 1). Siempre que sea posible, se debe retirar el material alogénico. Sin embargo, en ese momento, la paciente no era candidata a manejo endoscópico de las vías respiratorias del pulmón izquierdo o lobectomía debido a un riesgo inadmisible de complicaciones. El tratamiento se centró en mantener la permeabilidad del árbol bronquial derecho. También se consideró la posibilidad de una esofagectomía con ascenso gástrico, probablemente con interposición de colon, después de una recuperación nutricional y rehabilitación pulmonar para reducir los riesgos quirúrgicos. Se propuso la extracción de los biopolímeros en glúteos para evitar una migración continua. Teniendo en cuenta lo mencionado anteriormente y dada la severidad del proceso inflamatorio sistémico secundario a la presencia del material de relleno, se inició un pulso de metilprednisolona a una dosis de 500 mg/día durante tres días, con terapia inmunomoduladora de mantenimiento a largo plazo compuesta por prednisolona 15 mg/día, ciclosporina 50 mg/día, cloroquina 250 mg/día y colchicina 0.5 mg/día.
Después de dos semanas del tratamiento descrito anteriormente, la paciente informa una menor intensidad del dolor torácico, y se logró suspender el uso de oxígeno suplementario. Una nueva tomografía computarizada de tórax (Figura 1D) permitió observar una mejora en la obstrucción del bronquio fuente izquierdo y cambios en el parénquima pulmonar del lóbulo inferior ipsilateral, así como una disminución de la obstrucción esofágica a ese nivel. En el control endoscópico digestivo superior y la broncoscopia con fibra óptica, se observó una recuperación parcial de la permeabilidad del esófago y del bronquio fuente izquierdo. Dado la buena respuesta al tratamiento con varios inmunomoduladores, se aumentó la dosis de ciclosporina a 50 mg cada 12 horas. Durante su evolución, la paciente desarrolló una nueva neumonía que mejoró con piperacilina/tazobactam 3.375 g/6 horas durante diez días. Desafortunadamente, no hubo posibilidad de tratar quirúrgicamente la afectación esofágica y pulmonar ni los múltiples focos de biopolímeros en los glúteos. Debido a la inmunosupresión con alto riesgo de infecciones, complicaciones y mortalidad, no fue posible realizar procedimientos quirúrgicos, pero la paciente sobrevivió y su condición mejoró gracias al tratamiento recibido.
Se realizó un seguimiento terapéutico tres meses después del alta hospitalaria, encontrando que la paciente pesaba 51 kg. En este seguimiento, la paciente expresó su impresión sobre este caso complejo y habló sobre la necesidad de campañas de educación pública que expongan el peligro de la cirugía estética en lugares no autorizados. Asimismo, ha colaborado con grupos de pacientes en la presentación de sus casos y ha ayudado a prevenir que otras personas terminen en situaciones similares. Su impresión general es de gratitud al personal médico y esperanza de recuperación con terapia física y continuando con los medicamentos recetados. Durante el seguimiento clínico, persisten la disnea y la disfagia, pero la paciente informa una menor intensidad de los síntomas en comparación con el inicio de la hospitalización. Ella continúa con prednisolona 15 mg/día, ciclosporina 50 mg/día, cloroquina 250 mg/día y colchicina 0.5 mg/día, y se tiene la intención de disminuir la prednisolona a 10 mg/día de acuerdo con la tolerancia de la paciente.
Discusión
El ASIA es una expresión de la influencia de elementos externos sobre la patogénesis y pronóstico de las enfermedades autoinmunes y autoinflamatorias 1. En casos de implantes de silicona, se ha reportado una relación con el desarrollo de enfermedades autoinmunes y autoinflamatorias, pero no todo está claro 11. Un número creciente de reportes describe una asociación entre eventos que llevan a la fisiopatología de ASIA con cambios histopatológicos, como se describe en este reporte de caso 2,3.
Presentamos un caso de compromiso inflamatorio pulmonar y mediastinal severo secundario a la migración de un material alógeno tipo biopolímero desde su implante en la región glútea. La paciente fue diagnosticada con ASIA, ya que cumplía con tres criterios mayores y uno menor (Tabla 1), y no cumplía completamente con los criterios de clasificación para otra enfermedad autoinmune sistémica, ya que no presentaba disfunción renal, serositis, compromiso vascular, leucopenia, hemólisis autoinmune o dismotilidad esofágica. La paciente tenía un título alto de ANA sin la presencia de otros autoanticuerpos sugerentes de otra enfermedad autoinmune. Todos los hallazgos se podrían explicar por el material alógeno, como la obstrucción del esófago y el bronquio fuente izquierdo, que fue el principal problema en la paciente 1,3,7. Este mismo patrón se ha descrito en otras revisiones, en las cuales solo el 11% de los pacientes presentaban síntomas inespecíficos, lo que no descarta la posibilidad de que la enfermedad ocurra hasta 15 años después de la exposición al adyuvante 4.
La relevancia de este caso se basa en varios hechos: una respuesta inadecuada al manejo con esteroides sistémicos, la incapacidad de eliminar los adyuvantes debido a un alto riesgo quirúrgico debido al déficit nutricional, el deterioro en la función pulmonar y la afectación mediastinal extrínseca, situaciones relacionadas con ASIA, lo que limita las opciones terapéuticas. Existe relativamente poca información de calidad disponible para el diagnóstico y tamizaje de pacientes con ASIA, y el conocimiento sobre casos graves con compromiso sistémico y riesgo de muerte es aún más limitado 11,12. Aunque los criterios de diagnóstico para sospecha de ASIA están documentados, tienen alta sensibilidad y baja especificidad, lo que limita la caracterización específica de los pacientes y dificulta el establecimiento de protocolos de tratamiento acorde a su presentación.
En países de América Latina, especialmente en Colombia, Brasil y Venezuela, puede haber una alta prevalencia de ASIA relacionada con silicona. Un ejemplo es un estudio realizado en Venezuela. Una reevaluación de 82 pacientes con complicaciones previas asociadas a rellenos dérmicos inyectables mostró que seis años después de un tratamiento "exitoso" de sus signos y síntomas, más de un tercio mostró reactivación de los síntomas, y el 29% presentó manifestaciones sistémicas compatibles con ASIA 13.
Los biopolímeros se recomiendan para rellenar pequeñas áreas como arrugas o cicatrices. Sin embargo, en algunos países de América Latina se utilizan en cantidades mucho mayores para el aumento de glúteos y mamas en establecimientos ilegales, lo cual puede generar complicaciones graves rara vez documentadas en otros continentes 14. Sin embargo, con el aumento del número de procedimientos estéticos en todo el mundo, los casos de ASIA grave pueden volverse más comunes en todas partes, y los casos con compromiso severo y migración de material alógeno serían más probables. Por lo tanto, es esencial el reporte de casos representativos como este.
No hay información adecuada sobre el tratamiento de los casos graves, y siempre se sugiere la eliminación del material alógeno. Sin embargo, este es el primer caso reportado de ASIA con compromiso severo y migración al esófago y al bronquio fuente izquierdo con efectos obstructivos y la imposibilidad de tratamiento quirúrgico.
No existe una guía de tratamiento que indique el proceso a seguir una vez que se considera que un paciente cumple con los criterios de ASIA, ni una guía de tratamiento que pueda aplicarse a pacientes con compromiso grave debido a complicaciones mecánicas producidas por la migración del material alógeno 11,12. Se especula que las vías de migración del material alógeno en este paciente son dos vías principales; la primera puede ser la vía hematógena, que podría deberse a la angiogénesis en el área de inyección del material estimulada por la inflamación crónica. Además, la respuesta inmunológica local y los eventos mecánicos típicos del efecto de masa en los glúteos pueden destruir la integridad de la pared del vaso sanguíneo en el área y hacer que el material alógeno escape al lumen del vaso sanguíneo. Una vez en el torrente sanguíneo, puede migrar a diferentes sitios, como los capilares pulmonares, produciendo microembolias y una reacción inflamatoria local que podría resultar en fibrosis. Todos estos cambios de diseminación hematógena serían similares a los de los émbolos grasos en una fractura de cadera, por ejemplo, o a cómo ocurre la diseminación y embolismo de líquido amniótico en mujeres embarazadas. Por otro lado, se especula que la otra forma significativa de migración a distancia del material alógeno es la migración a través de los vasos linfáticos, que podría ocurrir a través del proceso de presentación antigénica en el que participan células como los macrófagos o las células dendríticas plasmocitoides, que toman parte del material extraño a través de la fagocitosis y lo procesan para presentarlo y activar a los linfocitos para establecer una respuesta celular aumentada y más específica con el fin de controlar o encapsular al invasor, como se hace con la tuberculosis, por ejemplo. Sin embargo, se considera que el estímulo mecánico y la degradación constante del material alógeno hacen que este proceso ocurra una y otra vez, causando que enormes cantidades de células cargadas de material foráneo migren repetidamente a través de los vasos linfáticos, lo que provoca que se acumule progresivamente a lo largo de los años en áreas con alta concentración linfática, como el conducto linfático derecho y, lo que es más importante, el conducto torácico. Esta última teoría explicaría completamente el desarrollo de autoinmunidad sistémica en esta paciente y el compromiso mecánico en el bronquio fuente izquierdo y el área adyacente. Además, la diseminación hematógena podría explicar los hallazgos intersticiales pulmonares en la TC de tórax de la paciente.
Este reporte de caso no solo resalta las complicaciones que pueden estar asociadas con el uso irresponsable de biopolímeros, sino que también plantea una pregunta ética, ya que no existe evidencia sólida ni estudios prospectivos que indiquen que la eliminación del material alógeno sea verdaderamente útil y justifique asumir el riesgo quirúrgico asociado11. Algunas publicaciones informan con éxito tratamientos con diferentes medicamentos inmunomoduladores, como altas dosis de prednisona, hidroxicloroquina, colchicina, ciclosporina y ciclofosfamida. Aunque no existe un tratamiento estándar, hay consenso en la evidencia de que en casos severos se debe administrar tratamiento sistémico 2,4,11.
La medicación administrada en este caso representa una nueva alternativa para la presentación grave de ASIA con compromiso mecánico e imposibilidad de remover el material alógeno, y se propone un tratamiento médico con terapia multifuncional basado en la revisión de la literatura y nuestra propia experiencia que podría ser útil en pacientes con compromiso sistémico severo. Sin embargo, se deben tener en cuenta las posibles complicaciones del tratamiento inmunomodulador a largo plazo, equilibrando el riesgo/beneficio e individualizando cada paciente.
Conclusión
ASIA es una entidad recientemente documentada con pocos criterios específicos. Hay algunas publicaciones que describen las características epidemiológicas de los pacientes susceptibles, y no hay información publicada que reconozca un tratamiento estándar. Se necesitan estudios poblacionales para identificar las mejores opciones de tratamiento. Casos como este pueden crear conciencia entre el personal de salud y los pacientes sobre el uso indiscriminado de materiales alógenos con fines estéticos.
References
1. Shoenfeld Y, Agmon-Levin N. “ASIA” - Autoimmune/inflammatory syndrome induced by adjuvants. J Autoimmun. 2011; 36(1): 4.8, doi: 10.1016/j.jaut.2010.07.003. [ Links ]
2. Vera-Lastra O, Medina G, Cruz-Dominguez MDP, Jara LJ, Shoenfeld Y. Autoimmune/inflammatory syndrome induced by adjuvants (Shoenfeld´s syndrome): Clinical and immunological spectrum. Expert Rev Clin Immunol. 2013; 9(4): 361-73. Doi: 10.1586/eci.13.2. [ Links ]
3. Perricone C, Colafrancesco S, Mazor RD, Soriano A, Agmon-Levin N, Shoenfeld Y. Autoimmune/inflammatory syndrome induced by adjuvants (ASIA) 2013: Unveiling the pathogenic, clinical and diagnostic aspects. J Autoimmun. 2013; 47: 1-16. Doi: 10.1016/j.jaut.2013.10.004. [ Links ]
4. Gutierrez-Gonzalez LA, Párraga deZB, Pérez-Alfonzo R. Psoriatic arthritis post biopolymer injection. Rev Latinoam Psoriasis Artritis Psoriásica. 2012; 6: 41-8. [ Links ]
5. Watad A, Rosenberg V, Tiosano S, Tervaert JWC, Yavne Y, Shoenfeld Y, et al. Silicone breast implants and the risk of autoimmune/rheumatic disorders: A real-world analysis. Int J Epidemiol. 2018; 47(6): 1846-54. Doi: 10.1093/ije/dyy217. [ Links ]
6. Watad A, Bragazzi NL, McGonagle D, Adawi M, Bridgewood C, Damiani G, et al. Autoimmune/inflammatory syndrome induced by adjuvants (ASIA) demonstrates distinct autoimmune and autoinflammatory disease associations according to the adjuvant subtype: Insights from an analysis of 500 cases. Clin Immunol. 2019; 203: 1-8. Doi: 10.1016/j.clim.2019.03.007. [ Links ]
7. Alijotas-Reig J. Human adjuvant-related syndrome or autoimmune/inflammatory syndrome induced by adjuvants. Where have we come from? Where are we going? A proposal for new diagnostic criteria. Lupus. 2015; 24(10): 1012-8. Doi: 10.1177/0961203315579092. [ Links ]
8. Soriano A, Butnaru D, Shoenfeld Y. Long-term inflammatory conditions following silicone exposure: The expanding spectrum of the autoimmune/inflammatory syndrome induced by adjuvants (ASIA). Clin Exp Rheumatol. 2014; 32(2): 151-4. [ Links ]
9. Janowsky E, Kupper L, Hulka B. Meta-analyses of the relation between silicone breast implants and the risk of connective-tissue diseases. N Engl J Med. 2000; 342(11): 781-90. Doi: 10.1056/nejm200003163421105. [ Links ]
10. Brown SL, Pennello G, Berg WA, Soo MS, Middleton MS. Silicone gel breast implant rupture, extracapsular silicone, and health status in a population of women. J Rheumatol. 2001; 28(5): 996-1003. [ Links ]
11. Pavlov-Dolijanovic S, Vujasinovic Stupar N. Women with silicone breast implants and autoimmune inflammatory syndrome induced by adjuvants: description of three patients and a critical review of the literature. Rheumatol Int. 2017; 37(8): 1405-11. Doi: 10.1007/s00296-017-3731-4. [ Links ]
12. Maijers MC, de Blok CJM, Niessen FB, van der Veldt AAM, Ritt MJPF, Winters HAH, et al. Women with silicone breast implants and unexplained systemic symptoms: A descriptive cohort study. Neth J Med. 2014; 71(10): 534-40. [ Links ]
13. González-Rendón MG, Larrazábal A, Suárez Á, Gutiérrez C, Ortiz-Cáceres W, de Waard JH, Pérez-Alfonzo Rl. Síndrome autoinmune/autoinflamatorio inducido por adyuvantes (ASIA) en pacientes dermatológicas a los cinco años posteriores a la colocación de material de relleno con fines cosméticos. Med Cutan Iber Lat Am. 2019; 47(1): 34-38. [ Links ]
14. Ricaurte AI, Castaño DA, Castro JA, De Paz DA, Echeverry DA. Alogenosis Iatrogénica vs Alogenosis Secundaria en Cali. A propósito de 12 casos. Colombia Forense. 2016; 3(2): 63-74. Doi: 10.16925/cf.v3i2.1778. [ Links ]
Recibido: 16 de Noviembre de 2020; Revisado: 18 de Enero de 2022; Aprobado: 27 de Diciembre de 2022











 text in
text in 



