Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombia Médica
On-line version ISSN 1657-9534
Colomb. Med. vol.54 no.4 Cali Oct./Dec. 2023 Epub Dec 29, 2023
https://doi.org/10.25100/cm.v54i4.5850
Articulo original
Terapia de resincronización cardiaca en insuficiencia cardiaca aguda y bloqueo de rama izquierda en un registro real
1 Hospital d'Olot i Comarcal de la Garrotxa, Emergency Department, Girona, Catalonia, Spain.
2Tissue Repair and Regeneration Laboratory (TR2Lab), Institut de Recerca i Innovació en Ciències de la Vida i de la Salut a la Catalunya Central (IrisCC), Girona, Catalonia, Spain
3Hospital d'Olot i Comarcal de La Garrotxa, Internal Medicine Department, Girona, Catalonia, Spain
4 Hospital General de Alicante, Emergency Department, Short Stay Unit and Hospitalization at Home Unit, Alicante, Spain
5 Instituto de Investigación Sanitaria y Biomédica de Alicante (ISABIAL), Alicante, Spain
6 Universidad Miguel Hernández, Alicante, Spain
7 University Hospital of Basel, Cardiology Department, Basel, Switzerland
8 Cardiovascular Research Institute Basel, Basel, Switzerland
9 The GREAT network, Rome, Italy
10 University of Barcelona, Emergency Department, Hospital Clínic, IDIBAPS, Barcelona, Catalonia, Spain
11 Hospital Doctor Peset, Emergency Department, Valencia, Spain
12 Hospital Universitario Central de Asturias, Emergency Department, Oviedo, Spain
13Hospital Universitari de Bellvitge, Emergency Department, Barcelona, Catalonia, Spain
14 l’Hospitalet de Llobregat, Barcelona, Catalonia, Spain
15Hospital Universitario de Burgos, Emergency Department, Burgos, Spain
16Hospital Virgen de Valme, Emergency Department, Sevilla, Spain
17Hospital Politécnico La Fe, Emergency Department, Valencia, Spain
18Hospital del Mar, Emergency Department, Barcelona, Catalonia, Spain
19Hospital Universitario Reina Sofía, Emergency Department, Murcia, Spain
Objetivos:
Determinar la prevalencia, características, momento de implantación y pronóstico de los pacientes con bloqueo de rama izquierda del haz de His (BRIHH) e insuficiencia cardiaca aguda (ICA) tratados con terapia de resincronización cardiaca (TRC) en un registro real.
Métodos:
Se analizaron las características de los pacientes con ICA y BRIHH en el momento de su inclusión en la cohorte EAHFE (Epidemiology Acute Heart Failure Emergency) para determinar la indicación de TRC, el momento de implantación y su impacto en la mortalidad por cualquier causa a 10 años.
Resultados:
729 pacientes con una mediana de edad de 82 años con una elevada carga de comorbilidades y dependencia funcional. La mediana de la fracción de eyección del ventrículo izquierdo (FEVI) fue del 40%. 46 pacientes (6%) fueron tratados con TRC en algún momento del seguimiento, con una mediana de tiempo de retraso para la implantación de la TRC de 960 dias (IQR=1,147 días) y al menos 108 pacientes no tratados cumplían criterios para TRC. Los pacientes que recibieron TRC eran más jóvenes, tenían comorbilidades diferentes, menor dependencia funcional (índice de Barthel más alto) y valores de FEVI más bajos. La mediana de seguimiento fue de 5.7 años (IC del 95%: 5.6-5.8) y la TRC no se asoció a cambios en la mortalidad a 10 años (HR ajustado: 1.33; IC del 95%: 0.72-2.48; p-valor 0.4). Cuando se comparó con pacientes no tratados que cumplían criterios para TRC, se observaron resultados muy similares (HR ajustado 1.34; IC del 95%: 0.67-2.68).
Conclusiones:
La implantación de la TRC se retrasó y se infrautilizó en pacientes con ICA y BRIHH. En estas circunstancias, la TRC no se asocia a una reducción de la mortalidad por cualquier causa a largo plazo.
Palabras clave: insuficiencia cardiaca; bloqueo de rama; terapia de resincronización cardiaca; mortalidad
Objectives:
To determine the prevalence, characteristics, timing of implementation and prognosis of patients with left bundle branch block (LBBB) and acute heart failure (AHF) treated with cardiac resynchronization therapy (CRT) in a real-life registry.
Methods:
We analysed the characteristics of patients with AHF and LBBB at the time of inclusion in the EAHFE (Epidemiology Acute Heart Failure Emergency) cohort to determine the indication for CRT, the timing of implementation and its impact on 10-year all-cause mortality.
Results:
729 patients with a median age of 82 years and there was a high burden of comorbidities and functional dependence. The median left-ventricle ejection fraction (LVEF) was 40%. Forty-six (6%) patients were treated with CRT at some point during follow-up, with a median time of delay for CRT implementation of 960 (IQR=1,147 days) and at least 108 more untreated patients fulfilled criteria for CRT. Patients receiving CRT were younger, had different comorbidities, less functional dependence (higher Barthel index) and lower LVEF values. The median follow-up was 5.7 years (95% CI: 5.6-5.8) and CRT was not associated with changes in 10-year mortality (adjusted HR 1.33, 95% CI: 0.72-2.48; p-value 0.4). When compared with untreated patients fulfilling criteria for CRT, very similar results were observed (adjusted HR 1.34, 95% CI: 0.67-2.68).
Conclusions:
CRT implementation was delayed and underused in patients with AHF and LBBB. Under these circumstances, CRT is not associated with a reduction in all-cause mortality in the long term.
Keywords: heart failure; bundle-branch block; cardiac resynchronization therapy; mortality
Contribución del estudio
| 1) Por qué se realizó este estudio? |
| Evaluar la implantación de la terapia de resincronización cardiaca en una serie de pacientes con insuficiencia cardiaca aguda y bloqueo de rama izquierda del haz de His. |
| 2) Cuales fueron los resultados mas relevantes del estudio? |
| La implantación de la terapia de resincronización cardiaca se retrasó y se infrautilizó en los pacientes con insuficiencia cardiaca aguda y bloqueo de rama izquierda del haz de His. En estas circunstancias, la terapia de resincronización cardiaca no se asoció a una reducción de la mortalidad por cualquier causa a largo plazo.. |
| 3) Que aportan estos resultados? |
| Estos resultados nos hacen reflexionar sobre el diagnóstico tardío de la insuficiencia cardiaca refractaria, y la infrautilización de la implantación de la terapia de resincronización cardiaca, muy recomendada en las guías. |
Introducción
La insuficiencia cardíaca (IC) es un síndrome clínico prevalente con altas tasas de morbilidad y mortalidad. El pronóstico de los pacientes con IC ha mejorado considerablemente en las últimas décadas, pero sigue siendo malo y la mejora en el pronóstico se ha limitado a aquellos con fracción de eyección reducida (ICFEr), aproximadamente el 50% de todos los pacientes con IC 1. La terapia de resincronización cardíaca (TRC) se aprobó en 2005 para tratar pacientes con insuficiencia cardíaca refractaria. En individuos adecuadamente seleccionados, la TRC mejora la función cardíaca, mejora la calidad de vida y reduce la morbilidad y la mortalidad 1,2. No obstante, evaluar la respuesta a la TRC es un desafío y diferentes estudios han demostrado que los pacientes con morfología de bloqueo de rama izquierda (BRI) tienen más probabilidades de responder favorablemente a la TRC. Las guías actuales recomiendan el uso de TRC en pacientes sintomáticos con IC en ritmo sinusal con una duración de QRS >150 ms y morfología de BRI y con una fracción de eyección del ventrículo izquierdo (FEVI) <35% a pesar de tratamiento médico óptimo para mejorar los síntomas y reducir la morbilidad. y mortalidad 2,3. La cuestión del momento de la TRC es controvertida y, como la eficacia del tratamiento médico puede ser limitada en pacientes con BRI, se ha sugerido una implantación más temprana de la TRC 3. Sin embargo, a pesar de ser una de las terapias más efectivas para tratar los síntomas de la ICFEr, hasta dos tercios de los pacientes elegibles no son remitidos a TRC y las causas de ello no se han investigado exhaustivamente. Además, existe una considerable heterogeneidad en el uso de TRC entre los diferentes países europeos, siendo Italia la que tiene las tasas de implantación más altas (seguida de Dinamarca y la República Checa) y Ucrania la más baja 4,5.
El objetivo del presente estudio fue determinar la indicación y el momento de implantación de la TRC y su impacto en el pronóstico en los pacientes con IC y BRI a partir de un registro de la vida real: la cohorte española EAHFE (Epidemiology Acute Heart Failure Emergency).
Materiales y Métodos
Población de estudio y selección de pacientes
El presente estudio es un análisis secundario de los pacientes incluidos en el registro EAHFE, cuyo diseño fue explicado previamente 6. Brevemente, la cohorte EAHFE es un registro multicéntrico prospectivo que incluye pacientes con IC aguda (ICA) atendidos en 45 Servicios de Urgencias (SU) españoles independientemente de su disposición final tras la primera presentación médica (ingreso en planta general, ingreso en unidad de cuidados intensivos o dado de alta a casa). Las visitas de seguimiento son obligatorias a los 90 y 365 días después del alta hospitalaria; posteriormente, se revisa anualmente el estado vital de los pacientes. El diseño de cohorte de la EAHFE fue aprobado por los Comités de Ética de todos los hospitales participantes. El estudio se realizó siguiendo los estándares éticos de la Declaración de Helsinki y se obtuvo el consentimiento informado por escrito de todos los pacientes participantes. Para el presente análisis secundario, se incluyeron pacientes del registro EAHFE con BRI, cuya información sobre el electrocardiograma (ECG) basal y estado vital estaba disponible. Se excluyeron de este análisis los pacientes con marcapasos o TRC en el momento de su inclusión en el registro.
Variables clasificatorias
Los pacientes con BRI fueron clasificados según fueran tratados o no con TRC. Esto incluyó a pacientes que recibieron TRC después de la compensación del episodio índice de ICA y pacientes a los que se les implantó TRC en algún momento durante su seguimiento. Aquellos que no fueron tratados con TRC en ningún momento durante el seguimiento se clasificaron según tuvieran o no criterios para TRC. Los criterios para que los pacientes con BRI fueran tratados con implantación de TRC eran tener una FEVI <35% para TRC y recibir un tratamiento médico óptimo.
Variables independientes
Se incluyeron edad y sexo, variables correspondientes al estado basal del paciente (índice de Barthel, New York Heart Association [NYHA] y FEVI), 15 comorbilidades (tabaquismo, hipertensión, dislipidemia, diabetes mellitus, enfermedad coronaria, valvulopatía, enfermedad arterial periférica). , enfermedad cerebrovascular, fibrilación auricular, insuficiencia cardíaca crónica, enfermedad renal crónica, enfermedad pulmonar obstructiva crónica, demencia, neoplasia activa y cirrosis hepática) y tratamiento basal.
Objetivos
El objetivo primario fue la mortalidad por todas las causas a los diez años de seguimiento. Se consideró el tiempo desde el día del alta hospitalaria posterior al tratamiento y estabilización de la descompensación. Los pacientes que fallecieron durante el episodio índice de ICA antes del alta (mortalidad hospitalaria) no se incluyeron en el análisis. La adjudicación de resultados fue realizada a nivel local por los investigadores principales de cada centro. Para ello, los investigadores locales se pusieron en contacto por teléfono con los pacientes o sus familiares, revisaron los informes médicos de los pacientes o consultaron el registro sanitario nacional (ya que el sistema sanitario público cubre a más del 99% de la población española) para comprobar el fallecimiento del paciente.
Análisis estadístico
Las variables cuantitativas se expresan como mediana y rango intercuartílico (RIC). Las variables cualitativas se expresan como número de pacientes y porcentajes. Se utilizaron las pruebas de chi-cuadrado o exacta de Fisher (según fuera necesario) para comparar la distribución de variables cualitativas en pacientes con y sin TRC. Para comparar variables cuantitativas se utilizó la prueba no paramétrica U de Mann-Whitney. La mortalidad por todas las causas a diez años para toda la cohorte se representó mediante el método de Kaplan-Meier. Se utilizó el método inverso de Kaplan-Meier para calcular la mediana del tiempo de seguimiento en la cohorte. Se utilizó un modelo multivariable de riesgos proporcionales de Cox para evaluar la asociación de la TRC con la muerte por todas las causas a 10 años. Para tener en cuenta el sesgo de indicación, ajustamos por motivos conocidos para la selección del tratamiento (es decir, motivos conocidos para indicar TRC), lo que resultó en un condicionamiento para: edad, sexo, tratamiento médico óptimo, ritmo cardíaco inicial, FEVI e índice de Barthel. Para evitar el sesgo de inmortalidad (es decir, los pacientes en el grupo de TRC no pueden haber fallecido hasta recibir la TRC. Por lo tanto, existe un intervalo durante el cual el evento de resultado no puede haber ocurrido), modelamos la TRC como una covariable dependiente del tiempo mediante la construcción de un conjunto dependiente del tiempo con la función tmerge del survival package del software R 7. Además de informar del Hazard ratio (HR) para los pacientes que recibieron TRC, se construyó un gráfico de efectos condicionales para representar la probabilidad de supervivencia de un sujeto "promedio" según recibiera o no TRC 8. Como análisis de sensibilidad, calculamos la HR ajustada para los pacientes que recibieron TRC utilizando como comparativa solo aquellos pacientes que no recibieron TRC pero si tenían criterios para la implementación de TRC.
Se aceptó significación estadística con un valor de p <0.05 o si el intervalo de confianza (IC) del 95% excluía el valor 1. Todos los análisis estadísticos se realizaron con el Statistical Package for Social Sciences versión 23.0 (IBM, Armonk, NY, EE. UU.) y la Fundación R para Computación Estadística (versión 4.1.2).
Resultados
El presente estudio incluyó a 729 pacientes con ICA y BRI no tratados previamente con marcapasos o TRC (Figura 1). Las características basales se presentan con detalle en la Tabla 1. Brevemente, los pacientes con ICA y BRI del registro EAHFE tenían una edad avanzada (mediana de edad 82 años), una alta presencia de comorbilidades (las más frecuentes eran hipertensión (84%), IC crónica (66%), dislipidemia (46%), diabetes mellitus (45%) y fibrilación auricular (43%) y algún grado de dependencia funcional (medida con el índice de Barthel). La mediana [RIQ] fue de 40 (25) y la categoría predominante según la FEVI fue la ICFER, que comprendió el 46% de los pacientes.
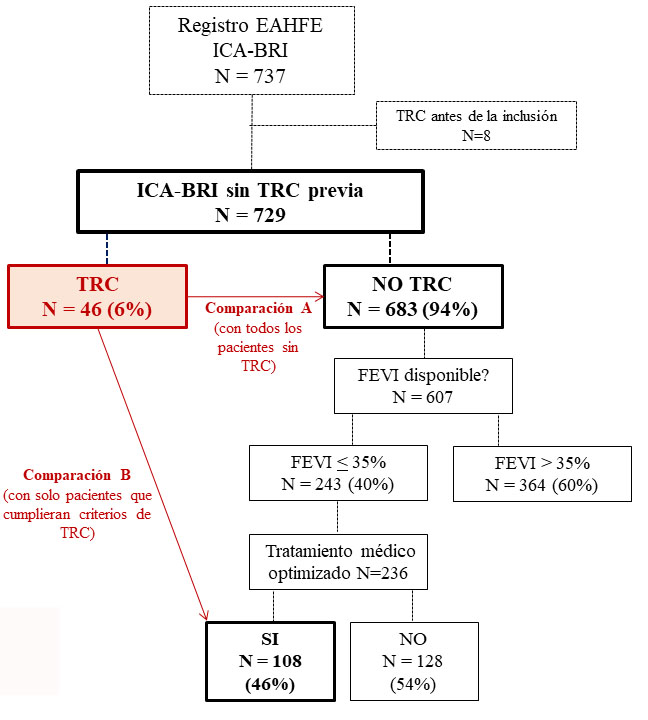
Figura 1 Diagrama de flujo para la inclusión y el análisis de los pacientes. *El tratamiento médico óptimo incluye inhibidores del sistema renina-angiotensina-aldosterona y betabloqueantes. Abreviaturas: ICA: insuficiencia cardiaca aguda; TRC: terapia de resincronización cardiaca; BRIHH: bloqueo de rama izquierda; FEVI: fracción de eyección del ventrículo izquierdo.
Tabla 1 Características basales y diferencias según terapia de resincronización cardíaca.
| [ | ICA con BRI N= 729 | Faltan N (%) | TRC N= 46 | No TRC (todos los pacientes) N= 683 | P* | No CRT (solo pacientes que cumplían criterios de TRC) N=108 | P* |
|---|---|---|---|---|---|---|---|
| Datos demográficos | |||||||
| Edad (años) - mediana [RIC] | 82 [13] | 0 | 66.9 [16.1] | 82.8 [11.9] | *** | 81.4 [11.9] | *** |
| Sexo femenino | 381 (52.3%) | 0 | 20 (43.5%) | 361 (52.9) | - | 46 (42.6%) | - |
| BMI (kg/m2) - mediana [RIC] | 27.6 [5.8] | 309 (42%) | 29.2 [20.3] | 27.4 [6.0] | - | 27.7 [5.9] | - |
| Comorbilidades | |||||||
| Fumador activo | 47 (6.4%) | 169 (23.2%) | 5 (13.5%) | 42 (8.0%) | * | 9 (10.2%) | - |
| Hipertensión | 612 (84.0%) | 1 (0.1%) | 33 (71.7%) | 579 (84.9%) | * | 92 (85.2%) | - |
| Dislipemia | 333 (45.7%) | 2 (0.3%) | 28 (60.9%) | 305 (44.8%) | * | 50 (46.3%) | - |
| Diabetes mellitus | 325 (44.6%) | 1 (0.1%) | 23 (50.0%) | 302 (44.3%) | - | 62 (57.4%) | - |
| Coronariopatía | 233 (32.0%) | 1 (0.1%) | 10 (21.7%) | 223 (32.7%) | - | 58 (53.7%) | *** |
| Valvulopatía | 211 (28.9%) | 1 (0.1%) | 14 (30.4%) | 197 (28.9%) | - | 41 (38.0%) | 0.372 |
| Enfermedad arterial periférica | 68 (9.3%) | 1 (0.1%) | 4 (8.7%) | 64 (9.4%) | - | 8 (7.4%) | 0.785 |
| Enfermedad cerebrovascular | 89 (12.2%) | 1 (0.1%) | 4 (8.7%) | 85 (12.5%) | - | 11 (10.2%) | 0.775 |
| Fibrilación auricular | 312 (42.8%) | 1 (0.1%) | 10 (21.7%) | 302 (44.3%) | ** | 45 (41.7%) | * |
| Insuficiencia cardiaca crónica | 478 (65.6%) | 24 (3.3%) | 27 (60.0%) | 451 (68.3%) | - | 90 (83.3%) | ** |
| Insuficiencia renal crónica | 198 (27.2%) | 1 (0.1%) | 12 (26.1%) | 186 (27.3%) | - | 38 (35.2%) | 0.270 |
| EPOC | 152 (20.9%) | 2 (0.3%) | 9 (19.6%) | 143 (21.0%) | - | 18 (16.8%) | - |
| Demencia | 69 (9.3%) | 54 (7.4%) | 0 (0%) | 68 (10.8%) | * | 9 (9.8%) | * |
| Cáncer active | 88 (12.1%) | 54 (7.4%) | 8 (18.6%) | 80 (12.7%) | - | 14 (15.2%) | - |
| Cirrosis | 6 (0.8%) | 54 (7.4%) | 0 (0%) | 6 (0.9%) | - | 0 (0%) | - |
| Estatus basal | |||||||
| Clase NYHA | 37 (5.1%) | ||||||
| I | 170 (23.3%) | 7 (16.7%) | 163 (25.1%) | - | 17 (16.8%) | ||
| II | 373 (51.2%) | 31 (73.8%) | 342 (52.6%) | 57 (56.4%) | - | ||
| III | 147 (20.2%) | 4 (9.5%) | 143 (22.0%) | 26 (25.7%) | |||
| IV | 2 (0.3%) | 0 (0%) | 2 (0.3%) | 1 (1.0%) | |||
| LVEF (%) - mediana [RIC] | 40 [25] | 76 (10.4%) | 35 [24] | 40 [25] | * | 30 [10] | *** |
| Preservada LVEF (≥50%) | 252 (34.6%) | 12 (21.6%) | 240 (39.5%) | - | 0 (0%) | *** | |
| Levemente Reducida LVEF (41-49%) | 64 (8.8%) | 3 (6.5%) | 61 (10.0%) | 0 (0%) | |||
| Reducida LVEF (≤40%) | 337 (46.2%) | 31 (67.4%) | 306 (50.4%) | 108 (100%) | |||
| Barthel índice (puntos) - mediana [RIC] | 90 [30] | 68 (9.3%) | 100 [0] | 90 [30] | *** | 95 [23] | *** |
| Tratamiento crónico domiciliario | |||||||
| Diuréticos de asa | 477 (65.4%) | 11 (1.5%) | 19 (41.3%) | 458 (68.2%) | *** | 83 (76.9%) | *** |
| RAASI | 463 (63.5%) | 11 (1.5%) | 35 (71.6%) | 428 (63.7%) | - | 108 (100%) | *** |
| BB | 369 (50.6%) | 10 (1.4%) | 23 (50.0%) | 346 (51.4%) | - | 108 (100%) | *** |
| ARM | 139 (19.1%) | 10 (1.4%) | 11 (23.9%) | 128 (19.0%) | - | 26 (24.1%) | - |
| Tratamiento óptimo 1 (RAASI +BB) | 256 (35.1%) | 11 (1.5%) | 21 (45.7%) | 235 (35.0%) | - | 108 (100%) | *** |
| Tratamiento óptimo 2 (RAASI+BB+MRA) | 56 (7.7%) | 11 (1.5%) | 8 (17.4%) | 48 (7.1%) | * | 26 (24.1%) | - |
ICA: insuficiencia cardiaca aguda; IMC: índice de masa corporal; EPOC: enfermedad pulmonar obstructiva crónica; TRC: terapia de resincronización cardíaca; RIC: rango intercuartílico; BRI: bloqueo de rama izquierda; FEVI: fracción de eyección del ventrículo izquierdo; ARM: antagonistas de los receptores de mineralocorticoides; NYHA: Asociación del Corazón de Nueva York; RAASI: inhibidores del sistema renina-angiotensina-aldosterona (incluye inhibidores de la enzima convertidora de angiotensina, antagonistas de los receptores de angiotensina o inhibidores de los receptores de angiotensina-neprilisina); BB: betabloqueantes
- p>0.05; * p<0.05; ** p<0.05;*** p<0.001
Cuarenta y seis pacientes (6.3%) fueron tratados con TRC en algún momento del seguimiento, con una mediana [RIC] de tiempo hasta la implantación de TRC de 960 (1,147) días. Al comparar a los pacientes tratados y no tratados (Tabla 1), los pacientes tratados con TRC eran más jóvenes, tenían diferentes comorbilidades (menos hipertensión, fibrilación auricular y demencia y más dislipemia y tabaquismo), menos dependencia funcional (mayores valores del índice de Barthel) y menores valores de FEVI. La única diferencia encontrada según el tratamiento fue que los pacientes del grupo TRC fueron tratados con menor frecuencia con diuréticos de asa.
Además de los 46 pacientes tratados con TRC, se detectaron 108 pacientes con FEVI menor o igual al 35%, con tratamiento óptimo (cumpliendo criterios para TRC según las pautas) en su evaluación inicial para su inclusión en la cohorte EAHFE, que no recibieron TRC en ningún momento durante el seguimiento. Esto significa que el dispositivo finalmente se implantó en sólo 3 de cada 10 pacientes (46 de 154) que cumplían los criterios de TRC. Las características asociadas a no recibir TRC en este subgrupo fueron similares a las observadas en todo el grupo de pacientes con BRI no tratados con TRC (Tabla 1).
Desenlace
La mediana de seguimiento fue de 5.7 años (IC 95%: 5.6-5.8). Las curvas de supervivencia de Kaplan-Meier para la mortalidad por todas las causas a 10 años estratificadas según la TRC se representan en la Figura 2A y las curvas de probabilidad de supervivencia para un paciente promedio de nuestra cohorte en el grupo con TRC o sin TRC se representan en la Figura 2B.
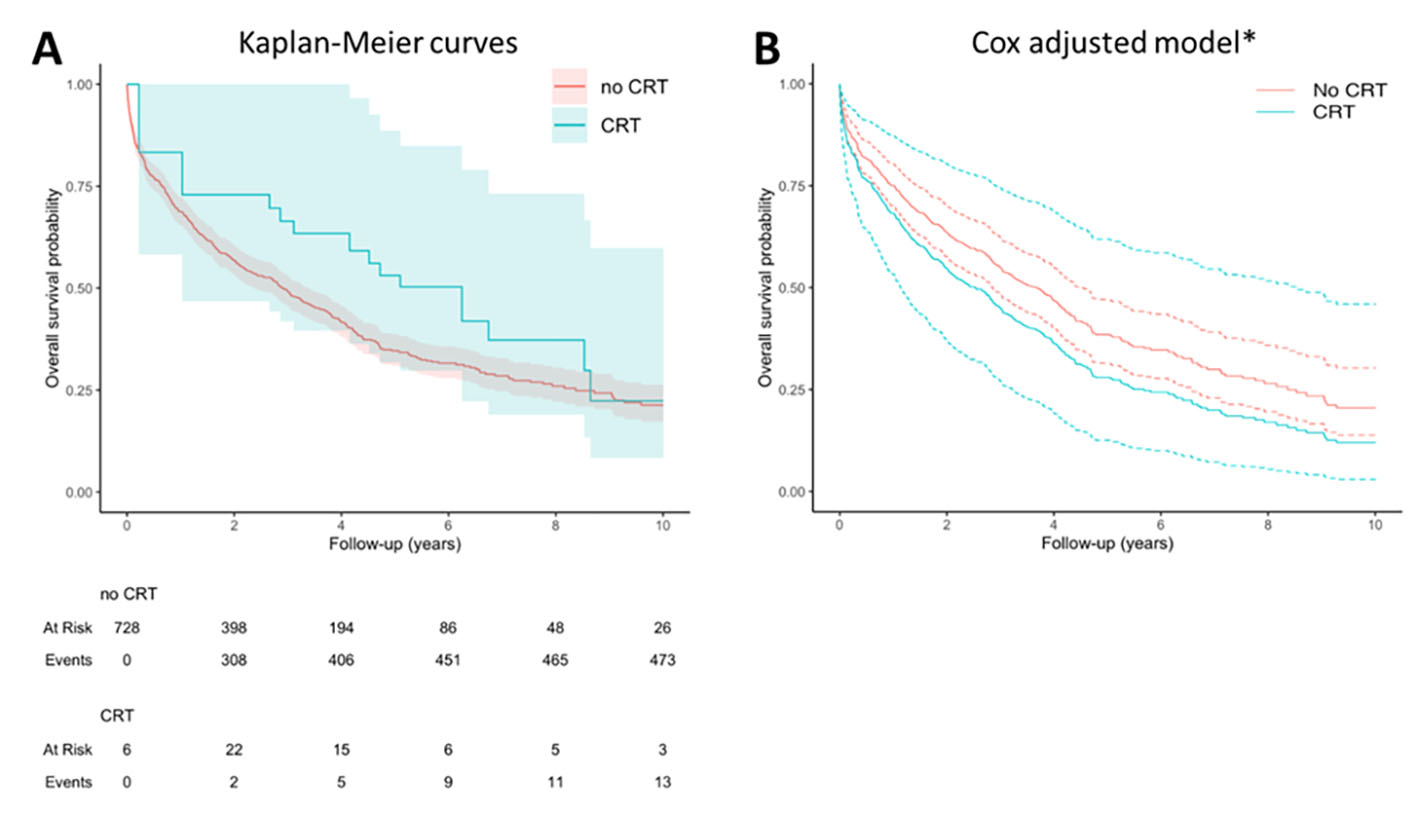
Figura 2 Análisis de supervivencia. El panel A muestra las curvas de Kaplan-Meier que comparan la supervivencia entre los 2 grupos: TRC (46 pacientes) vs no TRC (683 pacientes). La TRC se modela como una covariable dependiente del tiempo para evitar el sesgo de inmortalidad debido al hecho de que los pacientes en el grupo de TRC no pueden haber fallecido hasta recibir la TRC. Por tanto, hay un intervalo durante el cual el evento resultante no puede haber ocurrido. Por este motivo, a pesar de incluir 46 pacientes en el grupo de TRC, el número de pacientes en riesgo en este grupo en el momento cero es 6 en lugar de 46, y posteriormente el número de pacientes en riesgo aumenta (al ser tratados con TRC) o disminuye (a medida que fallecen o son censurados) durante el seguimiento. El panel B muestra la probabilidad de supervivencia obtenida en el modelo de Cox ajustado condicionado a un sujeto "promedio" según recibe o no TRC. *Condicionado a mediana edad (82), sexo femenino, sin fibrilación auricular, sin tratamiento médico óptimo, fracción de eyección del ventrículo izquierdo del 40% e índice de Barthel de 90 puntos. Abreviaturas: TRC: terapia de resincronización cardíaca
Cuando se comparó a los pacientes según si recibieron o no TRC, se halló una falta de evidencia que respalde la TRC como terapia beneficiosa para reducir la mortalidad a los 10 años (HR ajustado 1.33, IC del 95%: 0.72-2.48; valor de p= 0.4). El análisis de sensibilidad utilizando únicamente pacientes no tratados que cumplían los criterios de TRC mostró resultados similares (HR ajustado 1.34, IC del 95%: 0.67-2.68).
Discusión
En éste amplio registro de pacientes con ICA y BRI, encontramos que después de un seguimiento a largo plazo, la TRC solo se realizó en 46 (6%) pacientes, y la TRC se implantó después de una mediana de tiempo de casi tres años. Los 683 pacientes restantes no fueron tratados con TRC y, de aquellos de los que se disponía de información sobre la FEVI, 108 habrían sido candidatos potenciales para recibir TRC según las recomendaciones de las guías (FEVI <35% y tratamiento médico óptimo). Por tanto, al menos 154 de 729 pacientes (21%) eran candidatos para recibir TRC en el momento de su inclusión en la cohorte EAHFE, aunque sólo 3 de cada 10 fueron finalmente tratados a pesar del largo seguimiento realizado en el presente estudio. Otros estudios han reportado porcentajes de pacientes elegibles que oscilan entre el 5 y el 10% 9, pero estos estudios incluían pacientes no seleccionados hospitalizados por IC y no solo pacientes con BRI.
La edad avanzada, las comorbilidades y el estado funcional podrían explicar, en parte, la tardía y escasa implementación de la TRC. Otros factores que pueden haber contribuido a este retraso y a la baja implementación de la TRC son la FEVI conservada o ligeramente reducida (43%), pacientes levemente sintomáticos (clase funcional II de la NYHA en el 51% de los pacientes) en el momento de la inclusión, un porcentaje bajo de tratamiento médico óptimo para la ICFEr y/o la presencia de fibrilación auricular al inicio del estudio (43%).
La presencia de BRI en el contexto de IC constituye un marcador de enfermedad cardíaca más evolucionada y se asocia a un mayor riesgo de mortalidad por todas las causas 3,10. Por tanto, es importante, especialmente cuando la FEVI está reducida, valorar cuidadosamente la indicación de la TRC para mejorar el pronóstico. En vista de los resultados y, en consistencia con otros estudios, parece que la TRC se implanta con retraso, está infrautilizada 4,5,9 y hay margen de mejora para aumentar su uso, ya que los ensayos clínicos han demostrado que la TRC se asocia con una mejora en los síntomas del paciente, la capacidad funcional y la supervivencia.
En el presente estudio, el tratamiento con TRC no se asoció a una mejora del pronóstico a largo plazo a pesar de ajustar el análisis por posibles factores de confusión, así como por los sesgos de selección y de inmortalidad. El alto riesgo de mortalidad a los 10 años de seguimiento en pacientes de edad avanzada con comorbilidades después de un episodio de ICA (la supervivencia fue inferior al 25%) junto con el retraso en la implantación de la TRC probablemente superen los beneficios de implantar TRC en esta población. Además, es importante señalar que los estudios de TRC se realizaron en su mayoría hace 20 años y, por tanto, antes del uso generalizado de las terapias actuales para la IC, y que la terapia médica puede haber mejorado sustancialmente, de tal forma que, esta costosa intervención invasiva quizás ya no proporciona una menor mortalidad, aunque, todavía puede mejorar la calidad de vida.
Se deben considerar algunas limitaciones en este estudio. Primero, aunque se tuvieron en cuenta los factores de confusión por sesgo de indicación al ajustar por razones conocidas para la indicación del tratamiento con TRC (p. ej., ritmo sinusal, FEVI y tratamiento médico óptimo), no pudimos ajustar por todas las razones conocidas (p. ej., duración del QRS) ya que no estaba registrado en nuestro conjunto de datos. Como resultado, las comparaciones de riesgos para un resultado entre sujetos expuestos (CRT) y no expuestos (sin CRT) estarían sesgadas hacia un mayor riesgo entre los expuestos (CRT), lo que explica (en parte) por qué observamos una falta de evidencia de beneficios. en la mortalidad a 10 años para la TRC. En segundo lugar, la clasificación de los pacientes se basó en los valores de FEVI en el momento de la inclusión, que faltaban en el 10% de los casos. Además, la FEVI es un valor dinámico que puede cambiar a lo largo de la evolución e historia natural de la IC (mejorando en unos casos y empeorando en otros) y algunos pacientes pueden reclasificarse según los nuevos valores de FEVI. En el presente estudio no disponíamos de esta información que podría haber modificado los criterios para implantar la TRC.
References
1. McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, et al. ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Europ Heart J. 2021; 42(36): 3599-3726. doi: 10.1093/eurheartj/ehab368 [ Links ]
2. Cleland JGF, Bristow MR, Freemantle N, Olshansky B, Gras D, Saxon L,et al. The effect of cardiac resynchronization without a defibrillator on morbidity and mortality: an individual patient data meta-analysis of COMPANION and CARE-HF. Eur J Heart Fail. 2022; 24(6): 1080-1090. doi: 10.1002/ejhf.2524 [ Links ]
3. Glikson M, Nielsen JC, Kronborg MB, Michowitz Y, Auricchio A, Barbash IM, et al. 2021 ESC Guidelines on cardiac pacing and cardiac resynchronization therapy. Europace. 2022; 24(1): 71-164. doi: 10.1093/europace/euab232 [ Links ]
4. Raatikainen MJ, Arnar DO, Zeppenfeld K, Merino JL, Levya F, Hindriks G, et al. Statistics on the use of cardiac electronic devices and electrophysiological procedures in the European Society of Cardiology countries: 2014 report from the European Heart Rhythm Association. Europace. 2015; 17 Suppl 1: i1-75. doi: 10.1093/europace/euu300. [ Links ]
5. Mullens W, Auricchio A, Martens P, Witte K, Cowie MR, Delgado V, et al. Optimized implementation of cardiac resynchronization therapy: a call for action for referral and optimization of care: A joint position statement from the Heart Failure Association (HFA), European Heart Rhythm Association (EHRA), and European Association of Cardiovascular Imaging (EACVI) of the European Society of Cardiology. Eur J Heart Fail. 2020; 22(12): 2349-2369. doi: 10.1002/ejhf.2046 [ Links ]
6. Llorens P, Javaloyes P, Martín-Sánchez FJ, Jacob J, Herrero-Puente P, Gil V, et al. Time trends in characteristics, clinical course, and outcomes of 13,791 patients with acute heart failure. Clin Res Cardiol. 2018; 107(10): 897-913. doi: 10.1007/s00392-018-1261-z [ Links ]
7. Lévesque LE, Hanley JA, Kezouh A, Suissa S. Problem of immortal time bias in cohort studies: example using statins for preventing progression of diabetes. BMJ. 2010; 340: b5087. doi: 10.1136/bmj.b5087 [ Links ]
8. Bradburn MJ, Clark TG, Love SB, Altman DG. Survival analysis part II: multivariate data analysis--an introduction to concepts and methods. Br J Cancer. 2003;. 89(3): 431-436. doi: 10.1038/sj.bjc.6601119 [ Links ]
9. Osmanska J, Hawkins NM, Toma M, Ignaszewski A, Virani SA. Eligibility for cardiac resynchronization therapy in patients hospitalized with heart failure. ESC Heart Fail. 2018; 5(4): 668-674. doi: 10.1002/ehf2.12297 [ Links ]
10. Aguiló O, Castells X, Miró Ò. Mueller C, Chioncel O, Trullàs JC. The prognostic significance of bundle branch block in acute heart failure: a systematic review and meta-analysis. Clin Res Cardiol. 2023; 112: 1020-1043. doi: 10.1007/s00392-022-02105-z [ Links ]
Recibido: 13 de Octubre de 2023; Revisado: 22 de Noviembre de 2023; Aprobado: 29 de Diciembre de 2023











 text in
text in 



