1. INTRODUCCIÓN
Los pesticidas pueden ser considerados los milagros de la modernidad. Estos clústeres de átomos altamente estructurados y relativamente pequeños son unos de los principales agentes que han permitido disminuir la morbilidad y mortalidad por las infecciones transmitidas por diferentes plagas.
Muchas de las “moléculas milagro” pueden salvar vidas humanas, de manera indirecta, al ser usadas para el control de los vectores de enfermedades de importancia médica y veterinaria, al tiempo que se obtienen ganancias, por su venta, de billones de dólares por año; el desarrollo de cada uno de ellos es arduo y costoso, con enormes inversiones en su desarrollo, pero también con grandes beneficios.
Los mosquitos son conocidos como vectores de algunas enfermedades que son causadas por agentes patógenos. El Aedes aegypti es distinguido por transmitir Dengue, Zika y Chikungunya1; la trasmisión de la malaria se da por el Anopheles stephensi y la filariasis por Culex spp2. Actualmente existen más de 120 millones de personas que padecen filariasis, y más de 1400 millones en 73 países se encuentran en riesgo de padecer esta enfermedad.
Una forma de prevenir la infestación por mosquitos adultos es a través del uso de larvicidas organofosforados (temefos)3 o de inhibidores del crecimiento (piriproxifen)4. El uso continuo de los insecticidas sintéticos ha ocasionado el desarrollo de resistencia en los mosquitos5. Se plantea que los aceites esenciales son excelentes fuentes de compuestos bioactivos que pueden actuar como larvicidas, reguladores del crecimiento, inhibidores de la oviposición y repelentes, además de ser compuestos de fácil degradación y más seguros para los organismos no-objetivos como el ser humano6.
Por el interés de encontrar nuevas alternativas en el estudio de nuevas para el control de los mosquitos en su estado larval, en esta investigación se evaluaron aceites esenciales y extractos de plantas aromáticas y medicinales como posibles agentes larvicidas en Culex quinquefasciatus.
2. MATERIALES Y MÉTODOS
2.1 Reactivos
Los reactivos utilizados fueron: hexano, etanol, dimetilsulfóxido (DMSO), agua, (J.T Baker, grado analítico), hidrógeno fosfato de sodio, hidrógeno fosfato de potasio, Tween 20, yoduro de acetiltiocolina, ácido ditiobisnitrobenzoico, capsaicina, dihidrocapsaicina, acetilcolinesterasa de Electrophorus electricus, cloruro de sodio, cloruro de potasio, cloruro de calcio, sulfato de magnesio, temefos, y malation (Sigma-Aldrich).
2.2 Material vegetal
El material vegetal se cultivó en la finca El Limonal en el municipio de Piedecuesta (Santander, Colombia), con coordenadas geográficas: latitud 7°0.477’N, longitud 73°3.205’O y altitud de 1020 msnm. La identificación taxonómica fue realizada en el Herbario Nacional del Instituto de Ciencias Naturales de la Universidad Nacional de Colombia:
Mentha piperita L. de la familia Lamiaceae No. COL 574691;
Ocimum americanum L. de la familia Lamiaceae No. COL 574690;
Cymbopogon citratus (DC.) Stapf de la familia Poaceae No. COL 574692;
Chenopodium ambrosioides L. de la familia Chenopodiaceae No. COL 574695;
Eucalyptus globulus Labill. de la familia Miyrtaceae No. COL 574696;
Ruta graveolens L. de la familia Rutaceae No. COL 574697;
Rosmarinus officinalis L. de la familia Lamiaceae No. COL 573968;
Capsicum chinense Jacq. de la familia Solanaceae No. COL 558072;
Dieffenbachia seguine (Jacq.) Schott. de la familia Araceae No. COL 557711;
Urera baccifera (L.). Gaudich. Ex Wedd de la familia Urticaceae No. COL 557323.
Para la obtención de los AE se emplearon hojas, tallos y flores; para el extracto de C. chinense se empleó el fruto fresco, para el de D. seguine las hojas secas y para el de U. baccifera tallos y hojas secas. Tanto para los AE como los extractos se emplearon plantas de aspecto sano y robusto, en estado de madurez y floración.
2.3 Obtención de los extractos
Los extractos se obtuvieron por percolación, usando un equipo de maceración dinámica, en la cual el material vegetal se colocó en contacto con 150 mL de etanol durante tres días con agitación continúa durante 4 horas cada 24 horas. A los extractos alcohólicos se les separó el disolvente en un rotaevaporador, y las trazas se eliminaron conectando los balones a un manifold unido a una bomba de alto vacío (5 mmHg) durante cuatro horas. Todas las extracciones se hicieron por triplicado.
2.4 Obtención de los aceites esenciales
Los aceites esenciales se obtuvieron mediante hidrodestilación asistida por microondas. En un balón fondo redondo, equipado con una trampa Dean-Stark y dos condensadores tipo rosario y en espiral, se adicionó el material vegetal fresco (hojas, tallos y flores) de cada una de las plantas, en trozos pequeños, se les adicionó 500 mL de agua, la mezcla se calentó a ebullición, durante 75 minutos en tres sesiones de 25 minutos cada una.
2.5 Cromatografía de gases-espectrometría de masas
Los extractos se analizaron en un cromatógrafo de gases Agilent Technologies 7890A acoplado a un detector selectivo de masas Agilent Technologies 5975C, con inyector split/splitless (relación split 1:10) y columna HP-1MS (30 m x 0.25 mm D.I. x 0.25 μm df) con fase estacionaria 100%-fenil-poli(dimetilsiloxano).
La rampa de calentamiento utilizada en el horno cromatográfico fue: 50°C (5 min) @ 5°C/min hasta 200°C (5min) y @ 10°C/min hasta 260°C (20 min). Los espectros de masas se obtuvieron por ionización electrónica (70 eV) en un analizador cuadrupolar con rango de masas m/z 40-400, en el modo full scan. Las temperaturas de la cámara de ionización y de la línea de transferencia se mantuvieron en 230 y 285°C, respectivamente. Los datos cromatográficos y espectroscópicos se procesaron con el software de Agilent Technologies MSD ChemStation G1701 (Versión EA E.02.02.1431).
La identificación de los componentes de los aceites esenciales y extractos fue realizada comparando los espectros de masas obtenidos, con los reportados en las bases de datos Adams7 Wiley 1388, y NIST029.
2.6 Ensayo de actividad insecticida
Para implementar el bioterio se recolectaron los huevos de Culex quinquefasciatus en un colector de aguas lluvias en Bucaramanga, Santander, con coordenadas geográficas: latitud 7°6’11.3’’N, longitud 73°6’52.1’’W, y altura 947 msnm. El 10% de los huevos y larvas eclosionadas fueron enviados al Instituto de Salud de Bucaramanga para su caracterización entomológica.
La actividad larvicida se realizó siguiendo la metodología de la Organización Mundial de la Salud10 including bacterial larvicides and insect growth regulators (IGRs. Las concentraciones de los aceites esenciales y extractos se probaron de forma seriada desde 1000 hasta 1 ppm; un control. Para disolver el malatión se utilizó agua y para las muestras etanol.
Se colocaron lotes de 25 larvas en vasos plásticos desechables y se les adicionó delicadamente 33 mL de la solución correspondiente, se dispusieron controles positivos (agua), y controles negativos (etanol), a la concentración NOAEL, que es aquella a la que no se observa ningún efecto adverso sobre las larvas (2%).
Pasadas 72 horas de exposición se leyó la mortalidad, determinando el daño, muerte o alteración fisiológica en las larvas expuestas. Fueron consideradas muertas aquellas larvas a las que no se les pudo inducir el movimiento. Las larvas moribundas fueron adicionadas al número de larvas muertas; se consideraron como moribundas aquellas larvas incapaces de elevarse a la superficie o que no mostraron el buceo característico cuando son perturbadas.
Cada ensayo se hizo por triplicado, en semanas diferentes, con un fotoperiodo de 12 horas de luz y 12 horas de oscuridad. A partir de los porcentajes de mortalidad obtenidos, los datos se procesaron en función de la concentración, calculando los parámetros estadísticos con el método de regresión logarítmica en el programa BioStat 2009, a partir del cual se obtuvieron las Concentraciones Letales Media y CL95.
2.7 Ensayo de inhibición de la enzima acetilcolinesterasa
Para determinar la inhibición de la acetilcolinesterasa por los extractos y aceites, se utilizó la metodología de Ellman11 homogenates, cell suspensions, etc., has been described. The enzyme activity is measured by following the increase of yellow color produced from thiocholine when it reacts with dithiobisnitrobenzoate ion. It is based on coupling of these reactions: The latter reaction is rapid and the assay is sensitive (i.e. a 10 μL sample of blood is adequate. Se colocaron 50 μL de una solución del extracto o aceite esencial (en concentraciones seriadas desde 1000 hasta 0.5 ppm), disuelto en buffer fosfato salino de pH 7.5 y 50 μL de la AChE (0.25 U/mL). La placa se incubó a temperatura ambiente por 30 minutos y se adicionaron 100 μL de la solución sustrato de pH 7.5 [Na2HPO40.04 M, ácido 2,2´-dinitro-5,5´-ditio benzoico 0.2 mM, yoduro de acetiltiocolina 0.24 mM]. A los cinco minutos de iniciada la reacción se leyó la absorbancia, a 412 nm, en un lector de microplacas VERSAmax. Se utilizó galantamina como compuesto de referencia. Los ensayos se realizaron por triplicado; los cálculos de las IC50 y las gráficas se hicieron con el software SoftMax Pro 5.2 de Molecular Devices.
2.8 Ensayo de toxicidad y análisis de los cambios fenotípicos de los extractos etanólicos empleando el modelo embrionario del pez cebra
Se usaron los procedimientos reportados por Ali12, Eggert13, Peterson14 Rubinstein15 y adaptados por Puerto & Kouznetsov16.
Especímenes adultos del pez cebra (Danio rerio), de ambos sexos y de tipo salvaje, fueron separados en tanques de acuerdo con su género a 26 ± 2 °C bajo fotoperíodos naturales de luz y oscuridad. Los peces fueron alimentados dos veces por día y la calidad del agua fue monitoreada semanalmente, con el fin de adaptar a los peces a estas condiciones por dos semanas, antes de iniciar los experimentos.
Para la reproducción de los peces adultos, pequeños tanques de apareamiento fueron acondicionados en la tarde previa al experimento, donde en cada uno de estos tanques se ubicaron tres machos y una hembra. Estos tanques fueron aislados, sin ninguna perturbación de ruido o luz, hasta la mañana siguiente, cuando el apareamiento natural ocurrió.
Los peces adultos fueron reintegrados a sus respectivos tanques y los embriones fueron recolectados, lavados dos veces con buffer de Holtfreter (compuesto por 5 mM NaCl, 0.17 mM KCl, 0.4 mM CaCl2 y 0.16 mM MgSO4, al cual nombramos E3), y transferidos a una caja Petri. Los embriones fueron examinados periódicamente a través de un microscopio de disección con el fin de remover aquellos embriones muertos, no fertilizados, malformados o retrasados en su desarrollo.
Durante este período, los embriones fueron mantenidos en una incubadora a 28 ± 2 °C bajo fotoperíodos naturales de luz y oscuridad.
Los embriones seleccionados a 24 horas posteriores a la fertilización (hpf) fueron transferidos cuidadosamente desde la caja Petri a una microplaca de 96 pozos, ubicando un embrión y 200 μL de E3 por pozo.
2.8.1 Determinación de la CL50 en embriones del pez cebra
Para este experimento se emplearon 72 embriones en total, para evaluar la toxicidad de cada extracto con el fin de realizar tres experimentos independientes en tres diferentes placas, en cada una de ellas cada extracto fue evaluado tres veces en cada placa.
En cada placa se evaluó una serie geométrica de concentraciones, iniciando en 300 y finalizando en 4.68 μg/mL. La mortalidad acumulada fue monitoreada en un microscopio de disección 72 horas después de la exposición química (96 hpf). Se determinó la CL50 (expresada en mg de extracto/mL de solución) mediante el análisis de la Regresión Probit con el programa SPSS para Windows versión 19.0. Los datos se expresan con el error estándar de la media de los tres experimentos realizados en triplicado.
2.8.2 Análisis de los cambios fenotípicos usando el modelo embrionario del pez cebra
Los extractos de C. chinense, U. baccifera, C. officinalis fueron diluidos en el medio E3 con 2% v/v de DMSO y se prepararon alícuotas de 200 μL en una placa de 96 pozos en concentraciones de 100, 50, 25, 12.5, 6.25, 3.12, 1.56, 0.78 y 0.39 μg/mL.
Se utilizaron cuatro embriones como control, cada uno expuesto al medio E3 con un 2% v/v de DMSO. La placa embrionaria fue incubada a 28 ± 2° C bajo fotoperíodos naturales de luz y oscuridad, y los embriones fueron examinados a 48, 72 y 96 hpf utilizando un estéreomicroscopio trinocular OPTIKA (versión del modelo: SZM-1). Cada uno de estos experimentos fue realizado por duplicado.
3. RESULTADOS
3.1 Obtención de aceites esenciales y extractos
Los aceites esenciales de las plantas se aislaron con un rendimiento en peso fresco de: 1.6% para R. graveolens; 0.9% para O. americanum; 0.14% para M. piperita; 1.30% para E. globulus; 0.05% para R. officinalis; 0.15% para C. ambrosoides y 0.25% para C. citratus. Las características físicas de los aceites mostraron ser insolubles en agua, solubles en etanol y dimetilsulfoxido, de tonalidad amarillo pálido tenue para R. graveolens y M. piperita e incoloro para O. americanum.
Los extractos de las plantas se aislaron con un rendimiento de: 1.3% para D. seguine; 0.4% para U. baccifera y 0.6% para C. chinense.
3.2 Cromatografía de gases-espectrometría de masas
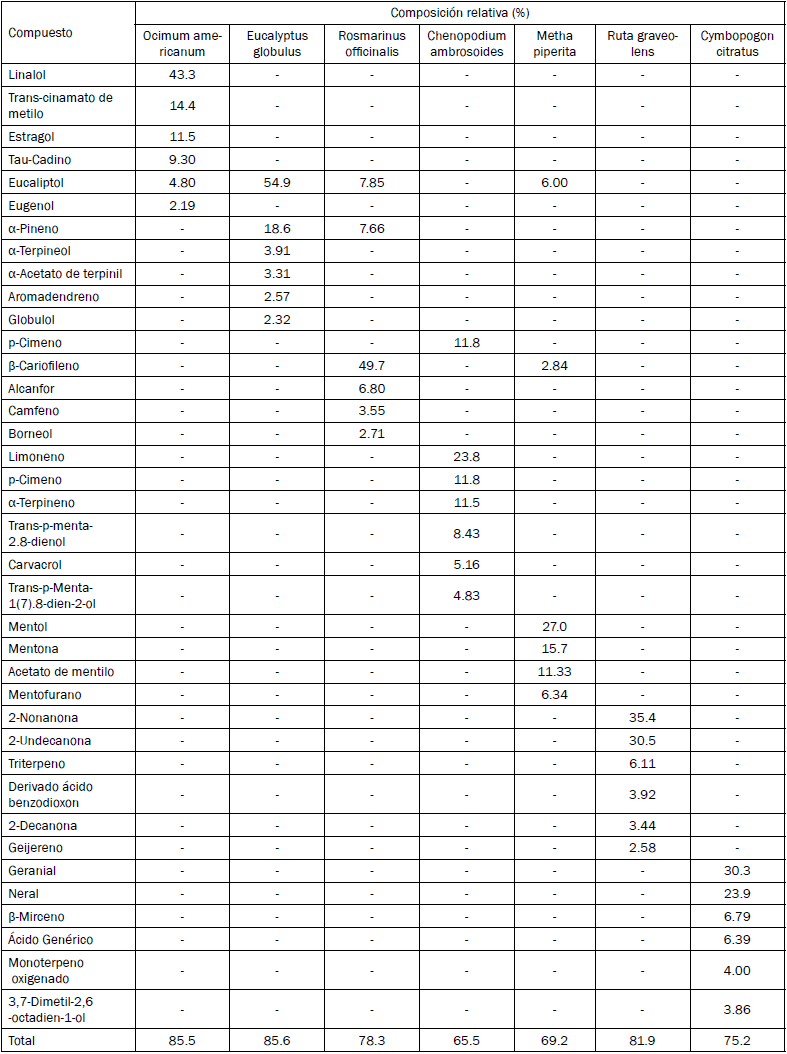
El análisis por CG-MS de la composición química, y la cantidad relativa de componentes de los extractos y aceites esenciales se muestran en las tablas I y II, respectivamente. Estos extractos presentaron compuestos químicos similares en su composición, por ejemplo, la amida docosenamida se presentó en el extracto C. chinense D. seguine y U. baccifera; el neofitadieno se presentó en los últimos dos extractos.
Tabla I COMPOSICIÓN QUÍMICA DE LOS EXTRACTOS DE C. CHINENSE, D. SEGUINE Y U. BACCIFERA
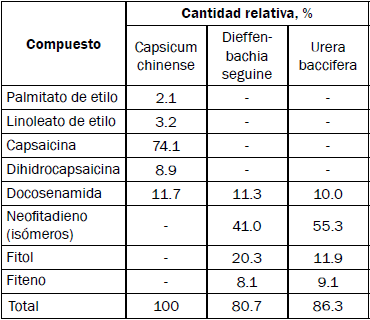
Fuente: Los autores
Los AE presentaron una composición química muy variada (ver tabla II), el eucaliptol, el α-pineno, y el β-cariofileno fueron los metabolitos secundarios, tipo terpenoides que se presentaron en dos o más de los AE obtenidos.
3.3 Estudio para determinar la actividad insecticida de los aceites esenciales y extractos
Los AE de R. graveolens (CL50 7.20±0.19 μg/mL), O. americanum (CL50 16.8±0.11 μg/mL) y C. ambrosioides (CL50 25.4± 0.5 μg/mL) son altamente activos, con concentraciones letales medias menores a 50 μg/mL; los AE de M. piperita (CL50 53.9±0.9 μg/mL), E. globulus (CL50 57.7±1.2 μg/mL) y C. citratus (CL50 75.5±3.1 μg/mL) son activos; con concentraciones letales medias entre 50 - 100 μg/mL y el AE de R. officinalis tiene moderada actividad con CL50 121.8±0.9 μg/mL. Por otro lado, los extractos de D. seguine (CL50 693.5±33 μg/mL), U. baccifera (CL50 873.9±39 μg/mL) y C. chinense (CL50 1056±4.4 μg/mL) son considerados como poco activos frente a las larvas de Culex quinquefasciatus en tercer instar. Las CL50 y CL95 de cada uno de ellos se muestran en la tabla III.
Tabla III ACTIVIDAD LARVICIDA E INHIBICIÓN DE LA ACHE DE LOS ACEITES ESENCIALES Y EXTRACTOS
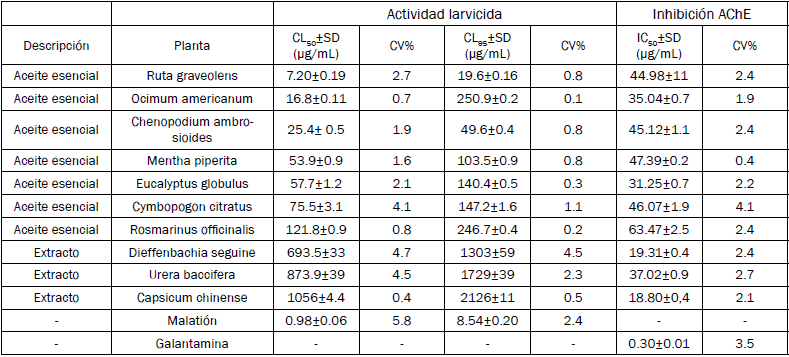
Fuente: Los autores
Las bioactividades dependen en gran medida de la composición química y puede verse afectada por la zona geográfica en donde se cultive la planta, y las condiciones climáticas. Algunos ejemplos de esto son los AE de Ocimum americanum, Chenopodium ambrosioides y Mentha piperita.
En Brasil, el AE de O. americanum quimiotipo cinamato de metilo (70.9%) mostró una CL50 de 67 μg/mL, transcurridas las 24 horas de exposición, frente a larvas de Aedes aegypti17. Con lo cual el AE es considerado como activo frente a esta cepa del laboratorio de la Secretaría de Salud del estado Ceará, Brasil. En esta investigación el AE aislado es quimotipo linalol (43.3%), y es altamente activo (CL50 16.8 μg/mL) para la cepa estudiada de Culex quinquefasciatus.
El AE de C. ambrosioides es quimiotipo limoneno (23.8%), y presentó una CL50 de 25.4 μg/ mL. La literatura reportó el quimiotipo α-terpineol (73.9%) como insecticida en larvas de Aedes aegypti, con CL50 de 35 μg/mL18. Siendo ambos quimiotipos altamente activos sobre las especies de mosquitos evaluados.
Se han encontrado reportes de actividad larvicida de algunas plantas del género Ruta. Para el caso del AE de Ruta chalepensis se observó variación en la composición química, según su forma de cultivo. Para las plantas silvestres el metabolito mayoritario fue la 2-nonanona (39.3%); para las plantas cultivadas en vivero, el metabolito mayoritario fue 2-undecanona (37.4%)19. Este cambio en el quimiotipo generó una leve variación en la actividad larvicida, siendo más activo el quimiotipo 2-undecanona con una CL50 de 33.18 μg/mL que el quimiotipo 2-nonanona CL50 35.66 μg/mL sobre larvas de Aedes albopictus. Para la Ruta graveolens cultivada de forma orgánica se encontró que su componente mayoritario es la 2-nonanona (35.4%) y su concentración letal media frente a las larvas de Culex quinquefasciatus fue de 7.20 μg/mL, siendo el AE con mejor actividad.
Seis AE de Mentha piperita (cultivadas en Gran Bretaña, Rusia y República Checa) han sido estudiados sobre larvas en tercer instar de Culex quinquefasciatus20. Estos AE no presentaron el metabolito secundario acetato de mentilo; el cual se mostró en un 11.33% en las plantas cultivadas en la finca El Limonal. De estos seis AE, tres presentaron una composición similar a la mostrada por el AE de Mentha piperita que se expone en la tabla II. Estos tres AE presentaron CL50 variables, oscilando entre 83 y 104 μg/mL transcurridas las 24 horas de exposición. Para el caso de las larvas de Culex colectadas en Bucaramanga, la CL50 fue de 53.9 μg/mL tras 72 horas del ensayo.
Igualmente, se reportó el efecto que presentan los AE de varias especies de Eucalyptus (Globulus ssp. Maidenii, Globulus ssp. Globulus) cultivados en Argentina, sobre larvas de Aedes aegypti (cepa CIPEIN)22. En ambos aceites, el 1,8-cienol o eucaliptol fue el metabolito mayoritario con porcentajes de 77.91 y 76.66%, respectivamente. Para el caso del Eucalyptus globulus de esta investigación, el eucaliptol se presentó en un 54.9%, siendo este el compuesto mayoritario.
Los porcentajes de mortalidad de las variedades de eucaliptos argentinos no superaron el 20%, siendo más activo la variedad Eucalyptus globulus ssp. Maidenii que la Eucalyptus globulus ssp globulus con 13±23.1 y 4±7.7%, respectivamente21. La susceptibilidad de los Culex quinquefasciatus colectada en Bucaramanga el AE de Eucalyptus globulus (quimiotipo mentol 27.0%) fue de 57.7 μg/mL pudiendo considérese este aceite como activo.
Los aceites esenciales estudiados en este trabajo presentaron una mayor bioactividad que los extractos frente a las larvas de Culex quinquefasciatus, y muestran un alto potencial como nuevos larvicidas, entre los cuales se pueden destacar la R. graveolens, O. americanum y C. ambrosioides.
3.4 Actividad inhibitoria de aceites esenciales y extractos frente a la enzima acetilcolinesterasa
La inhibición de la acetilcolinesterasa (AChE) es el mecanismo más común de acción insecticida. Para este procedimiento la actividad de la enzima se midió fotométricamente a 412 nm, por el incremento del color amarillo producido por la tiocolina, procedente de la hidrólisis de la acetilcolina, cuando esta reacciona con el ion ditiobisnitrobenzoato para formar el anión del ácido tiobisnitrobenzóico, que es de color amarillo. De esta manera fue posible establecer la actividad acetilcolinesterásica de los extractos y aceites.
Las cuatro muestras más activas fueron: el extracto de C. chinense con una IC50 de 18.80 μg/mL, seguido por el extracto de D. seguine con 19.31 μg/mL, por el AE de E. globulus 31.25 μg/mL y el de O. americanum con 35.04 μg/mL. Para los demás aceites esenciales las concentraciones inhibitorias medias de la enzima estuvieron entre 44 - 64 μg/mL y para el extracto de U. baccifera la IC50 37.02 μg/mL (ver tabla III).
Los inhibidores de la AChE, como los insecticidas organofosforados, usados comúnmente para el control de los artrópodos, son altamente tóxicos; pero las larvas, cuando fueron expuestas a los extractos y AE de origen natural no mostraron los efectos característicos de envenenamiento por inhibición de este target biológico. Muchos de los aceites y extractos no han sido reportados en la literatura como inhibidores de la acetilcolinesterasa, en ningún caso se encontraron comportamientos como inhibidores irreversibles de la enzima, esto es un punto favorable al evitarse el bloqueo de la enzima, lo cual llevaría a una intensa toxicidad aguda y crónica.
3.5 Toxicidad y cambios fenotípicos en el pez cebra
Para estudiar la toxicidad de los extractos etanólicos de Capsicum chinense, Dieffenbachia seguine, Urera baccifera y el AE de Ruta graveolens fue empleado el protocolo de Puerto & Kouznetsov16; se encontró que estos extractos y el AE son moderadamente tóxicos (10 < CL50 < 100 mg/L)22. El extracto de Capsicum chinense presentó una CL50 de 39.7 mg/L, siendo el extracto con menor toxicidad sobre este modelo, seguido por Urera baccifera 33.84mg/L, Dieffenbachia seguine 32.15 mg/L y Ruta graveolens 13.33 mg/L. La toxicidad de los extractos y el AE de Ruta graveolens es comparable con moléculas de origen natural, como por ejemplo la teobromina presente en el cacao con concentración letal media de 150.46 mg/L22. Una vez se determinó la CL50, se estableció un rango de concentraciones por debajo de este, para estudiar los cambios fenotípicos en el pez Danio rerio.
En general, todos los embriones tratados con los extractos, a dos o tres concentraciones por debajo de la respectiva CL50, no manifestaron ningún cambio fenotípico visible durante las primeras horas de exposición. Sin embargo, a una o dos concentraciones cercanas a la CL50 se observó un desarrollo anormal de las somitas, que son las responsables de dar lugar a la mayor parte del esqueleto axial y a la musculatura alrededor de la espina dorsal, permitiendo identificar el mecanismo de acción y los efectos tóxicos previos a la muerte del embrión.
Los embriones que presentaron retraso en el desarrollo, finalmente murieron. Sin embargo, aquellos embriones que no presentaron ningún cambio fenotípico visual alcanzaron las etapas posteriores de desarrollo después de 96 hpf, sin ningún tipo de evidencia que indicara que su morfología o embriogénesis difiriera de la del control.
Es importante resaltar que la actividad inhibitoria de la AChE por el extracto de C. chinense (IC50 18.80 μg/mL) se encuentra por debajo de la CL50 (39.7μg/mL) en el Danio rerio; al igual que en D. seguine (IC50 19.31 μg/mL; CL50 32.15 μg/mL), de lo que se puede inferir que inhibir la actividad de la enzima no resulta ser letal para el pez, o bien que el mecanismo de acción por el cual el pez muere al ser expuesto al extracto, no está relacionado con la inhibición de colinesterasas, de la misma forma que tampoco causa cambios fenotípicos, daños teratogénicos o malformaciones en el desarrollo.
4. CONCLUSIONES
Se puede considerar que los aceites esenciales y extractos evaluados en esta investigación presentan un alto potencial como larvicidas en Culex quinquefasciatus. De los estudios de inhibición de la enzima acetilcolinesterasa y los ensayos de toxicidad sobre el pez Danio rerio, es posible considerar que estos productos tienen baja toxicidad sobre las colinesterasas de los mamíferos y cambios fenotípicos en el modelo vertebrado del pez cebra.