Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Ingenierías Universidad de Medellín
Print version ISSN 1692-3324On-line version ISSN 2248-4094
Rev. ing. univ. Medellín vol.10 no.19 Medellín July/Dec. 2011
ARTÍCULOS
EFECTO DE LA CONCENTRACIÓN DEL METIL PARATIÓN Y EL EXTRACTO DE LEVADURA COMO FACTORES DE SELECCIÓN DE MICROORGANISMOS DEGRADADORES DEL PESTICIDA A PARTIR DE SUELOS CONTAMINADOS
Effect of Methyl Parathion Concentration and Yeast Extract as Factors for Selecting Pesticide Degrading Microorganisms from Polluted Soils
L. R. Botero*; N. Nagles**; J.C. Quintero***; G. A. Peñuela****
* Liliana Rocío Botero Botero. Bióloga. M. Sc. Candidata a doctora en Biología. Docente investigadora. Coordinadora Grupo de investigaciones en Biodiversidad, Biotecnología y Bioingeniería (GRINBIO). Universidad de Medellín, Carrera 87 No. 30-65, Centro de laboratorios Laboratorio de Biotecnología, Bloque 3-202, Medellín-Colombia. Tel: 057-3405675, lbotero@udem.edu.co.
** Nelson Nagles Vergara. Ingeniero Ambiental estudiante de maestría. Grupo de Diagnóstico y Control de la Contaminación (GDCON). Sede de Investigaciones Universitarias, Universidad de Antioquia, Calle 62 No. 52-59, Laboratorio 232, Medellín-Colombia, Tel: 057-2196571. nelsonnagles@udea.edu.co
*** Juan Carlos Quintero. Ingeniero Químico M. Sc., Ph. D., Docente investigador. Coordinador Grupo de Bioprocesos. jcquinte@udea.edu.co. Universidad de Antioquia (Colombia). Calle 67 No. 53-108. Of. 18-219. Teléfono:057-2195536
**** Gustavo Antonio Peñuela Mesa. Químico M. Sc., Ph. D., Docente investigador. Coordinador del Grupo de Diagnóstico y Control de la Contaminación (GDCON). Sede de Investigaciones Universitarias, Universidad de Antioquia, Calle 62 No. 52-59, Laboratorio 232, Medellín-Colombia, Tel: 057-2196570. gpenuela@udea.edu.co
Recibido: 25/08/2010
Aceptado: 12/08/2011
RESUMEN
El aislamiento y cultivo de microorganismos con capacidades para degradar los contaminantes ambientales es importante para implementar planes de biorremediación. En este estudio se evaluó el efecto del extracto de levadura tanto en la capacidad de asimilación microbiana del pesticida organofosforado metil paratión, como en los procesos de aislamiento de microorganismos útiles para de degradar este pesticida. Los microorganismos evaluados fueron obtenidos de suelo fresco fumigado históricamente con este pesticida. Los ensayos se efectuaron con medios sólidos definidos enriquecidos con metil paratión (0-60 mg L-1) y extracto de levadura (0-0.5 g L -1).
Se encontró que los microorganismos fueron capaces de asimilar hasta 5 mg L -1 del metil paratión en ausencia de extracto de levadura sin evidenciar efectos tóxicos. La capacidad de asimilación aumentó a 10 mg L-1 en los cultivos enriquecidos con 0.5 g L-1 de extracto de levadura.
El extracto de levadura en las dosis usadas no afectó el aislamiento de microorganismos. Sin embargo, el aislamiento por siembra directa en medios enriquecidos con metil paratión como única fuente de carbono se dificultó por el aporte de la materia orgánica del suelo que permitió el crecimiento de cepas tolerantes sin capacidad para degradar el pesticida.
Palabras clave: aislamiento, extracto de levadura, metal paratión, pesticida organofosforado.
ABSTRACT
Isolation and culture of microorganisms with capacity to degrade environmental pollutants are important for implementing bioremediation plans. This study is an evaluation of the yeast extract effect on both the microbial capacity to assimilate the organo-phosphorous pesticide methyl parathion and the isolation processes of microorganisms useful for degrading this pesticide. Microorganisms evaluated were obtained from fresh soil historically fumigate with this pesticide. Trials were conducted with defined solid means enriched with methyl parathion (0-60 mg L-1) and yeast extract (0-0.5 g L-1).
It was found that microorganisms were able to assimilate up to 5 mg L-1 methyl parathion with no yeast extract, without evidence of toxic effects. Assimilation capacity increased 10 mg L-1 in cultures enriched with 0.5 mg L-1 yeast extract.
Yeast extract in doses used did not affect the isolation of microorganisms. However, isolation through direct culture in means enriched with methyl parathion as the only source of carbon was difficult due to the addition of organic matter of soil, which allowed the growth of resistant strains with no pesticide degrading capacity.
Key words: isolation; yeast extract; methyl parathion; organo-phosphorous pesticide.
INTRODUCCIÓN
Los pesticidas organofosforados como el metil paratión (MP), causan problemas de contaminación y han sido usados en agricultura por más de 40 años para el control de plagas. Los efectos nocivos de la contaminación plantean el reto de buscar alternativas económicas de tratamiento como la biorremediación. Esta técnica, basada en la capacidad que tienen los microorganismos para eliminar los contaminantes plantea la búsqueda de fuentes de microorganismos y el desarrollo de estrategias para su aislamiento y cultivo.
Paradójicamente, la presencia de contaminantes induce la selectividad y la disminución de la diversidad microbiana convirtiendo el ambiente contaminado en potencial fuente de microorganismos. En estos ambientes contaminados, los microorganismos tolerantes a este factor de estrés desarrollan y utilizan respuestas enzimáticas y fisiológicas especializadas de manera natural, degradando el contaminante presente en el suelo [1, 2].
En los laboratorios, la capacidad para usar el pesticida como fuente de carbono y/o fósforo se ha utilizado tradicionalmente para aislar microorganismos con capacidad para la degradación de este y otros pesticidas organofosforados como el MP [3-6].
Frecuentemente, para la preparación de los medios de cultivos se ha usado el extracto de levadura (EL) en diferentes concentraciones como fuente de nitrógeno. Esta mezcla compleja ha sido reportada en estudios orientados al aislamiento de microorganismos con capacidad para hacer uso del pesticida [7]; asimismo se ha utilizado en estudios que evalúan la capacidad de degradación de pesticidas organofosforados [8-11] y, en algunos casos, se ha reportado su efecto benéfico en los procesos de degradación [8] y en algunos estudios de evaluación de la toxicidad de los pesticidas [12]. A pesar de los efectos benéficos del aporte nutricional del EL reportado, su naturaleza compleja y su aporte de carbono podrían afectar los resultados cuando se asume el pesticida como la única fuente de carbono.
En este trabajo se evalúa el efecto del EL en la toxicidad y asimilación del pesticida MP y su influencia en los procesos de aislamiento de microorganismos con capacidad para degradarlo mediante técnicas de aislamiento directo en medios sólidos, aplicadas a muestras de suelo como fuente microbiana.
1 MATERIALES Y MÉTODOS.
1.1 Recolección y preparación de suelos para el aislamiento
Se recolectaron suelos de cultivos tecnificados de algodón ubicados en el municipio de Lorica (departamento de Córdoba-Colombia) en los cuales se ha aplicado históricamente el MP.
Para la recolección de los suelos, se tomaron muestras del primer horizonte a 10 cm de profundidad usando instrumental estéril; las muestras se depositaron en bolsas estériles, las cuales fueron transportadas y mantenidas en el laboratorio en condiciones de enfriamiento a 4oC. Para los ensayos se disminuyó manualmente el tamaño de los agregados y posteriormente se tamizó a 2 mm usando implementos limpios y desinfectados.
1.2 Productos químicos
Para hacer los cultivos fueron usados NaCl, KH2PO4, K2HPO4, (NH4)2SO4, MgSO4, ZnSO4 7H2O, MgCl2, ácido bórico, CoCl2, CuSO4, NiCl2, FeSO4, EDTA glucosa y agar, grado analítico, marca Merck. Methión 48 EC (Concentrado líquido emulsionable de MP, comercializado por la empresa Agroser SA y que contiene 480 g L-1 del principio activo).
1.3 Medios y condiciones de cultivo
Para los cultivos se prepararon medios selectivos, con 1.5 g L-1 de K2HPO4, 0.5 g L-1 de KH2PO4, 1 mg L-1 de (NH4)2SO4, 0.21 g L-1 de MgSO4 7H2O y 15 g L-1 de agar estos se esterilizaron con calor húmedo (15 libras, 20 min). Posteriormente los medios fueron enriquecidos con 0.5 mL de una solución de sales minerales (400 mg L-1 de ZnSO4 7H2O, 20 mg L-1 de MgCl2 4H2O, 10 mg de ácido bórico, 50 mg de CoCl2 6H2O; 200 mg de CuSO4, 10 mg de NiCl2, 500 mg de FeSO4 y 250 mg de EDTA) estéril (filtración 0,45 & $181;m). Se evaluaron tres concentraciones de EL (0, 0.05 y 0.5 gL-1) y de seis de MP (0, 5, 10, 20, 40 y 60 mg L-1) para un total de 18 tratamientos; los ensayos fueron hechos por triplicado.
Para determinar el número de unidades formadoras de colonia por gramo de suelo (UFC g-1) se prepararon diluciones seriadas de suelo usando buffer salino (8 g L-1de NaCl, 1.21 g L-1de K2HPO4 y 0.34 g L-1 de KH2PO4); se sembró en cada caja 1 mL de cada dilución y se hizo el recuento en aquellas en la cuales se presentaron entre 30-300 colonias. Los cultivos fueron mantenidos en condiciones de oscuridad a 28oC por 8 días.
1.4 Análisis estadístico
Para la determinación de las diferencias en el porcentaje de tolerancia microbiana de los suelos como consecuencia de la adición del MP se analizó la de varianza, considerando diferencias significativas entre tratamientos aquella con p menores a 0.05. Para las comparaciones entre tratamientos se aplicaron las pruebas de rangos múltiples y de contrastes por pares.
2 RESULTADOS
2.1 Toxicidad del MP
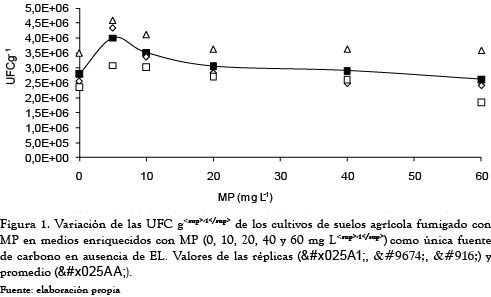
Los análisis estadísticos mostraron que no hay diferencias significativas en el crecimiento microbiano entre los tratamientos con MP cuando no se incluye EL en los medios de cultivo (p = 0.2132). El test de rangos múltiples en este caso diferenció tan solo dos grandes grupos superpuestos: uno formado por las dosis 60-0-40-20-10 mg L-1 y otro que incluyó las dosis 0-40-20-10-5 mg L-1 de MP diferenciando tan solo los valores de 60 mg L-1 (alta toxicidad) y 5 mg L-1 (de baja toxicidad). Las pruebas de contrastes por pares pudieron separar estadísticamente las respuestas de crecimiento de los medios enriquecidos con 5 mg L-1 de MP con un valor más alto de UFC g-1 que el resto de los tratamientos. Como se aprecia en la figura 1, los controles sin EL presentaron crecimiento en todos los cultivos, aun en las dosis de 0 mg L-1 de MP; el valor máximo de UFC g-1 fue el obtenido con la dosis de 5 mg L-1 de MP (4.3x106 UFC g-1). Al incrementar la concentración de MP por encima de 5 mg L-1 se presentó disminución en el crecimiento microbiano. En general, los valores de UFC g-1 fueron superiores para las concentraciones de MP entre 5-40 mg L-1, en comparación con los controles sin MP.
2.2 Efecto del EL en la toxicidad del MP
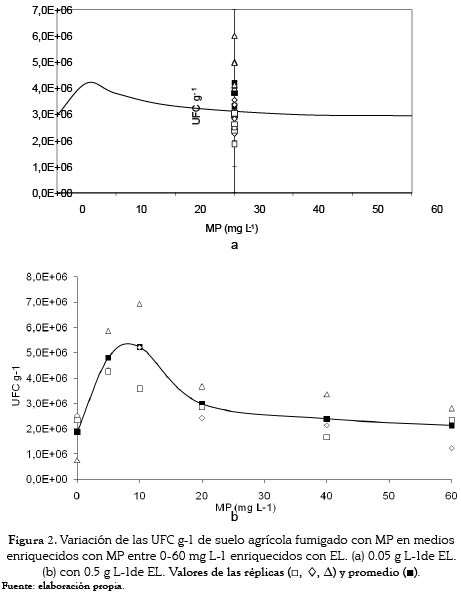
Los análisis estadísticos mostraron que no se presentaron diferencias significativas entre los tratamientos con MP cuando se incluyó EL en concentraciones de 0.05 g L-1 a los medios de cultivo (p= 0.7213), en este caso, el test de rangos múltiples no diferenció grupos. La prueba de contrastes por pares tampoco detectó diferencias entre los tratamientos. A pesar de estos resultados, al observar la figura 2a se puede apreciar un ligero aumento con la concentración de 5 mg L-1 de MP.
Para los ensayos con EL en concentraciones de 0.5 g L-1, los análisis estadísticos mostraron diferencias significativas entre los tratamientos (p=0.0058). El test de rangos múltiples para esta concentración de EL diferenció dos grandes grupos: uno donde se ubicaron los valores promedio de UFC g-1 más bajos (0-60-40-20 mg/L de MP), y otro grupo que incluyó las dosis 5 y 10 mg L-1 de MP, en las que se presentaron los mejores crecimientos. Como se aprecia en la figura 2b, en los cultivos realizados con la concentración más alta de EL (0.5 g L-1) se favoreció el crecimiento microbiano hasta los 10 mg L-1 el MP disminuyendo posteriormente.
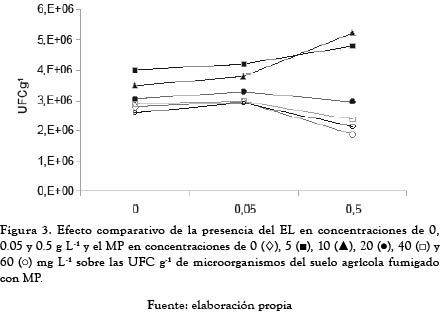
El efecto comparativo del EL que se presenta en la figura 3 muestra un aumento del número de UFC g-1 con las dosis de 0.05 g L-1 de EL para todas las dosis del pesticida y, sin embargo, en las dosis altas de EL, este genera un aumento de la toxicidad que disminuye los recuentos en las dosis altas de 20, 40 y 60 mg L-1 de MP y una disminución de la toxicidad en las dosis más bajas de 5 y 10 mg L-1 de MP.
3 DISCUSIÓN
3.1 Toxicidad del MP
El aumento de los valores de UFC g-1 como resultado de la adición del MP, cuando son usadas dosis bajas (5 mg L-1), podría ser considerado como evidencia de la capacidad microbiana de hacer uso de este compuesto. Se hace evidente el efecto tóxico del MP en dosis superiores a 5 mg L-1 en ausencia de EL con la disminución del crecimiento microbiano, sin embargo, a pesar del efecto tóxico, en general, los valores de UFC g-1 fueron superiores para las concentraciones de MP entre 5-40 mg L-1 en comparación con los controles sin MP. Esto muestra que la adición de MP hace un aporte importante de nutrientes a los microorganismos del suelo que ha sido sometido a sucesivas aplicaciones del pesticida como ha sido reportado por los estudios hechos por múltiples autores [3-6, 11, 13-15].
3.2 Efecto del EL en la toxicidad del MP
Es factible que para las dosis bajas de EL de 0.05 g L-1, ni el EL ni el MP afectan significativamente el crecimiento microbiano ya que ni el test de rangos múltiples ni las pruebas de contrastes por pares pudieron detectar diferencias entre los tratamientos sobre el número de UFC g-1. Sin embargo, el incremento de los recuentos microbianos en dosis bajas de pesticida (5 mg L-1) (figura 2a) en presencia de EL en las dosis mayores usadas de 0.5 g L-1 apoya lo reportado por diversos autores quienes afirman que los pesticidas organofosforados pueden ser mejor aprovechados por los microorganismos presentes en los suelos en presencia de EL [8, 10, 11].
Para los ensayos hechos con EL en concentraciones de 0.5 g L-1, se observó cómo el EL disminuyó la toxicidad e incrementó la capacidad de asimilación del pesticida, y los mejores crecimientos microbianos fueron los obtenidos en las dosis más altas de 10 mg L-1, sin embargo, fue evidente que al incrementar la concentración del pesticida por encima de 10 mg L-1, este se convirtió en un factor de selección microbiano que afectó su sobrevivencia. A pesar del efecto tóxico del MP en dosis altas de EL de 0.5 g L-1, se observó que, para todas las concentraciones de MP, los valores de recuento microbiano fueron, en términos generales, superiores a los obtenidos para los controles a los que no se les adicionó MP, y mostraron que el EL pudo disminuir el efecto tóxico del MP e incrementar la capacidad de los microorganismos para degradarlo.
Como se puede apreciar en la figura 3, el crecimiento microbiano en ausencia aparente de fuentes de carbono ( MP y EL) muestra que el EL no es el compuesto que soporta el crecimiento microbiano de cepas tolerantes que carecen de potencialidades para degradar el pesticida que lo convertiría en un factor que causante de interferencia en los aislamientos de microorganismos útiles para la degradación del pesticida; esto apoya las metodologías usadas por algunos autores quienes utilizaron medios enriquecidos con 5 g L-1 de EL para aislar Pseudomonas sp. con capacidad para degradar MP [16].
Para fines de aislamiento microbiano, el hecho de que se hubieran presentado crecimientos en los cultivos con valores promedio de 2,8x106 UFC g-1 sin MP y sin EL, evidencia que, al parecer, los microorganismos encontraron fuentes de nutrientes y energía en los remanentes de sustrato proveniente del suelo y que estos son suficientes para permitir su desarrollo. Estos resultados mostraron que la premisa, tradicionalmente expuesta en la literatura por diversos autores que recomiendan el uso del pesticida como única fuente de carbono para el aislamiento de microorganismos con potencialidades para degradarlo [17], puede no ser suficiente factor de selección que garantice el crecimiento exclusivo de microorganismos con potencialidades para degradarlo, cuando se implementan procesos de aislamiento por cultivo directo en medios sólidos y suelo como fuente de microorganismos. Los resultados apoyan, sin embargo, que las dosis altas de MP de 60 mg L-1 disminuyen los recuentos microbianos, lo cual soporta su aplicabilidad como factor de selección por efectos de toxicidad. Este factor de selección podría favorecer el crecimiento de microorganismos con capacidad de degradación de pesticidas.
4 CONCLUSIONES
El uso del pesticida como única fuente de carbono puede no ser suficiente factor de selección que garantice el crecimiento exclusivo de microorganismos con capacidad de asimilación del MP cuando se implementan procesos de aislamiento por cultivo directo en medios sólidos y suelo como fuente de microorganismos. Las dosis altas de MP de 60 mg L-1 pueden ser usadas como factor de selección. En estos procesos, el EL disminuye el efecto tóxico del MP e incrementa la capacidad de asimilación del MP en los microorganismos.
5 AGRADECIMIENTOS
Agradecemos a COLCIENCIAS por su soporte económico, a los grupos de investigación GEMA, GDCON y GRINBIO por su apoyo logístico, a Aleida Ochoa Higuita por su apoyo técnico y a la Universidad de Antioquia y a la Universidad de Medellín por el apoyo general que han hecho posible el desarrollo de este estudio.
REFERENCIAS
[1] S. A. Wakelin et al., ''Habitat selective factors influencing the structural composition and functional capacity of microbial communities in agricultural soils,'' Soil Biology and Biochemistry, vol. 40, no. 3, pp. 803-813, 2008. [ Links ]
[2] B. K. Singh et al., ''Cross-enhancement of accelerated biodegradation of organophosphorus compounds in soils: Dependence on structural similarity of compounds'', Soil Biology and Biochemistry, vol. 37, no. 9, pp. 1675-1682, 2005. [ Links ]
[3] D. G. Karpouzas, y B. K. Singh, ''Microbial Degradation of Organophosphorus Xenobiotics: Metabolic Pathways and Molecular Basis,'' Advances in Microbial Physiology, vol. 51, pp. 119-225, 2006. [ Links ]
[4] G. Heiss et al., ''npd gens functions of Rhodococcus (opacus) erythropolis HL PM-1 in the inicial stops of 2,4,6-trinitrophenol degradation,'' Microbiology vol. 148, no. 3, pp. 799-806, 2002. [ Links ]
[5] H. Goedicke, y R. Winkler, ''On the residue of methyl parathion in soil,'' Pflanzenschutz Nachrichten Bayer, vol. 30, no. 5, pp. 100-101, 1976. [ Links ]
[6] J. S. Karns et al., ''Use of microorganisms and microbial systems in the degradation of pesticides,'' en Biotechnology in agricultural chemistry, H. M. LeBaron et al., eds., pp. 156-170, Washington, D.C.: American Chemical Society, 1987. [ Links ]
[7] V. Ramani, ''Effect of pesticides on phosphate solubilization by Bacillus sphaericus and Pseudomonas cepacia,'' Pesticide Biochemistry and Physiology, vol. 99, no. 3, pp. 232-236, 2011. [ Links ]
[8] C. Katsuyama et al., ''Complementary cooperation between two syntrophic bacteria in pesticide degradation,'' Journal of Theoretical Biology, vol. 256, no. 4, pp. 644-654, 2009. [ Links ]
[9] P. R. Fisher, y J. Appleton, ''Isolation and characterization of the pesticide-degrading plasmid pJP1 from Alcaligenes paradoxus,'' Journal of Bacteriology, vol. 135, no. 3, pp. 798-804, 1978. [ Links ]
[10] L. M. Nelson, ''Biologically-induced hydrolysis of parathion in soil: Isolation of hydrolyzing bacteria '' Soil Biology and Biochemistry., vol. 14, no. 3 pp. 219-222, 1982 [ Links ]
[11] M. Sharmila et al., ''Effect of yeast extract on the degradation of organophosphorus insecticides by soil enrichment and bacterial cultures,'' Canadian Journal of Microbiology, vol. 35, no. 12, pp. 1105-1110, 1989. [ Links ]
[12] Y.-H. Zhang et al., ''Prediction for the mixture toxicity of six organophosphorus pesticides to the luminescent bacterium Q67,'' Ecotoxicology and Environmental Safety, vol. 71, no. 3, pp. 880-888, 2008. [ Links ]
[13] P. H. Howard, Handbook of Environmental Fate and Exposure Data for Organic Chemicals, Chelsea: Lewis Publishers, 1991, 712 p. [ Links ]
[14] S. R. Caldwell, y F. M. Raushel, ''Detoxification of organophosphate pesticides using a nylon based immobilized phosphotriesterase from Pseudomonas diminuta,'' Applied Biochemistry and Biotechnology, vol. 31, no. 1, pp. 57-73, 1991. [ Links ]
[15] L. L. Harper et al., ''Dissimilar plasmids isolated from Pseudomonas diminuta MG and a Flavobacterium sp. (ATCC 27551) contain identical opd genes,'' Applied Environmental Microbiolology, vol. 54, no. 10, pp. 2586-2589, 1988 [ Links ]
[16] G. Chaudhry et al., ''Isolation of a methyl parathion-degrading Pseudomonas sp. that possesses DNA homologous to the opd gene from a Flavobacterium sp.,'' Applied Environmental Microbiolology, vol. 54, no. 2, pp. 288-293, 1988. [ Links ]
[17] S. Malghani et al., ''Isolation and characterization of a profenofos degrading bacterium,'' Journal of Environmental Sciences, vol. 21, no. 11, pp. 1591-1597, 2009. [ Links ]