Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Biotecnología en el Sector Agropecuario y Agroindustrial
Print version ISSN 1692-3561
Rev.Bio.Agro vol.10 no.1 Popayán Jan./June 2012
USO DE HOJARASCA DE ROBLE y BAGAZO DE CAÑA EN LA PRODUCCIÓN DE Pleurotus ostreatus
USE OF THE OAK DEAD LEAVES AND SUGAR CANE BAGASSE IN THE Pleurotus ostreatus PRODUCTION
USO DA SERAPILHEIRA DE CARVALHO E BAGAÇO DA CANA NA PRODUÇÃO DO Pleurotus ostreatus
PILAR SUDIANY VARGAS1, JOSE LUIS HOYOS2, SILVIO ANDRÉS MOSQUERA3
1 Ing. Forestal. Facultad de Ciencias Agropecuarias. Universidad del Cauca. Popayán. Colombia.
2 Mg. Ingeniería. Profesor Asociado Facultad de Ciencias Agropecuarias. Universidad del Cauca. Popayán. Colombia.
3 Mg. Ingeniería. Profesor Titular Facultad de Ciencias Agropecuarias. Universidad del Cauca. Popayán. Colombia.
Correspondencia: jlhoyos@unicauca.edu.co
Recibido para evaluación: 10/05/2011. Aprobado para publicación: 21/03/2012
RESUMEN
Se evaluó hojarasca de roble en un relicto de bosque en la Vereda La Capilla de Cajibío (Cauca) durante 6 meses, como sustrato para el crecimiento del hongo Pleurotus ostreatus, eligiendo árboles maduros con DAP entre 35 y 37 cm, obteniéndose un promedio de 7,41 kg de hojarasca por árbol. Se evaluó el crecimiento del hongo en hojarasca mezclada con bagazo de caña y 5 sustratos: T1: bagazo 100%, T2: roble 100%, T3: roble 75% y 25% de bagazo, T4: roble 50% y 50% bagazo y T5: roble 25% y 75% bagazo, logrando eficiencias biológicas de 221,1%, 44,35%, 52,78%, 90,30% y 109,12% respectivamente. Se observó relación inversa entre el contenido de hoja de roble y las eficiencias debido a la naturaleza coriácea y cerosa de la hoja. La mayoría de los carpóforos presentaron 5 a 12 cm de diámetro y contaminación causada por hongos competidores del género Trichoderma sp. Se detectaron cambios en la composición del sustrato agotado, principalmente incremento de minerales y proteínas y disminución de fibra en el bagazo de caña y en la hojarasca de roble, siendo apto para alimentación de animales poligástricos por el contenido de proteína micelial, presencia de celulosa y menor contenido de lignina.
PALABRAS CLAVES: Quercus humboldtii, Eficiencia biológica, Tamaño de carpóforos.
ABSTRACT
In order to assess the use as growing substrate for the fungus Pleurotus ostreatus, falling of the oak dead leaves in a forest relict in La Capilla rural area, Cajibio (Cauca) was evaluated during 6 months, choosing mature trees with a chest height diameter (DAP) between 35 and 37 cm were chosen, getting an average of 7,41 kg of dead leaves per tree. Fungus growing in oak dead leaves mixed with sugar cane bagasse and 5 substrates: T1: bagasse 100%, T2: oak 100%, T3: oak 75% and bagasse 25%, T4: oak 50% and bagasse 50% and T5: oak 25% and bagasse 75% reaching biological efficiencies of 221,1%, 44,35%, 52,78%, 90,30% and 109,12% respectively. Was an inverse association between the content of oak leaf and efficiencies due to the nature leathery and waxy leaf. Most of the carpophores showed 5 and 12 cm and contamination caused by competing fungi of the Trichoderma sp. genus. Changes were detected in the depleted substrate composition, mainly minerals and protein increase and decrease of fiber in the bagasse and oak litter, being suitable for animal feed polygastric for mycelial protein content, presence of cellulose and lower lignin content.
KEYWORDS: Quercus humboldtii, Biological efficiency, Carpophores size.
RESUMO
Avaliamos a produção de serapilheira em uma floresta na aldeia La Capilla de Cajibío, (Cauca), por 6 meses, como substrato para o crescimento do fungo Pleurotus ostreatus, escolhendo árvores maduras com DAP entre 35 e 37 cm, produzindo uma media de 7,41 kg de lixo por árvore. Avaliou-se o crescimento do fungo em folhas misturadas com bagaço de cana e 5 substratos: T1: bagaço de 100%, T2: carvalho de 100%, T3: carvalho 75% e 25% de bagaço, T4: carvalho 50% e bagaço 50% e T5: carvalho de 25% e 75% do bagaço, alcançando eficiências biológicas de 221,1%, 44,35%, 52,78%, 90,30% e 109,12%, respectivamente. Era uma associação inversa entre o conteúdo de folha de carvalho e eficiência devido à natureza de couro, folha waxy. A maioria dos carpóforos mostrou 5 a12 cm de diâmetro e contaminação causada por fungos competidores do gênero Trichoderma sp. Foram detectadas alterações na composição do substrato esgotado, principalmente aumento de minerais e proteínas e decresceu na fibra o bagaço de cana e folhas de carvalho, sendo apropriado para alimentar animais poligástricos, para à proteína micelial disponível, presença celulose e teor de lignina reduzido.
PALAVRAS CHAVE: Quercus humboldtii, Eficiência biológica, Tamanho do carpóforos
INTRODUCCIÓN
Actualmente, el desarrollo de actividades productivas en cultivos agrícolas y forestales y los procesos industriales relacionados con estos, generan grandes cantidades de residuos considerados de bajo valor económico: la perspectiva de estos residuos está progresando ya que a nivel mundial se están usando en la producción de energía y otros procesos.
El roble (Quercus humboldtii), una especie que se encuentra entre 1.500 y 3.000 msnm, es maderable y de fácil comercialización. En el Cauca ocupa un área de gran dimensión y produce un volumen importante de hojarasca que se incorpora al suelo, por lo que se hace necesario implementar un modelo sostenible de aprovechamiento que beneficie al bosque y también a la comunidad [1]. La hojarasca del roble hace parte del suelo del bosque y de un ciclo natural de regeneración del follaje que cuenta con alto contenido en lignocelulosa, minerales y carbohidratos; esta hojarasca es colonizada por bacterias y hongos que propician el proceso de descomposición de polímeros [2]. De otro lado, un subproducto de la industria panelera que se obtiene en grandes cantidades en Colombia y en el Cauca es el bagazo de la caña panelera (Saccharum officinarun) que posee elevado contenido de celulosa y hemicelulosa aptos para el cultivo de hongos comestibles como el Pleurotus ostreatus, el cual se alimenta de material vegetal como cáscaras, semillas, madera entre otros [3].
Los hongos del género Pleurotus son los más fáciles y menos costosos de producir, debido a la alta adaptabilidad, agresividad y productividad, además tienen la habilidad de descomponer troncos de madera y crecer sobre en diferentes residuos orgánicos. Presentan buen desarrollo en la mayoría de maderas duras, sobre los productos secundarios de la industria maderera, en la paja de los cereales, la caña de azúcar y bagazos, residuos de café, hojas de plátano y cáscaras de semillas oleaginosas [3]. Los nutrientes necesarios para el crecimiento y desarrollo de los hongos comestibles son fundamentalmente carbohidratos (celulosa y hemicelulosa), compuestos nitrogenados (por adición de compuestos que poseen nitrógeno como los sulfatos de amonio, urea o gallinaza) y minerales [4].
Estudios previos han reportado que la producción del hongo Pleurotus ostreatus a partir de desechos agrícolas (aserrín, pulpa de café, hoja de caña y pasto King Grass) encontrando que se puede producir a gran escala sobre pasto King grass y hoja de caña, pero presentó inconvenientes para crecer sobre pulpa de café por contaminación con otros microorganismos [5], lo cual se corrigió mejorando los métodos de esterilización del sustrato; el protocolo establecido puede ser aplicado por los pequeños caficultores [3]. El desarrollo del hongo sobre cascarilla de café, pasto King Grass, vainas de arveja, vainas de fríjol y espárragos indicó que el agua hirviendo fue el método más efectivo para la desinfección de los sustratos y que el mejor fue la vaina de fríjol, en contraste con la cascarilla de café que presentó los más bajos rendimientos por su menor porcentaje de proteína [6].
Otros autores [7] valoraron la producción del hongo en cascarilla de café y vainas de fríjol, así como el efecto del sustrato agotado adicionado como enmienda al suelo en cultivo de maíz y fríjol, en dos cosechas: en la primera, T2 (50% cascarilla y 50% vaina de fríjol) permitió aumentar la producción en 11% sobre T1 (100% cascarilla de café), aunque el análisis de varianza no mostró diferencias significativas entre ellos. En la segunda cosecha solo se evaluó el sustrato con 100% de cascarilla como enmienda del suelo y disminuyó las concentraciones de otros elementos como Ca, Mg, K, P, entre otros [7].
En la zona cafetera, se evaluó el crecimiento del hongo sobre residuos (pulpa de café, aserrín de tallo de café, borra de café, granos deteriorados de café, cisco de café, bagazo de caña, película plateada de café, cascarilla de arroz y hoja de plátano); obteniendo que el sustrato de mayor rendimiento fue la mezcla de pulpa de café con bagazo de caña, seguido por la mezcla de borra de café con tamo de arroz y cascarilla de arroz, pero la mejor formulación fue la mezcla de aserrín de tallo y pulpa de café, por su alta disponibilidad y con eficiencia biológica de 88,9% [3].
En un trabajo similar se valoró la producción del hongo sobre tres sustratos a base de pulpa de café (S1: 100% pulpa de café; S2: 50% pulpa de café + 50% bagazo de caña; S3: 50% pulpa de café + 50% pasto de corte King Grass),con cuatro métodos de esterilización (N: no esterilización; Q: esterilización química; V: esterilización con vapor de agua y E: esterilización con agua en ebullición), siendo el mejor tratamiento con agua en ebullición, mostrando diferencias significativas entre los tratamientos en la segunda etapa de producción y la prueba de Duncan reportó que T1 (79,3%) fue el mejor sustrato [8]. Se estudió el potencial de residuos como astillas de álamo, astillas de eucalipto, mezcla de paja de trigo y eucalipto, y paja de trigo para sustrato, encontrando que la paja de trigo y la mezcla de paja de trigo más eucalipto son aptos para el cultivo de Pleurotus ostreatus [9].
El objetivo del presente trabajo fue evaluar el potencial del uso de la hoja de roble en la inclusión de las formulaciones convencionales de sustratos para hongos comestibles y su efecto en los parámetros productivos.
MÉTODO
El relicto de bosque de roble en el cual se cuantificó y colectó la hojarasca está ubicado en la Vereda La Capilla del Municipio de Cajibío, Departamento del Cauca, a una altura de 1.765 msnm con precipitación de 2.000 mm anuales, temperatura promedio de 19°C y clima templado [10]. El invernadero en el que se realizó la incubación y la fructificación del Pleurotus ostreatus se localiza en Popayán, Departamento del Cauca, a 1.738 msnm, temperatura media de 19°C y humedad relativa del 77% [11]. Se usó el laboratorio de biotecnología de la Facultad de Ciencias Agropecuarias de la Universidad del Cauca, Vereda Las Guacas, para las pruebas microbiológicas de la hojarasca de roble y pruebas de secado de los sustratos.
Obtención y cuantificación de hojarasca y bagazo de caña. Se ubicaron 12 trampas de 50 cm de diámetro y 50 cm de profundidad, a 1 m del suelo para la evaluación de la producción de hojarasca de roble [12] en árboles con 22 y 25 m de altura medida con el Hipsómetro de Merrit y diámetro a la altura del pecho (DAP) de 35 y 37 cm medido con cinta diamétrica, siendo estos parámetros indicadores de árboles de gran porte [13]. Los árboles se seleccionaron según muestras representativas para un área de 2.500 m2 [14] y la cuantificación de la hojarasca se hizo cada 15 días durante 6 meses (septiembre a febrero). El bagazo de caña se obtuvo del trapiche El Lago ubicado en la zona y se depositó en bolsas de yute para la desinfección.
Cultivo del hongo. Una vez colectados los materiales para el sustrato, se realizó el cultivo siguiendo un diseño completamente al azar con cinco tratamientos y tres réplicas para un total de 15 unidades experimentales de 2 kg cada una: T1: 100% bagazo de caña o testigo; T2: 100% roble; T3: 75% de roble y 25% de bagazo de caña; T4: 50% de roble y 50% de bagazo de caña y T5: 25% de roble y 75% de bagazo de caña. Se realizó el análisis de varianza (ANAVA) y la prueba de Tukey con un a=0,05, para determinar diferencias significativas entre las fórmulas, en la etapa de colonización y producción. Se siguieron los siguientes procesos:
Adquisición del hongo. La semilla del hongo se adquirió de FUNGITECH de Bogotá, en granos de cebada.
Adecuación del sustrato. Recolectada la hoja de roble, se secó con radiación solar hasta obtener una humedad del 10%, con el objeto de facilitar el triturado. Se remojó 24 horas, ya que esta hoja tiene una superficie coriácea, lo que impide la absorción de humedad y la colonización del hongo. El bagazo de caña no fue pretratado como la hojarasca de roble; para la desinfección del material se aplicaron dos tratamientos térmicos: vapor de agua a 60°C durante 9 horas [15] e inmersión en agua en ebullición en diferentes tiempos (0, 2, 4, 6, 8, 10 horas), el efecto del tratamiento se evaluó sembrando el material tratado en cajas de Petri con medio Papa-Dextrosa-Agar (PDA), durante 2 días.
Inoculación. La semilla del hongo se retiró de la nevera 3 horas antes para acondicionarla y se sembrarla sobre el sustrato a temperatura ambiente; el sitio de inoculación se desinfectó con solución de hipoclorito de sodio a 250 ppm. La tasa de inoculación fue del 4% y se agregó 3% de carbonato de calcio para evitar el desarrollo de microorganismos. Se empacó en bolsas transparentes de polipropileno y posteriormente en bolsas plásticas negras para contribuir a su debido desarrollo, luego de lo cual se hicieron 40 perforaciones de 1 cm de diámetro a cada bolsa para regular la humedad en el sustrato.
Incubación. Se realizó en invernadero desinfectado con cal y cubier to con plástico transparente y polisombra para evitar la exposición directa a la radiación. La temperatura de incubación fue de 18 a 20°C y las bolsas se suspendieron a una altura de 1,5 m, separadas unas de otras por 50 cm.
Fructificación. Se retiró la bolsa negra para dar lugar al crecimiento de los primordios, con una temperatura de 18 a 19°C y 80 a 85% de humedad relativa. Estas condiciones se consiguieron humedeciendo el cuarto con agua potable mediante 2 a 4 microaspersiones por día. Los bloques fueron separados a 70 cm para dar espacio al crecimiento de los carpóforos y facilitar su recolección.
Cosecha. Los hongos se cosecharon cuando su parte superior estuvo plana (momento en el cual alcanza su máximo crecimiento), cortando por la base del tallo en el punto de unión con el sustrato.
Variables de respuesta
Se utilizaron los siguientes indicadores:
Colonización. Se tomó un patrón de medida de 8 cuadrículas de 4x5 cm y se midió el área colonizada en la superficie de la bolsa (porcentaje de colonización) [6].
Contaminación. Igual que en la colonización (porcentaje de contaminación).
Producción de setas. Se evalúo la producción en cada unidad experimental, tomando el peso de las setas obtenidas, evaluando 3 cosechas consecutivas con un tiempo de 10 días entre cada una, determinando la eficiencia biológica (EB) en cada tratamiento así [16]:

Calidad de las setas. Se tuvieron en cuenta el color, la forma, el olor, el tamaño y el estado fitosanitario de los hongos.
Tiempo de evaluación. Se evaluaron las unidades durante 2 meses, período de la incubación del micelio y fructificación de la seta.
Análisis proximal del sustrato inicial y final. Se determinaron los contenidos de proteína, grasa, fibra, carbohidratos, ceniza y extracto no nitrogenado [17].
RESULTADOS
Cuantificación de hojarasca. Octubre presentó la mayor cantidad de hojarasca con 3,29 kg y septiembre la menor con 1,50 kg, con un promedio por árbol de 7,41 kg, mostrando una caída de hojas permanente, coincidiendo con [14] en la uniformidad de la distribución de la hojarasca sobre el suelo.
Los valores se compararon con los de un relicto de bosque montano andino en donde se reportaron 7.877,2 kg/ha.año de hoja verde con una densidad de 358 árboles/ha, para un promedio de 11 kg/ árbol cada 6 meses, valores ligeramente superiores al del bosque submontano, debido posiblemente a las condiciones ambientales predominantes y a la ubicación de las trampas: elevados valores de hojarasca se alcanzan con trampas ubicadas a mayor altura [18], por lo que trampas ubicadas a 1 m del suelo podrían no interceptar la hojarasca que queda atrapada por las epífitas, por la vegetación intermedia y sotobosque. Otro aspecto a considerar es que la zona presenta intervención antrópica y de animales, lo que puede generar ambientes contrastantes (matriz antrópica y bosque) que interactúan entre sí a través de un límite o borde, los ambientes son zonas transicionales donde el microclima, la vegetación y la fauna pueden verse afectados, produciéndose un efecto de borde [19].
Cultivo del hongo. En el tratamiento térmico con vapor a 60°C durante 9 horas hubo contaminación superior al 50% en la hoja de roble, que contribuyó con la exterminación de la flora bacteriana protectora del sustrato que compite con microorganismos, aumentando el ataque por Trichoderma spp y otros [20]. Cuando se usó el tratamiento por inmersión en agua a 90°C usando diferentes tiempos (0, 2, 4, 6, 8 y 10 horas), a partir de 2 horas se observó un efecto de inhibición en la contaminación.
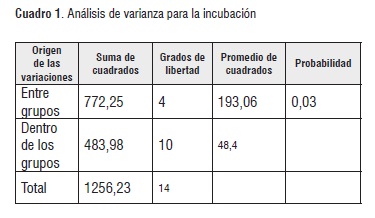
El hongo competidor propagado en medio PDA coincidió con el hongo presente en el cultivo, un moho verde spp (vigoroso colonizador de la materia orgánica, especialmente si esta tiene elevada proporción de carbohidratos) que cuando está presente en la semilla acidifica el sustrato y dificulta el crecimiento del micelio, disminuye la producción a temperaturas entre 22 y 27°C, humedad alta y pH bajo [15]. Teniendo en cuenta estos resultados, se inició el cultivo con mejores condiciones higiénicas, sin embargo, se evidenció contaminación en los tratamientos (excepto T1). El análisis de varianza mostró diferencias significativas (Cuadro 1) entre los tratamientos, siendo T2 el de mayor porcentaje de contaminación con 35%, seguido de T3 con 10%, T4 con 5,3% y T5 con 3,9%.
Colonización. El análisis de varianza indicó que la colonización en el día 8 presentó diferencias significativas para a=0,05 (Cuadro 2), en tanto que la prueba de Tukey indicó que T1 (a) fue diferente de T3, T4 y T5 (b) los cuales presentaron promedios de colonización menores y T2 representada con (c), fue la fórmula con más bajo porcentaje de colonización del micelio (Cuadro 3).


El análisis de varianza del día 16 arrojó comportamiento diferente en los 5 tratamientos: según la prueba de Tukey, los tratamientos T1, T4 y T5 (a) no son diferentes entre sí arrojando los promedios de colonización más altos, pero los tratamientos T2 y T3 (b) son diferentes con promedios de colonización más bajos. En el día 20, el T1 no se valoró por cuanto colonizó completamente a los 16 días y fue aislado para continuar con la etapa de fructificación. Los tratamientos restantes no presentaron diferencias significativas. El cuadro 3 muestra que la colonización o crecimiento del micelio del hongo (en porcentaje) aumentó con el tiempo (20 días) en todos los tratamientos, siendo el bagazo de caña el de mayores niveles en el día 16, mientras que el roble obtuvo una colonización mayor en el día 20, 5 días después del bagazo.
El alto grado de colonización del bagazo de caña se debe a su estructura con fibras longitudinales y diámetros diferentes: las fibras corticales sirven de sostén y las fibras medulares para la circulación de agua y sales con una consistencia esponjosa [21]. La estructura de la hoja de roble es esclerófila o coriácea debido al desarrollo del tejido esclerenquimático rico en lignina, además de tener recubrimiento ceroso en la cutícula [22], originando que la degradación de celulosa y hemicelulosa sea más lenta, ya que los microorganismos deben primero degradar la lignina suavizando el sustrato para llegar a dichas macromoléculas [23], sumado a la baja capacidad de retención de humedad en la superficie, afectando el crecimiento del micelio [24].
Producción de setas. El cuadro 4 presenta la producción de setas, en donde la primera cosecha (Figura 1) se presentó luego de 4 semanas de iniciado el ciclo de cultivo.


El tratamiento T1 arrojó 248,33 g por unidad experimental de 2 kg de sustrato, siendo mayor a 228,33 g y 121,67 g en cosechas posteriores, con comportamiento similar en las otros tratamientos. La producción de setas tuvo disminución durante las cosechas por el agotamiento del sustrato que pierde peso y materia orgánica [15], implicando una disminución en la cantidad de nutrientes y por tanto disminución en el rendimiento. La producción promedio de hongos en sustrato de pulpa de café en la primera cosecha fue de 248,33 g, pero con unidades experimentales de 3 kg, lo que indica 86 g/kg de sustrato [10], mientras que el bagazo de caña en la primera cosecha arrojó 248,33 g con una unidad experimental de 2 kg, con un valor de 124,17g/kg de sustrato, valor mayor que el de pulpa de café; otros sustratos como la pulpa y el pasto King Grass arrojaron valores de 385 g/kg de sustrato y 128,33 g/kg de sustrato respectivamente [8], valor mayor que los mencionados, por lo que se puede deducir que la producción promedio de hongos es diferente en cada sustrato por lo que debe ser evaluado según su naturaleza física y química.
Se determinó el rendimiento (porcentaje en base seca) de las setas producidas en cada tratamiento, utilizando como indicador la eficiencia biológica (EB), obteniéndose valores para T1 de 221,1%, T2 de 44,4%, T3 de 52,8%, T4 de 90,3% y T5 de 109,1%. A mayor contenido de bagazo de caña mayor EB por la composición y estructura que permite buena aireación y capacidad para retener humedad, registrándose eficiencias biológicas de 108% y superiores de 195% [7]. Los bajos rendimientos de algunos sustratos lignocelulósicos se pueden mejorar mediante compostaje, utilizando mezclas de lignocelulósicos y con aditivos minerales u orgánicos [25].
El bajo valor de EB en T2 se debe a la naturaleza del sustrato, ya que la hoja de roble es esclerófila y se relaciona con su dureza por la lignina que evita el marchitamiento de las hojas en condiciones de sequía [26]. El cultivo de P. ostreatus en hojarasca de almendro (Terminalia catappa) reportó una eficiencia biológica de 44,47%, la cual es similar a la obtenida en la hojarasca de roble, ya que el almendro tiene hojas coriáceas, mientras que en bagazo de caña los resultados fueron de 221,1%, similar a [7] que reportaron EB de 195,65% en bagazo de caña con semillas de guayaba.
El análisis de varianza para la eficiencia biológica (Cuadro 5) arrojó diferencias significativas entre los tratamientos y la prueba de Tukey indicó que T1(a) es diferente de los tratamientos restantes, presentándose como aceptables los tratamientos T4(c) y T5(b). Se presentaron diferencias entre la primera, segunda y tercera cosecha, debido a la composición fisicoquímica, lo cual hace que la disponibilidad de los nutrientes necesarios para el crecimiento y desarrollo del hongo P. ostreatus se dé en distintos grados, sumado al agotamiento de las mismas [5].
Calidad de las setas. El color de las setas en los primeros días de fructificación fue gris claro y disminuyó de intensidad a medida que creció, para finalmente ser de color blanco castaño con sabor agradable, lo cual se considera normal [27]. La forma del sombrero o el píleo fue redonda, con la superficie lisa, abombada y convexa, en forma de ostra o concha. El tamaño de las setas cosechadas en su madures se caracterizó por alcanzar diámetros de 5 a 12 cm y peso entre 50 y 80 g, al igual que [23].
Composición nutricional de sustratos. Los resultados de los análisis proximales iniciales y finales de los sustratos de hoja de roble y del bagazo se muestran en el Cuadro 6: Los hongos son organismos que degradan eficientemente la lignina gracias a las enzimas que metabolizan [28], razón por la que se observan diferencias entre el sustrato inicial y el final debido al agotamiento que sufre el sustrato, perdiendo peso y disminuyendo los nutrientes, afectando el rendimiento de producción [15].
El incremento del porcentaje de cenizas se debió a la adición de 5% de carbonato de calcio en la adecuación, como protector y antagonista de algunos microorganismos competidores, además de controlar la acidez de dicho sustrato [29], mientras que el extracto etéreo se incrementó debido a la pérdida de materia orgánica, lo que hace que se incremente su concentración [3].
El considerable contenido de extracto no nitrogenado puede obedecer a que en esta fracción se agrupan mono y disacáridos, la parte soluble de la celulosa, pentosanas y lignina, hemicelulosas, almidón, inulina, toda clase de azúcares, materias pécticas, ácidos orgánicos y otras materias solubles libre de nitrógeno [30], que junto con la fibra bruta, constituyen la principal fuente de carbono necesaria para los procesos metabólicos y para la formación de estructuras celulares [31]. Este hecho explica la tardanza en la incubación en el sustrato a base de hoja roble por la presencia de lignina que actúa como compactante de la estructura del complejo lignocelulósico, impidiendo una colonización completa de P. ostreatus y la penetración de las enzimas destructivas en la pared celular, dificultando la digestibilidad de la fibra. La fibra bruta está constituida por hemicelulosa, celulosa y lignina; su contenido disminuyó, lo cual es favorable porque las especies de Pleurotus son capaces de degradar materiales ricos en estos compuestos. El incremento en la proteína bruta indica que el P. ostreatus tiene una alta capacidad de síntesis de proteína en el crecimiento sobre el bagazo de caña [24].
CONCLUSIONES
El sustrato de hojarasca de roble arrojó resultados aceptables para la producción de P. ostreatus, con una eficiencia biológica de 44,35%, sin embargo, para alcanzar valores superiores es necesario realizar pretratamientos que permitan el ablandamiento de las fibras, así como formular el sustrato con materiales asequibles a la degradación por el hongo.
La contaminación en el cultivo fue controlada aplicando tratamiento térmico con inmersión en agua en ebullición por tiempos superiores a 2 horas, además de controlar las condiciones ambientales y sanitarias del cuarto de incubación y fructificación de las setas.
El sustrato agotado mostró una disminución significativa en la materia orgánica, contenido de lignina, celulosa y hemicelulosa, indicio de una degradación parcial del sustrato. En el sustrato ciento por ciento hojarasca de roble no hubo una degradación eficiente de la lignina por parte del P. ostreatus, debido a la naturaleza dicho sustrato, lo que afectó la colonización del micelio y la producción de carpóforos.
El sustrato agotado por el hongo P. ostreatus puede ser evaluado en la alimentación de rumiantes, debido al contenido de proteína micelial disponible, celulosa para su biota intestinal y menor contenido de lignina la cual no es digerida por estos animales. Además, también puede ser utilizado como compost en el suelo, incrementando los niveles de materia orgánica.
AGRADECIMIENTOS
Los autores expresan su agradecimiento a la Universidad del Cauca por el recurso humano y las instalaciones facilitadas para el desarrollo del proyecto.
REFERENCIAS
[1] DANTART, A. y FERNANDEZ, A. Por tal de Ciencia y Tecnología. Robledales en Colombia [online]. Available: URL: http://e-ciencia.com/recursos/monografias/ecologia/robledales-en-colombia.html [citado 25 de febrero de 2010] [ Links ].
[2] JOHNSON, E. y CATLEY, K. American Museum of Natural History. Lacias vida en la hojarasca. [online]. Available: URL: http://cbc.amnh.org/center/pubs/pubscbcinverts.php?npid=23[citado15 marzo de 2010] [ Links ].
[3] RODRÍGUEZ, N. y JARAMILLO, C. Cultivo de hongos comestibles del género Pleurotus sobre residuos agrícolas de la zona cafetera. Chinchiná (Caldas): Cenicafé, 2005, p. 5-52. [ Links ]
[4] SARDSUD, U. Nutricional requirements of Pleurotus ostreatus. Phillipine Agriculturist, 64 (1), 1981. [ Links ]
[5] PAZ I., NARVAEZ, HURTADO L. Eficiencias de sustratos de origen vegetal para la producción del hongo Pleurotus ostreatus en Timbío, Cauca [Tesis Administración de Empresas Agropecuarias]: Popayán (Colombia): Fundación Universitaria de Popayán, 1995, p. 35-45. [ Links ]
[6] ASTAÍZA, P., PAZ, I., ORTIZ, B. y URBANO, Z. Determinación de una metodología para la utilización de residuos agrícolas (cascarilla de café, pasto de corte, espárrago, vainas de fríjol y arveja) generados en el Municipio de Popayán y evaluación del efecto de los sustratos en la producción de setas (Pleurotus ostreatus) [Tesis Ingeniería Agroindustrial]. Popayán (Colombia): Universidad del Cauca, Facultad de Ciencias Agropecuarias, 2002, p. 48-54. [ Links ]
[7] BONILLA, A. y PAZ, I. Evaluación de la cascarilla de café como sustrato para la producción de Pleurotus sp y posterior uso como enmienda para el suelo en cultivos de fríjol y maíz [Tesis Ingeniería Agroindustrial]. Popayán (Colombia): Universidad del Cauca, Facultad de Ciencias Agropecuarias, 2005, 101 p. [ Links ]
[8] SARASTI, A. y MUELAS, W. Evaluación de la producción de setas comestibles orellanas (Pleurotus ostreatus) sobre cuatro sustratos a base de pulpa de café, tratados con tres diferentes métodos de esterilización en el Municipio de Piendamó [Tesis Ingeniería Agropecuaria]: Popayán (Colombia): Universidad del Cauca, Facultad de Ciencias Agropecuarias, 2008, p. 52-68. [ Links ]
[9] ARNERO, M.T., QUIROZ, M.S. y ALVAREZ, C.H. Utilización de Residuos Forestales Lignocelulósicos para Producción del Hongo Ostra (Pleurotus ostreatus). Información Tecnológica, 21 (2), 2010, p. 13-20. [ Links ]
[10] COLOMBIA. MUNICIPIO DE CAJIBÍO. Plan de Ordenamiento Territorial del Municipio de Cajibío, Departamento del Cauca. Cajibío (Colombia): 2002. [ Links ]
[11] COLOMBIA. AEROPUERTO GUILLERMO LEÓN VALENCIA. Cartas climatológicas medias mensuales. Popayán (Colombia): 2010. [ Links ]
[12] STOCKER, C., THOMPSON, A., FITZSIMON, K. and THOMAS, R. Annual patterns of litterfall in lowland and tableland rainforest in tropical Australia. Biotropica, 27, 1995, p. 412-420. [ Links ]
[13] NIETO, V.M. y RODRÍGUEZ, J. Juglans neotropica Diels. In Species descriptions. Part II. Corporación Nacional de Investigación Forestal. Bogotá (Colombia), 2006, p. 680. [ Links ]
[14] HIGUERA, D. y MARTÍNEZ, E. Hojarasca y los flujos de nutrientes en el dosel de robles neotropicales bosque nublado – Colombia [onine]. Available: URL: http://www.lyonia.org [citado 28 de enero de 2010] [ Links ].
[15] GARCÍA, M. Cultivo de setas y trufas. 3 ed. Madrid (España): Mundi Prensa, 1998. 260 p. [ Links ]
[16] SALMONES, D., WALISZEWSKI, K.N and GUZMÁN, G. Use of some agroindustrial lignocellulose by products for edible mushroom Volvariella volvacea cultivation. Revista Internacional de Contaminación Ambiental, 12, 1996, p. 69-74. [ Links ]
[17] COLOMBIA. SERVICIOS QUÍMICOS INDUSTRIALES DEL CAUCA (SERVIQUÍMICA). Popayán (Colombia): 2010. [ Links ]
[18] VENEKLAAS, E.J. Litterfall and nutrient fluxes in two montane tropical rain forests, Colombia. J. Trop. Ecol., 7, 1991, p. 319-336. [ Links ]
[19] GOMEZ, J. y GALEANO, G. Influencia de los factores modeladores sobre el efecto de borde, en un relicto de bosque altoandino en Colombia. Acta Biológica Colombiana, 9 (2), 2004. [ Links ]
[20] VELÁZQUEZ, M., CEDEÑO, G., FARNET, A. y SAVOIE, J. Estudio preliminar de la microflora bacteriana termotolerante de la pulpa de café y la paja de trigo con potencial de inhibición contra Trichoderma viride en el cultivo de Pleurotus spp. Revista Mexicana de Micología, 22, p. 33-39. [ Links ]
[21] CENTRAL DE INSUMOS Y MATERIAS PRIMAS PARA LA INDUSTRIA ALIMENTARIA LTDA. Manual para la elaboración de panela y otros derivados de la caña. Colombia: 1992, p 29. [ Links ]
[22] DAVIDSE, G., SÁNCHEZ, M. and KNAPP, S. Flora Mesoamericana: Psilotaceae a Salviniaceae. México: Universidad Autónoma de México, vol. 1, 1995, p. 86. [ Links ]
[23] GUZMÁN, G. El cultivo de los hongos comestibles, con especial atención a especies tropicales y subtropicales en esquilmos y residuos agro-industriales. México: Instituto Politécnico Nacional, 1993, p. 245. [ Links ]
[24] MONTOYA, S. y RESTREPO, G. Evaluación de la síntesis de proteína a partir del crecimiento vegetativo de Pleurotus sp. sobre residuos de algarrobo y uva pasa. Revista Universidad de Caldas, Enero-Diciembre, 2006, p. 23 – 31. [ Links ]
[25] ARENAS, M. Evaluación de numerosos sustratos para el cultivo del hongo Pleurotus ostreatus [Tesis Ingeniería Agronómica]. Medellín (Colombia): Universidad Nacional de Colombia, Facultad de Ciencias Agropecuarias, 1992, 64 p. [ Links ]
[26] ZAMORA, R. y PUGNAIRE, F. Ecosistemas mediterráneos: análisis funcional. Asociación Española de Ecología Terrestre. Consejo Superior de Investigaciones Científicas, 2001, p 109. [ Links ]
[27] GUARÍN, J. y RAMÍREZ, R. Estudio de factibilidad técnico-financiero de un cultivo del hongo Pleurotus Ostreatus [online]. Available: URL: http://www.javeriana.edu.co/biblos/tesis/ingenieria/tesis79.pdf [citado febrero 2 de 2010] [ Links ].
[28] PLATT, M.W., HADAR, Y., HENIS, Y. and CHET, I. Increased degradation of straw by Pleurotus ostreatus sp. florida. European Journal of Applied Microbiology and Biotechnology, 17 (2), 1983, p. 140-142. [ Links ]
[29] GAITÁN, R., SALMONES, D., PÉREZ, R. y MATA, G. Manual práctico del cultivo de setas: aislamiento, siembra y producción. México: Instituto de Ecología, 1 ed., 2006, p. 4 - 20. [ Links ]
[30] BERNAL, I. Evaluación fisicoquímica y bromatológica de la Guayaba Agria (Psidium araca) en dos estados de maduración. Revista CENIC Ciencias Biológicas, 36, 2005. p. 18. [ Links ]
[31] SÁNCHEZ, J. y ROYSE, D. La biología y el cultivo de Pleurotus spp. México. Limusa. Noriega Editores, 2001, p. 141-156. [ Links ]













