Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Biotecnología en el Sector Agropecuario y Agroindustrial
Print version ISSN 1692-3561
Rev.Bio.Agro vol.11 no.1 Popayán Jan./June 2013
ESTUDIO QUÍMICO Y ACTIVIDADES ANTIOXIDANTE Y BACTERICIDA DE Ganoderma applanatum
CHEMICAL STUDY AND ANTIOXIDANT AND BACTERICIDE ACTIVITIE FROM Ganoderma applanatum
ESTUDO QUÍMICO E ATIVIDADE ANTIOXIDANTE E BACTERICIDA DO Ganoderma applanatum
MIGUEL SEGUNDO GUZMÁN N.1 , GILMAR GABRIEL SANTAFÉ P.2, MILADIS MARGOTH SALCEDO L.3, ALBERTO ANTONIO ANGULO O.4
1 Químico. MSc. Docente Departamento de Química, Facultad de Ciencias básicas, Universidad de Córdoba, Montería, Colombia.
2 PhD. Profesor titular Departamento de Química, Universidad de Córdoba Facultad de Ciencias básicas, Universidad de Córdoba, Montería, Colombia.
3 Químico. Departamento de Química, Facultad de Ciencias básicas, Universidad de Córdoba, Montería, Colombia.
4 MSc. Profesor asociado Departamento de Química, Facultad de Ciencias básicas, Universidad de Córdoba, Montería, Colombia.
Correspondencia: msegundoguzman@correo.unicordoba.edu.co
Recibido para evaluación:05/06/2012. Aprobado para publicación: 20/12/2012
RESUMEN
Los hongos han estado en la cumbre de la medicina oriental desde hace 2000 años, los productos derivados de estos organismos actualmente presentan los más altos volúmenes de venta en el mercado de alimentos saludables en países como Taiwán y China. Del extracto etanólico del hongo macromiceto Ganoderma applanatum se aisló por Cromatografía en Columna sobre silica gel la fracción esterólica. Los esteroles presentes en esta fracción fueron analizados por Cromatografía de Gases de Alta Resolución acoplada a Espectrometría de Masas (CGAR-EM), lográndose la identificación de 9 compuestos esteroidales, seis de los cuales, los compuestos 1, 3, 4, 7, 8 y 9 se reportan por primera vez en G. applanatum. Al evaluar la actividad antioxidante del extracto etanólico mediante los métodos ABTS y DPPH se encontraron valores de IC50 = 15,274 µg/mL y 20 µg/mL, respectivamente, mientras que para el extracto de diclorometano se obtuvieron valores de IC50 = 10,78 µg/mL para ABTS y 27,82 µg/mL para DPPH. Los extractos etanólico y de diclorometano mostraron buena actividad bactericida a una concentración de 150 mg/mL frente a la bacteria Staphylococcus aureus.
PALABRAS CLAVES: Cromatografía de Gases, ABTS, DPPH, Staphylococcus aureus.
ABSTRACT
Fungus have been at the top of oriental medicine for 2000 years, the products derived from these organisms now have the highest sales volume in the health food market in countries like Taiwan and China. The sterolic fraction was isolated from the ethanolic extract obtained from mushroom G. applanatum by chromotaghaphy columns on silica gel. Its chemical analysis was done through High Resolution Gas Chromotaghrophy coupled to Mass Expectrometry identifying 9 sterolic compounds, six of which compounds 1, 3, 4, 7, 8 and 9 are reported for the first time in G. applanatum. The evaluation of the antioxidant activity for the ethanolic extract was carried out by DPPH and ABTS methods finding values IC50 of 15,274 µg/mL and 20 µg/mL, respectively. While for the dichloromethane extract values were IC50= 10,78 mg/mL for ABTS and 27,82 g/mL for DPPH. The ethanolic and dichloromethane extracts showed good bactericidal activity at a concentration of 150 mg/mL against the bacterium S. aureus.
KEY WORDS: Gas Chromotaghrophy, ABTS, DPPH, Staphylococcus aureus.
RESUMO
Os fungos têm estado no topo da medicina oriental há 2.000 anos, os produtos derivados dessas organismos atualmente têm o maior volume de vendas no mercado de alimentos saudáveis em países como Taiwan e China. Extracto etanólico do fungo macromiceto Ganoderma applanatum foi isolado por cromatografia em coluna de sílica gel esterol fracção. Esteróis presentes nesta fracção foram submetidos a Cromatografia Gasosa do Alta Resolução acoplada a Espectrometria de Massa (HRGC-MS), permitindo a identificação de 9 compostos esteróides, seis dos quais os compostos 1, 3, 4, 7, 8 e 9 são relatados pela primeira vez em G. applanatum. Na avaliação da actividade antioxidante de extracto de etanol por ABTS e métodos DPPH foram encontrados valores de IC50 = 15,274 µg/mL e 20 µg/mL, respectivamente, enquanto que para os valores de extracto de diclorometano foram IC50 = 10,78 µg/mL para ABTS e 27,82 µg/mL para DPPH. Extractos etanólicos e diclorometano mostraram boa actividade bactericida a uma concentração de 150 mg/mL contra Staphylococcus aureus.
PALABRAS CHAVES: Cromatografia Gasosa, ABTS, DPPH, Staphylococcus aureus.
INTRODUCCIÓN
Los procesos oxidativos han sido relacionados con múltiples afecciones, entre las que se encuentran aquellas que involucran el deterioro del sistema nervioso central; además son causantes de alteraciones de un buen número de productos relacionados con la industria alimenticia debido principalmente, al detrimento de sus propiedades organolépticas. En respuesta a esta problemática, en los procesos industriales se ha tenido que recurrir al uso de algunos agentes antioxidantes de origen sintético como el Hidroxitolueno butilado (BHT) y el Hidroxianisol butilado (BHA), aunque existen sospechas de que estos dos compuestos son responsables de daños en el hígado y carcinogénesis [1]. Los antioxidantes constituyen un tipo de aditivos alimentarios destinados a impedir o retardar las oxidaciones catalíticas y el enranciamiento natural provocado por la acción de diversos agentes como el aire, luz, calor y radiación. Con este conocimiento, diversos autores han dedicado esfuerzos para demostrar el valioso potencial de algunos materiales subutilizados o de escaso interés comercial, como fuente de compuestos antioxidantes, este es el caso de los hongos comestibles y medicinales [1].
A través de los años, el cuerpo fructífero de los hongos ha sido de gran utilidad en el mundo de la medicina, recientemente, el interés en su estudio se ha incrementado debido, fundamentalmente, a que se han encontrado metabolitos secundarios que podrían potencialmente ser utilizados en la industria farmacológica para el tratamiento de diferentes enfermedades y aplicaciones en el sector agroindustrial, en este grupo de setas estudiadas se encuentran las del género Ganoderma. Varios cientos de compuestos químicos con diversas estructuras, tales como triterpenoides, polisacáridos, proteínas, aminoácidos, nucleósidos, esteroides, alcaloides, ácidos grasos y enzimas, han sido aislados del micelio y cuerpo fructífero de diferentes especies del género Ganoderma. Algunos de estos compuestos han demostrado tener una gran aplicabilidad en la farmacología [2,3]. Esta amplia gama de metabolitos secundarios es debida principalmente a que los hongos son incapaces de sintetizar macromoléculas a partir del dióxido de carbono y la energía procedente de la luz por el hecho de no poseer clorofila, por lo tanto, su biogénesis está condicionada principalmente por el tipo de nutrientes que conforman el sustrato donde se desarrollan, además de las condiciones climáticas que los rodean, haciendo que hongos presentes en regiones diferentes o que crezcan en sustratos que varíen en composición, puedan alterar y cambiar su metabolismo generando una amplia variedad de compuestos químicos [4].
En la bibliografía especializada se ha documentado que hongos del género Ganoderma (G. lucidum, G. tsugae, G. applanatum, G. concinna) biosintetizan sustancias que generan importantes beneficios en la salud de animales y humanos por tener efectos hepatoprotectivos, antioxidantes, protección cardiovascular y antibacterial, entre otros [2,5,7].
En trabajos realizados en nuestro grupo de investigación se informó sobre la identificación de cinco nuevos productos naturales aislados del hongo Ganoderma lucidum, y tres del hongo Ganoderma concinna, a los cuales les fue evaluada su capacidad antioxidante obteniendo resultados promisorios [8].
Enmarcados por el contexto anterior, en este trabajo se propone estudiar químicamente el extracto etanólico del hongo Ganoderma applanatum y determinar su posible actividad antioxidante y antibacterial.
MÉTODO
Recolección
Los especímenes del hongo Ganoderma applanatum fueron recolectados en la sede principal de la Universidad de Córdoba, en Montería, zona tropical caracterizada por una temperatura 28°C, humedad relativa del 80% y precipitación promedia anual de 1200 mm, 48 m.s.n.m.
Extracción
El material recolectado fue sometido a percolación en etanol y posteriormente concentrado obteniéndose de esta forma el extracto etanólico crudo. Posteriormente, el extracto etanólico (23,1 g) fue sometido a fraccionamiento mediante partición con una mezcla de diclorometano-agua en una proporción (1:1); este procedimiento se repitió dos veces (2 X 200 mL) para garantizar la máxima extracción de los componentes, obteniéndose una fase acuosa y una orgánica, esta última se separó y se destiló a presión reducida obteniéndose el subextracto de diclorometano (15,9 g).
Fraccionamiento cromatográfico
2 g del subextracto de diclorometano se sometieron a un proceso de separación y purificación mediante cromatografía en columna desarrollada sobre sílica gel (0,063-0,2 mm, Merck®) utilizando como fase móvil un gradiente de polaridad desde Hexano-AcOEt (5:1) hasta MeOH. El monitoreo fue realizado por cromatografía en capa delgada (CCD) con cromatoplacas de aluminio de sílica gel 60F 254 y un espesor de 0,2 mm utilizando como fase móvil mezclas de los solventes antes mencionados y colesterol como sustancia de referencia. La detección se llevó a cabo por medio de una lámpara ultravioleta marca CAMAG (con longitudes de onda de 254 y 366 nm), y solución de ácido fosfomolíbdico al 5% en etanol con posterior calentamiento, como revelador.
Cromatografía de gases de alta resolución acoplada a espectrometría de masas. El análisis por cromatografía de gases de alta resolución acoplada a espectrometría de masas (CGAR-EM) para la fracción esterólica se realizó en un equipo Hewlett Packard 6890 (Columna Capilar HP5 30 m, 0,33 mm diámetro interno y 25 µm de espesor. Gas de arrastre He a 1mL/min., modo split 1:10. Temperatura desde 90°C hasta 310 °C a 10°C/min.), acoplado a un espectrómetro de masas 5973 (70eV en modo scan).
Evaluación de la Actividad antioxidante
Método DPPH. Muestra: se evaluaron los extractos etanólico y el subextracto de diclorometano, para esto se prepararon por triplicado soluciones con concentraciones de 5, 10, 20, 40, 80 y 100 µg/ml del extracto etanólico, en DMSO y posteriormente diluidas con solución de DPPH medidas a una absorbancia ajustada a 0,311, en un espectrofotómetro UV/VIS GENESYS 20, hasta completar 2 ml en el tubo de reacción. Blanco de la muestra: a 20 µl de cada concentración se le adicionaron 1980 µl de Metanol. Referencia: a 20 µl de DMSO se le adicionaron 1980 µl de solución madre de DPPH y se introdujeron en tubo de reacción. Después de incubar a temperatura ambiente por 30 min en la oscuridad se procedió a leer la absorbancia a 517 nm, lo que permitió encontrar el porcentaje de inhibición. Posteriormente, se graficó el porcentaje de inhibición vs la concentración de la muestra para obtener el IC50 es decir, la concentración necesaria para captar el 50% de los radicales libres de DPPH[9].
Método ABTS. Muestra: se prepararon por triplicado soluciones de 1, 5, 10 y 15 ppm del extracto etanólico y el subextracto de diclorometano en DMSO y posteriormente diluidas con solución de ABTS (2,2-azino-bis(3-etilbenzotiazolina-6-sulfonato de amonio) con una absorbancia ajustada a 0.702 nm hasta completar 2 ml en el tubo de reacción. Blanco de la muestra: a 20 µl de cada concentración se le adicionaron 1980 µl de buffer fosfato pH: 7,33. Referencia: a 20 µl de buffer fosfato se le adicionaron 1980 µl de solución de ABTS y se determinó la variación de la absorbancia a 734 nm, luego se graficó el porcentaje de inhibición vs la concentración de la muestra para obtener el IC50.
Evaluación de la Actividad Bactericida
El ensayo de actividad bactericida se realizó empleando el método de Difusión con Disco en Agar, usando las bacterias Staphylococcus aureus (Gram+) y Escherichia coli (Gram-). Se preparó una solución con las bacterias a 108 CFU/mL (Turbidez= McFarland estándar 0,5). La suspensión bacteriana en estudio (Staphylococcus aureus y Escherichia coli) se inoculó de manera uniforme sobre la superficie de una caja de petri que contenía agar Mueller-Hinton. Posteriormente se colocaron sobre la superficie del agar, sensidiscos de papel de 7 mm (Whatman, No. 3) impregnados con cantidades estandarizadas de los agentes antimicrobianos (extracto etanólico y subextracto diclorometano a concentraciones de 200, 150 y 100 mg/mL). Para este ensayo fue tomado como control negativo el solvente usado para preparar las soluciones (DMSO) y como control positivo sensidiscos comerciales de cloramfenicol (30mg); las pruebas se realizaron por triplicado. Luego del período de incubación (24 horas a 36 °C ±1 °C) se midió el diámetro de la zona de inhibición alrededor de los sensidiscos (halo de inhibición) [10].
RESULTADOS
A partir del fraccionamiento cromatográfico (CC) del subextracto de diclorometano se obtuvo la fracción esterólica, el análisis por CGAR-EM permitió la elucidación estructural de 9 compuestos, todos de tipo esteroidal, de los cuales a continuación se presentan algunos datos espectroscópicos, la cadena lateral se abrevia como (CL):
4-metil-ergosta-22-en-3β-ol 1
EMIE, m/z [414]+ (100%), 371 (M+-isopropil) (19,9), 353 (M+-isopropil-H2O) (44.5), 287(M+-CL-2H) (34,1), 316 (M+-CL(C22)) (19,9), 287 (M+-CL-2H) (34,1). Fórmula molecular: C29H50O.
Ergosta-5,7,22-trien-3β-ol 2 (Ergosterol)
EMIE, m/z [396]+ (58,1%), 381(M+-Metilo)(18,2), 378 (M+-H2O)(2,6), 363 (M+-Metilo-H2O)(100), 337(M+-59) (33,0), 271(M+-CL) (9,4), 253(M+-CL-H2O) (52,1), 211(Fisión anillo D-H2O) (24,5) y 143(M+-H2O-Fisión anillo C-metilo) (41,8). Fórmula molecular: C28H44O.
4,4-dimetil-ergosta-5,7,25(26)-trien-3β-ol 3
EMIE, m/z [410]+ (27,9%), 392 (M+- H2O) (11,0), 377(M+-H2O-CH3) (53,6), 284(M+-CL-CH3) (20,6), 267 (37,8), 213 (32,7), 158 (M+-H2O-fisión del anillo C) (27,8), 69 (100). Fórmula molecular: C29H46O.
Ergosta-5,7,9,24(28)-tetraen-3β-ol 4
EMIE, m/z [394]+ (15,5 %), 376(M+-H2O)(19,9), 361(M+-H2O-CH3) (10,2), 281(M+-CL (C20-C22)(4,9) , 251(M+-H2O-L) (100), 209 (26,0), 69 (53,6). Fórmula molecular: C28H42O.
Ergosta-7,22-dien-3β-ol 5
EMIE, m/z [398]+ (28,7%), 383(M+-CH3) (9,6), 380(M+- H2O) (3,7), 300(M+-C7H14) (17,2), 273(M+-CL) (28,7), 271(M+-CL-2H) (100), 255 (M+-CL-H2O) (14,7), 253(M+-CL-H2O-2H) (28,7), 231(Fisión del anillo D) (17,2), 213(Fisión del anillo D-H2O) (26,8), 165 (49,1), 145(M+-H2O-fisión del anillo C-CH3) (42,2). Fórmula molecular: C28H46O.
Ergosta-7-en-3β-ol 6
EMIE, m/z [400]+ (100%), 385 (M+-CH3) (33,3), 367[M+-(CH3+H2O)] (13,3), 273 (M+-CL) (22,1), 255 (M+-CL-H2O) (91,4), 246 (7,7), 231(Fisión del anillo D) (18,6), 213(Fisión del anillo D-H2O) (33,3) y 145(M+-H2O-fisión del anillo C-CH3) (30,1). Fórmula molecular: C28H48O
4,4-dimetil-ergosta-7,24(28)-dien-3β-ol 7
EMIE, m/z [426]+ (78,1%), 411(M+-CH3) (29,0), 393 (M+-CH3-H2O) (100), 301(M+-CL) (5,3), 281 (M+-CL-H2O-2H) (9,6), 251 (M+-CL-H2O-2H-2CH3) (39,2). Fórmula molecular: C30H50O.
17-isopropil-Δ5,7-3β-idroxiandrostadieno 8
EMIE, m/z [314]+ (17,2%), 399(M+-CH3) (3,3), 281 (M+-H2O-CH3) (4,5), 271(M+-CL) (17,2), 253 (M+-H2O -CL) (4,5), 230 (Fisión del anillo D) (17,2), 213(Fisión del anillo D- CH3) (20,1), 147 (60,5), 69(100). Fórmula molecular: C22H34O.
Estigmasta-5,22-dien-3β-ol 9
EMIE, m/z [400]+ (48,6%), 394 (M+-H2O) (13,0), 380 (M+-Metilo-H2O) (25,2), 369(M+-isopropil) (8,5), 300 (M+-CL(C22)) (25,2), 273 (M+-CL) (15,4), 271(M+-CL-2H) (59,0), 255 (M+-CL-H2O) (77,3), 207 (Fisión anillo D-H2O) (48,6), 55 (100). Fórmula molecular: C29H48O.
Es importante destacar que los compuestos 1, 3, 4, 7, 8 y 9 se reportan por primera vez en Ganoderma applanatum.
El compuesto Ergosta-5,7,22-trien-3β-ol 2 (Ergosterol) presentó en el cromatograma un tiempo de retención (tr) de 23.066 min. Este compuesto se encuentra en gran cantidad en algunas especies comestibles de hongos y se convierte en vitamina D2 por reacciones fotoquímicas mediante la radiación ultravioleta, además es materia prima para la síntesis de biomoléculas de interés agroquímico como ecdisoma, esteroles altamente oxigenados y brassinoesterol [11], el cual aumenta el metabolismo y la eliminación de los plaguicidas, lo que podría ser de beneficio para reducir la ingesta humana de pesticidas residuales en cultivos vegetales [12].
Al realizar la evaluación de la actividad antioxidante del extracto etanólico mediante los métodos ABTS y DPPH se encontraron valores de IC50=15,27 µg/mL y 20 µg/mL, respectivamente, mientras que para el subextracto de diclorometano se obtuvieron valores de IC50=10,78 µg/mL para ABTS y 27,82 µg/mL para DPPH. Estos resultados fueron comparados con los mostrados por el ácido ascórbico (IC50=4,28 µg/mL), un antioxidante natural ampliamente reconocido y aplicado en la industria alimenticia [13]. Los valores presentados en el cuadro 1, son expresados como capacidad antioxidante equivalentes al ácido ascórbico (AAEAC; µmol de ácido ascórbico/g de muestra) y muestran que el subextracto de diclorometano del hongo Ganoderma applanatum posee buena capacidad captadora de radicales libres, estos resultados están de acuerdo con los reportados por Smina y col. en los que G. lucidum mostró significativa actividad captadora de radicales libres, la cual está asociada a la presencia de compuestos triterpénicos que son utilizados como mecanismo de defensa contra sustancias oxidantes [6]. Además, se deduce que las sustancias con capacidad antioxidante presentes en el extracto etanólico del hongo se distribuyen en el fraccionamiento por reparto hacia la fracción medianamente polar de diclorometano, mejorando el resultado de la actividad antioxidante frente al radical ABTS, mientras que con el radical DPPH disminuye su capacidad captadora de radicales libres, lo que podría atribuirse a que la molécula de DPPH químicamente es más estable en comparación con la de ABTS.
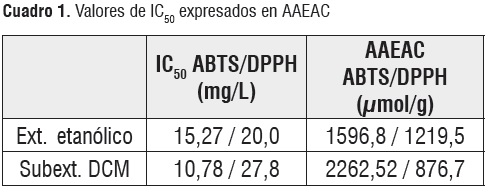 Cuadro 1
Cuadro 1En cuanto a la evaluación de la actividad bactericida mediante el método de difusión con disco en agar, se llevó a cabo por triplicado a tres concentraciones de 200, 150 y 100 mg/mL, encontrándose resultados positivos a 150 mg/mL frente a la bacteria Staphylococcus aureus, para el extracto etanólico y el subextracto de diclorometano, lo cual está de acuerdo con la bibliografía, donde se reporta una moderada actividad inhibitoria en el género Ganoderma con referencia al crecimiento de este tipo de bacterias [12]. Ninguno de los extractos presentó resultados positivos frente a la bacteria Escherichia coli a ninguna de las concentraciones evaluadas.
CONCLUSIONES
Se aislaron e identificaron químicamente 9 compuestos esteroidales, seis de los cuales, los compuestos 1, 3, 4, 7, 8 y 9 se reportan por primera vez en Ganoderma applanatum. El extracto etanólico así como el subextracto de diclorometano mostraron buena actividad antioxidante mientras que el extracto de diclorometano también mostró buena actividad bactericida, comportamiento que propone al hongo G. applanatum como una fuente promisoria de sustancias bioactivas.
REFERENCIAS
[1] SÁNCHEZ, W.F., MURILLO E. y MÉNDEZ J. Potencial antioxidante de residuos agroindustriales de tres frutas de alto consumo en el Tolima. Scientia et Technica, 46, 2010, p. 138-143. [ Links ]
[2] RUSSELL, R. and PATERSON, M. Ganoderma: a therapeutic fungal biofactory. Phytochemistry, 67, 2006, p. 1985–2001. [ Links ]
[3] SONIAMOL, J., KAINOOR, K.J., VARUGHESE G. and SABULAL B. A new epoxidic ganoderic acid and other phytoconstituents from Ganoderma lucidum. Phytochemistry Letters, 4, 2011, p. 386–388. [ Links ]
[4] GARCÍA, C.M. and COLLADO I.G. Secondary metabolites isolated from Colletotrichum species. Nat. prod. Rep., 20, 2003, p. 426. [ Links ]
[5] SHENG-XIANG, Y., ZHAO-CHENG, Y., QIANG-QIANG, L., WEN-QUAN, S. and HARTMUT, L. Toxic lanostane triterpenes from the basidiomycete Ganoderma amboinense. Phytochemistry Letters, 5, 2012, p. 576-580. [ Links ]
[6] SMINAA, T.P., MATHEWA, J., JANARDHANANA, T. and DEVASAGAYAMB, K. Antioxidant activity and toxicity profile of total triterpenes isolated from Ganoderma lucidum (Fr.) occurring in South India. Environmental Toxicology and Pharmacology, 32, 2011, p. 438-446. [ Links ]
[7] DANDAN, L., ZHENG, H., ZHIGANG, L. and YANGA, B. Chemical composition and antimicrobial activity of essential oil isolated from the cultured mycelia of Ganoderma japonicum. Journal of Nanjing Medical University, 23(3), 2009, p. 168-172. [ Links ]
[8] SANTAFÉ, G., ZULUAGA, J., ANGULO, A., TORRES, O. y PÉREZ, C. Química y actividades antioxidante y bactericida del extracto etanólico del hongo Ganoderma lucidum. Scientia et Técnica, 33, 2007, p. 329-332. [ Links ]
[9] GUZMÁN, M., SANTAFÉ, G., ZÚÑIGA, N., TORRES, O. y ANGULO A. Actividad antioxidante y estudio químico del hongo Pleurotus djamor recolectado en Córdoba. Biotecnología en Sector Agropecuario y Agroindustrial, 7(2), 2009, p. 63-69. [ Links ]
[10] VALGAS, C., MACHADO, S., SMANIA, E. and SMANIA, A. Screening methods to determine antibacterial activity of natural products. Brazilian Journal of Microbiology, 38, 2007, p. 369-380. [ Links ]
[11] RIVERA, A., NIETO, J., VALENCIA, I. y MEISER, A. Composición y cuantificación por Cromatografía de Gases Acoplada a Espectrometría de Masas de la fracción esterólica de once hongos Colombianos. Revista Colombiana de Química, 2(31), 2002, p. 95-102. [ Links ]
[12] JIAN, X., ZHANG, Y., JING, X., TAO, J., YAN, H., KAI, S., YUN, L. and QUAN, J. Brassinosteroids promote metabolism of pesticides in Cucumber. J. Agric. Food Chem., 57, 2009, p. 8406-8413. [ Links ]
[13] GUTIÉRREZ, T., HOYOS, O. y PÁEZ M. Determinación del contenido de ácido ascórbico en Uchuva (Physalis peruviana L.), por Cromatografía Líquida de Alta Resolución (CLAR). Biotecnología en Sector Agropecuario y Agroindustrial, 5(1), 2007, p. 70-79. [ Links ]
[14] SMANIA, A., DELLE, F., SMANIA, E., and CUNEO, S. Australian Ganoderma: identification, growth y antibacterial properties. Int. J. Med., 1, 2004, p. 325-330. [ Links ]













