Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Biotecnología en el Sector Agropecuario y Agroindustrial
Print version ISSN 1692-3561
Rev.Bio.Agro vol.12 no.1 Popayán Jan./June 2014
EVALUACIÓN DE PROPIEDADES ANTIOXIDANTES DE PARTE COMESTIBLE Y NO COMESTIBLE DE PITAHAYA, UCHUVA Y MANGOSTINO
EVALUATION OF ANTIOXIDANT PROPERTIES OF EDIBLE PORTION AND WASTE OF PITAHAYA, UCHUVA AND MANGOSTIN
AVALIAÇÃO DAS PROPRIEDADES ANTIOXIDANTES DA PARTE COMESTÍVEL E RESÍDUOS DA PITAHAYA, UCHUVA, E MANGOSTINO
LUIS DANIEL DAZA1*, ANDREA VERONICA HERRERA2, ELIZABETH MURILLO3, JONH JAIRO MENDEZ4.
1 Universidad del Tolima. Grupo de Investigación de Productos Naturales. Ingeniera Agroindustrial. Ibagué, Colombia.
2 Universidad del Tolima. Grupo de Investigación de Productos Naturales. Ingeniero Agroindustrial. Ibagué, Colombia.
3 Universidad del Tolima, Facultad de ciencias. Grupo de Investigación en Productos Naturales. Químico, MSc., Docente. Ibagué, Colombia
4 Universidad del Tolima, Facultad de ciencias. Grupo de Investigación en Productos Naturales. Licenciado, PhD, Docente. Ibagué, Colombia.
Correspondencia: danieldaza08@hotmail.com
Recibido para evaluación: 08-11-2011. Aprobado para publicación: 28-04-2014.
RESUMEN
En este trabajo se evaluó el contenido de fenoles en los macerados etanólicos provenientes de la parte comestible (pulpa) y no comestible (semilla y cáscara) de Pitahaya (Cereus triangularis), Uchuva (Physalis peruviana) y Mangostino (Garcinia mangostana). Además se estudió comparativamente el potencial de los extractos para inhibir la peroxidación lipídica en una mantequilla elaborada artesanalmente. La concentración de compuestos fenólicos en la cáscara de Garcinia mangostana (590,9±3,9 mg EAG/g), resultó ser la más elevada entre los materiales analizados, contradictoriamente la pulpa de este fruto fue la porción con el contenido de fenoles (55,5±07 mg EAG/g). La actividad antioxidante mostró una relación directa con el contenido de compuesto fenólicos, con valores de coeficiente de correlación de 0,988, 0,961 y 0,998 para la Uchuva, Pitahaya y el Mangostino respectivamente. Todos los extractos mostraron actividad frente a la peroxidación lipídica y tres de ellos, cáscara de mangostino (CM), semilla de mangostino (SM) y pulpa de Uchuva (PU) mostraron mayor inhibición que el BHT, A.A y PC1 (producto comercial 1), mostrándose como materias primas promisorias para el uso en la industria alimentaria y cosmetica.
PALABRAS CLAVE: Peroxidación lipídica, Cereus triangularis, Physalis peruviana, Garcinia mangostana
ABSTRACT
This work evaluated the phenolic content in ethanolic macerated from edible portion (pulp) and non-edible portion (seeds and peel) of Pitahaya (Cereus triangularis), Physalis (Physalis peruviana) and Mangosteen (Garcinia mangostana). Besides the potential was studied comparatively extracts for inhibiting lipid peroxidation in a handcrafted butter. The concentration of phenolic compounds in the peel of Garcinia mangostana (590,9±3,9 mg EAG/g) was found to be the highest among the materials tested, contradictorily the pulp of this fruit showed lower content of phenols (55,5±07 mg EAG/g). The antioxidant activity showed a direct relationship with the content of phenolic compounds with correlation coefficient values of 0,988, 0,961 and 0,998 for the Physalis, and Mangosteen Pitahaya respectively. All extracts showed activity against lipid peroxidation and three of them, mangosteen peel (CM), mangosteen seed (SM) and pulp Uchuva (PU) showed greater inhibition than BHT, AA and PC1 (commercial product 1). This fruits appearing as promising materials for use in the food and cosmetic industries.
KEYWORDS: Lipidic peroxidation, Cereus triangularis, Physalis peruviana, Garcinia mangostana
RESUMO
Neste trabalho foi avaliado o conteúdo fenólico dos extratos etanólicos da parte comestível (polpa) e não comestível (sementes e casca), de Pitaya (Cereus triangularis), Uchuva (Physalis peruviana) y Mangostino (Garcinia mangostana). Além disso, foi comparado o potencial dos extratos na inibição da peroxidação lipídica em manteiga elaborada artesanalmente. A concentração de compostos fenólicos na casca de Garcinia mangostana (590,9±3,9 mg EAG/g), foi a mais elevada entre os extratos analisados, contraditoriamente a polpa desse fruto apresentou o conteúdo mais baixo de fenólicos (55,5±07 mg EAG/g). A atividade antioxidante mostra uma relação direta com o conteúdo de compostos fenólicos, com valores de coeficiente de correlação de 0,988, 0,961 e 0,998 para a Uchuva, Pitahaya e o Mangostino, respectivamente. Todos os extratos mostraram capacidade de inibir a peroxidação lipídica e três deles, casca de Mangostino (CM), semente de Mangostino (SM) e polpa de Uchuva (PU) mostraram maior inibição que o BHT, AA e PC1 (produto comercial 1), mostrando-se matérias primas promissoras para ser utilizado em indústrias alimentícias e cosméticas.
PALAVRAS-CHAVE: Peroxidação lipídica, Cereus triangularis, Physalis peruviana, Garcinia mangostanaINTRODUCCIÓN
El Departamento del Tolima, ubicado en la zona centro-occidental de Colombia, posee condiciones agroecológicas favorables tales como disponibilidad de tierras, diferentes pisos térmicos y una excelente localización geográfica respecto a los mercados nacionales, lo que lo convierte en potencialmente apto para el desarrollo de una amplia y variada gama de productos agrícolas, entre los que se destacan las frutas exóticas.
Por otra parte, diversas investigaciones han sugerido que el consumo de frutas y vegetales reduce el estrés oxidativo y modifica el perfil lipídico, con lo cual se reduce el riesgo de enfermedades causadas por radicales libres y el elevado colesterol sanguíneo [4]. El uso de antioxidantes de origen vegetal, tales como los ácidos fenólicos, flavonoides, tocoferoles en la industria alimentaria, cobra cada día mayor importancia debido al efecto anticarcinogénico, antidiabético y otros beneficios atribuidos para la salud humana [5, 6, 7, 8].
El objetivo de este trabajo fue determinar la capacidad antioxidante de la fracción comestible y residuos agroindustriales de Mangostino, Uchuva y Pitahaya utilizando una mantequilla preparada artesanalmente como modelo y relacionar dicha actividad con la presencia de compuestos fenólicos, buscando con ello fomentar el aprovechamiento de la fracción no comestible al utilizarlos como fuente alternativa para la obtención de antioxidantes naturales y a su vez reducir el impacto ambiental generado por el desaprovechamiento de estos materiales.
MÉTODO
Material vegetal
Se utilizaron semillas, cáscara y pulpa de Pitahaya amarilla (Cereus triangularis) y Uchuva (Physalis peruviana) obtenidos de mercados locales de la ciudad de Ibagué, la fruta de Mangostino (Garcinia mangostana) fue colectada en el Municipio de Mariquita
Adecuación del material y obtención de extractos
Los frutos fueron sometidos a un proceso de selección, lavado, segmentación (cáscara, pulpa y semilla) y secado en estufa (45-55°C/48 h). El material seco se trituró hasta conseguir un polvo fino. Una porción de las muestras se maceró con etanol (1:10 w/v materia seca/solvente), con remoción del solvente cada 24 h hasta el agotamiento de la muestra. Los extractos crudos se filtraron, se concentraron a presión reducida y se almacenaron (4°C) en frascos ámbar debidamente rotulados hasta su utilización.
Determinación cuantitativa de fenoles
Para la cuantificación de fenoles se hizo uso del reactivo de Folin-Ciocalteau (FC), siguiendo la metodología descrita por Dastmalchi et al. [9], con algunas modificaciones. A una alícuota del extracto (0,1 mL) se adicionó agua destilada (6 mL), reactivo FC (0,5 mL) y carbonato de sodio (1,5 mL, 20%), la mezcla se aforó con agua destilada a 10 mL y se incubó a temperatura ambiente en oscuridad (2 h). La absorbancia de las muestras se leyó a 760 nm en un espectrofotómetro Thermo Scientific Helios g, contra un blanco de reactivos disueltos en agua. El ácido gálico se utilizó para preparar una curva de calibración (0-700 mg/mL). La ecuación de la recta obtenida se estableció como: y = 0,001X-0,009, R2=0,997, la cual sirvió de base para calcular la concentración de las muestras. Los resultados se expresaron como miligramos equivalentes de ácido gálico por gramo de material seco (mg EAG/g).
Actividad antioxidante
Determinación de la capacidad antioxidante en un modelo de peroxidación lipídica en mantequilla. Para evidenciar la habilidad de los fitocompuestos contenidos en los extractos para inhibir la peroxidación lipídica se utilizó como sustrato una mantequilla preparada artesanalmente a base de crema de leche, a fin de garantizar la ausencia total de preservants antioxidantes.
La mantequilla elaborada fue clarificada sometiéndola a calentamiento (70°C/3 h) en vaso de precipitados y con agitación moderada, produciendo la separación de las fases. La fase lipídica se pasó a través de tela filtrante y por papel filtro [10]. La calidad del producto se estableció a través de la determinación de la humedad, densidad, cenizas, grasa, índice de refracción, acidez, índice de peróxido, índice de saponificación e índice de yodo, según metodología de la A.O.A.C. 1990 [11]. Dos mantequillas comerciales se utilizaron como controles.
Análisis estadístico
Todas las determinaciones químicas se efectuaron por triplicado. Cada réplica se analizó individualmente y los datos fueron reportados como la media de tres determinaciones (n=3±SD). Los análisis de varianza y diferencia entre las muestras fueron determinados por test de rangos múltiples de Duncan usando el programa estadístico Statgraphics. Versión estudiantil. Un nivel de p<0,05 fue usado como criterio para determinar las diferencias estadísticas.
RESULTADOS
Denominación de extractos vegetales
Para mayor comprensión del texto, los macerados etanólicos de los diferentes materiales vegetales se mencionarán a lo largo del trabajo de la siguiente manera: pulpa de Uchuva (PU), semilla de Uchuva (SU), cáscara de Uchuva (CU), pulpa de Pitahaya (PP), semilla de Pitahaya (SP), cáscara de Pitahaya (CP), pulpa de Mangostino (PM), semilla de Mangostino (SM) y cáscara de Mangostino (CM).
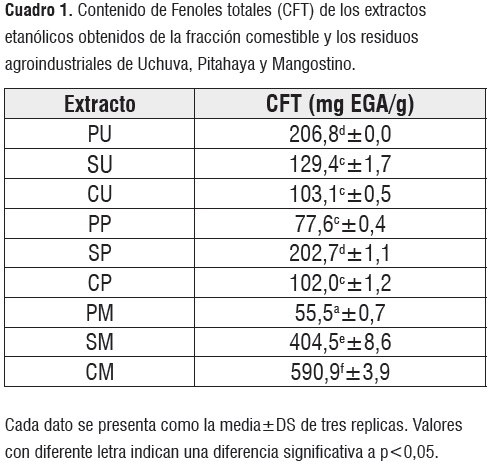
Contenido de fenoles totales
La identificación cuantitativa de compuestos fenólicos presentes en un material vegetal constituye uno de los primeros pasos para la determinación de la actividad antioxidante de estos [14], y adicionalmente puede proveer algún indicio de otras actividades biológicas. Los valores obtenidos en la cuantificación de fenoles en los diferentes extractos evaluados muestran contenidos que oscilan en un rango de 55,5 mg EAG/g a 590,9 mg EAG/g (cuadro 1). La mayor cantidad de compuestos fenólicos fue encontrado en CM seguido de SM, PU, SP, SU, CU, CP, PP y PM respectivamente.
Comparando estos resultados con la literatura, fueron reportados valores más bajos de fenoles totales para pulpa de Uchuva (40,45 y 39,15 mg EAG/100 g de muestra) cáscara de mangostino (195 mg EAG/g de extracto; 24,9 mg EAG/g) y para la pulpa y cáscara de pitahaya (42,4; 39,7 mgEAG/100) [19, 20, 21, 22, 23]. Adicionalmente, se hallaron reportes que difieren de nuestros resultados, para el contenido de fenoles de la pulpa de mangostino (263,3 mg EGA/g de fruta seca) [24]. La variación de los resultados puede deberse a diferencias en variedad de los frutos, factores medioambientales composición y naturaleza química de los constituyentes de cada matriz.
ACTIVIDAD ANTIOXIDANTE
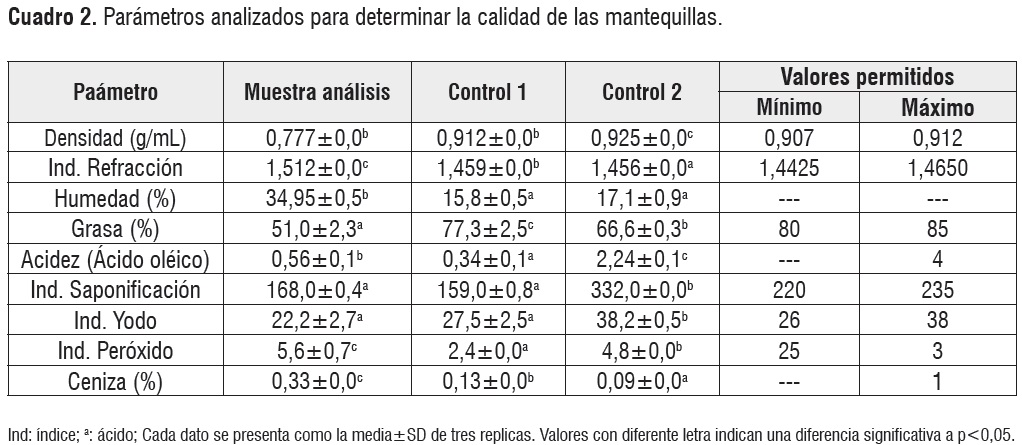
Determinación de calidad de la mantequilla
La caracterización físico química de la mantequilla usada como modelo y los productos comerciales utilizados como controles para la determinación del potencial antioxidante de los materiales analizados muestran diferencias estadísticas en la mayoría de los parámetros determinados, adicionalmente se observa claramente que la mantequilla elaborada artesanalmente no cumple con las especificaciones de la norma (Cuadro 2), sin embargo este material se constituye en un modelo optimo para la evaluación de la actividad de los extractos debido a que carece de aditivos que potencien o inhiban la actividad de los compuestos presentes en los extractos.
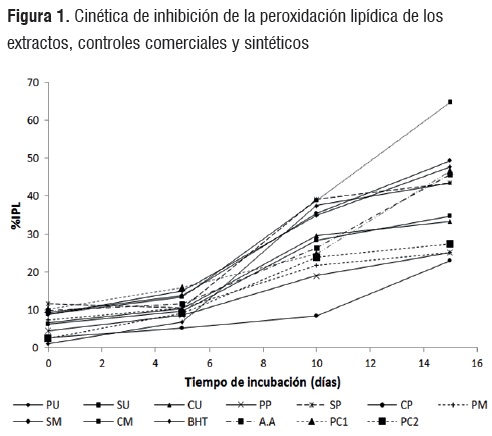
Cinética de inhibición de la peroxidación lipídica de los extractos
En la figura 1 se puede observar el potencial antioxidante de los extractos y controles utilizados, evaluado mediante el seguimiento de la inhibición de la peroxidación lipídica. En todo el ensayo se evidencio una buena relación tiempo-respuesta antioxidante, es decir con el aumento del tiempo de incubación hay un aumento en la respuesta inhibitoria, observándose la mayor potencialidad de todos los extractos al tiempo 15 días (360 horas de incubación).
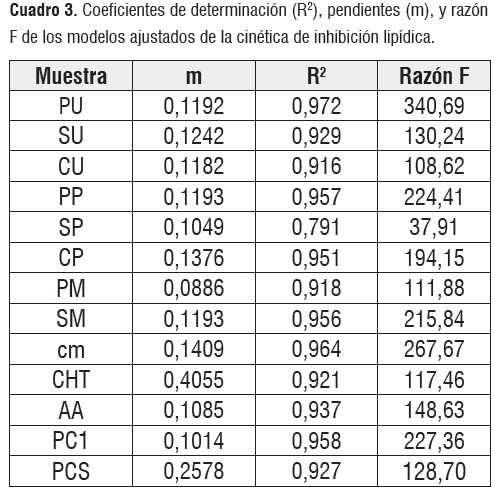
El análisis de comparación de modelos alternativos realizó un ajuste de las curva de cinética de inhibición de la peroxidación lipídica, los valores de las pendientes (m), coeficientes de determinación (R2) y valor F de los modelos (cuadro 3), indican un buen ajuste al modelo exponencial en cada una de las cinéticas. La actividad antioxidante de los extractos, patrones y controles utilizados en el ensayo se evidencia desde el tiempo de incubación cero y va en aumento a medida que el tiempo de incubación se hace más prolongado, esto posiblemente se debe a que la matriz alimentaria utilizada como modelo no es una matriz purificada y por lo tanto contiene hidroperóxidos y compuestos pro-oxidantes que pueden dar inicio a la reacción de oxidación antes de iniciar el análisis.
Los resultados de actividad antioxidante al día 15 (360 h) mostraron que los extractos CM, PU y SM fueron los más activos de cada fruto con una inhibición de la peroxidación lipídica de 64,8%, 47,8% y 43,4 respectivamente, en contra posición las fracciones de cada fruto que mostraron menor actividad fueron CP (23%), PM (25,1%) y CU (33,3%), importa mencionar que son las fracciones no comestibles las que se mostraron mas activas, además de tener los mayores contenidos de compuestos fenólicos. Adicionalmente se observó que tres de los extractos evaluados CM, SM y PU tuvieron mayor efecto en la inhibición de la peroxidación lipídica al final del tiempo de incubación que PC1 un producto comercial sometido a procesos tecnológicos de refinamiento y enriquecido con compuestos que lo protegen de daños como la peroxidación lipídica, el BHT (antioxidante sintético) y el ácido ascórbico estos dos últimos son sustancias puras con una elevada actividad antioxidante utilizadas a nivel farmacológico e industrial [25, 26], la respuesta observada por parte de los extractos para inhibir la peroxidación lipídica en la mantequilla puede deberse a que en estos no solo están contenidos compuestos fenólicos, por el contrario son una mezcla de diversos metabolitos como ácido ascórbico, carotenos entre otros nutrientes que pueden interactuar antagónica o sinérgicamente, siendo esta ultima interacción una posible explicación para el elevado potencial antioxidante mostrado por los extractos [27].
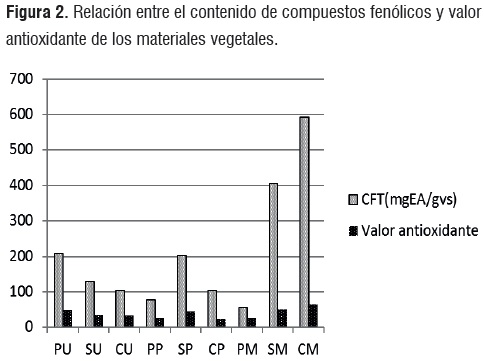
Una comparación entre el contenido fenólico total y la respuesta final de inhibición de la peroxidación lipídica arrojó valores de correlación (r) de 0,988, 0,961 y 0,998 para la Uchuva, la Pitahaya y el Mangostino respectivamente (figura 2), lo anterior indica que la capacidad de los extractos para inhibir la peroxidación lipídica esta estrechamente relacionada con la presencia de compuestos de naturaleza fenólica.
Nuestros resultados sugieren que los materiales vegetales del interés de este trabajo, incluidos la parte comestible y la no comestible, se constituirían en fuente de antioxidantes aplicables en la industria, lo que mejoraría el futuro promisorio agroindustrial de estos frutos tropicales e incrementaría su valor agregado.
CONCLUSIONES
Todos los extractos analizados en este estudio mostraron capacidad para inhibir la peroxidación lipídica en un modelo alimenticio aunque con diferente eficiencia. La actividad antioxidante mostrada por la fracción no comestible (semilla y cáscara) del fruto de mangostino (Garcinia mangostana) la posicionan como un fruto promisorio no sólo por su contenido de metabolitos secundarios asociados a su capacidad antioxidante sino además por su potencialidad agroindustrial. Son necesarios estudios in vivo para establecer los beneficios reales de estas materias vegetales.
AGRADECIMIENTOS
Los autores agradecen el soporte económico de la Oficina de Investigaciones y Desarrollo Científico y el apoyo logístico del Departamento de Química de la Universidad del Tolima.
REFERENCIAS
[1] AGRONET. Estadisticas [online]. 2011. Disponible: http://www.agronet.gov.co. [citado 20 de Noviembre de 2012] [ Links ]
[2] OLIVEIRA, L., PORTO, A. and TAMBOURGI, E. Production of xylanase and protease by Penicillium janthinellum CRC 87M-115 from different agricultural wastes. Bioresource Technology, 97, 2006, p. 862-867. [ Links ]
[3] MOURE, A., CRUZ, J., FRANCO, D., DOMINGUEZ, M., SINEIRO, J., DOMINGUEZ, H., NUÑEZ, M. and PARAJÓ, C. Natural antioxidants from residual sources. Food Chemistry, 72, 2001, p. 145-171. [ Links ]
[4] RAHMAT, A., ABU BAKAR, M.F., FAEZAH, N. and HAMBALI, Z. The effects of consumption of guava (Psidium guajava) or papaya (Carica papaya) on total antioxidant and lipid profile in normal male youth. Asia Pacific Journal of Clinical Nutrition, 13, 2004, p. S106 [ Links ]
[5] CHOI, Y., JEONG, S. and LEE, J. Antioxidant activity of methanolic extracts from some grains consumed in Korea. Food Chemistry, 103, 2007, p.130-138. [ Links ]
[6] FAN, J., DING, X. and GU, W. Radical-scavenging proanthocyanidins from sea buckthorn seed. Food Chemistry, 102, 2007, p. 168-177. [ Links ]
[7] IQBAL, S. and BHANGER, M. Stabilization of sunflower oil by garlic extract during accelerated storage. Food Chemistry, 100, 2007, p. 246-254. [ Links ]
[8] SIDDHURAJU, P. and BECKER, K. The antioxidant and free radical scavenging activities of processed cowpea (Vigna unguiculata L.) See extracts. Food Chemistry, 101, 2007, p. 10-19. [ Links ]
[9] DASTMALCHI, K., DORMAN, D., KOSARB, M., and HILTUNEN, R. Chemical composition and in vitro antioxidant evaluation of a water-soluble Moldavian balm (Dracocephalum moldavica L.) extract. LWT-Food Science and Technology, 40(240), 2007, p. 239-248. [ Links ]
[10] ÖZKANLI, O. and KAYA, A. Storage stability of butter oils produced from sheep’s non-pasteurized and pasteurized milk. Food Chemistry, 100, 2007, p. 1026-1031.
[11] AOAC INTERNATIONAL. Oficial methods of analysis Association of Official Analytical Chemist. 14 ed. Arlington (USA): 1984. [ Links ]
[12] IQBAL, S. and BHANGER, M.I. Stabilization of sunflower oil by garlic extract during accelerated storage. Food Chemistry, 100, 2007, p. 246-254. [ Links ]
[13] YEN, G., DUH, P. and CHUANG, D. Antioxidant activity of anthraquinones and anthrone. Food Chemistry, 70, 2000, p. 307-315. [ Links ]
[14] BECKER, E.M., NISSEN, L.R. and SKIBSTED, L.H. Antioxidant evaluation protocols: food quality or health effects. European Food Research and Technology, 219, 2004, p. 561-571. [ Links ]
[15] GEORGE, S., BRAT, P., ALTER, P., and AMIOT, M.J. Rapid determination of polyphenols and vitamin C in plant-derived products. Journal of Agricultural and Food Chemistry, 53(5), 2005, p. 1370-1373. [ Links ]
[16] HUANG, D., OU, B., and PRIOR, R.L. The chemistry behind antioxidant capacity assays. Journal of Agricultural and Food Chemistry, 53(6), 2005, p. 1841-1856. [ Links ]
[17] MAJCHRZAK, D., MITTER, S. and ELMADFA, I. The effect of ascorbic acid on total antioxidant activity of black and green teas. Food Chemistry, 88, 2004, p. 447-451. [ Links ]
[18] ZHANG, D. and HAMAUZU, Y. Phenolics, ascorbic acid, carotenoids and antioxidant activity of broccoli and their changes during conventional and microwave cooking. Food Chemistry, 88, 2004, p. 503-509. [ Links ]
[19] RESTREPO, A. Nuevas perspectivas de consumo de frutas: Uchuva (Physalis peruviana L.) y Fresa (Fragaria vesca L.) mínimamente procesadas fortificadas con vitamina E [Tesis Magíster en Ciencia y Tecnología de Alimentos]. Medellín (Colombia): Universidad Nacional de Colombia, Facultad de Ciencias Agropecuarias, 2008, 107 p. [ Links ]
[20] BOTERO, A. Aplicación de la Ingeniería de Matrices en el desarrollo da la uchuva mínimamente procesada fortificada con calcio y vitaminas C y E [Tesis Magíster en ciencias farmacéuticas énfasis en alimentos]. Medellín (Colombia): Universidad de Antioquía, Facultad de química farmacéutica, 2008, 185 p. [ Links ]
[21] NACZK, M., TOWSEND, M., ZADERNOWSKI, R. and SHAHIDI, F. Protein-binding and antioxidant potential of phenolics of mangosteen fruit (Garcinia mangostana). Food Chemistry, 128, 2011, p. 292-298. [ Links ]
[22] MAISUTHISAKUL, P., SUTTAJIT, M. and PONGSAWATMANIT, R. Assessment of phenolic content and free radical-scavenging capacity of some Thai indigenous plants. Food Chemistry, 100, 2007, p. 1409-1418. [ Links ]
[23] WU, L., HSU, H., CHEN, Y., CHIU, C., LIN, Y. and HO, J. Antioxidant and antiproliferative activities of red pitaya. Food Chemistry, 95, 2006, p. 319-327. [ Links ]
[24] MUÑOZ, U., DASTMALCHI, K., BASILE, M. and KENNELLY, E. Quantitative high-performance liquid chromatography photo-diode array (HPLC-PDA) analysis of benzophenones and biflavonoids in eight Garcinia species. Journal of Food Composition and Analysis, 25, 2012, p. 215-220. [ Links ]
[25] GARCIA, H. and FATIBELLO, O. Simultaneous determination of butylated hydroxyanisole (BHA) and butylated hydroxytoluene (BHT) in food samples using a carbon composite electrode modified with Cu3(PO4)2 immobilized in polyester resin. Talanta, 81, 2012, p 1102-1108. [ Links ]
[26] QUIRÓS, A., FERNANDEZ, M. and LOPEZ, J. A screening method for the determination of ascorbic acid in fruit juices and soft drinks. Food chemistry, 116, 2009, p. 509-512 [ Links ]
[27] ROMANO, C., ABADI, K., REPETTO, V., VOJNOV, A. and MORENO, S. Synergistic antioxidant and antibacterial activity of rosemary plus butylated derivatives. Food chemistry, 115, 2009, p. 456-461. [ Links ]