Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Biotecnología en el Sector Agropecuario y Agroindustrial
Print version ISSN 1692-3561
Rev.Bio.Agro vol.13 no.2 Popayán July/Dec. 2015
https://doi.org/10.18684/BSAA(13)86-93
DOI: http://dx.doi.org/10.18684/BSAA(13)86-93
HIDRÓLISIS ENDO-ENZIMATICA Y PRODUCCION DE ETANOL A PARTIR DEL BANANO DE RECHAZO
ENDO-ENZYMATIC HYDROLYSIS AND ETHANOL PRODUCTION FROM BANANA REJECTED
ENDO-HIDRÓLISE ENZIMÁTICA E PRODUÇÃO DE ETANOL DE BANANA DE REJEIÇÃO
CARLOS A. GUEVARA-BRAVO1, HÉCTOR A. ARENAS2, CARLOS A. PELÁEZ-JARAMILLO3
1 Universidad del Quindío, Programa de Química. Dr. Ciencias Químicas. Armenia, Colombia.
2 Universidad de Antioquia,Grupo Interdisciplinario de Estudios Moleculares. Ingeniero Químico. Medellín, Colombia.
3 Universidad de Antioquia, Grupo Interdisciplinario de Estudios Moleculares. Dr. Química. Medellín, Colombia.
Correspondencia: caguevara@uniquindio.edu.co
Recibido para evaluación: 3 de Diciembre de 2014. Aprobado para publicación: 14 de Octubre de 2015.
RESUMEN
Los polisacáridos del banano de rechazo verde (Variedad Cavendish AAA), de la zona de Urabá, fueron hidrolizados eficientemente, utilizando tratamiento endoenzimático a altas temperaturas. Posteriormente los azúcares simples fueron extraídos y los jugos resultantes fermentados con levaduras comerciales. Al final del proceso se determinó la concentración de etanol y se calcularon los rendimientos. Primero, se desarrollaron experimentos a escala de 1,0 Kg y se determinaron las mejores condiciones de hidrólisis: Concentración de etileno exógeno (50 ppm), temperatura (33°C) y cantidad de Ca(OH)2 (10 g/Kg de banano), adecuada para la extracción. Teniendo como referencias las condiciones anteriores, fue escalado el proceso a 40 Kg, para determinar la metodología de extracción de los azúcares (en contracorriente), mediante la utilización de lechada de cal (1,0%), para precipitar los sólidos, centrifugación y posterior neutralización con H2SO4 hasta pH 5,5. Finalmente los jugos ricos en azúcares fueron fermentados con levaduras a 5 g/L, donde se alcanzó un rendimiento de 52 mL de etanol/Kg de banano. Estos resultados indican que el proceso es promisorio para producir alcohol a gran escala, Sin embargo se debe mejorar, para que sea competitivo con los rendimientos obtenidos con de caña de azúcar (86 mL de etanol/Kg de caña).
PALABRAS CLAVE: Fermentación, Extracción, Etileno, Escalamiento, Enzimas.
ABSTRACT
Polysaccharydes from bananas rejected (Cavendish AAA group) from Urabá were hydrolyzed efficiently using a endo-enzymatic treatment at high temperatures. Subsequently the simple sugars were extracted and the resultant juices were fermented with commercial yeast. Finally ethanol concentration was determined and the yields calculated. First, experiments at 1,0 Kg scale were developed and were determined the better hydrolysis condition: exogenous ethylene concentration (50 ppm), temperature (33°C) and Ca(OH)2 amount (10 g/Kg of banana), suitable for extraction. Taking as references the before conditions, was scaled up the process at 40 Kg level, where was determined the better sugars extraction methodology (cross-current), by means of utilization of lime solutions (1,0%), for solids precipitation, centrifugation and after neutralization with H2SO4 at pH 5,5. Finally the rich sugars juices were fermented with yeast at 5 g/L, where was found a maximum relation of 52 mL of ethanol/kg of banana. This results suggest that the proposal process is promissory to produce ethanol at large scale, but is necessary to improve the efficiency to be competitive with yields gets a industrial level with sugar cane (86 mL of ethanol/Kg of sugarcane).
KEYWORDS: Fermentation, Extraction, Ethylene, Escale up, Enzymes.
RESUMO
Polissacarídeos bananas rejeitados (AAA variedade Cavendish) da região de Urabá, foram hidrolisados de forma eficiente usando tratamento endoenzima em altas temperaturas. Posteriormente açúcares simples foram extraídos e sucos fermentados resultando leveduras comerciais. Após o processo, a concentração de etanol foi determinada e os rendimentos foram calculados . Em primeiro lugar, as experiências foram desenvolvidas 1,0 Kg de escala e foram determinadas as melhores condições de hidrólise : Concentração de etileno exógeno (50 ppm), temperatura (33°C) e a quantidade de Ca(OH)2 (10 g/kg bananas), adequado para a extração. Tomando como referência as condições acima, o processo foi dimensionada para 40 kg, a metodologia para a determinação de extração de açúcares (contracorrente), usando leite de cal (1,0%) para precipitar sólidos, centrifugação e subsequente neutralização com H2SO4 a pH 5,5. Finalmente sumos de açúcar elevados foram fermentado com levedura a 5 g/L, em que um caudal de 52 mL de etanol/kg de banana foi atingido. Estes resultados indicam que o processo é promissor para a produção de escala álcool, no entanto deve ser melhorada, para torná-lo competitivo com os rendimentos obtidos com a cana (86 mL de etanol/kg de cana).
PALAVRAS CHAVE: Fermentação, Extracção, Etileno, Scaling, Enzima.
INTRODUCCIÓN
La producción colombiana de bananos de rechazo (no apto para exportación) en la zona de Urabá se estima en 250.000 ton al año, de las cuales 140.000 son usadas para satisfacer el consumo nacional y 110.000 para la producción de compost y alimentación animal [1]. La fruta está concentrada en las empacadoras y además contiene carbohidratos entre 22 y 25% en peso húmedo [2], que pueden ser utilizados para la producción de etanol. Sin embargo, la mayoría de los carbohidratos presentes en los bananos verdes son polisacáridos complejos y por lo tanto no están disponibles para ser metabolizados por las levaduras; así que se hace necesario realizar la hidrólisis de estos carbohidratos, en su mayor parte almidón, para convertirlos en azúcares simples [3]. En el caso específico del banano, se ha investigado sobre la implementación de diversos procesos hidrolíticos como la hidrólisis ácida y exo-enzimática [4].
La hidrólisis endo-enzimática (hidrólisis endógena o maduración inducida), es un proceso ampliamente usado en la cadena de comercialización de diversas frutas, entre ellas el banano. Este proceso se basa en la activación de los enzimas endógenos (amilasas, celulasas, pectinasas etc), mediante la aplicación de etileno (hormonas de la maduración), y en condiciones controladas de temperatura y humedad relativa [5], con el fin de obtener una fruta con características organolépticas deseadas por el consumidor final [6]. La desactivación de éste proceso ha sido también estudiada, principalmente mediante el bloqueo de la hormona etileno, realizando la aplicación de 1-MCP (1-Metilciclopropeno), con el objetivo de extender la vida de los frutos [7].
Si se desea proyectar la producción de etanol a nivel industrial, a partir de los carbohidratos de los frutos verdes de banano, se requieren condiciones más fuertes, con el fin de obtener la mayor cantidad de azúcares fermentables en el menor tiempo posible, independiente de las características organolépticas finales. Por lo tanto, es posible utilizar concentraciones elevadas de la hormona etileno, temperaturas mayores a las del ambiente y % de humedad relativa cercana a los valores máximos. A pequeña escala, se ha dedicado especial atención al efecto de la concentración de etileno y la temperatura en recipientes de vidrio [8] y a las cinéticas del cambio de color y textura de los frutos a altas temperaturas [9]. Además, se ha determinado el comportamiento de los enzimas endógenos, por ejemplo de α y β amilasas a diferentes temperaturas [10], de la pectatoliasa (PEL) [11] y los efectos inhibitorios de extractos sobre la polifenol-oxidasa [12].
La extracción acuosa de los azúcares fermentables, presentes en el fruto hidrolizado, es el siguiente paso para la obtención de jugos con alto contenido de sólidos solubles, que se pueden fermentar. Se han utilizado bananos maduros sin cáscara, molidos y luego sometidos a extracción con solo agua caliente [13]. Se ha comparado el efecto de las extracciones enzimáticas y mecánicas con respecto al rendimiento y composición del jugo [14]. Se ha utilizado la hidrólisis exo-enzimática a bananos maduros (Musa sapientum Linn.), utilizando pectinasas y α-amilasas comerciales, por separado, como pre-tratamiento antes de la producción de vinos [15]; el uso de pectinasas comerciales a concentraciones entre 0,01 y 0,05% v/w y entre 30-60°C, para la obtención de jugos de banano y posterior filtración en tela [16]. También, con el objetivo de determinar la influencia de la microestructura y el contenido de taninos en la extracción de jugos a partir de banano; se realizaron exámenes microscópicos de las secciones de pulpa y se determinó que los taninos liberados durante la ruptura, facilitan la liberación del jugo [17].
Algunas investigaciones se han realizado con el objetivo de evaluar todas las etapas involucradas en el proceso de producción de etanol a partir de bananos. Hammond analizó el potencial de los bananos maduros en la producción de alcohol [18]. A partir de bananos verdes se consiguieron eficiencias superiores al 95% en un sistema enzimático de SSF, utilizando glucoamilasas, enzimas pectinolíticas y levadura [19].
Los objetivos de ésta investigación fueron: la determinación a escala de laboratorio, de las mejores condiciones de hidrólisis endo-enzimática de los polisacáridos presentes en el banano verde y determinar los reactivos necesarios para la extracción; posteriormente se escaló el proceso a un nivel de 40 Kg para establecer las metodologías adecuadas de extracción de los azúcares fermentables y los rendimientos de la fermentación alcohólica.
MÉTODO
Material vegetal
Bananos verdes de rechazo provenientes de la zona de Urabá fueron comprados en la Central Minorista de la ciudad de Medellín, sin desgajar, libres de daños y posteriormente fueron lavados, desinfectados con solución de hipoclorito 0,1% v/v y finalmente pesados individualmente.
Métodos analíticos
Tanto las pérdidas de peso de los bananos completos como el peso de cáscara y pulpa fueron realizados en una balanza analítica OHAUSS con 1 ± 0,001 g. Para la determinación de sólidos solubles, se tomaron 2,0 g de pulpa de banano triturada y centrifugada; el sobrenadante se usó para la medición directa en el refractómetro y la medida fue reportada como °Brix. La cuantificación de azúcares reductores se realizó por el método del DNS (Ácido 3,5 dinitro salicílico), donde 100 µL de jugo fueron diluidos a 10 mL y una alícuota de 500 µL fue mezclada con 500 µL de DNS y calentados a baño de agua hirviendo durante 12 min. Posteriormente se adicionaron 2 mL de agua destilada y finalmente se determinó la Absorbancia a 540 nm; la cuantificación se realizó tomando como base una curva de calibración elaborada con glucosa. La concentración de etanol se determinó en un cromatógrafo de gases Agilent 6890N, con detector FID, H2 como gas de arrastre, columna Carbowax 20M de 50 m de longitud. La metodología fue la siguiente: 50°C durante 1 min, calentamiento a 20°C/min hasta 150°C, y estabilización por 2 minutos, rampa a 30°C/min hasta 200°C y estabilización por 1 min. Una curva de calibración desde 5 a 500 ppm, fue preparada usando etanol grado cromatográfico para determinar la relación entre el área del pico y la concentración.
Hidrólisis endo-enzimática y extracción a escala de laboratorio
Para determinar la concentración óptima de etileno, se utilizaron 10 recipientes de vidrio, con sistema de cerrado hermético y acondicionados con válvulas para la inyección de gases (etileno: Mezcla de maduración 'Azetil' conteniendo etileno 5% Cryogas®). En cada recipiente se colocaron siete (7) bananos verdes pesados y se inyectó etileno, de tal forma que las concentraciones dentro del sistema alcanzaran 25, 50, 100 y 200 ppm y adicionalmente el control (0,0 ppm). Por lo tanto se utilizó un diseño experimental de bloques completos al azar con de 5 tratamientos con dos réplicas.
Todos los experimentos se realizaron por duplicado a temperatura ambiente (25°C). Fue monitoreada la concentración de sólidos solubles (°Brix), en la pulpa 24, 66, 88 y 114 horas, tomando un banano por vez, al azar, de cada recipiente. La concentración de etileno que permitió obtener la mayor concentración de sólidos solubles en la pulpa, fue utilizada para los siguientes experimentos. El efecto de la temperatura fue determinado utilizando los recipientes descritos anteriormente. Se utilizaron doce (12) recipientes de vidrio conteniendo siete (7) bananos verdes cada uno; a todos les fueron inyectados una concentración fija de etileno comercial (anteriormente establecida) y dejados en reposo por 24 horas a temperatura ambiente para inducción de la maduración. Pasado este tiempo, los recipientes fueron trasladados a incubadoras donde las temperaturas se establecieron en 29, 33, 37°C y se dejó un control a temperatura ambiente. Los experimentos se realizaron por duplicado. Durante los experimentos se monitoreo la pérdida de peso, °Brix en la pulpa y en la cáscara y el peso de pulpa a 0, 24, 48, 60, 66, 88 y 114 horas. Para realizar estos fue necesario extraer un banano del recipiente, al azar, en cada estadio de la maduración y destruirlo para obtener los datos experimentales. Para la extracción de los jugos fueron utilizadas 70 mL de disoluciones acuosas de Ca(OH)2 a diferentes concentraciones (1, 2.5, 5, 10 y 15% p/v), a 80°C, que fueron mezcladas con 100 g de bananos molidos. Después de un tiempo de contacto de 15 min, las mezclas fueron centrifugadas y se determinó el volumen obtenido de los jugos, así como la concentración de sólidos solubles (°Brix). Los experimentos se realizaron por triplicado.
Hidrólisis endo enzimática y extracción a escala de 40 Kg
Fueron utilizados aproximadamente 40 Kg de bananos verdes sin desgajar, pesados y lavados con solución de hipoclorito 0,1% y colocados en cámara de maduración. Fueron inyectados 50 ppm de la mezcla de maduración (etileno). La cámara se mantuvo sellada durante 24 horas, manteniendo la humedad relativa =85% y la temperatura de 25°C. Pasado éste tiempo, se abrió la cámara y se permitió el intercambio de gases con el ambiente. Durante el resto del proceso, se aumentó la temperatura a 33°C y se mantuvo la humedad relativa, abriendo periódicamente la cámara y usando un ventilador y un humidificador. Para la extracción, los bananos hidrolizados a 33°C durante 66 h, fueron triturados enteros en un molino de tornillo sin fin y sus azúcares extraídos con 3 diferentes metodologías, a saber: 1. Extracción en una etapa, adicionando 100 mL/Kg de banano de lechada de cal al 10%, mezclado y centrifugado a 1000 rpm. 2. Extracción en dos etapas. Adición de 100 mL/Kg de banano de lechada de cal al 10% a 70°C, mezclado y centrifugación y nuevamente adición a la torta de banano, agua caliente 200 mL/Kg de banano, mezclado y centrifugación. 3. Extracciones en contracorriente en 3 etapas (Figura 1). Este proceso es más complejo y para evaluarlo se utilizaron varios lotes de 40 Kg de bananos. Se pretendió implementar un proceso de extracción similar al de caña de azúcar. En estos procesos, el material con el mayor contenido de sólidos solubles es puesto en contacto con un líquido que contiene una concentración de sólidos solubles obtenida del contacto con un material sólido más agotado.
Fermentaciones
Los jugos de banano a pH básico, obtenidos en la etapa anterior fueron neutralizados con H2SO4 concentrados hasta pH 5,5, esterilizados y filtrados. Las fermentaciones fueron realizadas en erlenmeyers de 500 mL de capacidad, llenados hasta un 60% con jugos de banano de cada uno de los tratamientos. Los jugos fueron inoculados con levadura comercial a una concentración de 5 g/L y el recipiente fue adaptado a una trampa de gases para promover la fermentación; pasadas 72 horas, se determinó la concentración de etanol por cromatografía gaseosa.
RESULTADOS
Con respecto a la hidrólisis endo-enzimática, en la Figura 2 se observa el efecto de la concentración de etileno sobre los °Brix en la pulpa a diversos tiempos de hidrólisis.
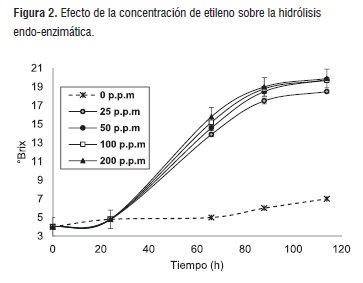
El test de rango múltiple realizado a 88 horas de hidrólisis endo-enzimática, indica que no hay diferencias estadísticamente significativas entre las concentraciones utilizadas a (200, 100, 50 ppm), pero si se encuentran diferencias con la concentración de 25 ppm con un nivel de confianza del 95%. También hay diferencias significativas con respecto al blanco. Estos resultados concuerdan con la bibliografía donde se indica que en algunos tratamientos, usando apenas 0,1 mg/L de etileno inducen la hidrólisis endo-enzimática en bananos [20]. En tratamientos comerciales, para lograr las características organolépticas deseadas, es común el uso de 100 a 1000 ppm. Utilizando como base los resultados, se determinó continuar los siguientes experimentos, usando la concentración de 50 ppm.
En la Figura 3, se observa el comportamiento de los sólidos solubles (°Brix), en la pulpa, cuando se realiza la hidrólisis endo-enzimática a diferentes temperaturas. La mayor cantidad de sólidos solubles en la pulpa (22,5 °Brix), se obtuvieron después de 66 horas de transcurrido el proceso a una temperatura de 33°C y una Humedad relativa de 85-90%. En este tiempo, se encontraron diferencias estadísticamente significativas entre el tratamiento a 33°C y los realizados a 29 y 25°C. Esto quiere decir que la actividad enzimática, principalmente de celulasas y amilasas se ve aumentada con la temperatura, hasta alcanzar un límite a los 37°C donde se presenta inhibición enzimática.
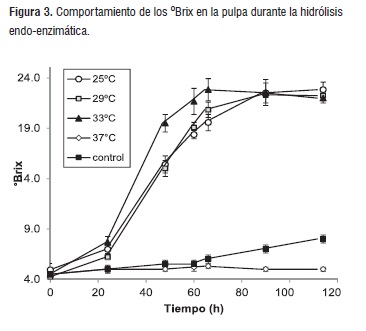
Cabe anotar que la temperatura aquí enunciada corresponde a la de la cámara utilizada para la hidrólisis y no la temperatura interna de los bananos. Transcurridas 88 horas, se nota un leve descenso de los sólidos solubles en el tratamiento a 33°C, hasta alcanzar los obtenidos a 25 y 29°C, lo que puede ser indicativo de la degradación de los azúcares provocada por fermentación.
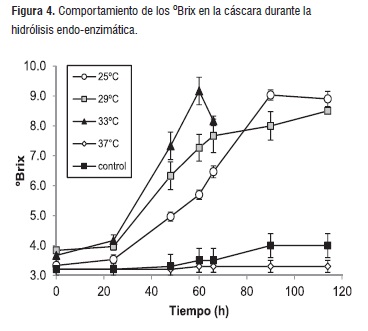
El comportamiento de la cáscara en éste proceso se observa en la Figura 4. Se alcanzaron la mayor cantidad de sólidos solubles (9,2 °Brix), transcurridas 60 horas del experimento a 33°C. Se encontró que en ese momento, existen diferencias estadísticamente significativas entre los tratamientos de 33, 29 y 25°C. Nuevamente, se puede notar que al aumentar la temperatura, se disminuye el tiempo necesario para alcanzar la mayor cantidad de sólidos solubles (°Brix) y que transcurridas 88 horas, la cantidad de sólidos solubles empieza a disminuir en el tratamiento a 33°C.
Es de importancia anotar que la coloración de los bananos durante los proceso a alta temperatura no cambia, permaneciendo de coloración verde; esto concuerda con resultados que indican que a temperaturas mayores de 25°C, hay baja actividad clorofilasa que conduce a la degradación incompleta de clorofila y la formación de color amarillo es inhibido e indica que se presenta un estrés por calor en la fruta [21, 22].
En la Figura 5, se relaciona la pérdida de peso del fruto con la temperatura de hidrólisis endo-enzimática. Inicialmente, se presenta una mayor velocidad de pérdida de peso en los experimentos a 29°C, pero transcurridas 88 horas no se presentan diferencias estadísticamente significativas. A las 66 horas, tiempo en el cual se alcanza la mayor cantidad de sólidos solubles en la pulpa a una temperatura de 33°C, no presentan diferencias estadísticamente significativas entre los tratamientos.
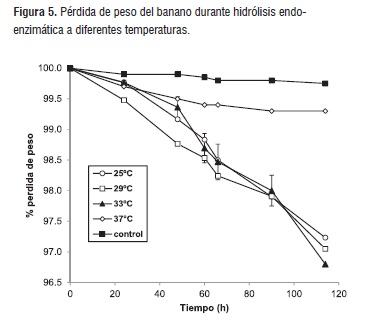
Esta pérdida de peso es atribuida a la deshidratación por la exposición a altas temperaturas y la degradación de los azúcares en la respiración de los bananos. El tratamiento a 37°C, produce una disminución rápida del peso de los bananos en los estadios iniciales posiblemente debido la rápida deshidratación del fruto, pero luego esta tendencia disminuye debido a la inhibición de los procesos enzimáticos por la temperatura.
Los bananos hidrolizados a 33°C fueron utilizados para realizar la extracción de los azúcares fermentables. Inicialmente, se determinó la concentración óptima de solución de lechada de cal en la extracción. Los resultados son expuestos en el cuadro 1:
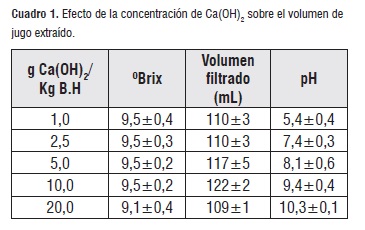
El jugo extraído en las concentraciones de 5, 10, 20 g de Ca(OH)2/Kg banano fue translúcido de color amarillo verdoso, lo que indica la separación óptima de los sólidos. Para posteriores ensayos se determinó utilizar la concentración de 10 g Ca(OH)2/Kg banano. Sin embargo un pH de 9,4 en el jugo hace necesaria una neutralización, antes de iniciar la fermentación, con H3PO4, tal como se realiza con el jugo de caña.
Para la etapa a escala de 40 Kg, se redujo la proporción de agua utilizada, para evitar la excesiva dilución de los azúcares y por tanto concentraciones de etanol bajas al final de la fermentación. En los ensayos realizados a 40 Kg, las pérdidas de peso, por hidrólisis endo-enzimática ascendieron a 5,1% ± 0,78 y al quitar los pedúnculos, las pérdidas ascendieron a 8,6%±1,7. Este aumento en las pérdidas con respecto a los experimentos a nivel de laboratorio (2,5%) es debido a que en los experimentos a mayor escala, los bananos fueron hidrolizados, sin quitar los pedúnculos, con el objetivo de simular un proceso industrial.
Estos pedúnculos fueron retirados antes de la molienda, reduciendo la materia prima disponible. En el cuadro 2, se presentan los rendimientos obtenidos con cada uno de los sistemas de extracción y la concentración de etanol después de la fermentación de los jugos.
El Análisis estadístico indicó que no hay diferencias significativas en el proceso de dos extracciones secuenciales (52,2±5,1) y el proceso de extracción en contracorriente (52,1± 1,5). Ambas extracciones pueden ser usadas, sin embargo la extracción en contracorriente necesita una mayor cantidad de tiempo y energía, para ser realizada. Estos resultados indican que el procedimiento de extracción en 2 etapas es promisorio.
Sin embargo, el rendimiento de todo el proceso es bajo, si se compara con el proceso de obtención de alcohol a partir de caña de azúcar, donde se logran hasta 144 g de Azúcares reductores/Kg de caña de azúcar [23]. La cantidad de Etanol obtenido en todo el proceso, por Kg de materia prima es también bajo si se compara con la cantidad de etanol obtenida de caña de azúcar (hasta 85 mL/Kg).
CONCLUSIONES
La hidrólisis endo-enzimática es una alternativa viable, para la obtención de azúcares fermentables a partir del banano verde de rechazo y su posterior fermentación alcohólica. Con los experimentos realizados a dos escalas diferentes se obtuvieron resultados complementarios y satisfactorios, que permitirán el desarrollo de procesos a escala piloto. Sin embargo, es de anotar que los rendimientos de producción de etanol por kilogramo de banano verde, distan mucho todavía de los rendimientos a partir de caña de azúcar y por tanto próximos estudios deben enfatizar en la optimización del proceso hidrolítico.
AGRADECIMIENTOS
Los autores agradecen a COLCIENCIAS por su apoyo económico, en la realización de esta investigación.
REFERENCIAS
[1] AFANADOR, A. M. El Banano Verde de Rechazo en la Producción de Alcohol Carburante. Revista Escuela de Ingeniería de Antioquia EIA, 3, 2005, p. 51-68. [ Links ]
[2] AGAMA, E., NÚÑEZ, M., ÁLVAREZ, J. and BELLO, L. Physicochemical, digestibility and structural characteristics of starch isolated from banana cultivars. Carbohydrate polymers, 124, 2015, p. 17-24. [ Links ]
[3] PERONI, F., SIMAO, R., CARDOSO, M., SOARES, C., LAJOLO, F. and CORDENUNSI, B. In vivo degradation of banana starch: Structural characterization of the degradation process. Carbohydrate polymers, 81, 2010, p. 291-299. [ Links ]
[4] GUEVARA, C., ARENAS, H., MEJIA, A., y PELAEZ, C. Obtención de etanol y biogás a partir de banano de rechazo. Información Tecnológica, 23(2), 2012, p.19-30. [ Links ]
[5] WILLS, R.B.H., HARRIS, D.R., SPOHR, L.J. and GOLDING, J.B. Reduction of energy usage during storage and transport of bananas by management of exogenous ethylene leves. Postharvest Biology and Technology, 89, 2014, p. 7-10. [ Links ]
[6] SOZMEZDAG, A., KELEBEK, H. and SELLI, S. Comparison of the Aroma and Some Physicochemical Properties of Grand Naine (Musa acuminata) Banana as Influenced by Natural and Ethylene-treated Ripening. Journal of Food Processing and Preservation, 38(5), 2014, p. 2137-2145. [ Links ]
[7] BOTONDI, R., DE SANCTIS, F., BARTOLONI, S. and MENCARELLI, F. Simultaneous application of ethylene and 1-MCP affects banana ripening features during storage. Journal of the Science Food and Agriculture, 94, 2014, p. 2170-2178. [ Links ]
[8] SOARES, F.D., DANTELA, D., MOREIRA, S.H., BORGES, J.L., PERALTA, R.F. and SALVADOR, F.S.R. Study of Banana (Musa aaa Cavendish cv Nanica) Trigger Ripening for Small Scale Process. Brazilian Archives of Biology and Technology, 51(5), 2008, p. 1033-1047. [ Links ]
[9] FREITAS, J., REZENDE, R. and RODRIGUES, F. Colorimetric indicator for classification of bananas during ripening. Scienti Horticulturae, 150, 2013, p. 201-205. [ Links ]
[10] PERONI, F., CARDOSO, B., AGOPIAN, R., LOURO, R., NASCIMENTO, J., PURGATTO, E. and CORDENUNSI, B. The cold storage of green bananas affects the starch degradation during ripening at higher temperatura. Carbohydrate polymers, 96, 2013, p. 137-147. [ Links ]
[11] WANG, J., JUAN, X., SHENG, P. and HUA, H. Changes in resistant starch from two banana cultivars during postharvest storage. Food Chemistry, 156, 2014, p. 319-325. [ Links ]
[12] JU-HUA, L., GUANG-HONG, C., CAI-HONG, J., JIAN-BIN, Z., BI-YU, X. and ZHI-QIANG, J. Function of a citrate synthase gene (MaGCS) during postharvest banana fruit ripening. Postharvest Biology and Technology, 84, 2013, p. 43-50. [ Links ]
[13] CALLIGARIS, S., FOSCHIA, M., BARTOLOMEOLI, I., MAIFRENI, M. and MANZOCCO, L. Study on the applicability of high-pressure homogenization for the production of banana juices. Food Science and Technology, 45, 2012, p.117-121. [ Links ]
[14] YU, Y., XIAO, G., WU, J. and XU, Y. Comparing characteristic of banana juices from banana pulp treated by high pressure carbono dioxide and mild heat. Innovative Food Science and Emerging Technologies, 18, 2013, p. 95-100. [ Links ]
[15] CHEIRSILP, B. Processing of Banana-Based wine Product Using Pectinase and a-amilasa. Journal of Food Process Engineering, 31, 2008, p. 78-90. [ Links ]
[16] TCHEWONPI, S., JONG, E., KARMAKAR, S. and DE, S. Optimisation of low temperature extraction of banana juice using commercial pectinase. Food Chemistry, 151, 2014, p. 182-190. [ Links ]
[17] KYAMUHANGIRE, W., KREKLING, T., REED, E., and PEHRSON, R. The microstructure and tannin content of banana fruit and their likely influence on juice extraction. Journal of the Science of Food and Agriculture, 86, 2006, p. 1908-1915. [ Links ]
[18] BELLO, R., LINZMEYER, P., BUENO, C., SOUZA, O., WESTRUPP, S. and MARANGONI, C. Pervaporation of ethanol produced from banana waste. Waste Management, 34, 2014, p. 1501-1509. [ Links ]
[19] BELLO, R., SOUZA, O., SELLIN, N., MEDEIROS, S. and MARANGONI, C. Effect of the microfiltration phase on pervaporation of etanol produced from banana residues. Computer Aided Chemical Engineering, 31, 2012, p. 820-824. [ Links ]
[20] DU, L., YANG, X., SONG, J., ZHUANGZHUANG, M., ZHANG, Z. and PANG, X. Characterization of the stage dependency of high temperature on green ripening reveals a distinct chlorophyll degradation in banana fruit. Scientia Horticulturae, 180, 2014, p. 139-146. [ Links ]
[21] XIAOTANG, Y., SONG, J., FILLMORE, S., PANG, X. and ZHANG, Z. Effect of high temperature on color, chlorophyll fluorescence and volatile biosynthesis in green-ripe banana fruit. Postharvest Biology and Technology, 62, 2011, p. 246-257. [ Links ]
[22] BENJAMIN, Y., GÖRGENS, J.F. and JOSHI, S.V. Comparison of chemical composition and calculated etanol yields of sugarcane varieties harvested for two growing seasons. Industrial crops and products, 58, 2014, p. 133-141. [ Links ]
[23] ROLZ, C. and DE LEON, R. Ethanol fermentation from sugarcane at diferente maturities. Industrial crops and products, 33, 2011, p. 333-337. [ Links ]













