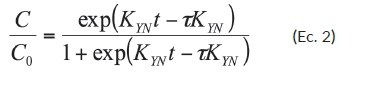INTRODUCCIÓN
La contaminación de los cuerpos de agua causada por el incremento de contaminantes tóxicos derivados de los efluentes de origen antropogénico es un problema ambiental que enfrenta el hombre actualmente. Entre los residuos más peligrosos se encuentran los metales pesados como el níquel y el plomo, los cuales aunque se presenten en bajas concentraciones impactan negativamente sobre la biota acuática y la salud humana, ocasionando padecimientos tales como: problemas respiratorios, debilidad en el sistema inmune, afecta los riñones, el hígado, hipertensión, alteraciones genéticas y neurológicas, cáncer e incluso la muerte [1]. Las vías de exposición son principalmente la ingestión de suelo y polvo contaminados siendo la inhalación una vía de entrada que puede ser significativa [2]. La exposición prolongada a iones de plomo puede causar daños renales debido a la sobreproducción de especies de oxigeno reactivas, siendo uno de los síntomas el incremento de la presencia de proteinura con predominio de proteínas de bajo peso molecular derivadas del plasma de acuerdo con lo reportado por Cabral et al. [3]. Asimismo, puede desencadenar deterioro de la memoria, tiempos de reacción prolongados y capacidad reducida para comprender [4]. Por otro lado, la exposición a iones de níquel produce nauseas, vómitos, diarrea, vértigo, lasitud, dolor de cabeza, dificultad para respirar, aumento del tamaño del riñón, reducción de la capacidad fertilizante, aparición de células cancerígenas y sarcomas, mutaciones genéticas, entre otros síntomas de acuerdo con el reporte de la Organización Mundial de la Salud (OMS) [5].
Asimismo, la OMS estableció que la concentración máxima de iones de metales pesados en fuentes hídricas no debe superar el rango de 0,01-1 ppm; sin embargo, actualmente se reportan concentraciones hasta de 450 ppm en los efluentes [6-7]. Por lo anterior, se hace necesario el tratamiento de aguas para la remoción de metales pesados y entre los métodos más usados están: precipitación, tratamiento electroquímico, separación por membrana, evaporación y coagulación, entre otros; pero, debido a sus altos costos, alta producción de lodos y remoción incompleta, resultan poco eficientes y desfavorables; siendo esta la razón por lo que se han experimentado nuevas tecnologías sostenibles para su remoción, de manera que reemplacen los métodos convencionales de tratamiento de aguas residuales industriales, mediante el uso de residuos agrícolas como bioadsorbentes de bajo costo, eficientes y reutilizables [8,9 ].
En éste contexto, con el fin de reducir los costos operativos y mejorar los tiempos de operación del proceso de tratamiento de aguas, muchos estudios se han llevado a cabo mediante el uso de residuos de origen natural con abundante disponibilidad, entre estos están: conchas de mar, conchas de cangrejo, cáscaras de huevo, semillas y cáscaras de frutas, residuos de palma, de arroz y zeolitas, cáscara de cacao, zuro de maíz, cáscara de yuca y ñame, cáscara de naranja, palma africana, cuya efectividad depende de la naturaleza del biomaterial usado [10-13].
Qi y Pichler [14], valoraron el comportamiento de la adsorción competitiva de As(III), As(V), Sb(III) y Sb(V) por ferrihidrita, evaluándose sistemas de múltiples componentes (binarios, ternarios y cuaternarios); encontrándose en los sistemas binarios que el Sb (III) tuvo una influencia inhibidora más fuerte sobre la adsorción de As (III) que Sb (V), y As (V) tuvo un efecto inhibidor más fuerte sobre la adsorción de Sb (V) que el As (III), por su parte en sistemas ternarios NO3 -, PO4 3- y SO4 2- no compiten con la adsorción de As (III) y Sb (III) mientras que NO3 - y SO4 2- tampoco tuvieron efecto distinto sobre la adsorción de As (V) y Sb (V), sin embargo el PO4 3- competía con As (V) y Sb (V) para sitios de superficie; siendo los datos de adsorción ajustados de mejor forma por el modelo de Freundlich
Ahora bien, en sistema continuo existen una gran variedad de modelos los cuales se emplean en la descripción y predicción de las curvas de ruptura de adsorción en un lecho fijo para sistemas en fase líquida y gaseosa [15]. Varios investigadores han usado los modelos de modelos de Adams-Bohart, Yoon-Nelson, Thomas y BDST para modelar la remoción de contaminantes en solución, como por ejemplo plomo y cadmio sobre lecho de cáscaras de cacao [16], azul de metileno sobre cascarilla de arroz [17] y Blue 39 sobre carbón activado comercial [18].
La explotación de la fruta o corozo de palma africana de aceite (Elaeis guineensis) produce biomasa residual, entre las cuales, se encuentra la tusa o raquis; encontrándose el volumen de producción en Colombia en 6 millones de ton/año aproximadamente. De acuerdo con Se extraen de acuerdo con lo reportado por Fedepalma 8682 t/h de fruto de palma de aceite africana en 43 plantas instaladas en el país; de las cuales, 1755 ton/h son residuos. En Colombia, se incrementó la producción de palma africana en un 38% entre el 2011 y 2016. Del total de la fruta procesada el 20,22 % corresponde a tusa, el 13,65% a fibra del mesocarpio y el 5,63% a cuesco. Por lo anterior, la cantidad de biomasa residual producida en el 2016 fue de 1.264.311 ton de tusa, 853.504 ton de fibra del mesocarpio y 352.031 ton de cuesco [19,20]. Por su parte, la producción de ñame (Dioscorea rotundata) de acuerdo a estadísticas de la Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO), 59 países en el mundo reportaron producción de ñame en el año 2010, ocupando los tres primeros lugares Nigeria con 29.148.200 toneladas equivalente al 59,9% de la producción mundial, Ghana con 5.960.490 toneladas el 12,2% y Costa de Marfil con 5.700.000 toneladas el 11,7%. En el ranking de los veinte países con mayor producción de ñame Colombia se ubica en el puesto once con una producción de 395.374 toneladas aportando el 0,8% de la producción mundial en 2010 [20]. Asimismo, la FAO reporta que las cáscaras de ñame equivalen entre el 10% y 15% del producto poscosecha, lo cual generaría entre 39537,4 ton y 59306,1 ton de residuos de ñame.
En el sentido de aprovechar los residuos generados en la explotación de palma aceitera y ñame, en la presente investigación se propone analizar el comportamiento del proceso de bioadsorción simultánea y las interacciones competitivas entre iones de plomo y níquel empleando el modelo de Thomas, Yoon-Nelson y Adams-Bohart usando como bioadsorbente bagazo de palma aceitera africana (BP) y cáscara de ñame (CÑ) en columna y posteriormente se realizó inactivación de la biomasa tratada.
MÉTODO
Preparación del bioadsorbente
De acuerdo con el procedimiento realizado por Lara et al. [16], inicialmente se lavaron las cáscaras con agua destilada para retirar taninos, resinas de azúcares reductoras y demás impurezas superficiales que puedan interferir en el proceso de adsorción; posteriormente, el material fue secado en un horno Esco, Modelo Isotherm®OFA-32-8 a 100˚C durante 24 h, por último se redujo el tamaño en un molino de cuchillas marca Corona durante 20 min y se clasificó el tamaño con un tamiz tipo Shaker de acero inoxidable AISI 316 de laboratorio, donde se seleccionó 0,5 mm como tamaño de partícula [21-23].
Modificación de las biomasas
El bagazo de palma de cera (BP) y las cáscaras de ñame (CÑ) fueron tratadas químicamente con ácido cítrico 0,6 M en una relación 40 g/200 mL biomasa-ácido, agitando a 200 rpm en un Shaker a 60°C por 2 h. Luego los bioadsorbentes se filtraron y lavaron con agua destilada para retirar restos de ácido, y secados a 55°C durante 24 h [24]. En estudios anteriores se verificó la eficacia de la modificación de la biomasa mediante análisis Espectroscopia Infrarroja con Transformada de Fourier (FTIR) [11 ].
Preparación de agua sintética
Se prepararon dos soluciones de Ni (II) y Pb (II) tomando 0,0799 g de Sulfato de níquel (NiSO4) y Nitrato de plomo Pb(NO3)2 de grado analítico marca Merck disolviéndolo en 100 mL de H2O, diluyendo hasta llevar cada una a la concentración de 100 ppm. Posteriormente se preparó 1 L de solución con contenido equimolar de Pb(II) y Ni (II) mezclando 500 mL de cada solución. Luego, se estudió la cinética de cada metal para determinar el mejor tiempo de contacto a 25°C [25,26].
Pruebas de adsorción en sistema lecho fijo
Se llevaron a cabo los ensayos de adsorción competitiva en un equipo a escala de laboratorio consistente en un recipiente de alimentación del agua sintética preparada en el laboratorio, la cual se bombeó al sistema de lechos a través de una bomba compacta y sumergible, con flujo de agua máximo de 230 L/h, 2 W de poder y altura máxima de 0,62 m. El sistema constó de un control de flujo que permitió regular el paso del agua al lecho y tomar las muestras, la columna que contenía la biomasa poseía una capacidad máxima de 140 mL, diámetro de 6,6 cm. Se trabajó a un pH de 6 establecido en investigaciones anteriores [24] y un lecho de biomasa con tamaño de partícula de 0,5 mm establecido también previamente [11] con una densidad de empaque en peso de 10 g y altura de 5,5 cm. Finalmente, las muestras se recogieron en tubos de ensayos debidamente rotulados. Después de puesto en marcha el sistema de adsorción, se tomaron muestras de 5 mL a los 10 min y 20 min, y luego cada media hora hasta completar 2,5 h, con el fin de observar el comportamiento de la biomasa para remover cada metal y el tiempo que tardaba cada lecho en alcanzar la concentración de ruptura (5% de la concentración inicial, es decir, C/Co=0,005). Las alícuotas se analizaron usando un espectrómetro de absorción atómica ICE 3500, para conocer la concentración final de los metales en la solución [18].
Los datos obtenidos de los ensayos de adsorción se ajustaron a los modelos más utilizados reportados en la literatura, los cuales son: Yoon- Nelson, Thomas y Bohart-Adams, mediante la minimización del error en Solver de Excel® y se escogió el modelo que mejor predijo el ajuste de los datos experimentales de acuerdo con el R2 y error estadístico [16,27-30]. El modelo de Adam-Bohart (ecuación 1) se usa en la descripción de la curva de ruptura por encima del punto de saturación del adsorbente [27,31]. Éste modelo asume que la velocidad de adsorción es proporcional a la capacidad de adsorción y a la concentración de la especie adsorbida, y está descrito por la ecuación 1, donde KAB es la constante cinética de Adams-Bohart en L.mg-1.min-1, N0 es la capacidad máxima de adsorción volumétrica en mg.L-1, V la velocidad lineal de flujo en cm.min-1, L la profundidad del lecho en cm, C0 la concentración inicial mg. L-1, Ct la Concentración del efluente en mg.L-1:
El Modelo Yoon-Nelson (ecuación 2), supone que la tasa de disminución de la probabilidad de adsorción para cada molécula de adsorbato es proporcional a la probabilidad de adsorción adsorbato y la probabilidad de avance sorbato en el adsorbente [30,31]. Éste modelo se representa en la ecuación 2 donde KYN es la constante de Yoon-Nelson en min-1, y Yτ es el tiempo requerido para adsorber el 50% del adsorbato inicial en min:
El modelo de Thomas (ecuación 3) es frecuentemente utilizado para describir las curvas de ruptura de adsorción en un sistema de columna de lecho fijo que sigue la cinética de adsorción-desorción de Langmuir. Este modelo se puede expresar con la ayuda de la cinética de reacción reversible de segundo orden donde no se produce dispersión axial, donde KTh es la constante de Thomas en mL.min-1.mg-1, Q0 la concentración máxima de soluto en fase sólida en mg/g, X la cantidad de adsorbente en la columna dada en g, y Q es velocidad de flujo en mL.min-1 [32,33].
RESULTADOS
Capacidad de Adsorción competitiva de níquel (II) y plomo (II)
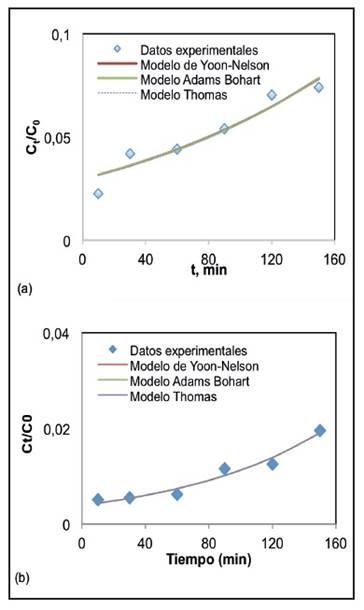
En el sistema por lecho fijo, la adsorción competitiva mostró que la concentración residual final en solución al transcurrir 150 min fue menor para el plomo que para el níquel 95,57% y 99,20% en cáscara de ñame (CÑ) respectivamente, como se puede observar en la Figura 1, mientras que usando bagazo de palma (BP) se obtuvieron porcentajes de adsorción de 92,58% y 98,04% para níquel y plomo, respectivamente; lo cual se espera debido a la rápida saturación de los sitios activos debido a la competencia de los iones por estos. De acuerdo con la Figura 1 en el sistema continuo de lecho fijo la adsorción competitiva mostró que la concentración residual en solución fue menor para el plomo que para el níquel, ya que la cinética evidenció que el plomo tuvo mayor capacidad de adsorción, alcanzándose mayores porcentajes de remoción con los dos biomateriales utilizados.
A partir de las Figuras 1 y 2 se evidenció que el tiempo de saturación incrementó a medida que aumentó el tiempo de contacto entre el agua residual y el adsorbente, ocasionando un mayor porcentaje de remoción, lo cual es causado por la porosidad de las biomasas y así, la disponibilidad de sitios de biosorción generada por el incremento en tiempo de residencia [36]. De la figura 2 se puede observar que con el método utilizado los grupos funcionales presentes en la superficie del bagazo de palma presentaron mayor afinidad por el Ni (II) y la cáscara de ñame presentó mayor afinidad por el Pb (II) con tiempo de ruptura de 90 min para ambos procesos.
Del comportamiento de los iones metálicos estudiados reportados en las figuras 1 y 2 se deduce que debido al efecto de la competencia por los sitios activos el contaminante más débil, en éste caso el Níquel, mostró una tendencia mucho más pronunciada en sus curvas de ruptura, lo cual se debe a que los compuestos adsorbidos fuertes y débiles toman los sitios activos libremente al aumentar el tiempo, siendo los más fuertes los que toman los sitios activos, aumentando así la dificultad de adsorción del contaminantes más débil, alejándose con el fluido a granel; causando por lo tanto que la concentración local del componente adsorbido más débil dentro del adsorbedor de lecho fluidizado sea mayor; lo anterior coincide con lo reportado por Kamar et al. [37] y Sulaymon et al. [38]. De acuerdo con Sulaymon et al. [38] el componente clave en el agua residual es la especie tóxica cuya concentración en el efluente de la columna primero excede el límite de descarga establecido por las regulaciones, determinando así el tiempo de servicio de la columna y por lo tanto también la tasa de uso de biomasa en el proceso. Por lo tanto, en el presente estudio, el plomo fue considerado el componente clave en el sistema binario.
Modelado de las curvas de ruptura del lecho empacado
Al realizar el modelado de los datos experimentales de adsorción competitiva en sistema continuo mostrados en las figuras 3 y 4 se encontró que el modelo que mejor los ajustó fue el de Thomas, ya que fue el que presentó el valor de R2 más cercano a la unidad y el menor error estadístico (SS); el ajuste a éste modelo es apropiado para los estudios realizados ya que implica flujo constante en columna sin dispersión axial coincidiendo con las condiciones evaluadas, además, el comportamiento concuerda con el modelo de isoterma de Langmuir o adsorción en monocapa y modelo cinético reversible de pseudo-segundo orden, lo cual coincide con lo reportado por Lara et al. [16], Tejada-Tovar et al. [27] y Gong et al. [39].
Cuadro 1 Parámetros de modelos cinéticos de adsorción competitiva de Ni(II) y Pb(II) usando cáscara de ñame (CÑ) en lecho fijo.

En la Figura 3 y 4 se observa el ajuste de los modelos cinéticos a los datos experimentales.
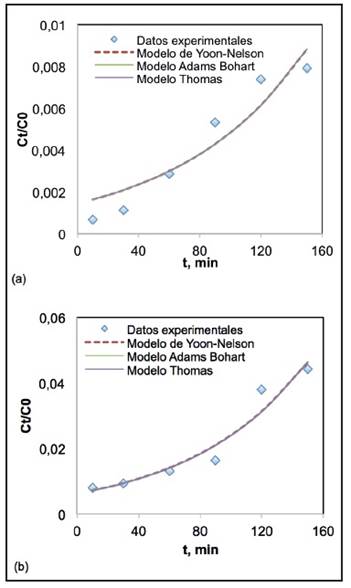
Figure 3 Modelos cinéticos para curva de ruptura de adsorción competitiva en lecho de cáscara de ñame a) Adsorción competitiva de níquel (II) y b) Adsorción competitiva de plomo (II).
Por su parte, Tsai et al. [29], encontraron resultados similares a los presentados en las Figuras 3 y 4, al evaluar la capacidad de adsorción simultánea de Pb(II), Cu(II) y Ni(II) usando bentonita revestida con quitosano (CCB) como medio adsorbente, hallando que los datos experimentales de adsorción se ajustaron con los modelos Adams-Bohart, Thomas y Yoon-Nelson, obteniendo coeficientes de correlación R2 mayores a 85%, comprobando la efectividad del CCB en la eliminación de Pb (II), Cu (II) y Ni (II) de una solución ternaria de metal.
Inactivación de la biomasa
Como se observa en la Figura 5, las concentraciones desorbidas de Ni(II) y Pb (II) son muy bajas y similares luego del proceso de inactivación por calcinación de las 4 biomasas trabajadas en la presente investigación: bagazo de palma (BP), bagazo de palma modificado con ácido cítrico (BPC), cáscara de ñame (CÑ) y cáscara de ñame modificada con ácido cítrico (CÑC).
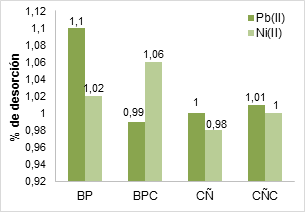
Figure 5 Desorción de níquel (II) y plomo (II) de cenizas de cáscara de ñame y bagazo de palma en solución ácida pH 2.
Por lo anterior, se muestra que un amplio porcentaje de los metales pesados tratados permanece en la ceniza y sólo un pequeño porcentaje de los mismos es liberado por efecto del ácido nítrico empleado para su desorción, lo cual indica que a temperaturas entre 600 y 700°C es posible estabilizar las biomasas y disminuir la liberación de los iones metálicos removidos de la solución, lo cual es un avance significativo para la tecnología de adsorción usando biomasa de origen vegetal, con el fin de poder realizar una adecuada disposición de los residuos que se puedan generar sin afectar al medio ambiente. Estos resultados se consideran aceptables comparando con otras investigaciones previas donde se observó que a pH altos los porcentajes de adsorción de Pb y Zn aumentan, siendo la biomasa residual a partir de alga la que presentó capacidad más baja de retención de Zn, al presentar desorción superior al 11% [25].
CONCLUSIONES
Al realizar el ajuste de los datos experimentales de la adsorción en sistema binario usando columna empacada y generar las curvas de ruptura, se encontró que el modelo que mejor describe los datos de remoción es el de Thomas, lo cual establece que el mecanismo de adsorción está controlado por un modelo cinético reversible de pseudo-segundo orden y que el comportamiento coincide con el modelo de isoterma de Langmuir. Se establece que la calcinación para la inactivación es un método eficiente y seguro, debido a que un amplio porcentaje los iones permanece en la ceniza y alrededor del 1% es liberado por el efecto de la solución de ácido nítrico empleada para las pruebas de desorción. Lo cual indica que a 700°C es posible estabilizar las biomasas y disminuir la liberación de los iones metálicos removidos de la solución, garantizándose la estabilidad de los iones metálicos dentro de la matriz utilizada como material de remoción.