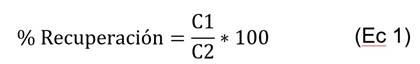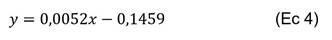INTRODUCCIÓN
La acrilamida es un compuesto orgánico de bajo peso molecular, que se forma en matrices alimentarias a partir de un proceso de deshidratación que supera los 120°C [1], principalmente por las reacciones de pardeamiento químico no enzimático como la reacción de Maillard, entre el aminoácido asparagina y los azúcares reductores [2]. Se ha demostrado la presencia de acrilamida en una amplia gama de alimentos, como las papas fritas [3], el plátano frito [2], los cereales [4], los frutos secos [5], el café tostado [6], sustitutos del café [7] y la panela [8].
En abril de 2002, un informe presentado por las autoridades suecas sobre la presencia de acrilamida en una gran variedad de alimentos sometidos a diferentes tratamientos térmicos atrajo la atención mundial, debido a que este compuesto está clasificado como una sustancia potencialmente carcinogénica para los humano [9]. La Comisión Europea estableció el reglamento 2158 el 20 de noviembre de 2017 en el cual se presentan medidas de mitigación y niveles de referencia para reducir la presencia de acrilamida en matrices alimentarias [4]. A continuación, se mencionan de forma general los productos alimenticios relacionados en dicho reglamento: patatas fritas y derivados de la papa, galletas, panes y sucedáneos de pan, cereales, productos de bollería, pastelería, repostería; biscotes, barritas de cereales, scones, cucuruchos, barquillos, café y sucedáneos del café. El nivel de referencia para papas fritas listas para el consumo es 500 µg kg-1 y para el café instantáneo es de 850 µg kg-1.
En los últimos años se han empleado diferentes técnicas analíticas para la cuantificación de acrilamida en alimentos; la cromatografía es una de ellas, y es el método más utilizado debido a su alta sensibilidad que depende, en gran medida, de la selección de detectores adecuados [5, 10]. Las técnicas de Cromatografía de Gases (CG) y Cromatografía Líquida de Alta Resolución (HPLC por sus siglas en inglés) se utilizan para la detección y cuantificación de acrilamida en alimentos [7].
A continuación, se presentan diferentes investigaciones que corroboran la efectividad de su uso: Albishri y El-Hady [11] emplearon Cromatografía Líquida de Alta Resolución con detector de Ultravioleta Visible (HPLC-UV por sus siglas en inglés) para cuantificar la cantidad de dicho compuesto en alimentos horneados como panes y fritos como snacks de papa reportando concentraciones de acrilamida de 150, 870, 330, 336, 66500, 70400 y 95000 µg kg-1 en pan fino, pan blanco, pan integral, pan baladí, papas crujientes, papas fritas Lay’s y Doritos, respectivamente, con valores de recuperación entre el 90,60 y el 109,80 %; así mismo, Marconi et al. [12] empleo el método de HPLC-DAD para la determinación de acrilamida en papas fritas, productos fritos a base de harina y shortbread, obteniendo valores de concentración en el rango de 278 µg kg-1 y 326 µg kg-1 para porcentajes de recuperación entre 90,50 y 99,10 %; de igual forma, en la investigación de Saraji y Javadian [13] desarrollaron un método de microextracción de gota y emplearon CG con detector de captura de electrones (DCE) para analizar el contenido de acrilamida presente en pan, papas fritas y galletas; la concentración de acrilamida encontrada fue de 1700 µg kg-1, 1240 µg kg-1, 1410 µg kg-1, respectivamente, con valores de recuperación entre el 98,00 y el 101,00 %.
Otra técnica ampliamente utilizada para detección de analitos es espectrometría de masas (EM), sin embargo, los iones de acrilamida no son específicos debido a la presencia de coextractivos que producen interferencias. Hasta la fecha, los métodos analíticos que verifican el nivel de acrilamida en alimentos procesados por medio de la MS deben de ir acompañados de un paso cromatográfico ya sea por HPLC o CG [12].
El objetivo del presente estudio fue evaluar el efecto de la cantidad de solución Carrez, el uso de ultrasonido, la cantidad de muestra y el tipo de dopaje, en el rendimiento de la extracción de acrilamidas en papas fritas, utilizando la técnica de HPLC.
MÉTODO
Materiales
Los snacks de papa frita empleados para la extracción, se adquirieron en la cafetería de la Universidad de Caldas, seleccionando una marca comercial al azar. Se utilizó estándar de acrilamida al 99% de pureza (AppliChem Panreac), n- Hexano grado HPLC al 99,00% de pureza (Merck) y agua ultrapura tipo I (sistema MilliQ). La solución Carrez consistió en una mezcla de sulfato de magnesio MgSO4 (Merck) y cloruro de sodio NaCl (Merck).
Instrumentación
La extracción y tratamiento de las muestras se realizó con ayuda de una centrifuga Eppendorf 5430, una balanza analítica Ohaus, un vórtex Dragon Lab Mx-S, un baño de ultrasonido Branson 2510 con una potencia máxima de salida de 100W. Las muestras fueron analizadas en un equipo de HPLC-UV Thermo U- Dionex Ultimate 3000, conformado por una bomba de vacío (Ultimate 3000), un automuestreador (Ultimate 3000), un compartimento de columna termostatizado (Ultimate 3000) y un detector ultravioleta visible (Ultimate 3000).
Condiciones cromatográficas
Se utilizó una columna Thermo Scientific™ Hypersil™ BDS C18 (150 mm x 4 mm x 5 μm tamaño de particular x 130 Å tamaño de poro); para la fase móvil se usó agua ultrapura tipo I en modo isocrático (sistema MilliQ). El análisis se llevó a cabo usando diferentes velocidades de flujo y longitudes de onda, temperatura del horno de 30ºC y un volumen de inyección de 20 µL.
Preparación de las soluciones estándar
Las soluciones stock fueron preparadas en agua ultrapura tipo I a partir de 8,2 mg de acrilamida disueltos hasta completar un volumen de 25 mL, para una concentración final de 328 mg L-1. De la solución madre, se obtuvieron diluciones de concentración 50, 200, 400, 600, 800, 1000, 1200, 1400 y 1600 µg L-1 con lo cual se obtuvo la curva de calibración para la cuantificación de acrilamida en las muestras.
Determinación de acrilamida: método de extracción
Se empleó el método de De Paola [7] modificado. Se tomó 1 g de muestra previamente triturado, se le adicionaron 10 mL de agua y se llevó a vórtex por 2 min. Posteriormente, se añadió el Carrez (4 g de MgSO4 y 0,5 g de NaCl), se agitó en vórtex por 2 min, se llevó a ultrasonido por 10 min a temperatura constante de 25ºC y se centrifugó a 5000 rpm durante 5 min. A continuación, se tomó la fase acuosa, se transfirió a un nuevo tubo falcón que contenía 2 mL de n- Hexano y se llevó a vórtex por 2 min. Posteriormente se realizó una nueva extracción, se retiró parte de la fase acuosa y se depositó en otro tubo falcón, seguidamente se llevó a vórtex por 2 min y centrífuga por 3 min a 5000 rpm. Finalmente, se tomaron 2 mL del sobrenadante, se pasaron por un filtro PVDF de 0,45 µm y se trasfierieron a un vial para su respectivo análisis por HPLC.
Dopaje de las muestras
Se tomó 1 g de papa frita, previamente triturada en un procesador de alimentos y pesada en un tubo falcón. Las muestras fueron dopadas, a partir de una solución estándar de acrilamida hasta lograr una concentración final de 8000 y 12000 µg kg-1 y se realizó el procedimiento de extracción según lo estipulado en la metodología. Se utilizaron dos tipos de dopaje en los cuales, en el primero los tubos falcón se dejaron en refrigeración durante 12 horas para garantizar que las muestras de papa absorbieran la solución adicionada y en el segundo caso se adicionó el estándar al principio de la extracción hasta lograr las concentraciones establecidas.
El porcentaje de recuperación se determinó a partir de la cantidad de acrilamida adicionada en comparación con la cantidad encontrada. El valor de la recuperación se estimó utilizando la ecuación 1.
Donde:
C1= Concentración del analito en la muestra fortificada.
C2= Concentración del analito agregado a la muestra.
Evaluación del método
El método analítico se evaluó en función de parámetros como linealidad, límite de detección y límite de cuantificación.
Evaluación de la linealidad
Este parámetro se calculó sobre la base de la curva de calibración. Se preparó una curva de calibración de 9 puntos y cada punto se analizó por triplicado. Se obtuvieron los datos de la concentración y el área promedio de las tres réplicas, se graficaron los resultados obtenidos y se verificó la linealidad del rango seleccionado a partir del coeficiente de regresión (r) ⩾ 0,99. Se aplicaron las pruebas F y t para determinar la existencia de error sistemático y la correlación entre los datos.
Límite de detección (LOD) y límite de cuantificación (LOQ). Se determinaron en función de la pendiente (S) de la curva de calibración y la mínima desviación estándar obtenida de la respuesta (σ), de acuerdo con las ecuaciones 2 y 3.
Análisis estadístico
Los análisis estadísticos se realizaron utilizando STATGRAPHICS (Centurión XVII). La significación estadística de las variables se probó aplicando la prueba t de Student. La homogeneidad de las varianzas se determinó con la prueba F de Snedecor. Los parámetros estadísticos fueron evaluados a un nivel de significancia de p < 0,05.
RESULTADOS
Para optimizar las condiciones de detección de acrilamida por HPLC-UV diferentes parámetros fueron investigados tanto para el método cromatográfico (longitud de onda y flujo) como para el método de extracción (cantidad de solución Carrez, uso de ultrasonido, cantidad de muestra y tipo de dopaje).
Optimización de las condiciones cromatográficas
Se evaluaron dos longitudes de onda y 10 velocidades de flujo, para determinar cuáles valores proporcionaban una mejor detección de la acrilamida presente en los snacks de papa.
Efecto de la longitud de onda
Se evaluaron las longitudes de onda de 200 y 210 nm en estándares de acrilamida y muestra dopada. Como se observa en los cromatogramas (figuras 1 y 2) los estándares presentaron buena simetría y resolución de pico en ambas longitudes de onda. A 200 nm los picos tenían una mayor área, sin embargo, cuando se realizaron las lecturas de los extractos de snack de papa a esta longitud de onda, se observó que el tiempo de retención de la acrilamida era diferente para el estándar y la muestra, lo cual dificulta la identificación del componente de estudio. A 210 nm se presentó un pico más definido en la muestra dopada con un tiempo de retención de 6,87 ± 0,186 min tanto para el estándar como para la muestra.
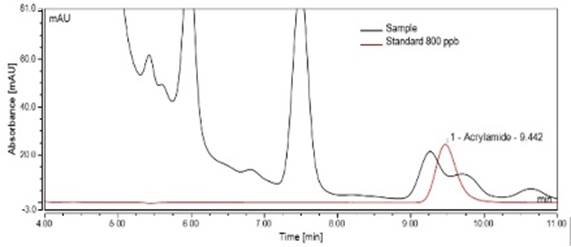
Figura 1. Cromatogramas del estándar y la muestra enriquecida. Estándar y muestra leídos a longitud de 200 nm y flujo de 0,3 mL min-1.
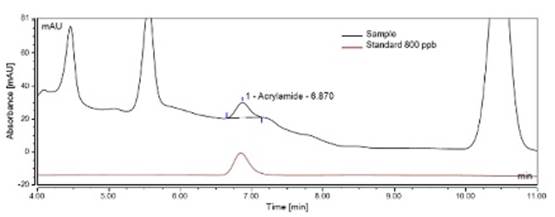
Figura 2. Cromatogramas del estándar y la muestra enriquecida. Estándar y muestra leídos a longitud de 210 nm y flujo de 0,4 mL min-1
En el estudio realizado por Meghavarnam y Janakiraman [14] emplearon una longitud de onda de 210 nm para la cuantificación de acrilamida en muestras de papa frita y pan, obteniendo buena resolución en los picos. Resultados similares fueron reportados por Qi et al. [15] quienes emplearon una longitud de onda de 205 nm para el análisis de acrilamida en papas fritas.
Efecto del flujo
Se evaluaron 10 velocidades de flujo en estándares de acrilamida, a una longitud de onda de 210 nm. En los cromatogramas obtenidos se evidenció que a un flujo de 0,1 mL min-1 los picos tenían una mayor área, pero a su vez un mayor tiempo de retención, lo cual hace más demorado el proceso de cuantificación de la acrilamida presente en las muestras de snack de papa. El flujo óptimo se determinó a partir de la curva de Van Deemter, la cual se obtuvo empleando los datos de tiempo de retención y ancho del pico del estándar de acrilamida a flujos desde 0,1 mL min-1 hasta 1,0 mL min-1.
La curva de Van Deemter representa la relación entre la velocidad lineal de la fase móvil y la altura equivalente de plato teórico (HETP por sus siglas en inglés). Las menores HETP se obtuvieron a velocidades lineales de 0,04 y 0,05 cm s-1 que corresponden a flujos de 0,3 y 0,4 mL min-1, respectivamente. A estas condiciones se logra la mejor eficiencia de la columna, lo cual es ideal en un análisis cromatográfico [16].
Se realizó un estudio adicional, donde se comparó la eficiencia de los flujos 0,3 y 0,4 mL min-1 con respecto a la concentración de acrilamida encontrada en los extractos. Ensayos a flujo de 0,3 mL min-1 presentaron problemas de identificación de pico y bajos porcentajes de recuperación a diferencia del flujo de 0,4 mL min-1 para el cual se obtuvo la mayor concentración y el mayor porcentaje de recuperación (72,43 %).
A partir de las condiciones estudiadas (flujo de 0,4 mL min-1 y longitud de onda de 210 nm), se analizó la presencia de acrilamida en muestras de snack de papa, obteniendo simetría y resolución adecuada de los picos, como se observa en la figura 3. En los cromatogramas del estándar se evidenció que no hay interferencia entre picos, sin embargo, para confirmar la pureza del pico correspondiente a acrilamida se empleó la técnica de HPLC-DAD. Este análisis mostró una pureza de pico del 99,90%, lo que confirmó la ausencia de interferencias.
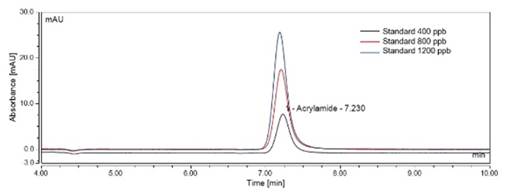
Figura 3. Estándar leído en el HPLC con detector UV. Estándares de concentración de 4000, 8000 y 12000 µg kg-1, leídos en el HPLC con detector UV a longitud de onda de 210 nm y flujo de 0,4 mL min-1
La técnica de HPLC para la cuantificación de acrilamida, ha sido empleada en diferentes matrices alimentarias como plátano frito [2], frutos secos (ciruelas, almendras, avellanas, pistachos y piñones) [5] y papa frita [3,17,18].
Efecto de la cantidad de solución Carrez
Para conocer la influencia de la cantidad de Carrez en la recuperación, se realizaron 3 extracciones en muestras de snack de papa previamente dopadas con 12.000 µg kg-1 del estándar de acrilamida, empleando cantidades diferentes de Carrez: 1) sin adición, 2) adicionando 4 g MgSO4 y 0,5 g NaCl y 3) adicionando 8 g MgSO4 y 1 g NaCl. Cuando se realizó el proceso de extracción sin la adición del Carrez no fue posible filtrar, debido a que la solución acuosa era muy viscosa, mientras que en los casos 2 y 3 se obtuvieron porcentajes de recuperación de 35,19 ± 0,92% y 41,54 ± 2,37%, respectivamente. Şenyuva y Gökmen [19] informaron que el uso de agua como solvente para la extracción de acrilamida da una suspensión espesa, debido a que los alimentos derivados de la papa están compuestos de altas cantidades de coloides y grasas que deben separarse durante la extracción, por lo cual se hace necesario el empleo de la solución Carrez y el uso de una relación de muestra disolvente 1:10 g de muestra/mL de agua para obtener un extracto más limpio y en cantidad suficiente debido a la gelatinización del almidón, que experimenta un poder de hinchamiento producto del tratamiento térmico del producto [20].
Durante la extracción se evidenció que con la presencia de solución Carrez en la suspensión, se obtenía una fase acuosa más limpia y de fácil filtrado, debido a la presencia de las sales, que por su acción clarificante, precipitan los coloides [20]. Además, se observó que el rendimiento de la extracción aumentó al adicionar mayor cantidad de solución Carrez. Al aplicar los estadísticos de prueba se encontró que p < 0,05, lo que indica que existen diferencias estadísticamente significativas entre las dos cantidades de Carrez empleadas en la extracción. Se seleccionó 8 g MgSO4 y 1 g NaCl de Carrez ya que esta cantidad proporcionó un mejor rendimiento.
Efecto de la aplicación de ultrasonido en el proceso de extracción
Se aplicó el método de extracción a dos muestras previamente dopadas con 12.000 µg kg-1 del estándar de acrilamida, sometiendo a ultrasonido sólo una de ellas. Los porcentajes de recuperación obtenidos fueron similares, siendo 35,19 ± 0,92% para la extracción con ultrasonido y 36,94 ± 2,20% para la extracción sin ultrasonido. De acuerdo con los valores obtenidos para las pruebas estadísticas, se puede afirmar que la aplicación del ultrasonido no afectó el contenido de acrilamida obtenido en la extracción, dado que no se encontraron diferencias estadísticamente significativas (p > 0,05) ni para las desviaciones estándar ni para las medias de las dos muestras analizadas.
Según investigaciones realizadas, para obtener cambios significativos en el rendimiento de la extracción con la aplicación de ultrasonido se deben someter las muestras a sonicación de 5 a 20 min con potencias de 130 y 250 W [14]. En la investigación realizada por Norouzi et al. [10] reportaron porcentajes de recuperación del 98,00% aplicando una potencia de ultrasonido de 138 W durante 5 min.
Efecto de la cantidad de muestra
Dos muestras de papa de diferente peso, previamente trituradas y enriquecidas con 12.000 µg kg-1 del estándar de acrilamida, fueron sometidas a extracción. Ambas fueron dopadas con el mismo estándar de acrilamida y para la obtención de sus extractos se empleó la misma cantidad de Carrez (4 g MgSO4 y 0,5 g NaCl). Los porcentajes de recuperación obtenidos para las muestras de 1 y 0,5 g fueron 35,19 ± 0,92% y 41,68 ± 1,40%, respectivamente. Al comparar los rendimientos de extracción de ambas muestras se evidenció un mayor valor para la muestra de 0,5 g, lo cual puede estar asociado con la cantidad de Carrez adicionada, ya que de acuerdo con lo mencionado anteriormente, influyó en el porcentaje de recuperación.
Estadísticamente se encontró que p<0,05, lo que indica que existen diferencias estadísticamente significativas entre las cantidades de muestra empleadas. Teniendo en cuenta que el mayor porcentaje de recuperación se obtuvo empleando 0,5 g de snack de papa en la extracción, se seleccionó dicha cantidad.
Galani et al. [4] en su investigación evaluó los niveles de acrilamida presentes en matrices alimentarias como cereales, leguminosas, raíces y tubérculos obteniendo buenos rendimientos de extracción al emplear 0,5 g como tamaño de muestra.
Efecto del tipo de dopaje
Con el fin de conocer la influencia del dopaje en el porcentaje de recuperación se evaluaron dos muestras, cada una enriquecida de forma diferente, la primera dopada 12 horas antes y la segunda dopada en el momento de la extracción. Se encontró que la adición del estándar al inicio de la extracción favorece el porcentaje de recuperación, además, se evidenció que el rendimiento de la extracción se ve afectado por el tiempo que permanece dopada la muestra, a mayor tiempo menor es el rendimiento, esto debido a que la acrilamida es un compuesto muy sensible a la luz y de fácil degradación, razón por la cual se ve afectada la concentración del analito en las muestras dopadas durante 12 h.
En el análisis estadístico se encontró que p < 0,05 para las medias, lo que indica que existen diferencias estadísticamente significativas entre los tipos de dopaje empleados. Se seleccionó el dopaje al inicio de la extracción porque proporcionó un mayor rendimiento de la extracción.
Aunque Gökmen [20] en su investigación expresó que al adicionar un estándar interno a una muestra de alimento es necesario permitir un periodo de incorporación antes de realizar la extracción. En este caso se vio afectado gravemente el porcentaje de recuperación obtenido para las muestras analizadas.
Una vez analizados los parámetros, tanto para la extracción como para la lectura de las muestras, se verificó la eficiencia de éstos en el rendimiento de la extracción. Dichos parámetros fueron: cantidad de Carrez (8 g MgSO4 y 1 g NaCl), sin aplicación de ultrasonido, cantidad de muestra 0,5 g y realizando el dopaje en el momento de la extracción, se usó una longitud de onda de 210 nm y un flujo de 0,4 mL min-1. Se corroboró la eficiencia de los parámetros al obtener porcentajes de recuperación superiores al 64,00% como se muestra en el cuadro 1.
Cuadro 1 Porcentaje de recuperación de acrilamida, obtenido para los extractos.
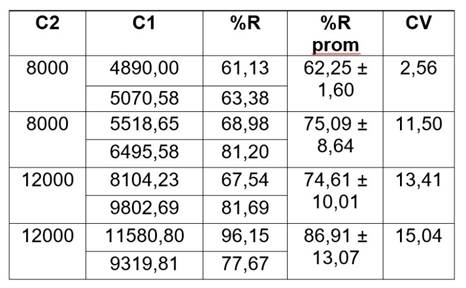
C1: Cantidad de acrilamida encontrada (µg kg-1) C2: Cantidad de acrilamida adicionada (µg kg-1) %R: Porcentaje de recuperación %R prom: Porcentaje de recuperación promedio CV: Coeficiente de Variación (%) * Extractos analizados a una longitud de onda de 210 nm y un flujo de 0,4 mL min-1
A pesar de los esfuerzos por aumentar el rendimiento en la extracción, los valores de recuperación no alcanzaron el 100 %. La alternativa para solucionar dicha situación es cambiar el solvente de extracción. Rosén y Hellenäs [21] en su investigación reportaron que la selectividad de extracción es bastante baja cuando se usa agua, por lo cual se requiere limpieza de la muestra, separación analítica eficiente y detección altamente selectiva.
Evaluación del método
Determinación de linealidad y sensibilidad. La linealidad entre el área de pico y la concentración se analizó mediante una curva de calibración obtenida con soluciones estándar de acrilamida en 9 concentraciones (50, 200, 400, 600, 800, 2000, 1200, 1.400 y 1.600 µg L-1) leídas por triplicado. La ecuación lineal obtenida por el método de mínimos cuadrados para acrilamida fue:
La linealidad del método en el intervalo de 50 a 1.600 µg L-1, presentó un coeficiente de determinación (r2) de 0,995. Las pruebas estadísticas corroboraron la linealidad de la curva, rechazándose la hipótesis nula (la no correlación entre X y Y), por lo que la correlación lineal es significativa. Adicionalmente, mostraron que no se encontró error sistemático.
La sensibilidad del método se determinó con el límite de detección (LOD) y el límite de cuantificación (LOQ) que se calcularon mediante la curva de calibración.
Los límites de detección y de cuantificación mostraron valores de 6,38 y 19,32 µg kg-1, respectivamente, encontrándose por debajo de la concentración más baja de la curva de calibración. Aunque el equipo detectó la concentración de 6,38 µg kg-1, no es confiable cuantificarla desde este nivel. Estadísticamente existe mayor confianza en cuantificarla con valores por encima de 19,32 µg kg-1. Mesias et al. [18] en su estudio establecieron como límite de detección de acrilamida para alimentos a base de papa un valor de 20 µg kg-1.
Cantidad de acrilamida presente en las muestras analizadas
Según la Resolución 2158 de 2017 del Reglamento expedido por la Unión Europea [1] se establece que los niveles de acrilamida presente en papas fritas deben ser iguales o menores a 500 µg kg-1. Según esto, se puede afirmar que el contenido de acrilamida presente en las muestras de snacks de papa de la marca comercial analizadas fue de 442,95 µg kg-1, valor que está por debajo de los niveles de referencia. Sin embargo, los “valores indicativos” presentados en el Reglamento 2017/2158 no son umbrales de seguridad, sino que sólo pretenden indicar cuando los valores sean superados, la necesidad de realizar una investigación y, generar medidas de control y mitigación.
CONCLUSIONES
Los parámetros evaluados influyen de manera importante en el rendimiento de las extracciones, excepto el ultrasonido, que fue el único que no presentó un efecto significativo sobre el porcentaje de extracción de la acrilamida.
Las condiciones de extracción que permitieron obtener un mejor rendimiento fueron: cantidad de Carrez (8 g MgSO4 y 1 g NaCl), cantidad de muestra de 0,5 g y dopaje en el momento de la extracción, flujo de 0,4 mL min-1 y longitud de onda de 210 nm.
El contenido de acrilamida encontrado en los snacks de papa estudiados está por debajo del valor de referencia establecido en el reglamento de la Unión Europea, siendo éste el referente para Colombia, debido a la inexistencia de regulación de la acrilamida en el país.