INTRODUCCIÓN
El uso indiscriminado de antibióticos promotores de crecimiento (APC) en los sistemas de producción animal ha incrementado la resistencia de bacterias patógenas intestinales, lo que provoca problemas sanitarios [1]. Las bacterias, como todos los seres vivos, tienen la capacidad de adaptarse a los cambios en el ambiente para mejorar su supervivencia. Junto a lo anterior, el ciclo biológico de las bacterias es corto, lo que eleva la probabilidad de presentar mutaciones que favorecen la resistencia [2]. Por otra parte, se ha observado que los microorganismos tienen la facultad de transmitir genes resistentes a otras especies bacterianas, lo que incrementa el problema [3].
Para evitar estas dificultades, las investigaciones se han enfocado en el uso de microorganismos que crean antagonismo con bacterias patógenas [4]. Dentro de este grupo, se encuentran las bacterias ácido lácticas (BAL), que se han estudiado de manera amplia en los seres humanos y algunas especies animales [5]. Al respecto, Lactobacillus casei ha mostrado efectividad en el control de bacterias patógenas y se ha descubierto que su antagonismo es producto de mecanismos como la disminución del pH del ambiente por la producción de ácido láctico, la producción de bacteriocinas, exclusión competitiva, y la estimulación del sistema inmune del huésped [4-6]. Todos estos mecanismos demuestran que L. casei es una bacteria con alto potencial para el manejo como microorganismo probiótico.
Sin embargo, el estudio de estos microrganismos en el cuy (Cavia porcellus) es escaso y falta mucho por comprender sobre la forma como interactúan con esta especie [7]. Al respecto, Aviles-Esquivel et al. [8] mencionan que el cuy es un animal herbívoro no rumiante, que se cría en la región andina de américa del sur como fuente de proteína. Se indica que el cuy se ha constituido en una especie productiva de alto rendimiento en los algunos países suramericanos, que ayuda a la seguridad alimentaria de zonas marginadas y con alto índice de pobreza [9].
De acuerdo a lo anterior, el objetivo de esta investigación fue determinar los efectos del suministro de L. casei en los parámetros productivos e histológicos del cuy (Cavia porcellus).
MÉTODO
Los experimentos fueron aprobados por el comité de ética de la Universidad de Nariño y los procedimientos se realizaron teniendo en cuenta las normas de bienestar animal de la República de Colombia.
Los análisis se realizaron en el laboratorio de investigación PROBIOTEC-FORAPIS, él área de cátedra y servicio de patología veterinaria de la clínica veterinaria Carlos Martínez Hoyos, el bioterio y laboratorios especializados de la Universidad de Nariño (Pasto, Colombia), situado entre los 2,500 y 2.800 msnm, tiene una precipitación de 980 mm, temperatura de 13,1°C y humedad relativa promedias del 73%, respectivamente. De igual manera, se utilizó el servicio de microscopia electrónica de la Universidad Nacional, Sede de Medellín (Colombia).
Se usó la cepa comercial Lactobacillus casei ATCC® 11456. Se ajustó el inóculo, y se realizaron pruebas de resistencia a pH de 7,5 y 9, siguiendo los procedimientos descritos por Jurado-Gámez et al.[10].
Para el ensayo in vivo se utilizaron 110 cuyes machos destetos (14 días de edad) de línea mejorada provenientes de una explotación particular tecnificada de cuyes del municipio de Tuquerres (Nariño, Colombia), con un peso promedio de 300± 0,5 g; los animales se distribuyeron en 4 tratamientos con 10 réplicas por tratamiento y 3 animales por réplica. Los tratamientos evaluados fueron: T1 alimento balanceado, forraje y agua destilada; T2 alimento balanceado, forraje y L. casei; T3 forraje y agua destilada; T4 forraje y L. casei. Los animales tuvieron un periodo de adaptación de cinco días, y el ensayo tuvo una duración de 40 días. El alimento balanceado no tuvo aditivos promotores de crecimiento y el agua destilada se usó como excipiente (placebo) en los tratamientos T1 y T4.
El inóculo (L. casei) se suministró de forma oral mediante un gotero, a razón de 5 mL/animal/día distribuido en dos tomas (2,0 mL cada suministro), la primera a las 7:00 am y la segunda a las 5:00 pm. Se utilizó una concentración de 1 x 109 UFC/mL en el inóculo. Para la dieta con suplemento se suministró 310 g de forraje y 30 g de alimento balanceado, y para los tratamientos con solo forraje, este se incrementó 50 g para un total de 320 g día.
Al final de la investigación, los animales fueron sacrificados mediante la administración intravenosa de Pentobarbital sódico (390 mg/mL) y difenilhidantoína sódica (50 mg/mL) a una dosis de 1 mL/kg peso. Se realizó evaluación macroscópica de los animales siguiendo la técnica de necropsia estandarizada por el laboratorio de patología de la Universidad de Nariño [11]. Se tomaron muestras del tracto gastrointestinal y se colocaron en formol buferado al 10% para fijación por 24 horas, luego se realizó el corte de duodeno, yeyuno e íleon y se ubicaron en cassettes para inclusión de tejidos debidamente rotulados; se les realizó inclusión en parafina y coloración de hematoxilina y eosina. Este procedimiento se realizó en las instalaciones de la fundación hospital San Pedro de Pasto (Colombia). De igual manera, se determinó el contenido de ácido láctico en la carne de cuy.
Se determinaron las variables productivas consumo de materia seca (CMS), ganancia de peso (GP) y conversión alimenticia (CA). De las muestras de sangre se determinó cuadro hemático, nitrógeno ureico (BUN) y creatinina, finalmente, se realizó análisis coprológico. La muestra de sangre fue obtenida por punción intracardiaca y las muestras de heces fueron tomadas directamente del colon al momento del sacrificio.
Los micropreparados de Hematoxilina y Eosina (H/E) de rutina se describieron y evaluaron histológicamente mediante visualización a través de microscopia óptica; para esto se tuvo como referencia histológica a Scundamure [13] y para la descripción de alteraciones microscópicas a Jubb et al. [13].
Las tinciones diferenciales fueron Tinción de Gram para identificación de bacterias Gram positivas y/o negativas; y ácido peryódico de Schiff (PAS) para detección de glucógeno y carbohidratos. Estas láminas se realizaron en la Corporación de patología veterinaria Corpavet® en la ciudad de Bogotá, Colombia.
Para precisar los hallazgos se emplearon marcadores monoclonales inmuno-histoquímicos de uso en humanos CD3 y CD79a a los bloques de parafina del tracto gastrointestinal de los animales para evaluar la expresión de linfocitos T y B del tejido linfoide asociado al intestino GALT.
Las muestras de los segmentos conservadas en glutaraldheido al 5% fueron analizadas en el Laboratorio de Microscopia electrónica de barrido de la Universidad Nacional, sede Medellín utilizando el protocolo para el procesamiento de este tipo de muestras definido por dicho Laboratorio.
La cepa láctica fue microencapsulada de acuerdo con lo descrito por Rodríguez et al. [14]; para ello, la bacteria se suspendió al 20% p/v (60 g de Maltodextrina y 60 g de Inulina en 280 mL de Inóculo bacteriano previamente ajustado) en relación 1:1 p/p la cual se agitó hasta homogenizar.
Se utilizó el equipo de secado por aspersión Secador Spray Bilon 6000s®, con una temperatura de entrada de 170°C y una temperatura de salida en un rango de 65 a 67°C con ciclo completo de 2 horas y 30 minutos. El material microencapsulado se empaquetó en recipientes oscuros de plástico previamente esterilizados y se almacenaron a temperatura ambiente (20 ± 2°C).
Las pruebas de resistencia a diferentes pH se evaluaron mediante un diseño irrestrictamente al azar. Los parámetros productivos, la química sanguínea y el hematocrito fueron analizadas mediante análisis de varianza con el procedimiento PROC GLM del paquete estadístico SAS University [15]. El peso inicial se incluyó como covariable para consumo de materia seca. La comparación de medias se realizó con el procedimiento LSMEANS a un nivel de significancia del 5%.
Para la caracterización microscópica, histoquímica e inmunohistoquímica del tracto gastrointestinal se empleó estadística descriptiva y registro fotográfico del proceso.
RESULTADOS
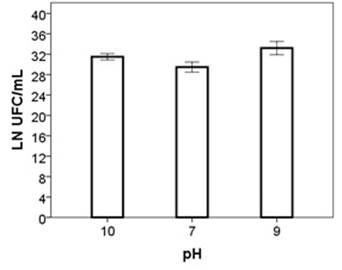
Los resultados mostraron que la bacteria fue resistente a pH básico, con un mayor crecimiento a pH 9 (p< 0,05; figura 1).
El suministro de agua destilada y el inóculo no mostraron problemas al momento de suministrarlos. Los resultados para consumo, ganancia de peso y conversión alimenticia se pueden observar en el cuadro 1 .
Cuadro 1 Valores de consumo de alimento, ganancia de peso y conversión alimenticia en cuyes.
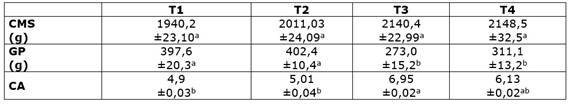
CMS: consumo de materia seca, GP: ganancia de peso, CA: conversión alimenticia.
Los valores indican que no hay diferencias en el CMS (p>0,05). La ganancia de peso fue menor para los tratamientos T3 y T4 (p< 0,05), mientras que la conversión alimenticia fue mas alta para el tratamiento T3 (p<0,05).
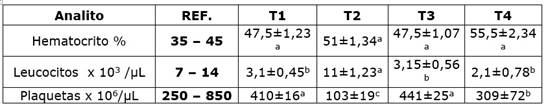
Los resultados del hemograma se observan en el cuadro 2. No hubo diferencia para el contenido de hematocritos (p> 0,05), mientras que los leucocitos y las proteínas totales fueron mayores en el T2 (p< 0,05); en cuanto a las plaquetas, se observa que T2 muestra el menor valor y los tratamientos T1 y T3 los valores más altos (p<0,05); los neutrófilos fueron menores para el T3 y los linfocitos fueron menores en el T4 y mayores en el T3 (p<0,05).
En el cuadro 2 se indican los resultados de BUN y creatinina. Se usaron como referencia los valores determinados por Washington y Van Hoosier [16]. El valor de creatinina fue diferente para el tratamiento T2 (p<0,05), tratamiento que presentó valores inferiores a los de referencia; los otros valores no difirieron y se encuentran dentro del rango reportado. En cuanto a BUN, los valores encontrados fueron similares (p> 0,05), pero mayores a los de referencia.
Las características macroscópicas del coprológico mostraron valores normales para la especie con coloración marrón oscura, consistencia líquida, presencia de moco y no se observaron parásitos. Para las características microscópicas (cuadro 2), los resultados fueron positivos para la presencia de Isoporas en los tratamientos T1 y T2 y positivo en T3 para tropozoitos ciliados.
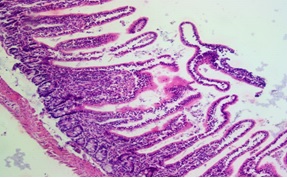
Las placas teñidas no mostraron lesiones representativas en los tratamientos con L. caseí, pero si se observaron lesiones en los tratamientos control (figura 2).
En la Figura 3A se presenta los tejidos de duodeno. Esta tinción fue positiva para todos los tratamientos y su capa presentaba mayor grosor y fue más evidente que en los controles.
En la Figura 3B se indica la marcación para linfocitos T (CD3). Inicialmente la imagen (B1) corresponde al control y la (B2) al segmento íleon del tratamiento 4 con fuerte inmunomarcación.
En la figura 3C se observa la marcación de linfocitos B (CD79). En la imagen (C1) del control positivo y la (C2) de duodeno, se aprecia fuerte inmunomarcación para linfocitos B. Se evidenció la presencia de ácido láctico en la carne de cuyes suplementados con cepas probióticas, con valores de 0,96 y 1,42 mg/g de carne; mientras que en los animales control no fue detectado.
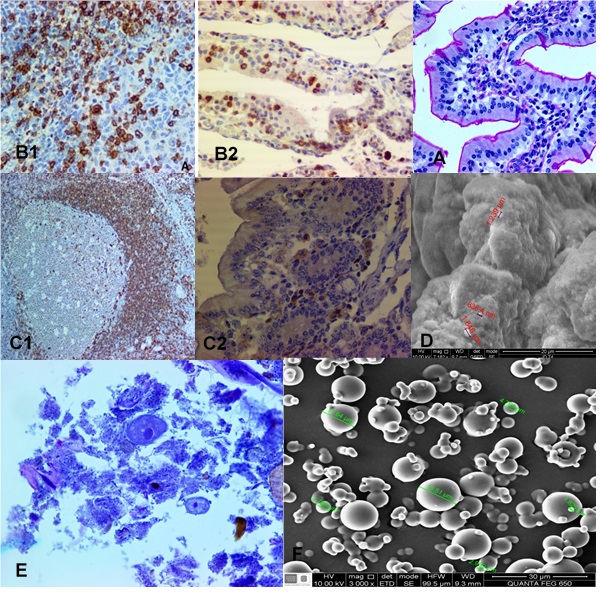
Figura 3. Tinciones de inmunohistoquímica, Alcian Blue y diferenciadoras para el intestino delgado; microfotografías del tejido intestinal de Cavia porcellus; y microencapsulado de Lactobacillus caseí. A: tinciónde células caliciformes; B1: marcación linfocitos T (testigo); B2: marcación linfocitos T (ileon T4); C1: marcación linfocitos B (testigo); C2: marcación linfocitos B (duodeno T4); D: microencapsulación; E: parásito Balantidium coli (colon T1); F: tamaño y forma del microencapsulado.
Otros hallazgos
En la Figura 3E se presenta la morfología del parasito Balantidium coli, el cual fue observado durante el análisis de las láminas de Hematoxilina y Eosina sobre todo en el colon. Este parásito se identificó en los tratamientos 1 y 3 los cuales no recibieron Lactobacillus casei. Los resultados de la microencapsulación se observa en la figura 3F, lo que indica que la bacteria fue microencapsulada de manera efectiva.
Los microorganismos candidatos a probiótico deben tener la capacidad de resistir los cambios en el pH del tracto gastrointestinal [17]. La zona del estómago presenta pH muy bajo, de alrededor de 3, lo que imposibilita el crecimiento microbiano y se constituye en una barrera efectiva para invasores bacterianos [18]. Sin embargo, los análisis realizados en otros estudios in vitro han demostrado que L. casei tiene la capacidad de resistir estos pH tan bajos [10]. Al respecto, Subramanian et al. [19] manifiestan que las BAL disponen de mecanismos para regular la concentración de hidronios en el interior de la célula, que les permite disminuir su contenido y con ello evitar la acidez de su medio intracelular.
Dado que el estómago no es la única barrera en el tracto gastrointestinal, la porción del intestino delgado presenta valores de pH alcalinos, que alcanzan valores de 10; esto se convierte en un problema para la sobrevivencia de las bacterias probióticas [20]. La evaluación de diferentes pH alcalinos demostró buena viabilidad de L. casei a estas concentraciones. Al respecto, Aliaga et al. [21] indican que el intestino del cuy llega a presentar un valor de pH alrededor de 8 que es inferior a pH 10 evaluado en esta investigación, lo que posibilita la sobrevivencia de L. casei en esta zona, que le permitiría competir con otros organismos presentes en el tracto gastrointestinal del cuy [22]. Liu et al. [23] indican que un crecimiento de 1 x 109 UFC/mL (20,72 Ln UFC/mL) es adecuado para colonizar el tracto gastrointestinal; al respecto, los valores encontrados en los distintos pH demuestran que la cepa tolera estas condiciones. Sin embargo, el crecimiento a pH 9 fue mayor, lo que indica que a estas condiciones, la cepa tiene mayores probabilidades de sobrevivencia.
En cuanto al consumo, Guevara y Carcelén [24] encontraron valores similares con el suministró de Lactobacillus y levadura. Por otra parte, Sáez-Lara et al. [25] indican que los probióticos no alteran la ingesta de los animales, corroborando los resultados encontrados. Aunque en otras especies, se ha observado una mejora en el consumo de los animales [26,27], todavía no existe un consenso al respecto, por lo que falta mayor información para tener resultados concluyentes [28,30].
Los resultados para la ganancia de peso se deben al alimento balanceado, ya que los tratamientos T3 y T4 recibieron solo forraje. Al respecto, Caicedo et al. [9] mencionan que el cuy tiene un mayor rendimiento productivo cuando la dieta de forraje es enriquecida con el suministro de alimento balanceado, factor que explica las diferencias encontradas entre tratamientos. Sin embargo, todos los valores son similares a los reportados por Ramos et al. [31], lo que indica que no se alteró de manera significativa el parámetro bajo las condiciones evaluadas. Para la conversión alimenticia, los resultados son similares a la GP y se pueden explicar bajo el mismo fenómeno [32].
Los hallazgos histológicos muestran que L. casei se adhirió al tracto digestivo y muestra características de agente controlador de organismos patógenos. Los trabajos de Gamboa et al. [33] y Santarmaki et al. [34] mencionan que esta característica es muy importante para evaluar cepas bacterianas con fines probióticos. Entre los mecanismos antagónicos se ha observado que L. casei produce bacteriocinas que tienen diferentes formas de acción [35], algunas afectan directamente la membrana celular de otros microorganismo, otras inhiben procesos metabólicos vitales para la célula y, en la mayoría de los casos, las BAL pueden disminuir el pH del medio con la producción de ácido láctico [36]; todos estos mecanismos pueden regular el crecimiento de otros microorganismo y crear una barreras protectoras para el organismo huésped [37].
De igual manera, los hallazgos en el análisis coprológico mostraron una disminución de parásitos como consecuencia de la acción inhibitorio de L. casei. Sin embargo, falta conocer mucho sobre los mecanismos de acción con este tipo de parásitos, para identificar que realmente los efectos observados son consecuencia de los tratamientos evaluados [38].
La inmunomarcación observada puede ser una respuesta al daño tisular generado por las lesiones encontradas en los tejidos, un probable crecimiento bacteriano o una reacción con el medio de cultivo suministrado. Estos resultados indican que para el caso de los cuyes, el suministro de una dieta líquida alteró las condiciones gastrointestinales de los animales. Al respecto, los estudios realizados por Bustios et al. [39] revelan que en especies que tienen un bajo consumo de agua de bebida y que suplen sus requerimientos de este importante nutriente a través de los alimentos consumidos, pueden presentar alteraciones en el tracto digestivo como consecuencia del suministro de una sustancia (agua), cuando estos no se encuentran adaptados a este tipo de suministro.
CONCLUSIONES
El suministro de Lactobacillus casei en cuyes (Cavia porcellus) no afecta los parámetros productivos de consumo de alimento y ganancias de peso, pero si mejora la conversión alimenticia de los animales alimentados solo con forraje; lo anterior demuestra que el suministro de la bacteria láctica puede ser una alternativa al uso de antibióticos en los sistemas de producción. La inmuno histoquímica y la tinción Alcian Blue demostraron ser una herramienta útil para determinar lesiones en cuy. Sin embargo, se debe continuar con la evaluación de la cantidad de inóculo a suministrar.