INTRODUCCIÓN
El ñame, Dioscorea spp. es un cultivo básico de la dieta de millones de personas habitantes en regiones tropicales y subtropicales del mundo, su valor nutricional respalda su importancia en la seguridad alimentaria (Kiba et al., 2020; Morse, 2021). En el Caribe colombiano es el tubérculo más cultivado, es básico de la dieta de sus pobladores y los excedentes son una fuente de ingresos (Pérez y Campo, 2016). El ñame, además de su consumo fresco ha ganado importancia en la industria farmacéutica Wumbei et al., 2019; Silva et al., 2021), igualmente, la presencia de polisacáridos con capacidad antioxidante, ha estimulado su consumo en la dieta humana (Zhou et al., 2021; Shao et al., 2022).
La producción mundial de ñame es de 74.321.794 t, de las cuales el 90 % son producidas en Nigeria con 50.052.977 t, seguido por Ghana 8.288.198 t, Costa de Marfil 7.148.000 t y Benín con 3.088.498 t; Colombia se ubica en el noveno lugar con 409.165 t, según la Organización de las Naciones Unidas para la Agricultura y la Alimentación (FAO, 2019). En Colombia, la producción en el 2019 fue de 302.893,82 t; donde el 77 % se produjo en la región Caribe, en los departamentos de Bolívar y Córdoba y Sucre con 111.064, 85.288 y 37.269 t, respectivamente, de acuerdo con el Ministerio de Agricultura y Desarrollo Rural (MADR, 2019), es un cultivo de economía familiar (MADR, 2020) que tiene como limitantes de la producción, la baja tecnología y bajos rendimientos (Kiba et al., 2020).
Las especies más cultivadas son Dioscorea alata L. y Dioscorea rotundata Poir (Campo y Royet, 2020), donde D. alata es la más susceptible a la antracnosis Colletotrichum gloeosporioides Penz (Campo et al., 2009). La antracnosis es considerada como la enfermedad más devastadora del cultivo en el mundo (Kwodaga et al., 2019; Ntui et al., 2021) cuyos síntomas se presentan inicialmente en las hojas, con la aparición de puntos rojos, que con el tiempo se necrosan, los tallos se ennegrecen y en los genotipos susceptibles se presenta necrosis apical y muerte descendente (Campo y Royet, 2020).
Los síntomas de la antracnosis en los genotipos de D. alata y D. rotundata, se manifiestan entre ellos con diferentes niveles de daño debido a la variabilidad genética entre los cultivares y a la diversidad patogénica de los aislados de C. gloesporioides (Onyeca et al., 2006; Jiménez et al., 2009). Los cultivares de D. alata más sembrados en la región Caribe colombiana se identifican con los nombres regionales de Diamante 22, Concha de coco y Osito, siendo los dos últimos los de mayor susceptibilidad, pero los más preferidos por el consumidor local (Campo y Royet, 2020).
La estrategia más recomendada para el manejo de la enfermedad es el manejo integrado (Campo y Royet, 2020), destacándose el uso de la resistencia genética, ya que el control químico presenta limitantes al detectarse la resistencia de aislados de Colletotrichum spp. a varias moléculas fungicidas empleadas en el manejo (Han et al., 2018; Arce et al., 2019); se reporta resistencia a carbendazim (Han et al., 2018) y a tebuconazol (Kim et al., 2020); además, el control químico no ha sido adoptado por los pequeños, los cuales no disponen de la tecnología ni del presupuesto para invertir en estrategias que involucren el empleo de agrotóxicos (Nwadili et al., 2017). Otra estrategia que se viene investigando a nivel In vitro es el uso de aceites esenciales y de extractos vegetales, con resultados promisorios (Pérez et al., 2017; Kwodaga et al., 2019). En el manejo de la enfermedad no se puede descuidar el manejo de las malezas, ya que 15 familias de arvenses se han reportado hospedantes de C. gloeosporioides y C. truncatum (Dentika et al., 2021).
La resistencia genética es la estrategia en la que más se ha investigado, obteniéndose resultados promisorios con cruzamientos inter específicos, sin embargo, aún no se ha logrado una buena calidad de tubérculos (Lebot et al., 2019). El mejoramiento clásico se dificulta por la baja tasa de compactibilidad de la biología floral de la especie y entre especies, siendo importante abordar otras estrategias de mejoramiento (Mondo et al., 2020). La identificación de genotipos con resistencia a la antracnosis en los bancos de germoplasma de ñame se ha realizado en diferentes ambientes, mediante experimentos en campo, casa de malla o laboratorio, bien sea con inoculaciones artificiales o evaluación en áreas epidémicas (Nwadili et al. 2017; Ayisah et al., 2019; Arya et al., 2019). La clasificación de la resistencia se realiza con escalas de severidad (Simons y Green, 1994), a los 120, 150, o 180 días después de la siembra (Onyeca et al., 2006). Correspondiendo para el Caribe húmedo colombiano con las fases fenológicas de máximo crecimiento vegetativo, tuberización media y máximo llenado del tubérculo respectivamente (Campo y Pérez, 2015). Otras investigaciones reportan exitosamente la evaluación de la resistencia de germoplasma a enfermedades, empleando herramientas estadísticas como la determinación del área bajo la curva de progreso de la enfermedad (Onyeca et al., 2006; Ariyo et al., 2014), sin embargo, la aparición de nuevas cepas de Colletotrichum spp. en los cultivos de ñame mucho más virulentas, hacen que el desarrollo de nuevas variedades con resistencia a la enfermedad sea cada vez más crítico (Ntui et al., 2021)
En Colombia, son pocos los estudios que se han realizado para identificar la resistencia de las diferentes colecciones de ñame a la antracnosis, lo cual es importante realizarlo periódicamente debido a la dinámica de poblaciones de Colletotrichum spp., causantes de la antracnosis, reportándose aislados con diferentes grados de virulencia; por lo tanto se plantea este estudio para evaluar la resistencia de las accesiones de D. alata y D. rotundata, pertenecientes a la colección de ñame de la Universidad de Córdoba, Colombia, a la enfermedad.
MÉTODO
Localización
La investigación se realizó en el banco de germoplasma de Dioscorea spp. del campus de la Universidad de Córdoba, ubicado en el municipio de Montería a 14 m.s.n.m. 8º 44’ latitud norte y 75º 53’ de longitud oeste con precipitación anual de 1.346,1 mm humedad relativa del 84 %, temperatura promedio de 27,4 ºC y brillo solar de 2.108,2 horas, según el Instituto de Hidrología, Meteorología y estudios Ambientales (IDEAM, 2020).
Establecimiento del experimento. En junio de 2015, se establecieron 84 accesiones de D. alata (Cuadro 1) y 28 accesiones de D. rotundata (Cuadro 2) en el campus de la Universidad de Córdoba, área endémica de la enfermedad (Pérez y Campo, 2016). Cada accesión fue sembrada en parcelas de dos surcos de 5 m de largo a 1 m entre plantas y entre surcos. La severidad de cada accesión se determinó evaluando tres plantas por surco, en los tercios inferior, medio y superior del dosel a los 120, 150 y 180 días después de la siembra DDS, empleando la escala de Simons y Green (1994).
Cuadro 1 . Accesiones establecidas de Dioscorea alata en el banco de germoplasma de la Universidad de Córdoba durante el año 2015.
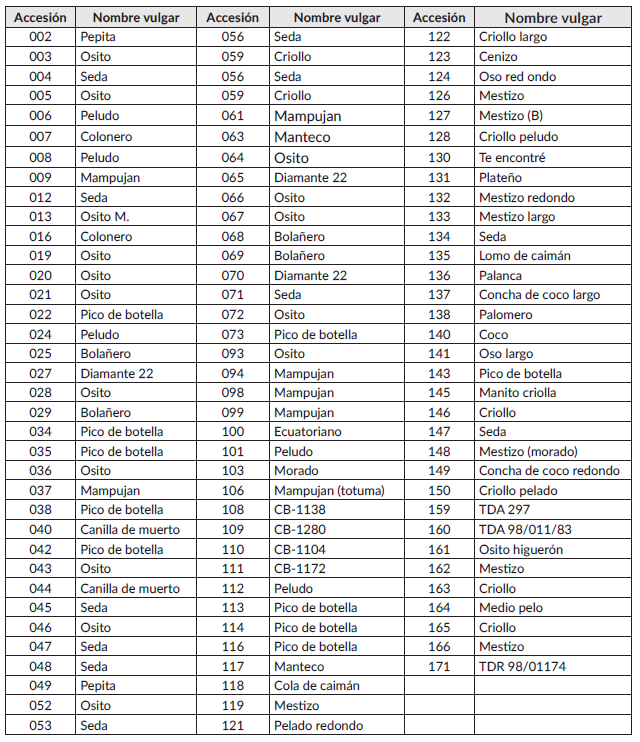
Cuadro 2 Accesiones establecidas de Dioscorea rotundata en el banco de germoplasma de la Universidad de Córdoba durante el año 2015.
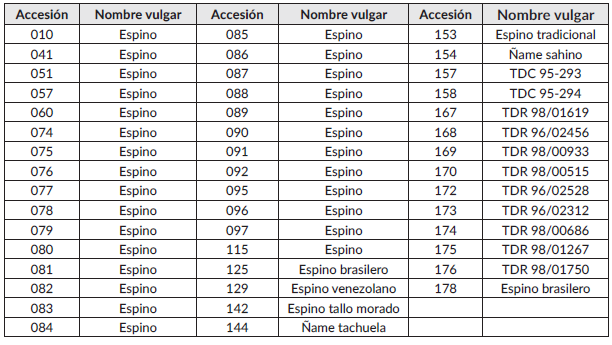
Clasificación de los genotipos por su resistencia a la antracnosis. El agrupamiento se realizó con los datos obtenidos con la escala de severidad empleando dos métodos: el primero se hizo siguiendo la metodología Simons y Green (1994) con modificaciones, agrupando como resistentes las accesiones con un daño foliar entre 0 y 12 % (clases 0, 1, 2 y 3), moderadamente resistentes, clase 4=entre 12 y 25 %; mediana susceptibilidad clase 5= entre 25 y 50 %; susceptible clase 6= > 50 %, a los 120, 150 y 180 días después de la siembra.
El segundo método fue el de agrupar las accesiones de acuerdo a la desviación estándar (DE) con la gran media; para esto se determinó el área bajo la curva de progreso de la enfermedad ABCPE, la cual se hizo con la integral de la severidad a los 120, 150 y 180 días después de la siembra (Campbel y Madden, 1990). Empleando el programa de Excel se asignó un rango para cada accesión, se estimó la gran media del rango y se clasificó la resistencia de cada genotipo basándose en la desviación estándar con la gran media, donde, de -2 a -1,1 desviaciones estándar DE se clasificaron como resistentes; de -1,0 a -0,1 DE como moderadamente resistentes; de 0,0 a 1,0 DE como moderadamente susceptibles y de 1,1 a 2,0 DE como susceptibles (Onyeka et al., 2006).
Finalmente, se determinó la relación lineal entre los parámetros de la enfermedad, escala de severidad, ABCPE y la tasa de progreso de la enfermedad. Este análisis fue realizado con el programa estadístico SAS (Statical Analysis Software) versión 9.4.
RESULTADOS
Las accesiones de ñame de D. alata y D. rotundata fueron afectadas por la antracnosis en diferentes grados de severidad, presentándose los primeros síntomas a partir de los 120 días después de la siembra DDS, en tanto que la epidemia se estableció aproximadamente desde los 160 DDS. La clasificación de la resistencia en los puntos críticos 120 y 150 DDS, no pudo realizarse por presentar baja severidad.
Con relación a las especies, las accesiones de D. alata fueron más susceptibles, presentándose a los 180 DDS una severidad media de 32,6 %, observándose presencia de la enfermedad en las 84 accesiones siendo la accesión 164 la menos afectada con 0,27 % y la más afectada fue la accesión 027 con 83,3 %. La media de la severidad de las accesiones de D. rotundata fue de 15,5 %, siendo la menos afectada la accesión 293 con 0,86 % y la más afectada la 086 con 55,2 %.
La distribución de la antracnosis en el dosel de la planta, independiente de la especie, se desarrolló de forma ascendente, manifestándose inicialmente en el tercio inferior. La severidad a los 180 DDS en promedio para D. alata en el tercio inferior fue del 40 %, mientras que en D. rotundata fue del 31 %. Las clasificaciones de la resistencia de las accesiones se presentan en las Cuadros 3 y 4, observándose variabilidad en la resistencia, siendo mayor en las accesiones de D. rotundata con un coeficiente de variación de 100 %, mientras que para D. alata fue de 62,75 %. El 38 % de las accesiones D. alata se agruparon con resistencia y mediana resistencia, mientras que para D. rotundata el 50 % se ubicaron entre resistentes y medianamente resistentes (Cuadro 5).
Cuadro 3 Clasificación de la resistencia de las accesiones D. alata a la antracnosis C. gloeosporioides, mediante los métodos de escala de notas (EN) y la suma de rangos.
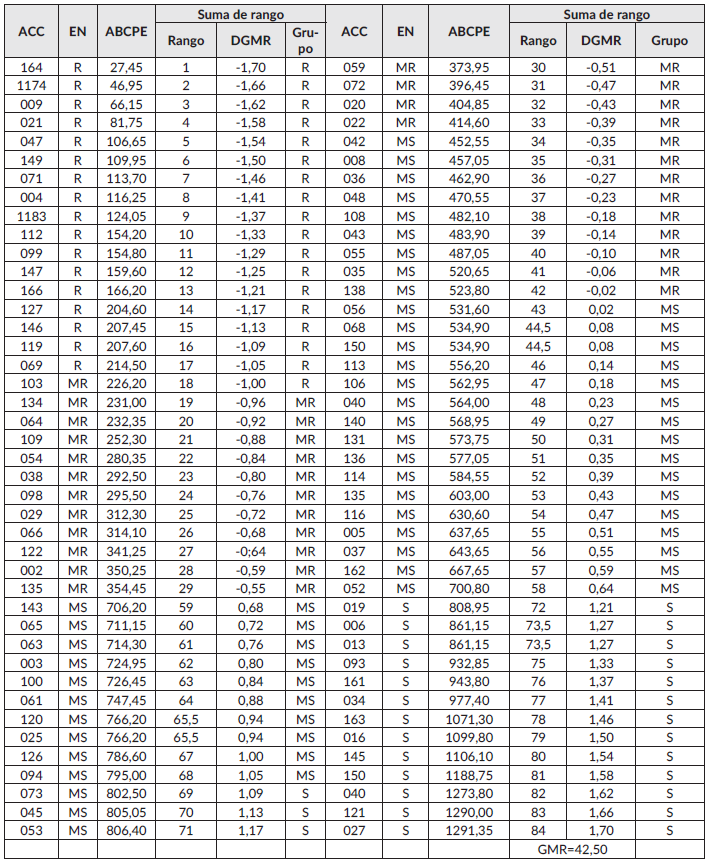
ACC: Accesión; EN: Escala de notas con severidad de la enfermedad a los 180 DDS; GMR: Gran media del rango; ABCPE: Área bajo la curva de progreso de la enfermedad a los 120, 150 y 180 DDS; DGMR: Desviación del rango de la gran media de rango [DGMR=(Rango-GMR)/D. Estándar del rango]; R: Resistente; MR: Medianamente resistente; MS: Medianamente susceptible; S: Susceptible.
Cuadro 4 Resistencia de accesiones de D. rotundata a la antracnosis C. gloeosporioides mediante los métodos de escala de notas y el de suma de rangos del área bajo la curva del progreso de la enfermedad.
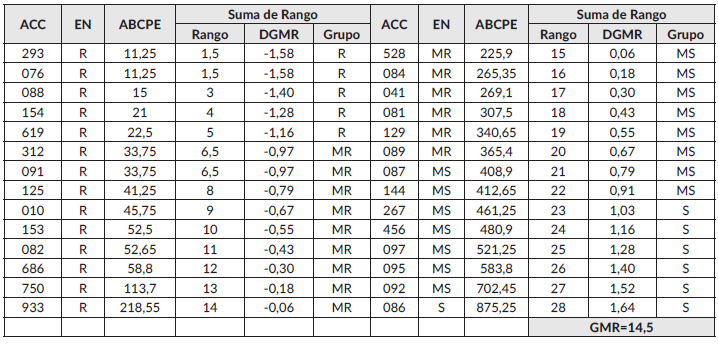
ACC: accesión; EN: Escala de notas con severidad de la enfermedad a los 180 DDS; GMR: Gran media del rango; ABCPE: Área bajo la curva de progreso de la enfermedad a los 120; 150 y 180 DDS; DGMR: Desviación del rango de la gran media de rango [DGMR=(Rango-GMR)/D. Estándar del rango]; R: Resistente; MR: Medianamente resistente; MS: Medianamente susceptible; S: Susceptible.
Cuadro 5 Agrupamiento por resistencia a la antracnosis, accesiones de D. alata y D. rotundata, mediante escala de notas (EN) y suma de rangos del área bajo la curva de progreso.
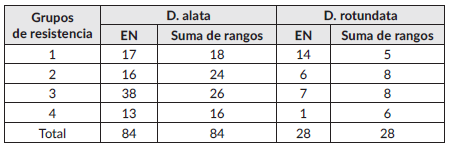
Grupos de resistencia: 1=Resistente; 2= Moderadamente resistente; 3= Moderadamente susceptible; 4=Susceptible. EN: escala de notas a los 180 días después de siembra DDS. Suma de rangos a los 120, 150, 180 DDS
La clasificación realizada con la escala de severidad a los 180 DDS y, mediante la suma de rangos del ABCPE, permitió identificar diferencias en cuanto a la resistencia de los genotipos, teniendo fuerte relación en las accesiones de D. alata, con el número de accesiones resistentes, coincidiendo en el 94 % de las accesiones y susceptibles el 81,25 % con los dos métodos de clasificación, mientras que las accesiones de D. rotundata no presentaron una buena relación entre los dos métodos.
El método de suma de rangos del área bajo la curva permitió clasificar con mayor claridad las accesiones de las dos especies en los cuatro grupos de resistencia, identificándose en la especie D. alata 18 accesiones resistentes, 24 moderadamente resistentes, 26 moderadamente susceptibles y 16 susceptible. En las 28 accesiones de D. rotundata, seis fueron resistentes, ocho moderadamente resistentes, ocho moderadamente susceptibles y seis susceptibles.
Relación entre los parámetros de la enfermedad. Las evaluaciones de severidad realizadas con la escala de severidad a los 120 y 150 DDS no mostraron relación con el área bajo la curva de progreso ni con la tasa aparente de infección, presentando una alta dispersión de los datos y un bajo coeficiente de determinación (datos no mostrados), por presentarse en esas épocas baja severidad en las accesiones de las dos especies oscilando entre 0 y 5 % de severidad. La severidad medida a los 180 DDS en las accesiones de D. alata y D. rotundata tuvo una fuerte relación lineal con el ABCPE y con la tasa aparente de infección con r= 0,99 para las dos especies (Figura 1); igualmente, la tasa de progreso de la enfermedad de las accesiones de D. alata y D. rotundata presentó correlación fuerte positiva con los niveles de severidad r= 0,98 y 0,99 respectivamente, sin embargo, el cultivar 059 de D. alata tuvo una mediana desviación de la línea de tendencia (Figuras 1A y 1C).

Figura 1 Relaciones entre la severidad de la antracnosis, en accesiones de ñame, a los 180 días, con el área bajo la curva de progreso ABCPE y la tasa de progreso de la enfermedad. A y C= D. alata; B y D= D. rotundata; (p=0,01)
La identificación de genotipos de ñame con resistencia a la antracnosis es una estrategia que se sigue implementando en los países productores gracias a la alta variabilidad que existe entre las diferentes colecciones de Dioscorea spp procedentes del INRA, IITA y otras que se encuentran en países caribeños, Sur América, países africanos, logrando identificar accesiones promisorias y estables en diferentes ambientes (Onyeca et al. 2006; Adefoyeke et al., 2008; Nwadili et al., 2017).
Durante el periodo de estudio, la antracnosis se estableció tardíamente en el banco de germoplasma de la Universidad de Córdoba, lo que impidió hacer la identificación de la resistencia a los 120 y 150 DDS, como lo proponen otros investigadores (Nwadili et al., 2017); luego, esas fechas críticas de evaluación y selección no siempre son las apropiadas para experimentos de campo cuando la epidemia se establece tardíamente (Onyeca et al., 2006), teniendo ventaja el uso del ABCPE por ser una medida integral, requiriendo mínimo dos evaluaciones, una al inicio de la epidemia y la otra al final (Ariyo et al., 2014).
El momento adecuado para identificar la resistencia de las accesiones con la escala de severidad fue a los 180 DDS cuando se obtuvo una buena distribución de la enfermedad en toda la colección. Comparando los métodos de agrupamiento de la resistencia a los 180 DDS, no hubo marcadas diferencias entre ellos, coincidiendo en las accesiones de D. alata, en la categoría resistente el 20,20 % y susceptibilidad del 15,40 %, mientras que con las accesiones de D. rotundata solo hubo relación para la categoría mediana resistencia de 21,40 % y mediana susceptibilidad del 25 % (Cuadro 5).
Independiente al método de selección, se afirma que la colección de Dioscorea spp de la Universidad de Córdoba tiene alta variabilidad de genes de resistencia a la antracnosis, agrupándose en las cuatro categorías, coincidiendo con la diversidad molecular de las accesiones de esta colección reportado por Rivera et al. (2012). La presencia de la enfermedad en diferentes fases fenológicas y su distribución espacial no uniforme, justifica la clasificación de la resistencia empleando el ABCPE para evitar escapes en la evaluación bajo condiciones de campo (Onyeka et al. 2006 y Nwadili et al., 2017).
CONCLUSIONES
El método más apropiado para clasificar la resistencia de las especies de Dioscorea spp., fue el de la suma de rangos del área bajo la curva de progreso de la enfermedad, permitiendo agrupar las accesiones de las dos especies en cuatro grupos de resistencia. Las accesiones identificadas como resistentes y moderada resistencia, pueden considerarse como genotipos promisorios, para futuros trabajos de mejoramiento genético o de liberación de clones con resistencia a la antracnosis.
Las accesiones de D. alata identificadas como resistentes fueron: 164, 1174, 009, 021, 047, 149, 071, 004, 1183, 112, 099, 147, 166, 127, 146, 119, 069, 103. En D. rotundata se identificaron como resistentes las accesiones: 293, 076, 088, 154, 619














