1. INTRODUCCIÓN
Ante el reto ambiental que enfrenta la industria petrolera por las exigencias en términos legislativos y comerciales, respecto a la cantidad de azufre permitido en los combustibles1-3, el proceso de Hidrodesulfuración (HDS) ha tomado mayor importancia y con él, las investigaciones orientadas al diseño de nuevos catalizadores que posean propiedades fisicoquímicas superiores a los de uso convencional, con el fin de encontrar nuevas alternativas que satisfagan las normas ambientales sobre emisiones de óxidos de azufre (SOx) y disminuyan el impacto económico que origina la presencia de azufre en el petróleo4-8. Motivo por el cual se han propuesto nuevas opciones que permitan obtener mejores resultados tales como: nuevas técnicas de síntesis, naturaleza de la fase activa y modificación del soporte9.
La y-alúmina es uno de los materiales cerámicos mesoporosos más importante y ampliamente utilizado en HDS10-12, debido a que posee alta área específica, sitios ácidos de Brónsted y Lewis, y excelente distribución de volumen y tamaño de poros13-19. Estudios recientes, han demostrado que por medio de la inserción de átomos como el cerio (Ce) en el soporte del catalizador modifica sus características fisicoquímicas, dando lugar a mejoras en las propiedades catalíticas (actividad, estabilidad térmica y tiempo vida útil)20,21. Por otro lado, se ha reportado que la adición de cerio a concentraciones bajas a la alúmina le provoca cambios texturales que incrementan su acidez Lewis (factor determinante en HDS, donde se tratan moléculas azufradas de alta basicidad)22. La posibilidad de generar las especies redox Ce3+ y Ce4+ que puedan favorecer la oxidación o reducción del metal activo y promotores presentes en el catalizador; así como también, la posible formación de compuestos intermetálicos del tipo Ce-Metal(23, 24). Además, la utilización de heteropolioxoaniones tipo Anderson como precursores catalíticos genera mejores resultados en procesos de HDS, debido a que presentan propiedades redox y ácidas asociadas al heteroátomo, disponibilidad de sitios de diferente reactividad en la estructura, preservación de la estructura en solución, relación metálica definida y uniformidad en la interacción con los soportes gracias a su ordenamiento regular25. Es por ello, que el propósito de este trabajo fue evaluar el efecto de la carga de Ce y el método de síntesis del soporte modificado con Ce en la actividad catalítica de hidrodesulfuración de tiofeno utilizando catalizadores a base de NiMo soportados sobre la alúmina modificada.
2. METODOLOGÍA
2.1 Síntesis de soportes y precursores catalíticos
2.1.1 Preparación de y-alúmina mesoporosa (γ-Al 2 O 3 )
Se mezcló en agua desionizada bajo agitación constante a 85°C, Al(NO3)3•6H2O, CO(NH2)2, C6H12O6 y C6H8O con una relación en masa de 1:10,9:0,54:0,1. Se ajustó el pH a 5 con hidróxido de amonio y se mantuvo durante 2h dando lugar a la formación de un gel, que posteriormente se secó a 110°C por 12 h (sólido color café) que luego se calcinó a 600°C por 5h (solido blanco)(26, 27).
2.1.2 Preparación de -alúmina dopada con cerio al 1% y 3% (γAl 2 O 3 -Ce)
Para la síntesis de 6g de alúmina dopado con cerio, se mezclaron en agua desionizada Al(NO3)3•6H2O, CO(NH2)2, C6H12O6, C6H8O y Ce(NO3)3•6H2O con una relación en peso para los dopados al 1% de 1:10,9:0,54:0,1:0,013 y 1:10,93:0,5405:0,1093:0,013 para los dopados al 3%. Con hidróxido de amonio se ajustó el pH a 5, se mezcló todo bajo agitación constante a 85°C y se mantuvo durante 2h. Se formó un gel que posteriormente se secó a 110°C por 12 h (sólido color café oscuro) que fue calcinado a 600°C por 5h (sólido color beige).
2.1.3 Preparación de -alúmina impregnada con cerio al 1% y 3% (Ce/γ-Al 2 O 3 )
Una vez obtenida la γ-Al2O3, esta se modificó con cerio por impregnación húmeda, tomando 3,9576 g de γ-Al2O3 e impregnándola a exceso de volumen de poro con 40 mL de solución acuosa de Ce(NO3)3•6H2O a las concentraciones de Ce deseadas (1% y 3%), agitando constantemente a 80°C hasta sequedad del disolvente. Por último, el sólido obtenido se secó a 105°C por 12h28.
2.1.4 Síntesis de heteropolioxomolibdatos de níquel tipo Anderson ((NH 4 ) 4 [NiMO 6 O 24 H 6 ]•5H 2 O)
La síntesis se llevó a cabo por coprecipitación de soluciones acuosas que contenían 10,330 g (NH4)6Mo7O24•4H2O de y 2,835g de Ni(NO3)2•6H2O a temperatura ambiente, bajo agitación constante con el pH ajustado entre 5 y 6. Posteriormente se filtró y lavó con agua destilada, se secó a 105°C por 12 h25,29,30.
2.1.5 Síntesis de precursores catalíticos (NiMo/Al 2 O 3 , NiMo-Ce/-Al 2 O 3 , NiMo/γ-Al 2 O 3 -Ce)
Se tomaron 3 g de los diferentes soportes sintetizados y se impregnaron a exceso de volumen de poro con 40 mL de solución acuosa de (NH4)4[NiMOgO24H6]•5H2O a la concentración de Mo al 15%, agitando constantemente a 50°C hasta sequedad del solvente. Por último, el sólido obtenido se secó a 105°C por 12h.
2.2 Caracterización de precursores catalíticos
Con el fin de establecer con claridad los factores que determinan la actividad catalítica se realizó la caracterización de los precursores catalíticos, el área específica se determinó por el método de Brünauer-Emmett-Teller (SBET) basado en la absorción física de N2 a la temperatura de 77K utilizando un sorptómetro marca Quantasorb (Quantachrome); antes de las medidas las muestras fueron desgasificadas a 300°C por 16 horas en vacío de 10-30 Torr. La identificación fases cristalinas de los materiales sintetizados se realizó por difracción de rayos X (DRX), en polvo utilizando un Rigaku Miniflex II con radiación CuK alpha operado a 30KV y 15mA; el ángulo de barrido fue de 20= 5-75° a tamaño de paso de 0.02° y una velocidad de adquisición de 0.08°/s. Los grupos funcionales presentes en los precursores oxídicos, se determinaron por espectroscopía infrarroja (FTIR) utilizando Shimadzu FTIR MODELO AFFINITY-1 dentro de un rango de barrido entre 400 y 4000 cm-1.
2.3 Medidas de actividad catalítica de hidrodesulfuracón de tiofeno
0,5g de cada precursor catalítico (NiMo/Al2O3, NiMo/Ce-γ-Al2O3, NiMo/γ-Al2O3-Ce) se activó por sulfuración, haciéndole pasar 0,33 mL/min de CS2 (2%vol)/n-heptano y 70 mL/min de hidrogeno durante 3h en un reactor de flujo continuo lecho fijo a 300°C y presión atmosférica. Posteriormente, se determinó la actividad catalítica utilizando una mezcla tiofeno (2%vol)/n-heptano a un flujo de 0,33 mL/min en presencia de 70mL/min H2. Durante el transcurso de reacción, se realizó monitoreo de tiofeno tomando muestras a 30 min, 90 min y 180 min (estado estacionario), y fueron analizadas por cromatografía de gases utilizando un cromatógrafo Agilent Technologies 7890B con detector FID y columna HP-5 170°C, con N2 como gas de arrastre.
3. RESULTADOS Y DISCUSIÓN
3.1 Caracterización de soportes y precursores catalíticos
3.1.1 Área específica (BET) de soportes y precursores catalíticos de Ni-Mo
En la tabla 1 se reportan los valores de área específica de los precursores catalíticos y de los soportes, calculados con el modelo de Brunauer-Emmett-Teller (BET).
Tabla 1 Área específica (BET) de soportes y precursores catalíticos de Ni-Mo.
| Material | Área específica BET (nr/g) |
| y-AlA | 149 |
| Y-AWVCc 1% | 146 |
| y-Al 2 0,-Cc 3% | 144 |
| Ce l%/y-Al,0, | 82 |
| Cc3%/y-AhO, | 66 |
| NiMo^y-AUO, | 61 |
| NiMoA-AUOj-Ce 1% | 76 |
| NiMo,/y-Al,0,-Ce 3% | 71 |
| NiMo h -Ce l%/y-Al 2 0, | 69 |
| NiMo„-Cc 3%/y-Al : 0, | 36 |
Las alúminas dopadas γ-Al2O3-Ce 1% y γ-Al2O3-Ce 3% reportaron valores de área muy cercanos a la alúmina γ-Al2O3 sintetizada, mientras que las alúminas impregnadas Ce 1%/γ-Al2O3 y 3%/ γ-Al2O3, resultaron ser inferiores en un 45%-55% respecto a la γ-Al2O3. Este comportamiento, en las alúminas impregnadas era de esperarse, debido al bloqueo de poros por la deposición de especies de cerio durante la impregnación31. La poca variación en los valores de área específica de las alúminas dopadas con cerio se asocia posiblemente al cerio que haga parte de la red cristalina de la alúmina. Los precursores catalíticos, tanto impregnados como dopados con cerio, la disminución de área específica es mayor, por la presencia de la fase Anderson sobre los soportes y/o a la deposición al interior de los poros32.
3.1.2 Espectroscopía infrarroja con transformada de Fourier (FTIR)
La figura 1 presenta los espectros FTIR de los soportes γ-Al2O3-Ce 1%, γ-Al2O3-Ce 3%, Ce 1%/γ-Al2O3 y Ce 3%/γ-Al2O3 identificados con las letras a, b, c y d respectivamente. Todos los espectros presentan bandas alrededor en 3500 cm-1-3200 cm-1 asignadas a los estiramientos de grupos O-H de la alúmina, mientras que en el rango de frecuencia más baja se observan entre 500 cm-1-470 cm-1 y 890 cm-1-800 cm-1 procedentes de los modos de tensión y las vibraciones del enlace Al-O. Las bandas entre 1680 cm-1-1570 cm-1 indican presencia de humedad en los materiales por contacto con el aire, lo cual concuerda con la naturaleza hidrofílica que poseen de los sólidos sintetizados33,34.
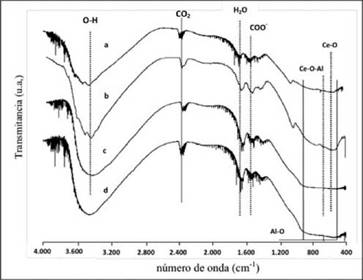
Figura 1 Espectros FTIR de los soportes: ( ) Al2O3-Ce1%, (b) Al2O3-Ce3%, (c) Ce1%/Al2O3 y (d) Ce3%/Al2O3.
) Al2O3-Ce1%, (b) Al2O3-Ce3%, (c) Ce1%/Al2O3 y (d) Ce3%/Al2O3.
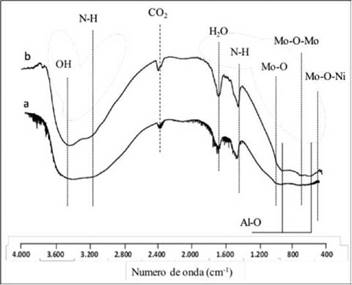
Alrededor de 544 cm-1 se reportan bandas que indica la presencia del enlace Ce-O que revelan la presencia de óxidos de cerio, y los espectros 1a y 1b presentaron además bandas entre 660 cm-1-670 cm-1, características del enlace tipo puente Ce-O-Al asociado al aluminato de cerio. La aparición de bandas entre 3370 cm-1-2270 cm-1 en todos los espectros se debe al CO2 aportado por el ambiente durante la medición21,35,36 y las bandas que se aprecian entre 1600 cm-1-1480 cm-1 están asociadas a los modos vibracionales de tensión de grupos carboxilatos generados posiblemente en el medio de síntesis (glucosa en medio ácido), que se encuentran enlazados con átomos de aluminio presentes en la superficie. Los polioxomolibdatos se caracterizan por la presencia de tres clases diferentes de vibraciones del enlace Mo-O: enlace Mo-O2 dioxo terminal, enlace puente Mo-O-Mo y enlace puente Mo-O-Ni. Además del contra-catión NH4+ y moléculas de agua que se encuentran coordinados por átomos de oxigeno del polioxomolibdato34. Es así como en los espectros FTIR de los precursores catalíticos presentados en la figura 2, Se observan en el rango entre 1000 cm-1-800 cm-1 debido a los estiramientos simétricos y anti-simétricos del enlace terminal Mo-O2 dioxo terminal, mientras que a frecuencias entre 750550 cm-1 corresponden a las vibraciones de las uniones puentes Mo-O-Mo, lo cual nos indica la presencia de óxidos Mo en los precursores. A frecuencias bajas de 450 cm-1 se observan vibraciones características del enlace tipo puente Mo-O-Ni. Dos bandas anchas entre 3300 cm-1-3200 cm-1 y 1470-1370 cm-1 asociados respectivamente a los estiramientos y las flexiones del enlace N-H, procedente de los grupos NH4 +, además bandas entre 1700 cm-1 y 1600 cm-1 procedentes de las flexiones del enlace O-H, producto de las aguas de cristalización de ambos grupos coordinados por átomos de oxígeno al polioxomolibdato34,37-39. La ausencia de bandas relacionadas a las especies de cerio presentes en los precursores catalíticos se deba a la deposición del polioxomolibdato en la superficie de los soportes modificados.
3.1.3 Difracción de rayos X (DRX) de los soportes y precursores catalíticos
Las señales de difracción de los soportes γ-Al2O3, Ce 1%/γ-Al2O3, Ce 3%/γ-Al2O3 son presentados en la figura 3. En la figura, los picos de difracción anchos y de poca intensidad a 20 = 37,58; 45,88 y 67,30 se deben a la presencia de γ-Al2O3 (JCPDF-010-0425)40. Los sólidos Ce 1%/γ-Al2O3 y Ce 3%/γ-Al2O3 muestran una mezcla de fases, Al2O3 gamma (JCPDF-010-0425), gibbsitacon2 =18,20; 20,22;40,46(JCPDF-96-901-5977), CeO2 a 2=28,65 (JCPDF-065-5923) y CeAlO3 a 2=41,58 (JCPDF-021-0175). La generación de la mezcla de fases de alúmina, puede ser debido a la falta de tratamiento térmico del sólido durante la calcinación por no completarse la transición total de fase gibbsita a gamma. Por otro lado, los picos de difracción para CeO2 y Ce2O3 son anchos y poco intensos respecto al fondo mostrando su poca cristalinidad.
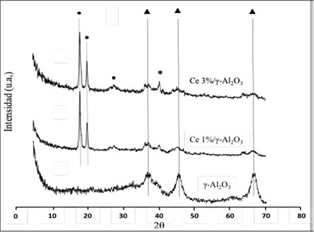
Figura 3 Difractogramas de rayos X de soportes impregnados con Ce. ( ) CeO2, (*) CeAlO3, (•) Al2O3-gibbsita y((
) CeO2, (*) CeAlO3, (•) Al2O3-gibbsita y(( )) -Al2O3.
)) -Al2O3.
En la figura 4 se presentan los difractogramas de rayos X de los soportes γ-Al2O3, γ-Al2O3-Ce 1%, γ-Al2O3-Ce 3%. En todos los difractogramas, se aprecian señales de difracción anchas a 20 = 37,58; 45,88; 67,30, características de γ-Al2O3 (JCPDF-010-0425); mientras que, γ-Al2O3-Ce 1% y γ-Al2O3-Ce 3% presentaron picos de difracción a 20 =18,20 y 20,22 anchos y de baja intensidad respecto al fondo, asociados a alúmina en fase gibbsita (JCPDF-96-901-5977). Para la muestra γ-Al2O3-Ce 3% se aprecia un pico de difracción de muy baja intensidad debido a CeO2 con 20 =28,65 (JCPDF-065-5923); no obstante, no se reportan señales de difracción de especies de CeAlO3 y CeO2 para γ-Al2O3-Ce 1% debido probablemente a la inserción de estas especies dentro de la red cristalina de la alúmina.
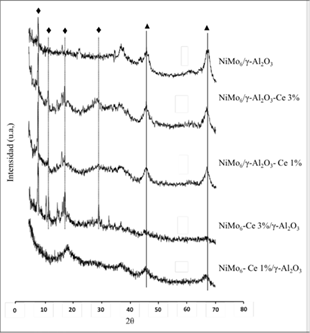
Figura 4 Difractogramas de rayos X de soportes dopados con Ce. (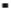 ) CeO2, (•) Al2O3-gibbsita y (
) CeO2, (•) Al2O3-gibbsita y ( )-Al2O3.
)-Al2O3.
Los difractogramas de rayos X de los precursores catalíticos NiMo6-Ce 1%/-Al2O3, NiMo6-Ce 3%/γ-Al2O3, NiMo6/γ-Al2O3-Ce 1%, NiMo6/γ-Al2O3-Ce 3% y NiMo6/γ-Al2O3 se muestran en la figura 5.
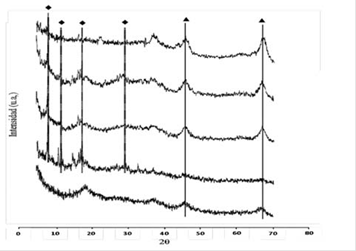
Figura 5 Patrones de difracción de rayos X de precursores catalíticos. (() (NH4)4[NiMo6O24H6]•5H2O y ( ) -Al2O3.
) -Al2O3.
En esta figura se observan dos señales de difracción anchas a 20 = 45,98; 66,98 características de la γ-Al2O3 (JCPDF-010-0425), y (NH4)4[NiH6Mo6O24]•5H2O a 20= 8,16; 11,78; 17,48 y 29,26 (JCPDF-22-0506).
Hay difractogramas que no se aprecia la presencia de polioxomolibdato posiblemente por el tamaño pequeño de los cristales y/o a la dispersión de estos sobre el soporte, mientras que los óxidos de cerio no se presentaron debido al anclaje de los polioxomolibdatos sobre el soporte modificado por cerio38.
3.2 Evaluación catalítica de hidrodesulfuración de tiofeno
Se evaluó cada uno de los catalizadores y soportes sintetizados en la hidrodesulfuración de tiofeno hasta estado estacionario (3 horas).
3.2.1 Evaluación catalítica de soportes y precursores catalíticosimpregnados con cerio
Al analizar los resultados obtenidos, se logró apreciar que los soportes presentan valores de conversión mucho más bajos que los obtenidos por los precursores catalíticos, lo cual concuerda con la literatura, teniendo en cuenta que la fase activa es Ni-Mo-S; sin embargo, se notó que los soportes modificados con cerio resultaron más activos que los no modificados, posiblemente por la formación de vacancias aniónicas32. Por otro lado, los precursores catalíticos con soportes impregnados con cerio exhiben mayores valores de conversión, mostrando que la presencia del cerio mejora la actividad catalítica, siguiendo el orden: NiMo6-Ce 3%/γ-Al2O3 > NiMo6-Ce 1%/γ-Al2O3 > NiMo6/γ-Al2O3 > Ce 3%/γ-Al2O3 > Ce 1%/γ-Al2O3 > Al2O3. Este comportamiento en actividad catalítica de los precursores con soporte impregnado, puede ser por el favorecimiento del apilamiento de fase activa que contribuye a tener más sitios activos presentes al momento de la reacción catalítica41.
3.2.1 Evaluación catalítica de soportes y precursores catalíticos dopados con cerio
El precursor NiMo6/γ-Al2O3 presentó menor conversión catalítica (73%) que los precursores catalíticos soportados sobre alúmina dopada con cerio, esta conversión estuvo relacionada con la cantidad de cerio en el soporte, siguiendo el orden: NiMo6/γ-Al2O3-Ce3% > NiMo6/-Al2O3-Ce1% > NiMo6/γ-Al2O3>γ-Al2O3-Ce3%>γ-Al2O3-Ce1%> Al2O3.
Los resultados observados en las figuras 6 y 7, demuestran que la concentración de cerio es determinante en la promoción catalítica de la reacción HDS independientemente del método de síntesis, es decir, a mayor concentración de cerio mayor conversión. La promoción catalítica está asociada a diversas razones, como: 1. Utilizar bajos contenidos de cerio para modificar texturalmente la alúmina que incrementan la acidez Lewis del soporte lo que resulta en una mayor interacción entre las moléculas de tiofeno y los metales activos depositados en la superficie del catalizador(21, 24). 2. Aumento de la estabilidad térmica de la alúmina impidiendo reducción de área superficial y por ende evitando la pérdida de centros activos de la superficie42; 3. Generación de un acoplamiento redox entre Ce3+-Ce4+ con la habilidad de promover la reducción u oxidación del óxido metálico o del metal activo23; 4. Generación de compuestos intermetálicos M-Ce que contribuyan a la reacción24. Al no observarse diferencia significativa entre valores de conversión de los catalizadores impregnados y dopados con cerio; correlacionamos con las áreas específicas (actividad intrínseca, tabla 2), y claramente se observa que los sólidos donde el cerio fue impregnado resultaron más activos, y que al aumentar su concentración aumenta su actividad catalítica. Este comportamiento indica, que estos precursorespresentan mayor cantidad de sitios activos por unidad de área, posiblemente por la presencia de apilamiento mayor como lo han reportado otros autores41.
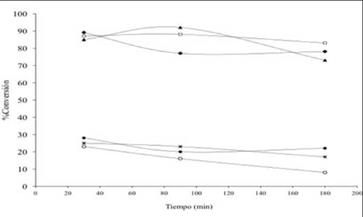
Figura 6 Actividad HDS de tiofeno en estado estacionario de alúmina impregnada con Ce y precursores catalíticos soportados sobre alúmina impregnada con Ce: (°)γ-Al2O3, (x) Ce 1%/γ-Al2O3, (•) Ce 3%/γ-Al2O3, ( ) NiMo6/γ-Al2O3, (() NiMo6-Ce 1%/γ-Al2O3, (□) NiMo6-Ce 3%/γ-Al2O3.
) NiMo6/γ-Al2O3, (() NiMo6-Ce 1%/γ-Al2O3, (□) NiMo6-Ce 3%/γ-Al2O3.
Figura 7 Actividad HDS de tiofeno en estado estacionario de alúmina dopada con Ce y precursores catalíticos soportados sobre alúmina dopada con Ce: (°) -Al2O3, (X) -Al2O3-Ce 1%, (•)γ-Al2O3-Ce 3%, ( ) NiMo6/ γ-Al2O3, (() NiMo6/ γ-Al2O3-Ce 1%, (□) NiMo6/ γ-Al2O3-Ce 3%.
) NiMo6/ γ-Al2O3, (() NiMo6/ γ-Al2O3-Ce 1%, (□) NiMo6/ γ-Al2O3-Ce 3%.
Tabla 2 Actividad intrínseca de los precursores catalíticos y soportes modificados con cerio en la HDS de tiofeno.
| Sólido | ", | Area | Actividad intrínseca |
| Conversión | m% | (mol de TWonv/m2min) xlO 6 | |
| A1,0, | X | 149 | 5,37 |
| AiA-Ccr/a | 17 | 146 | 11,6 |
| Al,0,-Cc3% | 19 | 144 | 13,2 |
| CclWAUO, | 15 | 82 | 18,3 |
| Cc3%/Al,0, | 20 | 66 | 30,3 |
| NiMcV Al,Oj | 73 | 61 | 118 |
| NiMofi-Cel%/Al;0, | 78 | 76 | 113 |
| Nimo(,-Cc3%/AI,0, | 80 | 71 | 222 |
| \uno Al.CVCd"., | 83 | 69 | 109 |
| Nimo,/Al,0,-Cc3% | 95 | 36 | 134 |
4. CONCLUSIONES
• Los soportes modificados con cerio presentaron área específica entre 66-146 m2/g, siendo los soportes impregnados los que presentaron menor valor.
• Los resultados de DRX revelaron la formación de una mezcla de alúmina en fase guibbsita y alúmina en fase gamma en los soportes impregnados con cerio, asociado a la falta de tratamiento térmico durante el proceso de síntesis. Los soportes dopados con cerio presentaron alúmina en fase gamma. Se develó además, que los precursores catalíticos presentan las fases cristalinas del polioxomolibdato de níquel, tipo Anderson (NH4)4[NiMo6O24H6]•5H2O.
• Los análisis de FTIR de los soportes dopados con cerio mostraron la presencia de óxidos de cerio y de aluminato de cerio, mientras los soportes impregnados reportaron la presencia de óxidos de cerio. Los espectros FTIR de los precursores catalítico reportaron las señales de Mo-O, Mo-O-Mo, Mo-O-Ni y N-H del grupo amino, características del polioxomolibdato de níquel, tipo Anderson (NH4)4[NiMo6O24H6]•5H2O.
• Los catalizadores cuyos soportes estaban modificados por cerio independientemente del método de inserción, muestran mejores resultados de actividad relativa que el catalizador de uso convencional. Los catalizadores cuyos soportes fueron dopados con cerio fueron los de los de mayor actividad, comportamiento asociado a la presencia de especies de cerio tanto en la superficie como al interior de la red cristalina del soporte. Se determinó, además, que ha mayor concentración de cerio mayor actividad presentan los catalizadores.
• Los catalizadores impregnados presentan mayor actividad intrínseca con resultados entre 33 y 66 (10-6) mientras que los dopados con cerio entre 32 y 39 (106), por lo cual se asume que este tipo de catalizadores presentan un mayor número de centros activos expuestos en la superficie por m2 en la superficie del catalizador.