1. INTRODUCCIÓN
Actualmente las necesidades energéticas del mundo se suplen principalmente de fuentes petroquímicas, carbón y gases naturales. Sin embargo, el uso y abuso de estas fuentes energéticas han generado preocupación debido a su inevitable extinción [1,2]. Se estima que, con el ritmo de extracción actual, estas reservas durarían alrededor de unos 40 años [3,4] por lo que hay gran prioridad en implementar nuevas fuentes de energía renovable. El biodiesel es un combustible atractivo que es biodegradable y poco contaminante [5], un método de producción es la reacción de transesterificación básica y/o ácida, de aceites de origen animal o vegetal [6]. Recientemente, se han desarrollado métodos de catálisis enzimática para la producción de biodiesel, en los cuales se utilizan lipasas como catalizadores para la transesterificación de los triacilglicéridos. Este tipo de catálisis ha generado buenos rendimientos de reacción, gastos energéticos bajos y procesos de producción más limpios [7]; además de aprovechar la versatilidad de las lipasas en los procesos de síntesis, ya que pueden catalizar reacciones en medio acuosos y en medio orgánicos [8].
Para la producción de biodiesel se requieren materias primas con contenido de triglicéridos que puedan ser convertidos a Biodiesel; generalmente estas materias primas son de origen vegetal proveniente de cultivos oleaginosos; en la actualidad se han reportado estudios empleando: aceite de higuerilla [9], aceite de palma [10], aceite de palma de vino [11], entre otras. Sin embargo, es necesario seguir apuntando hacia la búsqueda de nuevas alternativas de materias primas para la producción de biocombustibles, encaminadas fundamentalmente en los residuos de la industria alimenticia, los cuales no generarían conflictos de intereses con los productos primarios de la canasta familiar y además, se presentaría una alternativa de solución para productos que deben ser dispuestos adecuadamente como basura.
El corozo Bactris minor (Bactris minor (L) H.E. Moore, 1963), es una planta originaria de varias regiones colombianas, especialmente de la región caribe, siendo su fruto aprovechado para la producción de jugos y vinos de consumo humano. Estas industrias generan la almendra del corozo entre los materiales de desechos, lo que contribuye con la contaminación ambiental aumentando el volumen de basuras. Sin embargo, estudios han demostrado que estos residuos se caracterizan por tener un contenido en ácidos grasos hasta del 40% [12], potencialmente viable para ser usados en la producción de Biodiesel. Esta utilidad convertiría a estos residuos de la industria alimenticia en potencial materia prima para la industria de los biocombustibles. En esta investigación se presenta la alternativa de producir biodiesel mediante transesterificación de aceites extraídos de la almendra del corozo, Bactris minor, usando como catalizador una lipasa microbiana (Novozyme 435®). Aprovechando los materiales de desecho provenientes de la industria del Bactris minor, convirtiéndolos en productos de alto valor agregado, mediante un proceso de producción más limpio.
2. METODOLOGÍA
2.1 Desechos de corozo
Los residuos del fruto de corozo, B. minor, fueron colectados en el municipio de Puerto Colombia, departamento del Atlántico (0°59′32″ de latitud Norte; 74°57′10″ de longitud Oeste), y posteriormente secados en forma natural para facilitar la separación almendra-corteza. La almendra fue sometida a un proceso de reducción de tamaño de partícula mediante un molino de martillos; el producto pulverizado fue secado en un horno a una temperatura controlada a 100°C durante dos horas.
2.2 Extracción del aceite
La extracción del aceite se realizó mediante el método Soxhlet (sólido-líquido) utilizando hexano como solvente orgánico. Para evaluar el porcentaje de extracción (variable respuesta) se siguió un diseño de experimento factorial 23 en el cual se establecieron ocho experimentos con dos réplicas, para un total de 16 experimentos. Las variables consideradas y condiciones son descritas en la tabla 1. La temperatura se mantuvo constante en 80°C.
Tabla 1 Diseño factorial 23 para la extracción del aceite de la almendra del corozo, B. minor.
| Factores | Nivel Alto (+) | Nivel bajo (-) |
|---|---|---|
| Cantidad de muestra (g) | 30 | 10 |
| Volumen de solvente (mL) | 250 | 100 |
| Tiempo de extracción (h) | 12 | 3 |
Fuente: autores
El aceite crudo fue refinado parcialmente mediante un proceso de desgomado, para la separación de los fosfolípidos hidratables y no hidratables. El aceite extraído de la almendra del corozo, B. minor, fue caracterizado según lo indicado en las normas técnicas colombianas (NTC), tal como se describe en la tabla 2.
Tabla 2 Normas técnicas colombianas para la caracterización del aceite de corozo, B. minor.
| Parámetro | Unidades | Norma |
|---|---|---|
| Densidad | g/mL | NTC 336 |
| Humedad | % en masa | NTC 287 |
| Acidez | % ácido láurico | NTC 218 |
| Índice de yodo | g I2/100 g de aceite | NTC 283 |
| Índice de refracción | - | NTC 289 |
| Índice de saponificación | mg KOH/g de aceite | NTC 335 |
Fuente: autores
2.3 Perfil de ácidos grasos del aceite de corozo, B. minor
La identificación y cuantificación de los ácidos grasos se realizó por Cromatografía de Gases acoplada a Espectrometría de Masas (CG-EM). Previamente, el aceite de corozo, B. minor, se derivatizó y analizó según las normas ISO 5509 (2 edición, 2000) Animal and vegetable fats and oils-Preparation of methyl esters of fatty acids e ISO 5508 (2 edición, 1990) Animal and vegetable fats and oils-Analysis by gas chromatography of methyl esters of fatty acids. Posteriormente un volumen de 1,0 µL se inyectó en un Cromatógrafo de Gases TRACE 1310 equipado con una columna de acero inoxidable Rtx-1614® de 15 m de longitud, 0,25 mm de diámetro interno, 0,10 µm de espesor, rango temperatura de 330 - 360°C, y se usó Helio como gas portador. La velocidad de flujo constante del helio fue de 1,5 mL/min. El gradiente de temperatura se inició en 100°C durante 4 min, luego se incrementó hasta 160 °C a razón de 7°C/min durante 2 minutos. Este incremento se mantuvo hasta una temperatura de 220 °C durante 20 min. El volumen de inyección de la muestra fue de 1 µL, con modo de inyección tipo Split. El sistema de detección consistió en un MS/MS TSQ™8000 Evo Triple Quadrupolo con temperatura lineal de transferencia de 300 °C, fuente de iones a 200°C, modo de ionización por impacto de iones y rango de masas 50-400 masa/carga en modo de adquisición Full Scam. Se utilizó el software integrador (Xcalibur) para el procesamiento de los datos. Como estándar se utilizó el FAME® 0053.
2.4Transesterificación enzimática
Inicialmente se realizó un ensayo de prueba de transesterificación con la lipasa Novozyme 435®, con el propósito de establecer las condiciones del diseño experimental factorial 23, siguiendo el procedimiento descrito por Talukder [13]; este ensayo se realizó bajo las siguientes condiciones experimentales: 4% p/p de Novozyme 435®, temperatura de 40°C, relación molar aceite:metanol de 1:3, agitación de 200 rpm y un tiempo de reacción de 24 horas. Previamente, la enzima Novozyme 435® se mezcló con 2 g del aceite de B minor, en un vaso de precipitados, durante doce horas para su pretratamiento y activación [14]. El metanol se adicionó en tres fracciones de tiempo de la reacción: 0, 4 y 10 horas, para evitar la inactivación de la enzima. El sistema de reacción se mantuvo en agitación constante hasta completar un tiempo de 24 horas [13]. Los productos obtenidos se centrifugaron a 3500 rpm durante 30 min, con la finalidad de separar el catalizador enzimático.
Para evaluar el porcentaje de conversión de los metilésteres de ácidos grasos se siguió un diseño factorial dos a la tres (23) con dos niveles: alto (+) y bajo (-), también se incluyó un control (0). En este diseño resultaron ocho experimentos y dos réplicas. Los factores manejados fueron la temperatura, porcentaje de enzima y relación molar aceite:metanol; la variable de respuesta fue el porcentaje de rendimiento del biodiesel. El diseño factorial y los rangos para las variables se describen en la tabla 3. La agitación y tiempo de reacción se dejaron constantes en 200 rpm y 24 h, respectivamente.
2.5 Cromatografía en capa fina
Los productos de la transesterificación enzimática del aceite de corozo, B. minor, fueron analizados mediante cromatografía en capa fina (CCF), utilizando placas de sílice gel G60 F254 (Merck Millipore, Darmstadt, Germany) y como fase móvil una mezcla de 30 mL de hexano/éter etílico/ácido acético (90:10:1, v/v/v). La mezcla de los distintos componentes del aceite separados por CCF, fueron revelados al interior de una cámara saturada con vapores de yodo.
2.6 Cuantificación de los metilésteres de ácidos grasos por CG-EM
La cuantificación de la mezcla de los metilésteres de ácidos grasos (biodiesel) presentes en el aceite de corozo se realizó en un Cromatógrafo de gases Agilent 19091S-433UI, equipado con una columna HP-5 ms Ultra Inert 30 m largo x 250 µm diámetro interno x 0.25 µm de tamaño de partícula. Se usó helio como gas portador. El flujo de la columna fue de 1 mL/min, y el flujo total de 50 mL/min. El gradiente de temperatura se inició con 100°C durante 4 min, para la rampa de calentamiento 1 se incrementó a razón de 50°C/min hasta 230°C durante 10 min. La razón de cambio en la rampa de calentamiento 2 fue de 4°C/min hasta 256°C durante 0 min. Finalmente, la rampa 3 consistió en un cambio de 10°C/min hasta alcanzar una temperatura de 325°C.
El sistema de detección, el espectrómetro de masas, GC-MS 5977-MSP, contó con una temperatura lineal de transferencia de 350°C, fuente de iones a 200°C, energía 70 eV y un rango de masas 45-550 masa/carga. Para verificar la identificación de los metilésteres de los ácidos grasos, se empleó como estándar una mezcla de ésteres metílicos de ácidos grasos RESTEK® (Catálogo No. 35077).
2.7. Tratamiento estadístico
El análisis del diseño factorial se realizó con el paquete estadístico Statgraphics Centurión XVI. Con un nivel de confianza del 95 %, se realizó un análisis de varianza (ANOVA) para estimar los efectos de los factores principales y sus interacciones sobre las variables respuesta (% de rendimiento de aceite y % biodiesel) [15].
3. RESULTADOS
3.1 Extracción del aceite de la almendra del corozo, B. minor
En la tabla 4 se ilustran los resultados obtenidos mediante método Soxhlet para la extracción del aceite de la almendra del fruto de corozo.
Tabla 4 Rendimientos obtenidos durante el proceso de extracción del aceite.
| Experimentos | Cantidad de muestra (g) | Cantidad de solvente (mL) a | Tiempo de extración (h) | % (p/p) Rendimiento b |
|---|---|---|---|---|
| 1 | 10 | 100 | 3 | 38,49 ± 0,40 |
| 2 | 30 | 100 | 3 | 39,96 ± 0,04 |
| 3 | 10 | 250 | 3 | 38,19 ± 0,78 |
| 4 | 30 | 250 | 3 | 38,26 ± 0,51 |
| 5 | 10 | 100 | 12 | 38,92 ± 0,04 |
| 6 | 30 | 100 | 12 | 39,10 ± 0,71 |
| 7 | 10 | 250 | 12 | 38,85 ± 0,28 |
| 8 | 30 | 250 | 12 | 40,51 ± 0,04 |
Fuente: autores
a Hexano
b Valores promedios de dos repeticiones ± 1 desviación estandar
Los resultados presentados en la tabla 4 muestran que el porcentaje de extracción promedio del aceite de la almendra del corozo se encuentra entre el 38,19 y el 40,51 % utilizando hexano como solvente. Estos resultados se compararon con los porcentajes reportados para otras especies del corozo como la Palma de vino (Acrocomia aculeata (Jacq.) Lodd. ex Mart) de la cual se reportan porcentajes de 1,03% mediante el método de arrastre de vapor y relación masa de almendra:masa de agua de 1:2 [16]. Mientras que en esta misma investigación, mediante el método Soxhlet reportan un porcentaje de rendimiento del 42,90% en un tiempo de 5 horas, que comparados con los porcentajes alcanzados en este estudio, en un tiempo de 3 horas con el mismo método (entre 38,19 y 39,96%), se puede concluir que se obtuvieron mejores rendimientos de extracción, ya que se obtuvo un buen porcentaje de extracción en menor tiempo. De los rendimientos de extracción de aceite obtenidos experimentalmente en este trabajo, podría considerarse a la almendra de corozo una materia prima con un contenido oleaginoso de aceite de 38,5%-40% (en peso) por encima de otras materias primas como el algodón, maíz, girasol y soya. El aceite de corozo posee una composición de triglicéridos cercana al de la semilla de palma, palmiste y al cacahuate y por debajo al contenido oleaginoso del coco.
Se realizó un análisis estadístico con el software statgraphics a los resultados obtenidos con el diseño de experimentos para la extracción del aceite, con el objetivo de verificar como se comportaba la variable de respuesta rendimiento y la forma en que los factores seleccionados afectan esta variable. Con este análisis se estableció que no existen diferencias significativas entre los porcentajes de rendimiento reportados en la tabla 4, aún cuando las condiciones de extracción no eran las mismas (ANOVA: razón-F = 1.88 x 1028, valor-p = 0.057). El diagrama de Pareto, figura 1, muestra que los factores cantidad de muestra (ANOVA: razón F= 6,37; p= 0,0356), y la interacción cantidad de solvente/tiempo de extracción (ANOVA: F=6,18; p=0,0377) exhiben un efecto positivo sobre la variable respuesta (rendimiento de extracción del aceite) ya que sobrepasan los límites de los valores normales (línea azul), es decir al aumentar la cantidad de muestra y tiempo de extracción, se obtienen mayores porcentajes de rendimiento; por el contrario, los factores individuales: cantidad de solvente, tiempo de reacción, y sus interacciones, no son estadísticamente significativos para la variable respuesta (valor p > 0,05). En la tabla 5 se ilustran los resultados del análisis de varianza (ANOVA) para el porcentaje de rendimiento del aceite.
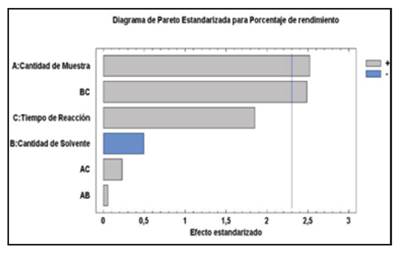
Fuente: autores
Figure 1 Standardized Pareto diagram to yields of the oil extracted from the almond of B minor.
Tabla 5 Análisis de Varianza para porcentaje de rendimiento del aceite extraído dela almendra del B minor.
| Fuente | Suma de Cuadrados | Gl | Cuadrado Medio | Razón-F | Valor-P |
|---|---|---|---|---|---|
| A: Cantidad de Muestra | 2,86456 | 1 | 2,86456 | 6,37 | 0,0356 |
| B: Cantidad de Solvente | 0,110556 | 1 | 0,110556 | 0,25 | 0,6333 |
| C: Tiempo de Reacción | 1,54381 | 1 | 1,54381 | 3,43 | 0,1010 |
| AB | 0,00140625 | 1 | 0,00140625 | 0,00 | 0,9568 |
| AC | 0,0232563 | 1 | 0,0232563 | 0,05 | 0,8258 |
| BC | 2,78056 | 1 | 2,78056 | 6,18 | 0,0377 |
| bloques | 0,0855562 | 1 | 0,0855562 | 0,19 | 0,6742 |
| Error total | 3,5973 | 8 | 0,449663 | ||
| Total (corr.) | 11,007 | 15 |
Fuente: autores
3.2 Caracterización del aceite de la almendra del corozo B minor
En la tabla 6 se resumen los resultados de la evaluación de las propiedades fisicoquímicas del aceite extraído de la almendra del corozo, B. minor. Los resultados encontrados están en concordancia con los reportados en la literatura para este tipo de aceites.
Tabla 6 Propiedades fisicoquímicas del aceite extraído de la almendra del corozo, B. minor.
| Parámetro | Resultado | Unidades |
|---|---|---|
| Acidez | 0,09% | % ácido Láurico |
| Índice de yodo | 29,80 ± 0,44 | g I2/100g de muestra |
| Índice de saponificación | 127,66 ±0,77 | mg KOH/g de muestra |
| Índice de refracción | 1,404 | - |
| Densidad | 0,9143 | g mL-1 |
| Humedad | 0,27±0,03 | - |
Fuente: autores
El valor de acidez para el aceite refinado extraído de la almendra del corozo, B. minor fue de 0,09 % (expresado en % ácido láurico). Este valor de acuerdo a la NTC 218 representa una cantidad mínima de ácidos grasos libres presentes en el aceite, originados por la lipólisis de los triacilglicéridos que forman el aceite; en este sentido se puede afirmar que el aceite de corozo, B. minor, extraído no ha experimentado una hidrólisis marcada, por lo que el contenido de acidez es bajo, lo que está en concordancia con la baja humedad reportada para el aceite (0,27%). Además esto no hace sea necesaria la previa neutralización del aceite antes de la reacción de transesterificación, y además que no se formen gomas durante la reacción de transesterificación del aceite [17,18].
El índice de yodo es un indicativo del grado de insaturación de una grasa y/o aceite. El valor de índice de yodo obtenido para el aceite de corozo, B. minor, fue de 29,80± 0,44 g I2/100 g; comparado este valor con el de otros tipos de aceites, como el de palma 55 g I2/100g, oliva 84 g I2/100g, soja 134 g I2/100g, girasol 132 g I2/ g100 y manteca de cacao 37 g I2/100g [16]; se puede inferir que este valor más bajo es debido a las pocas insaturaciones que presenta en su composición haciéndolo que se comporte más estable a la oxidación; siendo muy parecido al de los aceites de palmiste y de coco, 25,5 g I2/100g y 9,5 g I2/100g respectivamente [18].
El índice de saponificación promedio obtenido para el aceite de la almendra del corozo, B. minor, fue de 127,66±0,77 mg KOH/g de aceite. Este valor es relativamente bajo si se compara con otros valores reportados en la literatura para otras especies del corozo, tal como la Acrocomia aculeata, para el cual se han reportado valores de 205 mg KOH/g aceite [18], 241,9 mg KOH/g aceite [16], 232 mg KOH/g aceite [19] y para el aceite de palma 194,5 mg KOH g de aceite [20]. Por tanto se esperaría que la cantidad de jabón formada durante la reacción de transesterificación empleando el aceite extraído de la almendra del corozo, B. minor, sea baja, lo cual presenta ventajas sobre el rendimiento de la reacción.
El índice de refracción para el aceite extraído de la almendra del corozo, Bactris minor, fue de 1,404. Este valor bajo es consistente con la presencia de ácidos grasos saturados en la estructura química del aceite, el cual es cercano a los reportados en la literatura para otros tipos de aceites, aceite de coco 1,427 [21] almendra del fruto de la palma de corozo (Acrocomia aculeata) 1,456 [15], Acrocomia intumescens 1,411 [22], macauba 1,452 [23], aceite de palma 1,473 [24].
La densidad promedio a 25°C fue de 0,9143 consistente con los datos reportados para otras especies del corozo como la Palma de vino, 0,9210 a 20°C 15 y 0,9179 a 26°C [18].
La humedad promedio para el aceite de corozo, B. minor, fue de 0,27±0,03 %. Este valor es bajo y atractivo para llevar a cabo la reacción de transesterificación, puesto que un porcentaje de agua adecuado, favorece la activación del catalizador evitando la formación de productos saponificados como el jabón. Para otras especies del corozo como la acrocomia aculeata se han reportado valores de 6,70% [19]; 5,20% [18]; 6,66 % [16], los cuales son porcentajes altos en comparación con el porcentaje presentado por el aceite del corozo, B. minor; esta diferencia puede ser debida a que el aceite del corozo, B. minor, fue expuesto a un proceso de desgomado, en el cual se retira gran parte del agua remanente, mientras que para el aceite de la acrocomia aculeata los valores registrados son sin refinar [16,18,19]. No obstante el valor para el aceite de palma es equivalente a 0,25% [25], bastante similar al aceite de estudio.
En la tabla 7, se relaciona el perfil de ácidos grasos obtenido para el aceite de la almendra del corozo, B. minor. Se observa en la tabla, que los ácidos grasos saturados representan la mayor fracción (92,7%); siendo el ácido el láurico predominante con 65%, seguido del mirístico 20,8%. Estos porcentajes son mayores a los reportados por Belen et al [16] en otra especie del corozo Acrocomia acualeata Jacq.(50,9% para el ácido laurico y 13,9 % para el mirístico). Cabe señalar, que esta característica es la influyente para el bajo valor del índice de saponificación exhibido por el aceite de B minor., en comparación con otros aceites [16,18-20]. El alto porcentaje de ácidos grasos saturados también se ve reflejado en el estado sólido que presenta el aceite a temperatura ambiente.
Tabla 7 Perfil de ácidos grasos presentes en el aceite de la almendra del corozo B minor.
| Componente | Porcentaje (%) a |
|---|---|
| Ácido Láurico (C12:0) | 65,0 ± 1,13 |
| Ácido Mirístico (C14:0) | 20,8 ± 1,34 |
| Ácido Oleico (C18:1) | 7,3 ± 0,424 |
| Ácido Palmítico (C16:0) | 5,6 ± 0,212 |
| Ácido Esteárico (C18:0) | 1,3 ± 0,070 |
Fuente: autores
a valores promedios de dos repeticiones ± 1 desviación estándar.
La reacción transesterificación enzimática del aceite del corozo, B. minor, inicialmente fue realizada siguiendo el procedimiento descrito por Talukder [13]; esto con la finalidad de establecer como un ensayo control base para plantear el diseño de experimentos factorial 23. Se utilizó como catalizador enzimático Novozyme 435®, en una concentración del 4%, temperatura de 40°C. La adición del metanol se realizó en tres etapas para evitar la inactivación de la enzima, la relación molar aceite:metanol fue fijada en 1:3 con agitación de 200 rpm. Finalmente, para cuantificar la conversión de los triacilglicéridos presentes en el aceite se estableció un tiempo de reacción de 24 horas. El porcentaje de conversión de 21,44% fue determinado por GC-MS. La temperatura de reacción de 40ºC fue reportada previamente como la temperatura óptima en la que las lipasas presentan mayor actividad [26]; adicionalmente, la velocidad de agitación de la mezcla de reacción de 200 rpm, es la velocidad reportada como suficiente para eliminar problemas difusivos durante la reacción, sin alterar la composición de la enzima [26].
La figura 2 corresponde a los resultados de la CCF obtenidos para las muestras de aceite de corozo, B. minor, (AC), ensayo control (BdC) y las obtenidas mediante la aplicación del diseño factorial para la catálisis enzimática (Bd1-Bd9). En los resultados de la placa se pueden distinguir cualitativamente los triacilglicéridos del aceite y se verifica la formación de esteres de metilo en todas las reacciones (manchas en la parte superior de la placa), a excepción para la muestra de aceite de corozo identificada como AC.
En la tabla 8 se presentan los resultados del diseño factorial 23 utilizado para obtener las mejores condiciones para la reacción de transesterificación enzimática del aceite de la almendra del corozo, B. minor. Como puede observarse en la tabla, los porcentajes de rendimiento más bajos (11,89%) se obtuvieron con una relación molar aceite:metanol 1:1, 2% p/p de Novozyme 435® y temperatura de 50°C. De estos resultados se puede inferir que debido a la baja concentración de enzima, esta pudo ser inactivada al ser expuesta a la temperatura de 50°C; sin embargo se observó que un aumento en la relación molar aceite:metanol (1:5), propició rendimientos por encima del 58%, lo que indica un mayor porcentaje de conversión de los triacilglicéridos en sus respectivos esteres de metilo de cadena larga (biodiesel).
Tabla 8 Datos experimentales obtenidos de la transesterificación enzimática del aceite de la almendra del corozo, B. minor, con Novozyme 435®.
| Relación molar aceite metanol | Porcentaje de enzima | Temperatura | % Rendimiento |
|---|---|---|---|
| 1:1 | 2 | 30 | 15,11 ± 0,565 |
| 1:5 | 2 | 30 | 34,69 ± 1,004 |
| 1:1 | 8 | 30 | 23,37 ± 1,414 |
| 1:5 | 8 | 30 | 61,77 ± 2,44 |
| 1:1 | 2 | 50 | 11,89 ± 1,004 |
| 1:5 | 2 | 50 | 59,85 ± 2,333 |
| 1:1 | 8 | 50 | 22,25 ± 2,32 |
| 1:5 | 8 | 50 | 40,54 ± 0,445 |
Fuente: autores
La figura 3 corresponde al diagrama de Pareto del experimento de transesterificación con Novozyme 435®, para estudiar las variables que tuvieron mayor efecto sobre el rendimiento de la reacción. Se evidenció que el factor relación molar aceite:metanol (ANOVA: razón F=50,77; valor p =0,0001) y la interacción porcentaje de enzima/temperatura (ANOVA: razón F=6,45; valor p=0,0347) se desvían de los límites de los valores normales (línea azul), por tanto son estadísticamente significativos sobre la variable respuesta (% rendimiento), es decir, al aumentar la relación molar aceite:metanol, concentración de la enzima y temperatura, se ve favorecido el rendimiento de la reacción; a diferencia de los factores porcentaje de enzima, temperatura en forma individual, y sus interacciones: relación molar/porcentaje de enzima, y relación molar/temperatura, no son significativos ya que cuentan con un valor p > 0,05.
En la tabla 9 se ilustran los resultados obtenidos en el análisis de varianza (ANOVA) para % rendimiento de producción del biodiesel de corozo.
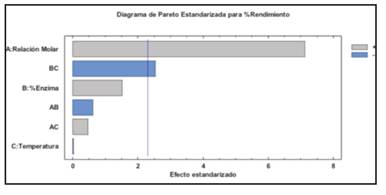
Fuente: autores
Figure 3 The Standardized Pareto diagram for yields of the enzymatic transesterification of the biodiesel corozo, B. minor.
Tabla 9 Análisis estadístico ANOVA del porcentaje de rendimiento del biodiesel enzimático del aceite de la almendra del corozo, B. minor.
| Fuente | Suma de Cuadrados | GI | Cuadrado Medio | Razón-F | Valor-P |
|---|---|---|---|---|---|
| A:Relación Molar | 3858,58 | 1 | 3858,58 | 50,77 | 0,0001 |
| B:%Enzima | 174,174 | 1 | 174,174 | 2,29 | 0,1685 |
| C:Temperatura | 0,0410063 | 1 | 0,0410063 | 0,00 | 0,9820 |
| AB | 29,4035 | 1 | 29,4035 | 0,39 | 0,5512 |
| AC | 17,1189 | 1 | 17,1189 | 0,23 | 0,6478 |
| BC | 490,29 | 1 | 490,29 | 6,45 | 0,0347 |
| Bloques | 1,05576 | 1 | 1,05576 | 0,01 | 0,9091 |
| Error total | 607,988 | 8 75,9985 | |||
| Total (corr.) | 5178,66 | 15 |
Fuente: autores
Al comparar los resultados obtenidos en esta investigación con los datos reportados en otros trabajos, en los que también utilizaron Novozyme 435® con otros tipos de aceites y alcoholes, se registran porcentajes de conversión del 46,1% [27] utilizando aceite de soya y etanol en relación molar 1:10, temperatura 40°C, 5% Novozyme 435®, 10% H2O y tiempo de reacción 6 horas [28]. Este porcentaje (46,1%) comparado con el obtenido en esta investigación (61,8%) es relativamente bajo. Esto puede atribuirse a que el tiempo de reacción, 6 horas, no fue suficiente para lograr una mayor conversión, ya que para la transesterificación enzimática se requieren mayores tiempos de reacción. Watanabe y colaboradores reportaron un porcentaje del 90% obtenido con una mezcla de aceite de soja y colza, tiempo de reacción 40 horas, temperatura 30°C, 4% Novozyme 435® y relación molar alcohol: aceite 1:3 [29].
4. CONCLUSIONES
El porcentaje de rendimiento del aceite extraído de la almendra de Bactris minor osciló entre 38,19 y 40,51 %, lo cual es consistente con lo reportado en la literatura para otras especies de corozo, adicionalmente se encontró que las mejores condiciones para la extracción son: 30 g de harina de corozo, 100 ml de hexano y 3 horas para tiempo de extracción.
Los ácidos grasos mayoritarios que constituyen el aceite de la almendra del corozo B minor son el ácido láurico con un porcentaje de 65% y el ácido mirístico con un porcentaje de 20,8%. Estos datos son consistentes con los datos reportados en la literatura para otras especies del corozo como la Palma de vino (Acrocomia aculeata).
De acuerdo a los resultados del análisis fisicoquímico realizado al aceite extraído de la almendra del corozo, B. minor, se puede concluir que cumple con las normas técnicas colombianas, lo cual lo convierte en una potencial materia prima para en las industrias de los biocombustibles.
Se comprobó cualitativamente la formación de los esteres metílicos de los ácidos grasos de cadena larga (Biodiesel) del aceite extraído de la almendra del corozo, B. minor, mediante CCF; y se obtuvo un porcentaje de conversión del biodiesel 62 % mediante transesterificación enzimática y las condiciones óptimas: relación molar aceite: metanol 1:5, 8% de Novozyme 435® y 30°C de temperatura.















