Introducción
La recolección adecuada de las muestras respiratorias es un paso sensible de la fase preanalítica en el diagnóstico de laboratorio de COVID-19 1. Aunque son mínimas las contraindicaciones para la toma de la muestra, debe conocerse las variantes anatómicas, como desviación del tabique o fosas nasales bloqueadas, para obtener las muestras adecuadas 2. El 30 % de los hisopados de pacientes clínicamente sintomáticos de COVID-19 dan un falso positivo y en poblaciones asintomáticas esta tasa es más alta 3. La cinética de la carga viral (ARN viral) es diferente en cada etapa de la enfermedad, su punto máximo es 4 - 6 días después del inicio de los síntomas y está directamente relacionado con la positividad de las pruebas 2,4,5.
La OMS y el CDC publicó las recomendaciones mundiales para la orientación al público y a los profesionales de la salud sobre el nuevo coronavirus (2019-nCOV) 6,7; en Colombia, el Ministerio de Salud y Protección Social generó lineamientos 8 y el Instituto Nacional de Salud (INS), los protocolos de manejo de las muestras 9. Sin embargo, el Ministerio, en la Circular 005 del 2020, determinó que la ruta de atención para la confirmación de casos sospechosos debía ser definida por la IPS, las Entidades Administradoras de Planes de Beneficio (EAPB) en conjunto con los entes territoriales siguiendo los protocolos de toma de muestras dados por el INS 8. Acompañando estas indicaciones, por ejemplo, la Sociedad de Cirugía de Bogotá Hospital San José, en su protocolo de Manejo Institucional, estableció que ”las muestras serán tomadas inicialmente por el personal de terapia respiratoria y según la demanda por otro profesional de la salud con entrenamiento” 10.
Por lo tanto, a continuación, presentamos los protocolos de recolección de muestras respiratorias de orofaringe y nasofaringe recomendados. Con esto contribuiremos a mejorar la calidad de la muestra para impactar directamente en el diagnóstico y manejo de pacientes con COVID-19.
Preparación y equipamiento
El equipo de protección personal (EPP) incluye gorro desechable, mascarilla de alta eficiencia (N95), pantalla facial (careta), gafas de succión, traje entero en material antifluido, doble guante desechable, bata en material antifluido y polainas 9,10. Antes de comenzar el procedimiento, etiquete los tubos de muestra y complete los formatos solicitados 10. Si es posible, debe ponerse y quitarse el EPP en presencia de un observador que asegure el procedimiento 8-11.
Absténgase de tener objetos personales (joyas, anillos, etc.), colóquese el traje entero y las polainas, pase al área limpia en la entrada de la unidad de aislamiento. Revise visualmente que todos los componentes EPP son correctos. Lávese las manos con agua y jabón (o solución a base de alcohol), póngase un par de guantes, la bata, gorro, máscara protectora N95, gafas, careta y el otro par de guantes sobre el puño de la bata 12.
Procedimientos toma de hisopados
Utilice hisopos de fibra sintética (poliéster) y mango plástico. No use hisopos de alginato de calcio o hisopos con ejes de madera, ya que pueden contener sustancias que inactivan virus e inhiben pruebas de PCR 9.
El hisopo nasofaríngeo es recomendado para el diagnóstico de COVID-19 en adultos y niños 7,11,13. Si toma hisopos nasofaríngeo y orofaríngeo, combine en un solo tubo para aumentar la sensibilidad de la prueba 7.
Pídale al paciente que se quite la máscara y se suene la nariz con un pañuelo para eliminar el exceso de secreciones. Retire el hisopo del empaque. Incline la cabeza del paciente hacia atrás, en ángulo de 45°, así los conductos nasales son más accesibles. Pídale al paciente que cierre los ojos para disminuir la leve molestia del procedimiento.
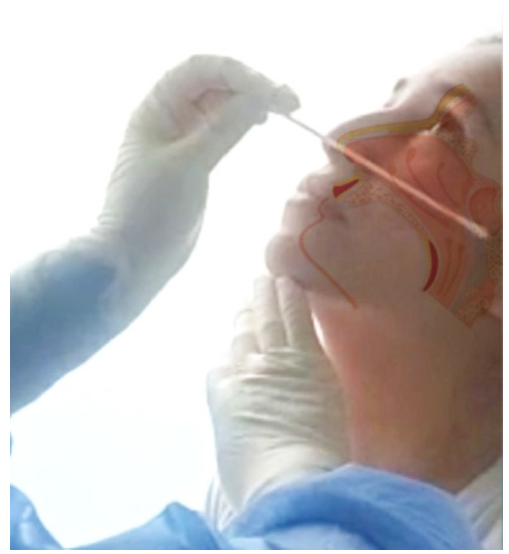
Hisopo nasofaríngeo: inserte el hisopo a través de la fosa nasal paralela al paladar (no hacia arriba) hasta que encuentre resistencia o la distancia sea equivalente a la del oído a la fosa nasal del paciente, lo que indica contacto con la nasofaringe. El hisopo debe alcanzar una profundidad igual a la distancia desde las fosas nasales hasta la abertura externa de la oreja. Frote y gire suavemente el hisopo varios segundos para absorber las secreciones. Retire lentamente el hisopo mientras lo gira. Si hay tabique bloqueado o desviado, use el mismo hisopo para obtener muestra de la otra fosa nasal 7. Complemente con el video disponible.
Hisopo orofaríngeo: con la ayuda de un bajalenguas presione la lengua. Inserte el hisopo en la faringe posterior y el área de las amígdalas. Frote el hisopo sobre los pilares amigdalinos y orofaringe posterior. No tocar lengua, dientes y encías 9,14.
El hisopo se introduce en el tubo que contiene 1,5 mL de medio de transporte viral, se rompe el mango del hisopo y se cierra el tubo. En caso de tomar los dos tipos de muestra, ambos hisopos deben colocarse en el mismo tubo de transporte viral 9.
Almacenamiento de las muestras
Almacene las muestras a 2 - 8° C hasta 72 horas después de la recolección. Si se espera un retraso en las pruebas o el envío, almacene las muestras a -70° C o menos, evitar la congelación y descongelación repetida de las muestras 7,9.
Embalaje/envasado y envío de las muestras
El embalaje de las muestras debe constar del recipiente principal hermético que contiene la muestra (hisopo en el medio de transporte), el embalaje secundario hermético impermeable que protege el recipiente primario y el embalaje exterior o terciario rígido que protege al empaque secundario mientras está en tránsito 15.
Retirar el equipo de protección personal
Retire bata y guantes, lávese las manos con agua y jabón. Póngase un nuevo par de guantes y retire la careta facial, límpiela y guárdela. Quítese los guantes, vuelva a lavarse las manos y póngase otro par de guantes; luego quítese la mascarilla N95 y siga las pautas institucionales para su eliminación. Finalmente, quítese el último par de guantes y lávese las manos.