Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Lasallista de Investigación
Print version ISSN 1794-4449
Rev. Lasallista Investig. vol.6 no.1 Caldas Jan./June 2009
Artículo original
Empleo del reactivo de Fenton para la degradación del colorante Tartrazina*
Use of Fenton's reagent to degrade the Tartrazine dye
Emprego do reativo de Fenton para a degradação do corante Tartrazina
Joan Amir Arroyave Rojas**, Luis Fernando Garcés Giraldo***, Julieta Mejía Trujillo****
* Artículo derivado de la investigación: "Degradación del colorante Tartrazina mediante el reactivo de Fenton" realizada entre febrero y agosto de 2008 y financiada por la Corporación Universitaria Lasallista.
** Ingeniero Sanitario, Candidato a Magíster en Ingeniería Ambiental.
*** Ingeniero Sanitario, Magíster en Ingeniería Ambiental, Especialista en Ingeniería Ambiental. Decano Facultad de Ingenierías, Corporación Universitaria Lasallista. Director Grupo de Investigación GAMA. Correo electrónico: lugarces@lasallista.edu.co.
**** Estudiante Ingeniería Ambiental, Corporación Universitaria Lasallista. Semillero de Investigación en Gestión y Medio Ambiente SIGMA. Grupo de Investigación GAMA.
Resumen
Objetivo. Evaluar la degradación del colorante Tartrazina empleando la reacción de Fenton. Se busca implementar una tecnología de oxidación avanzada para la remoción del colorante Tartrazina, ampliamente utilizado en la industria de alimentos en el medio local, nacional e internacional. Materiales y métodos. Se empleó un diseño experimental factorial aleatorizado con un reactor compuesto por una cuba de vidrio como reservorio, para el almacenamiento de la muestra problema y el lugar para la reacción de degradación; adicionalmente, se dispuso de un sistema interno de mezcla para mantener la solución homogénea en el periodo de experimentación, el cual se determinó en dos horas. Se utilizó una concentración inicial de 100 mg/L del colorante Tartrazina y se mantuvo la solución a un pH igual a 3.0. La degradación del colorante, se determinó mediante el empleo de la espectrofotometría UV/Visible a una longitud de onda de 425 nm. Resultados. Se logró la remoción y degradación del colorante Tartrazina empleando diferentes combinaciones de oxidación del reactivo de Fenton, sin embargo, el mejor porcentaje de remoción fue de 99,3 % mediante la combinación de 25 mg/L de Fe3+ y 0,4 %v/v del agente oxidante peróxido de hidrógeno. Conclusión. La reacción de Fenton es adecuada y logra elevados porcentajes de remoción y degradación del colorante azo Tartrazina.
Palabras clave: Tartrazina, colorante azo, hierro (III), peróxido de hidrógeno, industria de alimentos.
Abstract
Objective. To evaluate the degradation of Tartrazine dye by using the Fenton's reagent. We aim to implement an advanced oxidation technology in order to remove the Tartrazine dye, which is widely used in food industry locally, nationally and internationally. Materials and methods. A randomized factorial experimental design was used, with a reactor composed of a glass recipient as a reservoir to store the problem sample and the reaction place for the degradation. Additionally, an internal mixing system was arranged to keep the solution homogeneous during the experimental period (two hours). An initial 100 mg/L concentration of Tartrazine was used, and the solution was kept at a 3.0 pH level. The dye's degradation was determined by the use of UV/Visible spectrophotometry at a 425 nm wavelenghht. Results. The removal and degradation of the Tartrazine dye was achieved using different combinations of the Fenton's reagent's oxidation. The best removal percentage was, however, 99.3 % of the dye, by the combination of the Fenton's reaction corresponding to 25 mg/L of Fe3+ and 0,4 %v/v of the Hydrogen peroxide oxidation agent. Conclusion. Fenton's reaction is adequate and achieves high removal and degradation percentages of the azo Tartrazine dye.
Key words: Tartrazine, azo dye, iron (III), hydrogen peroxide, food industries.
Resumo
Objetivo. Avaliar a degradação do corante Tartrazina empregando a reação de Fenton. Procura-se implementar uma tecnologia de oxidação avançada para a remoção do corante Tartrazina, o qual é amplamente utilizado na indústria de alimentos a nível local, nacional e internacional. Materiais e métodos. Empregou-se um desenho experimental fatorial aleatorizado com um reator composto por uma cuba de vidro, como reservorio para o armazenamento da mostra problema e o lugar da reação de degradação; adicionalmente, dispôs-se de um sistema interno de mistura para manter a solução homogénea no período de experimentação, o qual se determinou em duas horas. Utilizou-se uma concentração inicial de 100 mg/L do corante Tartrazina e se manteve a solução a um PH igual a 3.0. A degradação do corante, determinou-se mediante o emprego da espectrofotometría UV/Visível a uma longitude de onda de 425 nm. Resultados. Se conseguiu a remoção e degradação do corante Tartrazina empregando diferentes combinações de oxidação do reativo de Fenton, no entanto, a melhor percentagem de remoção obtido foi de 99,3 % do corante mediante a combinação da reação de Fenton correspondente a 25 mg/L de Fé 3+ e 0,4 %v/v do agente oxidante peróxido de hidrogênio. Conclusão. A reação de Fenton é adequada e consegue elevadas percentagens de remoção e degradação do corante azo Tartrazina.
Palavras chaves: Tartrazina, corante azo, ferro (III), peróxido de hidrogênio, indústria de alimentos.
Introducción
La presencia de colorantes en los cuerpos de agua tiene graves consecuencias ambientales. Por un lado, dificultan la difusión del oxígeno y la luz1 al tiempo que producen un aspecto antiestético, y por otro son considerados como persistentes en el ambiente debido a su naturaleza química; ademas, algunos de sus precursores o subproductos son cancerígenos.
Los colorantes azoicos poseen en su estructura química un grupo (-N=N-) conjugado con anillos aromáticos en ambos extremos y son los más usados en la industria2,3. La Tartrazina posee los códigos E102 (UE)4 y Yellow 5 (FDAUSA)5 y pertenece a esta familia de colorantes, es ampliamente utilizada en la industria alimenticia y aunque es inocua en bajas concentraciones, su ingestión en grandes cantidades puede provocar reacciones alérgicas, como asma y urticaria. También está relacionada con la hiperquinesis en los niños y con tumores en la glándula tiroides, evidencias que han motivado a países como Noruega y Austria a prohibir su uso4.
Así mismo, se observa un potencial riesgo en aguas contaminadas con Tartrazina, la cual se debe remover de los vertimientos de las industrias de alimentos. Este proyecto buscó el desarrollo tecnológico de los procesos avanzados de oxidación (POA's) en la descontaminación de aguas residuales en nuestro país con contenidos de este colorante.
La Tartrazina es un producto sintético de amplio espectro; en investigaciones recientes se ha tratado de generar productos sustitutos para dicho colorante debido a los posibles efectos secundarios en los seres humanos.
Se recomienda a los titulares de productos clasificados como alimentos, cosméticos o medicamentos que contengan Tartrazina, proceder a modificar el registro sanitario6-9 e incluir la expresión "Contiene Tartrazina que puede producir reacciones alérgicas, tipo angioedema, asma, urticaria y shock anafiláctico", lo anterior, teniendo en cuenta las disposiciones expuestas por la sala especializada en medicamentos y productos biológicos de la comisión revisora dentro del concepto emitido en el acta No 1 de 20078,9.
La implementación de programas de producción más limpia, enmarcados en la disminución de vertimientos y efluentes contaminantes y en especial, la aplicación de tecnologías ambientalmente sostenibles10 en los procesos industriales, reducen la demanda de bienes y servicios ambientales en nuestros ecosistemas. Actualmente se encuentra en desarrollo la aplicación de tecnologías de procesos avanzados de oxidación (POAs)11-18, las cuales se basan en procesos de destrucción de los contaminantes por medio de sustancias químicas, conocidas como radicales libres hidroxilos, que tienen la propiedad de ser altamente oxidantes; dichos radicales reaccionan con el contaminante y lo transforman en compuestos inocuos al ambiente18-24.
Existen varias tecnologías disponibles para el tratamiento de efluentes con colorantes, entre las que se tienen algunos métodos físico-químicos como adsorción, coagulación-floculación, oxidación avanzada y filtración en membranas. Estos métodos, pueden llegar a ser muy efectivos, aunque son complejos y de difícil aplicación a gran escala; sin embargo, el desarrollo de tecnologías avanzadas de oxidación, propende por la implementación y conocimiento a nivel local y nacional sobre las aplicaciones de dichas tecnologías en la degradación de un sinnúmero de contaminantes ambientales como pesticidas11-16,20-22, colorantes14,17,18,23,24, residuos de laboratorios19, entre otros.
La reacción de Fenton11-14,20-22 es reconocida como una de las clásicas y más poderosas reacciones de oxidación en aguas. Esta reacción se realiza sin la presencia de radiación ultravioleta, pero, recientemente se ha demostrado que su poder oxidante puede ser incrementado significativamente, empleando radiación ultravioleta ó ultravioleta/visible (reacción de Fotofenton)11-14,20-22. El reactivo de Fenton es una mezcla de peróxido de hidrógeno e ion ferroso (Fe2+) que produce el radical libre hidroxilo (HO.) y el ion férrico (Fe3+)12,20.
Fe 3+ + H2O2 Fe 2+ + .O2H + OH+
El radical libre hidroxilo es la especie oxidante primaria, formada por la descomposición del peróxido de hidrógeno, catalizada por Fe2+ en ausencia de agentes quelatantes del ion ferroso. Es el segundo agente oxidante después del flúor (HO., Eo=-2.8 V vs. flúor, Eo=-3.0 V), y es capaz de realizar oxidaciones no específicas de algunos compuestos orgánicos11-22. Cuando se genera una concentración suficiente de radical libre hidroxilo y otros radicales, las reacciones de oxidación de los compuestos orgánicos pueden llegar hasta una total mineralización11-17. Este proyecto busca el desarrollo tecnológico de procesos avanzados de oxidación (POA's) para la descontaminación de aguas residuales para contenidos de Tartrazina.
El radical libre hidroxilo es la especie oxidante primaria, formada por la descomposición del peróxido de hidrógeno, catalizada por Fe2+ en ausencia de agentes quelatantes del ion ferroso. Es el segundo agente oxidante después del flúor (HO., Eo=-2.8 V vs. flúor, Eo=-3.0 V), y es capaz de realizar oxidaciones no específicas de algunos compuestos orgánicos11-22. Cuando se genera una concentración suficiente de radical libre hidroxilo y otros radicales, las reacciones de oxidación de los compuestos orgánicos pueden llegar hasta una total mineralización11-17.
Este proyecto busca el desarrollo tecnológico de procesos avanzados de oxidación (POA's) para la descontaminación de aguas residuales para contenidos de Tartrazina.
Materiales y métodos
Se empleó un reactor compuesto por una cuba de vidrio, que sirvió como reservorio para el almacenamiento de la muestra problema y como lugar de la reacción de degradación; adicionalmente, se dispuso de un sistema interno de mezcla para mantener la solución homogénea en el periodo de experimentación, el cual se determinó en dos horas. Se utilizó La Tartrazina a una concentración inicial de 100 mg/L y se mantuvo la solución a tratar a un pH igual a 3,0.
Se adicionó la concentración de catalizador (hierro (III)) y agente oxidante (peróxido de hidrógeno) correspondiente a la combinación de factores que se consignan en la tabla 1. Para lograr un desarrollo experimental apropiado y el cumplimiento de los supuestos de residuales, se ejecutaron tres réplicas de los ensayos de forma aleatoria.
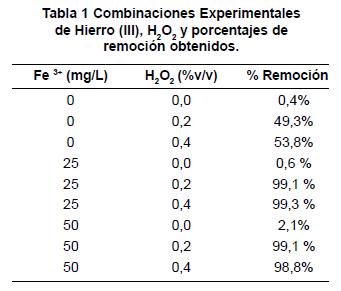
El diseño experimental utilizado en la investigación fue un diseño de dos factores (concentración de catalizados - Hierro (III) y agente oxidante - Peroxido de hidrogeno), completamente aleatorizado. Los niveles de cada uno de los factores se encuentran consignados en la tabla 1, adicionalmente, se realizaron tres réplicas por corrida experimental y al final de los ensayos se determinó la remoción del colorante mediante el empleo de la espectrofotometría UV/ Visible a una longitud de onda de 425 nm.
El modelo estadístico utilizado para el análisis de la información fue:
En donde, µ = Es el porcentaje medio de remoción o degradación del colorante Tartrazina en el modelo.
αi = Es el efecto del i-ésimo nivel del factor concentración de catalizador - hierro (III); i = 0, 25 y 50 mg/L.
βj = Es el efecto del j-ésimo nivel del factor concentración de agente oxidante - peróxido de hidrógeno; j = 0, 0,2 y 0,4 %v/v.
(αβ)ij = Es el efecto de la interacción entre los niveles i y j de los factores concentración de catalizador - hierro (III) y la concentración de agente oxidante - peróxido de hidrógeno.
Yijk = Es la k-ésima observación del porcentaje de remoción del colorante Tartrazina, observado en los niveles i y j de los factores concentración de catalizador - hierro (III) y la concentración de agente oxidante - peróxido de hidrógeno.
εijk = Es el k-ésimo término de error aleatorio.
Resultados y Discusión
En la tabla 1 y la gráfica 1 se muestran los resultados experimentales obtenidos de la remoción del colorante Tartrazina mediante el empleo de la reacción de Fenton, utilizando hierro (III) y peróxido de hidrógeno; se puede apreciar que la adición del agente catalizador de la reacción de Fenton hierro (III), en ausencia del agente oxidante (peróxido de hidrógeno), no favorece la reacción de degradación del colorante, debido a que se alcanzan porcentajes de remoción incipientes. Las combinaciones que representan el empleo de este proceso son: 25 mg/L de Fe3+ y 0 %v/v de H2O2 y 50 mg/L de Fe3+ y 0 %v/ v de H2O2 para las cuales se lograron porcentajes de remoción de 0,6 % y 2,1 % respectivamente, siendo éstos los más bajos de las combinaciones experimentales realizadas en la presente investigación, a excepción de la combinación en la cual no se aplicó ningún reactivo, es decir, 0 mg/L de Fe3+ y 0 %v/v de H2O2.
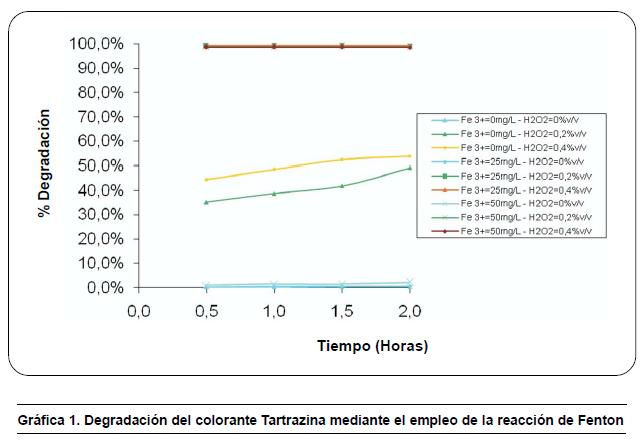
Por otro lado, se observa que el colorante azo Tartrazina, es un colorante que se degrada moderadamente por medio de la oxidación química con el reactivo peróxido de hidrógeno, al someterlo a las combinaciones y concentraciones de este proceso de oxidación; las cuales corresponden a los ensayos de 0 mg/L de Fe3+ y 0,2 %v/v de H2O2, y 0 mg/L de Fe3+ y 0,4 %v/v de H2O2, en los que se obtienen porcentajes de remoción para el periodo de reacción de dos horas iguales a 49,3 % y 53,8 % respectivamente. De acuerdo con los resultados obtenidos en la tabla 1 y la gráfica 1, la adición del catalizador hierro (III) genera un incremento sustancial en la degradación del colorante Tartrazina, para las cuatro combinaciones en las que se empleó con el agente oxidante peróxido de hidrogeno (H2O2), toda vez que se obtuvieron altos niveles de remoción en las dos horas de tratamiento de la muestra de agua con contenido del colorante Tartrazina. Las combinaciones en las que se emplean ambos reactivos corresponden al proceso de oxidación avanzada de la reacción de Fenton, debido a que deben presentarse el catalizador y el agente oxidante para que generen la producción de radicales libres hidroxilos, y a su vez, las reacciones y procesos de degradación y remoción del contaminante.
La combinación de 25 mg/L de Fe3+ y 0,4 %v/v de H2O2, alcanza el mejor porcentaje de remoción de los experimentos realizados con un 99,3% y un buen resultado en la degradación del colorante Tartrazina. De igual forma, se observa que las combinaciones experimentales de 25 mg/L de Fe3+ y 0,2 %v/v de H2O2, y 50 mg/L de Fe3+ y 0,2 %v/v de H2O2 logran una remoción similar; sin embargo, las diferencias de los porcentajes de remoción entre la primera combinación y las dos siguientes no es significativo. Por último, la combinación de 50 mg/L de Fe3+ y 0,4 %v/v de H2O2, alcanza una remoción del orden de 98,8%; todas las combinaciones experimentales que representan la reacción de Fenton logran resultados significativos desde el punto de la remoción del colorante. No obstante, analizando el factor económico de acuerdo con la adición de reactivos y concentraciones, la mejor combinación para lograr la remoción y degradación del colorante corresponde a 25 mg/L de Fe3+ y 0,2 %v/v de H2O2.
Como se aprecia en la gráfica 1, a medida que se incrementa el tiempo de tratamiento del agua residual con el contenido del colorante Tartrazina, se logra un mayor porcentaje de remoción, debido a que favorece las reacciones de degradación y formación de radicales libres hidroxilos, los cuales realizan la remoción del colorante.
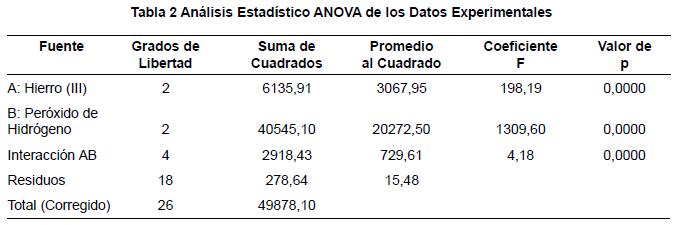
Como se observa en la tabla 2, el análisis estadístico de los datos experimentales, se hizo empleando un ANOVA, de acuerdo con los valores de P (p < 0,05) los factores de concentración de hierro (III) y agente oxidante (peróxido de hidrógeno) tienen una variación significativa en la variable respuesta, es decir, en el porcentaje de remoción del colorante Tartrazina y de esta forma la interacción doble entre ambos factores. Por lo tanto, los resultados del modelo estadístico empleado, sirven para explicar la degradación del colorante Tartrazina basado en los factores definidos, porque la regresión lineal del modelo estadístico posee un R2 = 0.934248. Por lo tanto, el modelo planteado describe adecuadamente el proceso de degradación de la Tartrazina mediante la reacción de Fenton.
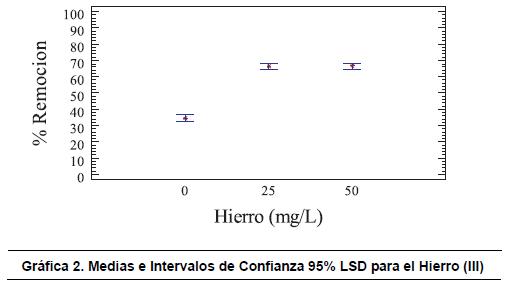
En la gráfica 2 se observa el método utilizado para identificar las diferencias significativas de Fisher (LSD), diferencias significativas entre las medias obtenidas experimentalmente entre 0 - 25 mg/L de hierro (III), y 0 - 50 mg/L de hierro (III); así como diferencias estadísticamente significativas a un nivel de confianza del 95,0%. Por otro lado, no se detecta una diferencia significativa en la variación de 25 - 50 mg/L de hierro (III).
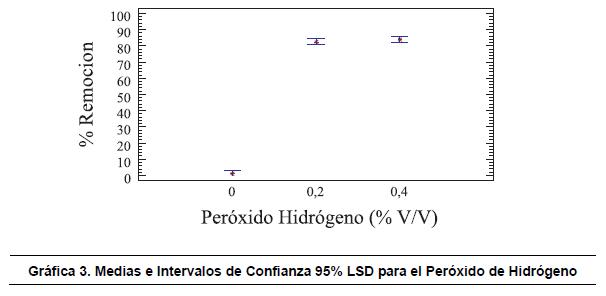
En la gráfica 3, se observa que para los intervalos del agente oxidante, peróxido de hidrógeno, con un nivel de confianza del 95%, las variaciones de las medias entre 0 - 0,2 %v/v y 0 - 0,4 %v/v de peróxido de hidrógeno, poseen diferencias significativas entre los niveles experimentales y la variable respuesta, es decir la remoción del colorante Tartrazina, mientras que para la variación entre 0,2 - 0,4 %v/v de peróxido no se presenta una variación significativa entre los dos niveles.
Conclusiones
El colorante Azo Tartrazina se puede degradar mediante el empleo de la reacción de Fenton, con porcentajes de remoción del 99,3%. Se evidencia que el empleo del proceso de oxidación avanzada es eficiente en la remoción del colorante Tartrazina para un tiempo de tratamiento de dos horas.
La implementación de tecnologías avanzadas de oxidación (TAO's), como la reacción de Fenton, demuestra poseer un amplio número de aplicaciones ambientales; uno de los principales grupos de sustancias químicas sintéticas que se emplean en la industria de alimentos son los colorantes azoicos, los cuales son estables y de difícil descomposición a condiciones ambientales debido a su estructura química y a los enlaces que posee el grupo azo. En la presente investigación se logra la remoción y degradación del colorante Tartrazina mediante la aplicación y el concurso de la reacción de Fenton y se avanza en el conocimiento y aplicación de una de las TAO's a nivel local, incrementando la oferta tecnológica para disminuir los impactos negativos sobre nuestro entorno natural inmediato y alcanzar un desarrollo sostenible mediante el empleo de tecnologías enmarcadas en la ejecución de programas de producción más limpia a nivel industrial, para este caso en particular, el sector industrial de los alimentos.
Referencias
1. SAWYER, Clair Nathan; McCARTY, Perry L. and PARKIN, Gene F. Chemistry for environmental engineering. 4 ed. Estados Unidos: McGraw Hill, 2001. P. 58. [ Links ]
2. RESTREPO GALLEGO, Mauricio, et al. Sustitución de tartrazina por betacaroteno en la elaboración de bebidas no alcohólicas. En: Revista Lasallista de Investigación. Julio-diciembre, 2006. vol, 3 no. 3, p. 7-12. [ Links ]
3. KAPOR, Marco André, et al. Electroanálise de corante alimentícios: determinacao de indigo carmín e tartazina. En: Eclética Química. 2001. vol. 26, no.1, p. 1-20. [ Links ]
4. COMUNIDAD EUROPEA. Decisión 202. (17, marzo, 2005) , relativa a los modelos de formularios necesarios para la aplicación de los reglamentos (CEE) No 1408/71 y (CEE) No 574/72 del Consejo (E001, E101, E102, E103, E104, E106, E107, E108, E109, E112, E115, E116, E117, E118, E120, E121, E123, E124, E125, E126 y E127) Texto pertinente a efectos del EEE y del Acuerdo UE-Suiza: Comunidad Europea, 2006. 25 p. [ Links ]
5. US FOOD AND DRUG ADMINISTRATION. CENTER FOR FOOD SAFETY AND APPLIED NUTRITION. La administración de medicamentos y alimentos de los Estados Unidos. Lanza una campaña educativa para informar a la comunidad hispana acerca de los peligros de comer ostiones crudos. [en línea]. Estados Unidos: FDA/Center for Food Safety & Applied Nutrition, December 29, 2003. [citado en 23 agosto 2008]. Disponible en: http://www.foodsafety.gov/~lrd/fpoyvibs.html [ Links ]
6. THE COCHRANE COLLABORATION. Exclusión de tartrazina para el asma alérgica. Revisión Cochrame traducida por RAM, F.S. y ARDERN, K.D. [en línea]. Oxford, Reino Unido: The Cichrame Collaboration, 2007. [citado en 23 agosto 2008]. Disponible en: http://www.cochrane.org/reviews/es/ab000460.html [ Links ]
7. COLOMBIA. MINISTERIO DE SALUD. Resolución 00580. (26, febrero, 1996). Por la cual se modifica el parágrafo primero de la Resolución 10593 de 1985. Bogotá DC: El Ministerio, 1996. 20 p. [ Links ]
8. COLOMBIA. MINISTERIO DE LA PROTECCIÓN SOCIAL. Resolución 005109. (29, diciembre, 2005). Por la cual se establece el reglamento técnico sobre los requisitos de rotulado o etiquetado que deben cumplir los alimentos envasados y materias primas de alimentos para consumo humano. Bogotá DC: El Ministerio, 2005. 8 p. [ Links ]
9. COLOMBIA. MINISTERIO DE LA PROTECCIÓN SOCIAL. Resolución 0670 (9, marzo, 2007). Por la cual se establece el reglamento técnico de emergencia sobre los requisitos fisicoquímicos y microbiológicos que deben cumplir los productos de la pesca, en particular pescados, moluscos y crustáceos para el consumo humano. Bogotá DC.: El Ministerio, 2007. 10 p. [ Links ]
10. ARROYAVE ROJAS, Joan Amir y GARCES GIRALDO, Luís Fernando. Tecnologías ambientalmente sostenibles. En: Revista de Producción Más Limpia. Julio-diciembre, 2006. vol. 1, no. 2, p. 78-86. [ Links ]
11. RED CIENCIA Y TECNOLOGÍA PARA EL DESARROLLO (CYTED). Temática VIII - G. Eliminación de contaminantes por fotocatálisis heterogénea. Brasil: Digital Grafic, 2001. p. 133. [ Links ]
12. ARROYAVE ROJAS, Joan Amir y CORREA OCHOA, Adrian Alexis. Fotodegradación de malatión usando colector solar. Trabajo de grado Ingeniero Sanitario. Medellín: Universidad de Antioquia. Facultad de Ingeniería. Departamento de Ingeniería Sanitaria. 2001, 104 p. [ Links ]
13. ARROYAVE ROJAS, Joan Amir; GARCÉS GIRALDO, Luis Fernando y CRUZ CASTELLANOS, Andrés Felipe. Fotodegradación del pesticida Mertect empleando fotofenton con lámpara de luz ultravioleta. En: Revista Lasallista de Investigación. Enero-junio, 2007. vol. 3, no. 2, p.19-24. [ Links ]
14. GARCES GIRALDO, Luís Fernando; MEJÍA FRANCO, Edwin Alejandro y SANTA MARÍA ARANGO, Jorge Julián. La fotocatálisis como alternativa para el tratamiento de aguas residuales. En: Revista Lasallista de Investigación. Enero- junio, 2004. vol. 1, no. 1, p. 83-92. [ Links ]
15. ARROYAVE ROJAS, Joan Amir; GARCÉS GIRALDO, Luis Fernando y CRUZ CASTELLANOS, Andrés Felipe. Fotodegradación de las aguas residuales con pesticida Mertect en la industria bananera empleando fotocatálisis con dióxido de titanio y lámpara de luz ultravioleta. En: Revista Lasallista de Investigación. Enero-junio, 2007. vol. 4, no. 1, p. 7-13. [ Links ]
16. ARROYAVE ROJAS, Joan Amir; GARCÉS GIRALDO, Luís Fernando y CRUZ CASTELLANOS, Andrés Felipe. Integración, productividad y responsabilidad ambiental: empleo de tecnologías avanzadas de oxidación para la degradación del pesticida Mertect. En: Congreso Asociación Colombiana de Ingeniería Sanitaria y Ambiental (50: noviembre, 2007: Santa Marta) y Congreso Bolivariano de la Asociación Interamericana de Ingeniería Sanitaria y Ambiental (12: noviembre, 2007: Santa Marta): Memorias. Santa Marta: ACODAL-.AIDIS, 2007. p 1-8. [ Links ]
17. GARCES GIRALDO, Luís Fernando, et al. Degradación de aguas residuales de la industria textil por medio de fotocatálisis. En: Revista Lasallista de Investigación. Enero-junio, 2005. vol. 2, no. 1, p.15-18. [ Links ]
18. GARCES GIRALDO, Luís Fernando. Cinética de degradación y mineralización del colorante naranja reactivo 84 en aguas. En: Revista Lasallista de Investigación. Junio-diciembre, 2005. vol. 2, no. 2, p. 21-25. [ Links ]
19. TELLO RENDÓN, Erick Danilo. Optimización de tecnologías fotocatalíticas de oxidación avanzada aplicada al tratamiento de residuos líquidos de laboratorio.Tesis Doctoral. Las Palmas de Gran Canaria: Universidad de las Palmas de Gran Canaria. Departamento de Química, 2000. 329 p. [ Links ]
20. GARCÉS GIRALDO, Luis Fernando, et al. Fotocatálisis y electrocoagulación para el tratamiento de aguas residuales: investigaciones y aplicaciones. Caldas: [S.N], 2007. p. 38. [ Links ]
21. RED COLOMBIANA DE SEMILLEROS DE INVESTIGACIÓN- NODO ANTIOQUIA. Avances en investigación formativa 2006. Medellín: Artes y letras, 2007. p. 44. [ Links ]
22. RED COLOMBIANA DE SEMILLEROS DE INVESTIGACIÓN- NODO ANTIOQUIA. Avances en investigación formativa 2007. 2 ed. Medellín: Aljara, 2007. 153 p. [ Links ]
23. GARCES GIRALDO, et al. Degradación de aguas residuales de la industria textil por medio de fotocatálisis, Op. cit. p.15-18. [ Links ]
24. GARCES GIRALDO, Cinética de degradación y mineralización del colorante naranja reactivo 84 en aguas, Op. cit. p. 21-25. [ Links ]














