Introducción
El período de transición es considerado como aquel lapso que transcurre desde tres semanas antes del parto hasta tres o cuatro semanas luego del parto (Stalling, 1999). Este es un período caracterizado por modificaciones dramáticas en el estado endocrino de las vacas, que las prepara para el parto y la lactogénesis (National Research Council, 2001). Como resultado de la intensa selección genética, la producción de leche se ha incrementado marcadamente, lo que ha originado un aumento en las demandas nutricionales y metabólicas de estos animales. Después del parto, durante el período de alta producción lechera y déficit energético, el útero, los ovarios y el eje hipotálamo-hipófisis deben restablecer su actividad. En este período se esperan la maduración hormonal del eje hipotálamo-hipófisis, cambios morfológicos e histológicos en el útero y el establecimiento de la nueva población folicular en el ovario que conducirá a la primera ovulación. Es así como varios mecanismos biológicos interactúan en este período y muchas veces pueden resultar en incapacidad para adaptarse eficazmente a la lactancia; mecanismos biológicos como adaptación metabólica, el estrés oxidativo, la función inmune y la capacidad de ingesta de alimento se pueden ver afectados por el balance energético negativo por el cual los animales transitan (Ariette et al., 2014).
El estado nutricional y metabólico tiene relación con el eje reproductivo y el eje somatotrópico en varios niveles. Cambios en la dieta pueden inducir respuestas rápidas en los niveles de metabolitos y hormonas con un papel importante en la regulación del crecimiento folicular (Gong, Lee, Garnsworthy, y Webb, 2002; Holtenius, Agena, Delavaud y Chilliard, 2003; Lucy, 2008).
Los niveles bajos de glucosa e insulina durante la lactancia temprana no son compatibles con la actividad ovárica, debido a que la glucosa es el principal sustrato energético en el ovario bovino y está relacionado directamente con las concentraciones del factor de crecimiento similar a la insulina 1 (IGF-I). Esta proteína también es considerada como una hormona metabólica que se une a los receptores de insulina y tiene un papel clave en el metabolismo de la glucosa en vacas lecheras de alta producción (Lucy, Escalante y Keisler, 2013). La disminución en la secreción de IGF-I causada por NEB podría alterar la producción ovárica de estradiol folicular, suprimiendo así la expresión del estro (Spicer et al., 1990).
Factores metabólicos como la insulina, la hormona del crecimiento (GH) y IGF-1 juegan un rol importante en el proceso de desarrollo y crecimiento folicular. Estos factores están asociados no solo con el desarrollo folicular, sino también con la función de las células foliculares (Shimizu, 2016). Estudios in vitro con inclusión de insulina en fragmentos de tejido hipotalámico de hembras de rata adulta ovarectomizadas han demostrado un aumento de la liberación de GnRH en respuesta a la insulina (Arias, Rodríguez, Szwarcfarb, Sinay y Moguilevsky, 1992). Adicionalmente, estudios en ovejas diabéticas han demostrado la necesidad de la insulina para la secreción pulsátil de LH (Bucholtz, Chiesa, Pappano, Nagatani, Tsukamura, Maeda y Foster, 2000).
Hay varios estudios que reportan la inclusión de compuestos de tipo energético lo que favorece el aumento de las concentraciones de insulina plasmática. Chung et al. (2009) mostraron que la concentración de insulina aumenta en respuesta a la suplementación con PG. Asimismo, otros autores evaluaron la inclusión de 500 mL de PG en vacas del día 7 al 42 de lactancia, obteniendo resultados positivos en cuanto al incremento en las concentraciones de insulina plasmática (Miyoshi, Pate y Palmquist, 2001).
El propilenglicol (PG) (1-2 propanodiol) es una molécula de 3 carbonos (C3H8O2) derivada del propileno. Cuando este se fermenta en el rumen se ha demostrado que disminuye la relación de acetato: propionato, lo que resulta en un patrón ruminal de ácidos grasos volátiles más glucogénicos, mientras que el pH por lo general no se ve afectado (Nielsen y Ingvartsen, 2004). Basados en la información anterior es lógico pensar que la suplementación con PG conduzca a un aumento en la cantidad de insulina disponible para todos los tejidos, incluyendo el ovario, lo que permitirá un reinicio temprano de la actividad ovárica posparto y una mejora en el desempeño reproductivo en estos animales.
Materiales y métodos
El trabajo experimental se realizó en la Estación Agraria Paysandú, propiedad de la Universidad Nacional de Colombia, sede Medellín, ubicada a 2400 m. s. n. m., con una temperatura promedio de 14 °C y una humedad relativa promedio de 80% en una formación ecológica de bosque muy húmedo, montano bajo (bmh-MB), según la clasificación de Holdridge (Holdridge, 1972). Se seleccionaron 20 vacas Holstein que estaban entre la segunda y la sexta lactancia y que se encontraban a 10 días de la fecha esperada del parto. Los animales pastorearon en praderas de kikuyo (Pennisetum clandestinum), sometidas al manejo tradicional con fertilización compuesta, y recibieron suplementación alimenticia con concentrado comercial acorde con su nivel de producción; quiere decir que por cada cuatro litros de leche producidos consumen un kilo de concentrado (relación 4:1). Las vacas se asignaron al azar a uno de los siguientes grupos de acuerdo con la suplementación con propilenglicol: grupo control (T0): sin inclusión de propilenglicol; grupo experimental (T1): 300 gramos por día de propilenglicol; grupo experimental (T2): 500 gramos por día de propilenglicol; grupo experimental (T3): 700 gramos por día de propilenglicol. En todos los casos el propilenglicol fue mezclado con el suplemento alimenticio y fue suministrado dos veces al día durante los dos ordeños, durante 10 días previos a la fecha esperada de parto y hasta los 20 días posparto. Los días 10 y 5 preparto, el día del parto y los días 5, 10, 15 y 20 posparto se obtuvieron muestras de sangre por punción de la vena yugular en tubos vacutainer® sin anticoagulante. Posterior a la obtención, las muestras se centrifugaron a 1500 gravedades por 15 min, para la separación del suero, los cuales se conservaron a -20 °C hasta su análisis. Se cuantificaron las concentraciones de insulina por el método ELISA con el kit AccuBind Elisa Microwells (Monobind Inc.), y utilizando un lector de placas Multiskan Spectrum, Termos-cientific. Los días 5,10, 15 y 20 posparto se determinó la actividad ovárica por ultrasonografía utilizando un ecógrafo de tiempo real y modo B (Pie Medical 240 Parus Vet), dotado con una sonda transrectal de doble frecuencia 6,0/8,0 MHz, siguiendo las recomendaciones de Pierson et al. (1988). Los folículos fueron definidos como estructuras esféricas no ecogénicas (negras) con una clara demarcación entre la pared y el antro folicular. El cuerpo lúteo fue definido como una estructura granulosa ecogénica con un borde bien definido con un estroma ovárico menos ecogénico. Se contó el número de folículos mayores a 2 mm, se midió el diámetro del cuerpo lúteo utilizando el caliper propio de la máquina. La reactivación ovárica se definió como la presencia de un folículo y / o un cuerpo mayor a 8 mm de diámetro (Risco et al., 1994).
Se realizó un análisis de medidas repetidas en el tiempo (4 tratamientos [0 PG / día, 300 PG / día, 500 mL PG / día y 700 mL PG / día] por 7 tiempos diferentes respecto al parto [-10, -5, 0, 5, 10, 15, 20 días), usando PROC MIXED de SAS (SAS, 2000). Se aceptaron diferencias estadísticamente significativas cuando p‹0.05. Para los parámetros reproductivos días abiertos e intervalo parto primer calor, se realizó un análisis de varianza usando datos transformados; esto con el objetivo de satisfacer los supuestos de las técnicas inferenciales; además, se realizaron contrastes entre tratamientos. Los datos fueron sometidos a transformación logarítmica para que la distribución de los residuales se aproximara a la normal. Se evaluó normalidad usando la prueba de Shapiro Wilk.
Resultados
Concentraciones de insulina
Las concentraciones promedio de insulina oscilaron entre 3.3 y 5.7 µUI / mL. Las concentraciones séricas de insulina no se afectaron significativamente con el nivel de inclusión de propilenglicol (tabla 1). El promedio aritmético más alto se observó con 700 g de PG. Estos valores están acordes con lo reportado por otros autores. Galvis et al. (2003) reportaron cantidades de insulina plasmática de alrededor de 3.5 y 4.56 µUI / mL entre12 días antes del parto hasta el día 24 posparto; estos mismos autores no encontraron diferencias entre períodos de muestreo. Por su parte, Kaneko (1997) reportó valores normales en ganado bovino entre 0 y 5 µUI / mL lo que indica que los valores encontrados en esta investigación están acordes con los reportados por estos autores.
Número y tamaño de folículos
El número de folículos y el diámetro folicular no presentaron diferencias significativas para los diferentes tratamientos (figura 1).Todos los folículos hallados tenían un diámetro entre 8 y 9 mm. Estos resultados no coinciden con los reportados por Galvis et al. (2007), quienes encontraron una mayor presencia de folículos menores a 6 mm en relación con los folículos mayores a 6 mm entre el día 10 y 20 posparto en vacas bajo condiciones similares de producción, pero en animales no suplementados con PG. En cuanto al número de folículos, los promedios oscilaron entre 2.4 y 2.8 folículos por período de muestreo (tabla 2). Estos datos son superiores a los encontrados por Galvis et al. (2007), quienes reportaron valores entre 1.1 a 1.7 folículos entre 6 y 9 mm, para los días 10 y 20 posparto, respectivamente.
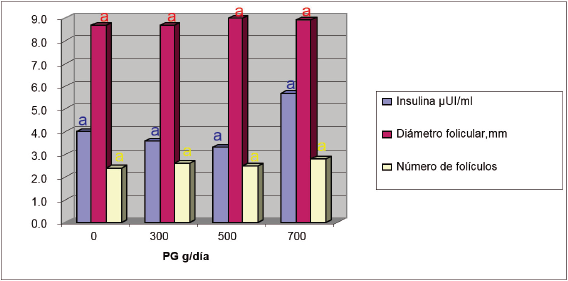
Fuente: elaboración propia, usando PROC MIXED de SAS versión 8.1
Figura 1 Medias de la concentración de insulina plasmática, diámetro y número de folículos en vacas Holstein sometidas a diferentes niveles de suplementación con propilenglicol (PG)
Tabla 2 Diferencias entre medias por período de muestreo para las diferentes variables
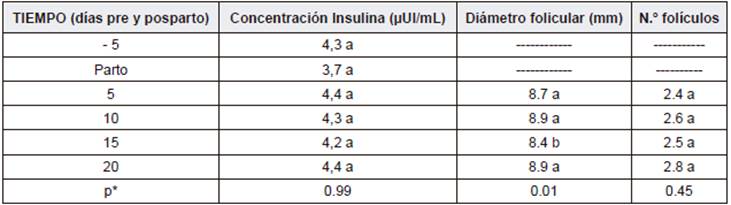
* Probabilidad de cometer el error tipo I
Letras diferentes en la misma columna indican diferencias estadísticamente significativas entre medias a p<0.05
Fuente: elaboración propia, usando PROC MIXED de SAS versión 8.1
No se observaron folículos menores a 6 mm. Una explicación para esta situación radica en la dinámica folicular típica a los 20 días posteriores al parto; es así como Lucy et al. (1991) realizaron un seguimiento por ultrasonografía a los 7, 16, 18, 20, 22 y 25 días posparto en 52 vacas, y encontraron que antes del día 25 el número promedio de folículos pequeños (3-5 mm) disminuyó, mientras que el número promedio de folículos de tamaño medio (6-9 mm) aumentó significativamente (p<0.01)a medida que transcurrían los días posparto.
Parámetros reproductivos
Los valores históricos de los parámetros reproductivos de los animales estudiados indican un intervalo parto al primer calor observado alrededor de 90 días, y unos días abiertos alrededor de 144 días (Evaluación reproductiva Interherd®, hato Paysandú 2008-2009). Según Hutchinson (2001), sería ideal que los días abiertos estén en menos de 110 días, y el intervalo parto primer calor observado, alrededor de 45 días. Lo anterior sugiere que el hato en estudio históricamente presenta parámetros reproductivos deficientes. Para cada uno de las variables evaluadas no se observaron diferencias significativas entre los diferentes tratamientos (figura 3); se observó una tendencia a la disminución de los días abiertos para el grupo con inclusión de 500 g del compuesto, sugiriendo que puede haber un efecto benéfico sobre este parámetro (tabla 3).
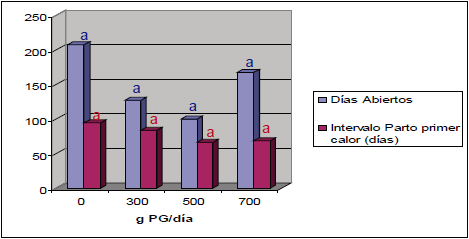
Fuente: elaboración propia, usando PROC MIXED de SAS versión 8.1
Figura 3 Medias para las variables reproductivas en función de la suplementación con propilenglicol (PG)
Tabla 3 Variables reproductivas en función de la suplementación con propilenglicol (PG)
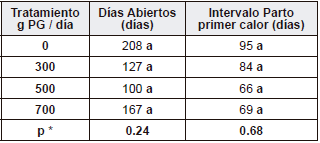
*Probabilidad de cometer el error tipo I.
Letras diferentes en la misma columna indican diferencias estadísticamente significativas entre medias a p<0.05
Fuente: elaboración propia, usando PROC MIXED de SAS versión 8.1
No se presentaron diferencias significativas en los parámetros reproductivos en función de la inclusión PG; sin embargo, se observó una tendencia leve (Pr>t =0.1169) a la disminución en los días abiertos cuando se suministró 500 g de PG por día (tabla 4).
Discusión
En el período de transición a la lactancia las vacas lecheras pasan por un estado de desbalance de muchos nutrientes, pero el limitante principal es la energía, porque de ella dependen muchos procesos metabólicos, endocrinos y fisiológicos en los animales. En circunstancias normales estos animales sufren un balance energético negativo (BEN), una condición que afecta directamente la fisiología del animal y lo enfrenta a diferentes actividades de tipo catabólico, con las cuales responde a las necesidades propias de este período; con la suplementación de propilenglicol (PG) se pretende minimizar los efectos adversos del BEN sobre el balance hormonal y la actividad ovárica de las vacas de alta producción lechera.
Un estudio hecho por Christensen et al. (1997) indica que las concentraciones plasmáticas de glucosa y de insulina alcanzaron su punto máximo en los primeros 90 minutos después de la administración vía oral de PG; estos resultados indican que es fácilmente disponible para la vaca y la mayoría del compuesto es rápidamente absorbido en el rumen y utilizado por el hígado para la gluconeogénesis.
Los diversos resultados obtenidos con la suplementación con PG pueden fundamentarse en lo anteriormente descrito; Miyoshi et al. (2001) y Grummer et al. (2004) midieron la insulina sérica dentro de las tres primeras horas luego de la administración de PG, mientras que otros autores tomaron la muestra más de 4 horas después (Rukkwamsuk et al., 2005), tratando de identificar el pico de secreción de insulina. Los resultados obtenidos en esta investigación no coinciden con los obtenidos por Rukkwamsuk et al. (2005), ya que la metodología de la toma de muestra y el tiempo de medición no fueron similares.
La toma de muestra para insulina se realizó entre las 5 y 6 horas posteriores de la administración de PG, momento en el cual es muy probable que los valores de insulina plasmática hayan retornado a los valores basales en todos los tratamientos. Adicionalmente, es muy probable que las condiciones en las que se realizó esta investigación no sean favorables al aumento de las concentraciones de insulina, presentación del BEN en los animales, propio del período de transición y que, a su vez, está asociado con presentación de bajas concentraciones de IGF-I, así como concentraciones de diferentes hormonas (Cortisol, leptina, hormonas tiroideas) que influyen en el metabolismo y pueden afectar la adaptación al BEN (Wathes et al., 2011).
Por otro lado, en el período de transición, disminuyen de manera significativa las concentraciones de insulina a la par que aumenta la secreción de somatotropina (Holtenius, Agena, Delavaud y Chilliard, 2003). La relación entre estas dos hormonas antagónicas hace que sea difícil obtener respuestas significativas en la secreción de insulina y más aún en la respuesta de los tejidos periféricos (Rhoads, Kim, Leury, Baumgard, Segoale, Frank, Bauman, Boisclair, 2004). Adicionalmente, las condiciones dietarias prevalentes en los sistemas de producción lechera especializada, en el trópico alto colombiano, aumentan la magnitud del BEN característico del período de transición a la lactancia, lo que, seguramente, limita la capacidad de secreción de insulina en los animales sujetos a estas condiciones. Galvis, Correa, Ramirez & Soler (2003), encuentran que, bajo condiciones similares a las hubo en este experimento, y con el mismo tipo de animales, el balance de energía al día 12 posparto osciló entre -20 y -35% de los requerimientos, mientras que en otra investigación, bajo condiciones similares, los valores de BEN oscilaron entre -10 y -25% de los requerimientos, al día 10 posparto (Galvis, Correa, Ramírez, y Soler, 2003). Si bien en esta investigación no se determinó el balance energético, los reportes anteriores, permiten inferir que los animales presentaron balances energéticos negativos de magnitud limitante para la obtención de respuestas fisiológicas favorables a la suplementación con PG. Al respecto, Chung et al., (2009), encontraron que la respuesta en la secreción de insulina plasmática, se vio afectada por la cantidad de propionato que escapa a la captura hepática y es capturado por el páncreas.
Esta cantidad de propionato depende de la cantidad de PG suministrado y de la cantidad de propionato generado en la fermentación ruminal. Estos resultados están acordes con los de Grummer et al., (2004), que indican que el PG produce un pico de secreción de insulina anterior al de secreción de glucosa, indicando que por sí solo, o a través de un metabolito derivado de él, como el propionato, estimulan la secreción de insulina. Desde luego la cantidad de propionato disponible para estimular significativamente la secreción de esta hormona depende de la cantidad de propionato generado en el rumen, el cual se produce en función directa de la cantidad de carbohidratos no estructurales en la dieta, y como lo han indicado diversos autores, bajo las condiciones en las que se llevó a cabo esta investigación son el componente dietario más limitante (Correa, Pabón y Carulla, 2008). Esta condición ya fue informada en trabajos previos con PG; es así como Armentano et al., (1984) reportan que la magnitud de la respuesta de la concentración de insulina en la sangre depende en gran medida de la cantidad de alimento ingerido.
Estudios realizados por Chung et al., (2007), mostraron que la concentración de insulina aumentó en un 200 a 400% a los 30 minutos posteriores a la administración del compuesto, usando dosis desde 307 hasta 1036 g. El momento de la toma de la muestra después de la administración de PG y la forma de administración puede afectar la concentración plasmática de insulina. Estos autores encontraron que la insulina plasmática fue mayor cuando se administró el PG en forma oral o intraruminal, comparado con la administración con la mezcla de la ración. Se puede sugerir que las principales condiciones para no encontrar aumento en los niveles de insulina plasmática en esta investigación son: la forma de suministro, ya que se dio mezclado con la ración; adicionalmente, las dosis utilizadas en la presente investigación fueron inferiores a las reportadas en la literatura como capaces de elevar significativamente las concentraciones plasmáticas de insulina.
Desde el punto de vista metabólico, la concentración puntual de un metabolito u hormona no siempre explica en forma satisfactoria las variaciones fisiológicas y / o productivas que pueden provocar en los animales. Muchos procesos fisiológicos responden a la estimulación acumulada de las señales metabólicas y / o endocrinas. Un ejemplo de esto fue reportado por Recabarren (1994), quien señala que se requieren altos niveles de insulina sostenidos en el tiempo para que, a nivel central, se estimule la producción y liberación de GnRH / LH. Para los animales de la presente investigación se puede inferir que la frecuencia del pulso de GnRH / LH, necesaria para generar folículos estereidogénicamente competentes, fue adecuada (Haughian, Ginther, Kot y Wiltbank, 2004), lo que puede sugerir que el balance hormonal (incluyendo la secreción de insulina) fue favorable, dado el número y el tamaño de estructuras encontradas. Sin embargo, en la presente investigación no se observaron estructuras superiores a 9 mm, lo que pudo ser debido al corto período de tiempo en el que se realizó el seguimiento de la actividad ovárica posparto, lo que impidió determinar si a través del tiempo podrían encontrarse diferencias de las poblaciones foliculares entre los diferentes tratamientos, lo que es posible, dado que en las vacas lecheras la reactivación del ciclo estral ocurre durante las primeras semanas de lactación con un intervalo a la primera ovulación variable (Risco, Drost, Thatcher, Savio & Thatcher, 1994). Estudios realizados con ultrasonografía (Lucy et al., 1991) reportaron que durante la segunda semana los animales reinician su actividad ovárica y desarrollan folículos dominantes ovulatorios, no ovulatorios y quistes, originando diferentes intervalos para la primera ovulación, según la estructura que se desarrolle. Si el BEN es uno de los principales factores que altera la dinámica folicular, es de esperar que en la presente investigación haya tenido profundos efectos sobre la respuesta a la suplementación con PG, pues bajo las condiciones en las que se realizó este experimento (condiciones dietarias y días en lactancia) es de esperar BEN de magnitudes significativas, lo que seguramente afectó la respuesta del ovario a las diferentes hormonas, incluyendo la insulina.
Lucy et al. (2003) evaluaron el efecto de la suplementación con PG sobre el intervalo parto primer celo, sin encontrar efectos significativos. Contrariamente Formigoni et al. (1996) reportaron que al día 96 posparto una baja proporción de animales suplementados con PG fueron aciclícos en comparación con animales control; asimismo, Butler et al. (2006) administraron una dosis diaria de 518 g de PG que resultó en una disminución del intervalo a la primera ovulación posparto (32 versus 44 días); la primera fase luteal fue más larga en animales suplementados con PG (13.4 versus 7.3 días), reflejándose en una mejor función luteal. Por el contrario, la administración de la misma cantidad del compuesto en ganado lechero desde el día 10 antes del parto hasta el día 25 posparto no tuvo efecto significativo en la proporción de folículos preovulatorios, quísticos o atrésicos (Hutchinson, 2001), lo que pudo ser debido a las diferencias en el estado de lactancia en el que fue suministrado en la duración de la suplementación con PG.
Conclusiones
El suministro de PG durante el período de transición a la lactancia no mostró evidencias que permitan concluir que su utilización favorezca significativamente el reinicio de la actividad ovárica posparto y el desempeño reproductivo de los animales. Respecto a su efecto sobre la secreción de insulina es necesario realizar otras investigaciones que centren sus objetivos en la dinámica de su secreción acorde con modo y tiempos de suministro.

















