Introducción
La cebolla (Allium fistulosum) llamada cebolla rama o junca en Colombia, ocupa un renglón importante en la producción agrícola del departamento de Risaralda y contribuye en el tercer renglón de productividad a nivel nacional superado por Boyacá y Nariño (DANE, 2014.). El principal requerimiento nutricional de A. fistulosum es el N. Entre las fuentes de este elemento, la gallinaza fresca se caracteriza por su rápida disponibilidad y aunque varía el contenido de este elemento de una gallinaza a otra se habla de un rango entre 1,0 a 3,5% en peso seco de N, 0,4 a 4,5% de P como P2O5 y 0,2 a 2,9% de K como K2O (ICA). Es así como los agricultores de la región han adoptado la aplicación de estos residuos como fuente exclusiva de este nutriente sin medir consecuencias a corto, mediano o largo plazo. Varios problemas por la aplicación de estiércol, han sido detectados incluyendo toxicidad por sales, acumulación de metales traza en las plantas (Meek 1974, Delgado et al., 2014) y transmisión al suelo y al agua de virus y bacterias que causan enfermedades en animales y al hombre (ICA), representando un riesgo para la salud de los consumidores (Diaz et al. , 2003, Delgado et al., 2014) Un indicador de respuesta sobre el efecto de estos residuos es la presencia microbiana, la cual reacciona rápidamente ante cambios del entorno ambiental.
Entre los microorganismos más estudiados en ambientes de producción agrícola están las bacterias fijadoras de nitrógeno (diazotróficas) heterótrofas de los géneros Azotobacter sp. y Azospirillum sp. y HMA, principalmente asociados a la captura y disponibilidad de N (Johansen et al., 1993) y P (Valadares et al., 2016) para las plantas, respectivamente. Las bacterias diazotróficas, también se asocian a la producción de sustancias promotoras de crecimiento (Ahemad & Kibret, 20I4), estas sustancias además de facilitar la adquisición de nutrientes o modular niveles hormonales en las plantas, actúan como biocontrol inhibiendo el desarrollo de agentes patógenos (Glick, 2012). Los géneros Azotobacter sp. y Azospirillum sp.predominan en suelos con pH cercano a la neutralidad. Cuando el pH es < 5 Azospirillum sp. se encuentra en forma esporádica y en suelos con pH < 4.5 no se logra su aislamiento (Caballero, sf). Por su parte Azoto-bactersp. es un género altamente sensible a la acidez y aunque es capaz de sobrevivir a pH entre 4.5 - 9.0 (Gül, 2003), su óptimo desarrollo lo consigue a pH entre 6.5 - 7.5. En suelos con pH < 6.0 generalmente es ausente o posee muy pocos miembros (Balandreau, 1986; Cardona & Sánches, 1998; Ei-Lattief Essam A. Abd, 2016). Azotobacter sp. a pesar de ser de vida libre, se desarrolla mejor alrededor de la rizosfera. Dóbereiner (1966) indica que la especificidad de este género con la rizosfera de una planta es más íntima que en otras bacterias diazotróficas, por lo tanto su abundancia está relacionada con la especie de planta asociada (Sariv & Ragoviv, 1963). Azospirllum sp. es más versátil y tiene la capacidad de adherirse a las raíces de diversas gramineas y a otras familias de plantas incluyendo algodón y tomate (Caballero, Sf; Levanony & Bashan, I99I). Por su parte, la distribución de hongos micorrízicos en el suelo puede ser afectada directamente por la humedad, materia orgánica y pH, donde una buena esporulación de HMA ocurre a pH entre 5 y 8 (Siqueira, I989). Sin embargo, el conocimiento del papel de las condiciones edáficas y climáticas en su establecimiento y efectividad aún es limitado (Serralde & Ramírez, 2004; Montaño, 2007).
Varios estudios han reportado la presencia de Azotobacter sp., Azospirillum sp. y HMA asociados a la rizosfera de cebolla y el efecto positivo en el desarrollo de la planta (Pulido & Cabrera, 2003; Agudelo & Casierra, 2004; Nemat et al., 20II), por lo tanto para estimar el efecto microbiológico de la gallinaza fresca y compostada sobre el cultivo de cebolla (A. fistulosum) se cuantificaron unidades formadoras de colonias (UFC) de los generos Azotobacter sp. y Azospirillum sp., así como también el número de esporas de HMA.
I. Materiales y métodos
Área de muestreo. El trabajo tuvo lugar en el departamento de Risaralda, Municipio de Pereira, vereda La Bella a una altura de I840 m.s.n.m., con temperatura promedio de 18 °C, precipitación anual de 2600 mm y humedad relativa de 90%. El material genético utilizado en las evaluaciones fue la variedad de cebolla de rama "La Pereirana", la cual ocupa un 48% del área cultivada en cebolla de la zona y que ha mostrado una amplia adaptación a las condiciones locales (Polanco & Gómez, 2017).
En el experimento se utilizó un diseño de bloques al azar, con cuatro tratamientos (Tabla 1) a partir de requerimientos en fertilización del cultivo y el análisis de suelos (Tabla 2)
Tabla 1 Tratamientos con incorporación de gallinaza en cultivo de cebolla (A. fistulosum)

Fuente: Las Autoras
Tabla 2 Propiedades químicas de suelo cultivado con cebolla (Allium fistulosum) en vereda La Bella, Risaralda, Colombia
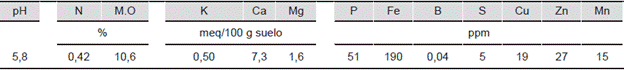
Fuente: Las Autoras
Recuento bacteriano. Fueron tomadas muestras de suelo rizosférico, que fue diluido en serie hasta 10-7 y se inocularon por triplicado 100 µL en medio de cultivo Ashby para el género Azotobacter sp. y FBN para el género Azospirillum sp. Los resultados se expresan en UFC después de 24 horas de incubación (Döbereiner et al., 1995).
Extracción y cuantificación de esporas de HMA. Se tomaron 10g de suelo rizosférico por triplicado. Las esporas fueron separadas mediante tamizado en húmedo y gradiente de sacarosa al 50% (peso/volumen) para establecer la densidad de esporas por gramo de suelo según la metodología sugerida por Gerdemann & Nicolson (1963).
Análisis estadístico. A los resultados obtenidos se les realizó análisis de varianza y pruebas de comparación de medias.
2. Resultados y discusión
El suelo estudiado es de textura franca, pH moderadamente ácido, niveles altos de materia orgánica, P, K y Ca, Cu, Zn. y Mn (Tabla 2). La textura, materia orgánica y pH son propicios para el cultivo de cebolla que requiere suelos sueltos ricos en materia orgánica y pH entre 5,7 y 7,4 (ICA y CORPOICA, 1996). Los generos Azotobacter sp. y Azospirillum sp. predominan en suelos con pH cercano a la neutralidad. El pH del suelo en este estudio fue de 5,8 beneficiando la presencia de Azospirillum sp., en concordancia con el estudio realizado por New & Kenedy (1989) en suelos con pH entre 3,3 y 7,2 donde los resultados indicaron mayor abundancia de este género en suelos con pH en un rango entre 5,6 - 6,7. Azotobacter sp. reflejó su sensiblidad a la acidez con menor presencia concordando con Balandreau, 1986; Cardona & Sánches, 1998; Ei-Lattief Essam A. Abd, 2016 quienes indican que en suelos con pH < 6.0 generalmente este grupo bacteriano es ausente o posee muy pocos miembros.
La acidez del suelo ejerce poco efecto sobre la sobrevivencia de las esporas de HMA (Alvarado et al., 2004), sin embargo un ligero aumento en el pH favorece la esporulación de los hongos micorrízicos (Peña et al., 2007). El número de esporas de este estudio que estuvo entre 44 y 9I por gramo de suelo obtenidas en los tratamientos T4 y TI respectivamente, no indica efectos negativo por influencia de pH ya que los resultados son similares a los encontrados en cultivos de cebolla con alta producción (Pagano & Fantini 2009; Peña et al., Sf.).
Recuento de Azotobacter sp., Azospirillum sp. y Hongos Micorrizicos Arbusculares
De modo general, Azospirillum sp. fue más abundante que Azotobacter sp. en cada uno de los tratamientos (Figura 1A). El recuento bacteriano reflejó mayor presencia de Azospirillum sp. (2,0 x I09 UFC) en el tratamiento con fertilización de síntesis química (T4) y menor en T2 (gallinaza compostada) con 5,0 x107 . Al comparar con estudios similares la densidad es alta (Pulido et al., 2003; Mujiyati, 2009). Este grupo bacteriano se caracteriza por ser de alta motilidad y poseer metabolismo versátil para la obtención de fuentes de C y N, contribuyéndole adaptación para establecerse en el entorno competitivo de la rizosfera y cambios rápidos en las condiciones ambientales (Hartmann & Zimmer, 1994). Azotobacter sp. presentó mayor presencia en T2 con 1,0 x107 UFC y la densidad más baja 2,0 x 105 en T4, contrario a lo observado en Azospirillum sp. (Figura 1A). A pesar de la diferencia entre tratamientos se considera una densidad poblacional alta considerando estudios reportados por Martyniuk & Martyniuk, (2002) y Córdova et al., (2009), quienes indican que este género rara vez excede varias miles de células por gramo de suelo, principalmente en suelos de regiones tropicales donde no es común encontrar cifras mayores de 103 UFC. Cassetari et al., (2016) en el trabajo sobre fijación biologíca de nitrógeno asociativa y de vida libre, enfatiza sobre la gran diversidad funcional de Azotobacter sp.y Azospirillum sp. y su potencial como bioindicadores en alteraciones ambientales.
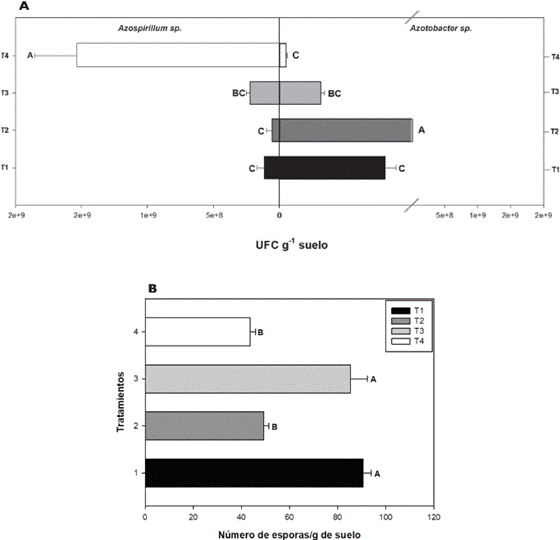
Figura 1A y B Recuento de Azospirillum sp. y Azotobacter sp. (A) y Hongos Micorrizicos Arbusculares (B) en suelo cultivado con cebolla (A. fistulosum) bajo influencia de gallinaza, en la vereda La Bella, Risaralda, Colombia. Letras iguales no difieren significativamente (Test de Tuckey).
HMA presentó mayor densidad de esporas por gramo de suelo en T1 con 91 unidades. Este resultado podría estar asociado a los altos contenidos de materia orgánica de la gallinaza (Estrada, 2005), siendo esto ya demostrado en el establecimiento de HMA, de acuerdo al estudio realizado en los Llanos Orientales, durante cinco años consecutivos, donde se evaluaron poblaciones nativas de HMA asociados a maíz, analizando su comportamiento bajo distintos tratamientos incluyendo gallinaza Serralde & Ramírez (2004). En este estudio también se hace referencia sobre el efecto inverso de altas tasas de mineralización sobre la presencia de HMA, lo cual podría explicar la menor densidad de esporas en gallinaza compostada encontradas en el presente estudio en comparación a gallinaza cruda (Figura 1B). El tratamiento de fertirrigación con 85 esporas por gramo de suelo también favoreció los HMA, sugiriendo que el componente hídrico desempeña un papel importante en este proceso, tal como ha sido reportado por (Lara, 1987, Montaño et al., 2007) a partir de resultados en el Altiplano mexicano Potosino-Zacatecano, donde se ha denotado que la variación de la capacidad de esporulación de los hongos, no sólo depende del hospedante al que los HMA se encuentran asociados sino también por la presencia de lluvias o períodos de sequía. En otro estudio en Zapotitlán de las Salinas, Puebla llevado a cabo por Reyes, (2000) el autor indica que pesar de que la esporulación fue ligeramente mayor en la época de lluvia, ésta no fue estadísticamente diferente a la cuantificada en época de secano, lo cual sugiere que a pesar del componente hídrico desempeña un papel importante en la esporulación, su dinámica es muy variable y debe asociarse con otros factores del entorno edáfico y probablemente la especie de micorriza debido a sus diversas estructuras de adaptación, ya que las condiciones edáficas modelan la composición de las poblaciones de HMA dentro de las cuales el pH del suelo y los contenidos de materia orgánica pueden ser empleados como indicadores del comportamiento de los HMA (Serralde & Ramírez, 2004).
Productividad del cultivo y densidad microbiana
En este estudio se confirma la versatilidad de Azospirillum sp., abundante en todos los tratamientos. Los resultados de mayor productividad con gallinaza cruda y fertirriego no tuvieron la misma tendencia que la densidad de Azospirillum sp. y Azotobacter sp. (Figura 1A), es probable que Azotobacter sp., entre otros factores se afecte por composición de la gallinaza la cual contiene Cu (Williams, 2013), elemento tóxico para estas bacterias incluso en muy bajas concentraciones (Gül (2003). Aumento en la producción de biomasa de la planta ha sido observado cuando se fertiliza conjuntamente con gallinaza fresca y bacterias del género Azospirillum sp., en Brachiaria (Parreira et al., 2015), Por su parte la densidad de esporas de HMA presentó una tendencia similar a la productividad del cultivo siendo mayor en T1 y T3, no obstante no se podría establecer si la planta fue beneficiada por la esporulación o viceversa, ya que las plantas pueden acceder al agua y a los nutrientes a través de sus propios sistemas radiculares, en lugar de hacerlo vía HMA, y la asociación planta-HMA requiere una parte significativa de la energía fijada por el huésped (Jakobsen, Smith & Smith, 2002; Fajardo, 2015). Los resultados podrían estar asociados a la alta suceptibilidad de la cebolla a ser colonizada por HMA (Tawaraya et al., 2001, Roman, 2003).
De otra parte, los exudados liberados a través de la raíz de la cebolla podrían haber influido en la germinación de las esporas, ya que este proceso requiere en muchos casos del estímulo de exudados radiculares (Daniels, 1984). Un efecto combinado entre Azospirillum sp., HMA y aplicación de gallinaza fue observado en plantas de sésamo donde ocurrió un aumento en la población de Azospirillum sp., en el número de esporas de HMA, así como en el contenido de N, P, y K y algunos parámetros de crecimiento de la planta (Abdullahi et al., 2013).
Lo que sí está reflejado en este estudio es que la gallinaza cruda no afecta negativamente los HMA como si ocurre con Azotobacter sp. y Azospirillum sp. Los resultados podrían estar asociados a la dependencia micorrízica de la cebolla tal como indican Tawaraka et al., (2001) y Pagano et al., (2009) en un estudio realizado en suelos brasileños donde se encontró alta esporulación de HMA en asociación con cebolla al compararla con un cultivo de lechuga.
Perspectivas del uso de gallinaza como fertilizante en el cultivo de cebolla.
Los resultados del presente estudio basados en ton/ha indicaron mayor productividad de cebolla con gallinaza fresca, seguida de fertirrigación, gallinaza compostada y fertilización de síntesis química. La presencia de los microorganismos estudiados en relación al rendimiento del cultivo indican un favorecimiento del uso de gallinaza en presencia de esporas de HMA, por su parte la prospección del establecimiento de Azotobacter sp. y Azospirillum sp, podría basarse en el replanteamiento del uso de gallinaza cruda hacia la compostación, esto con la expectativa de mitigar sus efectos ambientales y aprovechar mejor sus propiedades nutricionales. Adicionalmente y en concordancia con Patiño y Sanclemente, (2014) es importante considerar la ecología microbiana rizosferica de las plantas estudiadas.
3. Conclusiones
Los resultados obtenidos indican que la gallinaza cruda tiene un impacto positivo en el rendimiento del cultivo de cebolla y la esporulación de HMA, un efecto negativo en Azotobacter sp. con mejor desarrollo en la gallinaza compostada y en Azospirillum sp. sin respuesta relevante. El presente estudio aporta información sobre los efectos potenciales que la gallinaza puede generar en la diversidad y actividad microbiana del suelo y por ende su papel dentro del equilibrio y sustentabilidad del mismo. Sin embargo se hace necesario reforzar el presente planteamiento con futuros estudios con diversas comunidades microbianas y metodologías de mayor robustez.














