1. Introducción
Cryptococcus neoformans y C. gattii es un complejo (Kwon-Chung et al., 2017) con varias especies crípticas (Hagen et al., 2015). C. neoformans i ncluye las especies C. neoformans y C. deneoformans con cinco tipos moleculares y C.gattii con cuatro tipos moleculares (Meyer et al., 2009). A lo largo de este artículo se adopta la denominación más simple de C. gattii y C. neoformans. Las dos especies están asociadas con infecciones en humanos y animales (Rajasingham et al., 2017), causan criptococosis, entidad que, a nivel mundial, se relaciona principalmente con pacientes VIH+/SIDA (O'Halloran, Powderl y Spec, 2017); difieren por sus características genéticas, bioquímicas (Chen et al., 2017; Watkins, King y Johnston. 2017; Chang y Chen, 2015), ecológicas (May, Stone, Wiesner Bicanic, y Nielsen, 2015; Herkert et al., 2017), distribución geográfica (Rhodes et al., 2017, Cogliati et al., 2017), manifestaciones clínicas, tipo de huésped afectado y su respuesta a los tratamientos antimicóticos (Maziarz y Perfect, 2016).
Las excretas de aves en especial las de paloma (Columba livia) son la fuente principal de C. neoformans (Huamán et al., 2018; Menezes et al., 2014; Canónico-González; Adame-Rodríguez, Mercado Hernández, y Aréchiga-Carvajal, 2013), mientras que C.gattiise asocia con madera, corteza, flores, hojas de eucaliptos, almendros y otras especies de árboles (Escandón, Sánchez, Firacative y Castañeda, 2010; Vélez y Escandón. 2017; Springer et al., 2014). También, en ocasiones C.gattii se ha aislado en excretas de aves, en 2014, Kangogo, Boga, Wanyoike y Bill informaron un porcentaje bajo en heces de otra especie de paloma (Geopelia striata) y en 2016 Dongmo et al., estudiaron heces de murciélagos y palomas, y encontraron C. gattiien las de palomas, pero no especificaron el género.
Los trabajos citados muestran que el aislamiento de C. gattii en excretas de palomas es muy bajo comparado con la alta prevalencia de C. neoformansen distintas regiones del mundo y sugieren que debe existir algún factor o factores que determinan estos resultados, pero hasta ahora no hay estudios en condiciones controladas que comparen el crecimiento de estas especies en excretas positivas y negativas para C. neoformansque ayuden a dilucidar este fenómeno; el objetivo del presente estudio fue comparar el crecimiento en el laboratorio de C. neoformans y C gattii en extractos de excretas de palomas y describir los posibles factores que dificultan la proliferación de C. gattii en este sustrato.
2. Marco teórico
2.1. Criptococosis
La criptococosis es una micosis sistémica, oportunista del hombre y los animales, de curso subagudo a crónico, que afecta tanto a individuos inmunocomprometidos como inmunocompetentes (Herkert et al., 2017). La forma primaria es casi siempre pulmonar pero no necesariamente sintomática. Se adquiere por inhalación, aunque se han informado algunos casos con antecedentes de implantación. En su forma diseminada tiene marcado tropismo por el sistema nervioso central y más del 50% de los casos registrados tienen afección de tal sistema, sin embargo, pueden ocurrir lesiones a nivel de otros órganos (Williamson et al., 2017). La meningitis criptocócica es la micosis más frecuentemente asociada con pacientes con el síndrome de inmunodeficiencia adquirida (SIDA), con una morbilidad y mortalidad significante, y con menos frecuencia esta entidad se presenta en pacientes con leucemia, lupus eritematoso sistémico, enfermedad de Hodgkin, o que reciben terapia inmunosupresora. Sin embargo, se reconoce cada vez más que la enfermedad puede ocurrir en pacientes con sistemas inmunitarios aparentemente normales "inmunocompetentes" (Messina, Maziarz, Spec, Kontoyiannis, Perfect, 2017; George, Spec, Powderly, Santos, 2017).
La meningitis criptocócica es una infección cerebral que produce un estimado de 600.000 muertes y una carga global de casi I millón de casos por año (Lin, Shiau y Fang, 2014). La incidencia de casos de criptococosis en América Latina es de 5300 por año y Colombia es uno de los países con mayor incidencia, entre 1.001 a 2.500 casos (Rajasingham et al., 2017), con una media en la población general estimada en 2,4 casos por 106 habitantes, mientras que en los pacientes con SIDA se eleva a 3 casos por 103 (Lizarazo et al., 2007).
2.2 Agente etiológico
El complejo Cryptococcus neoformans/C. gattii agente etiológico de criptococosis son levaduras encapsuladas, que se reproducen por gemación casi siempre simple, rara vez múltiple. La célula es redonda, ovalada, usualmente de 4 a 6 micrómetros de diámetro (Kwon-Chung, et al., 2014). Crece tanto a 37°C como a temperatura ambiente, hidroliza la urea, no fermenta azúcares, asimila glucosa, galactosa, dulcitol, inositol, maltosa y sucrosa, pero no lactosa, ni nitratos, y utiliza la creatinina como única fuente de nitrógeno (Torres-Rodríguez, Alvarado-Ramírez, Gutiérrez-Gallego, 2008).
Este complejo fue considerado inicialmente una sola especie (C. neoformans), con dos variedades neoformansy gatiii las cuales se distinguieron por su diversidad antigénica en los serotipos A y D para la variedad neoformans y, los serotipos B y C para la var. gattii(Kwon-Chung, et al., 2014). El descubrimiento de dos teleomorfos diferentes (Kwon-Chung, 1976) condujo al reconocimiento de dos especies, C. neoformans y C. gattii que luego se verificó mediante datos de secuencia de todo el genoma (Kwon-Chung et al., 2014).
En la actualidad, se conoce que la especie neoformans presenta dos variedades C. neoformans var. grubii (serotipo A) con los tipos moleculares VNI (AFLPI), VNII (AFLPIA/ IB) y C. neoformans var. neoformans (serotipo D) VNIII (AFLP3), y la especie gattiipresentan los tipos moleculares VGI (AFLP4), VGII (AFLP6), VGIII (AFLP5) y VGIV (AFLP6). (D'Souza et al, 2011).
Las dos especies difieren en su morfología, hábitat, distribución geográfica, epidemiología, estructura inmunoquímica de la cápsula, afinidad por ciertos ácidos tricarboxílicos, asimilación del triptófano, inhibición de la ureasa por el ácido etilendiaminotetracético (EDTA), contenido de guanina-citosina, secuencia de ADN y en el metabolismo de los compuestos nitrogenados como la creatinina y la urea (Chen et al. 20I7;Watkins et al., 2017; Chang y Chen, 2015; May et al., 2015; Herkert et al., 20I7; Rhodes et al., 2017; Cogliati et al. 2017; Maziarz y Perfect, 2016).
El aislamiento del complejo C. neoformans/C. gattiia partir de muestras contaminadas, como excretas de aves, se hace en medios selectivos especiales como agar semilla de girasol (Helianthus annuus) (Pal y Baxter 1985). En este medio C. neoformans sintetiza la enzima fenoloxidasa que cataliza la oxidación de sustratos difenólicos en productos similares a la melanina, observándose colonias de color café que permiten diferenciarlas de otras levaduras como Candidau otras especies de Cryptococcus.
Para diferenciar C. neoformans de C. gattii se utiliza, entre otros el medio de canavaninaglicina-azul de bromotimol (CGB), dicha prueba se fundamenta en la particularidad que presenta C. gattii de ser resistente a la L-canavanina (aminoácido natural estructuralmente similar a la L-arginina), el cual es degradado por las cepas de esta variedad, liberando amonio como compuesto final. El amonio en el medio eleva el pH del mismo, que pasa de 5,8 a 7 o más, virando el color del medio de amarillo verdoso a un azul de cobalto, por la presencia del indicador azul de bromotimol (Pérez et al., 2003).
2.3 Hábitat de los agentes etiológicos
Cryptococcus neoformans var. grubii es un hongo ubicuo, se aísla con frecuencia de materiales contaminados con excretas de palomas y en menor proporción a partir del suelo, del aire, de los árboles, frutas, vegetales y excretas de otras aves. Las excretas de palomas suministran al hongo sustancias nitrogenadas de bajo peso molecular, como las purinas, xantinas, creatinina, ácido úrico y urea que explica su predilección por este sustrato. C. neoformans var. neoformans es encontrado principalmente en Europa y rara vez causa enfermedad (Spina-Tensini et al., 2017; Kamari, Sepahvand y Mohammadi, 2017), ambas variedades afectan con mayor frecuencia a pacientes inmunocomprometidos.
Cryptococcus gattii, tiene una distribución geográfica y un hábitat más restringido, se aísla usualmente de diferentes especies de árboles nativos de regiones tropicales y subtropicales como eucaliptos (Eucalyptus camaldulensis y E. tereticornis), almendros, abetos otras especies de árboles (Escandón et al. 2010; Vélez y Escandón. 2017, Springer et al., 2014) y en pocas ocasiones, de excretas de aves Abegg et al., (2006), en un estudio realizado con excrementos de Psitaciformes lo encontraron en el 13% de las muestras examinadas, Kangogo et al., (2014) lo hallaron en el 3.8% de heces de Geopelia striata (palomas).
3. Materiales y Métodos
Se recolectaron muestras de excretas de palomas (C. li-via) en el perímetro urbano de Cali, Colombia (3°27'N, 76°32'O) por el método recomendado por Mira et al. 1968. Además, en cada uno de los sitios de muestreo se determinó el tipo de alimento que se les daba a las palomas. Luego las excretas se procesaron de acuerdo con las recomendaciones de Pal y Baxter (1985) y Shields y Ajello (1966), se tomaron 10 g de la muestra que se colocaron en un matraz, se añadió 90 mL de solución salina estéril al 0,85% (dilución 1:10) y se agitó durante 5 minutos. La suspensión se dejó sedimentar durante 10 minutos y se transfirió 1 mL del sobrenadante a un tubo con 9 mL (dilución 1:100). Posteriormente cada dilución se sembró por duplicado en cajas de Petri que contenían agar semilla de girasol (Pal y Baxter 1985). Las cajas se incubaron durante I0 días a 25°C y se examinaron diariamente para visualizar el crecimiento de levaduras de color café, presuntivas de C. neoformans; luego, éstas se subcultivaron en tubos con agar Sabouraud dextrosa y se identificó con API 20C Aux (BioMérieux; Marcy-l'Etoile, Francia). Se confirmó que las cepas correspondían a C. neoformans con el medio de cultivo CGB (Pérez et al., 2003). Se seleccionó una muestra que fuera positiva para C. neoformans y otra negativa y con ellas se prepararon dos extractos: uno a partir de heces positivas para C. neoformans y otro de heces negativas. La muestra de excreta positiva fue de palomas cautivas, alimentadas exclusivamente con maíz, mientras que la negativa se obtuvo de un criadero de palomas mensajeras, éstas recibían alimento concentrado, diferentes granos, cereales y sales minerales.
Para cada uno de los extractos, se suspendieron 100 gramos de la muestra (positiva y negativa) en 900 ml de agua destilada y se centrifugaron a 3.000 r.p.m. durante 3 veces consecutivas. A continuación, el sobrenadante se pasó a través de filtros Millipore de 0,45 Lim. Cada extracto obtenido (solución madre) se dividió en alícuotas de 500 mL y se congelaron a -5°C. En el momento del ensayo se descongelaron las soluciones madre (positiva y negativa); luego se centrifugaron a 3000 r.p.m. durante 30 minutos con el fin de eliminar precipitados que hubiesen podido formarse, después se les añadió penicilina G (40 U/mL) y gentamicina (1,6 Lg/mL), se ajustó el pH a 6,5 y cada una de las soluciones se dividieron en dos. A una se añadió HEPES bicarbonato a una concentración de 10 mM, mientras que la otra no recibió solución amortiguadora. Así, se obtuvieron extractos positivos y negativos con y sin solución amortiguadora. Posteriormente, cada uno de estos extractos, con el fin de esterilizarlos se pasó a través de un filtro Millipore de 0,22 Lm. El control de la esterilidad se llevó a cabo en un caldo tioglicolato y 10 mL de cada extracto se envasaron en frascos estériles de 50 mL y se taparon con algodón, gasa y papel de parafina.
Para la inoculación de los extractos se utilizó C. neoformans aislado de excretas recolectadas en la ciudad de Cali y C. gattiiserotipo C (191C) obtenida del Instituto Nacional de Salud de Colombia, Bogotá DC, Colombia. Los ensayos se llevaron a cabo en cuatro fases como se indica en la Figura 1. En la primera y segunda se inocularon extractos positivos con y sin solución amortiguadora y en la tercera y cuarta fase, se inocularon extractos negativos con y sin solución amortiguadora.
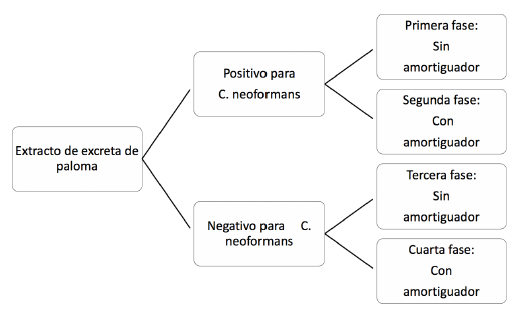
Fuente: Los autores
Figura 1 Diagrama de las fases de ensayo con los diferentes extractos de excretas de palomas.
En cada fase se utilizaron 96 frascos que contenían 10 ml del extracto, 48 de los cuales se inocularon con 1x105 células de C.neoformansy los restantes 48 con 1x105 células de Cgattii. Una vez inoculados, los frascos se incubaron en un agitador a I50 r.p.m., a 30°C durante 31 días. En los días 0, 1, 2, 4, 6, 8, 11, 14, 19, 24 y 31, se elegían al azar cuatro frascos de C. neoformans y 4 de C. gattii, se determinaba el pH de los extractos, las unidades formadoras de colonias (UFC) y la concentración de proteínas, ácido úrico y creatinina.
El pH se midió con un potenciómetro (LEEDS & NORTHRUP) calibrado con amortiguadores a pH 4, 7 y 10. El recuento de UFC/mL se determinó mediante la técnica de dilución en caja, de cada una de las diluciones se depositó por duplicado 0,1 mL en cajas de Petri con agar Sabouraud dextrosa, que se incubaron a temperatura ambiente durante 2-4 días, después se contaron las UFC/mL. Se utilizó la prueba de Biuret para determinar la concentración de proteínas; el método picrato alcalino, sin desproteinización para medir la concentración de creatinina y el método colorimétrico de ácido túngstico para la determinación del ácido úrico.
El análisis estadístico se realizó bajo la norma de distribución de tratamientos de un diseño de bloques completamente al azar (DBA) con arreglo factorial 4x2x11; donde el factor A correspondió a cuatro diferentes extractos de excretas de paloma; el B a los tratamientos con C. neoformans y C. gattii y el C lo constituyeron 11 tiempos de incubación (0, 1, 2, 4, 6, 8, 11, 14, 19, 24 y 31). Cada tratamiento se realizó con cuatro repeticiones. Los datos obtenidos se analizaron en SAS 9.1.3 versión 2007 y fueron sometidos a un análisis de varianza ANOVA y prueba de significancia de Tukey para comparar variaciones estadísticamente significativas (P<0,05).
4. Resultados
Primera fase: extracto positivo sin solución amortiguadora
La Figura 2 muestra los valores de pH y el crecimiento (UFC/mL) de las dos especies; el pH estuvo entre 7,1-8,5, con un promedio de 7,96 y una desviación estándar (DE) de 0,8. El mayor valor de pH se obtuvo el día 2 y no presentaron diferencias estadísticas significativas entre las dos especies.
Fuente: Los autores
Figura 2 Crecimiento de C. neoformans y C. gattii y cambios de pH en el extracto de heces de palomas positivos sin solución amortiguadora.
El desarrollo de las dos especies fue similar en los dos primeros días,el punto máximo de crecimiento de C.gattiifue 55,6x106 UFC/mL, luego disminuyó en forma significativa, el crecimiento promedio de esta especie fue 9,8x106 UFC/mL, mientras que las UFC/mL de C. neoformans permanecieron casi constantes, con un promedio de 49,0xI06 UFC/mL. En este medio de cultivo, el crecimiento de las dos especies presentó diferencias estadísticas significativas (P<0,001).
Segunda fase: extracto positivo con solución amortiguadora
La Figura 3 muestra que los valores de pH variaron entre 7,0-7,6 con un promedio de 7,47 y una DE de 0,05, no hubo diferencias significativas.
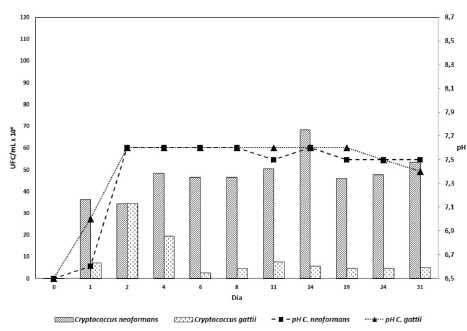
Fuente: Los autores
Figura 3 Crecimiento de C. neoformans y C. gattii y cambios de pH en el extracto de heces de palomas positivos con solución amortiguadora.
El crecimiento de las dos especies fue similar en los dos primeros días, C.gattii alcanzó un recuento de 34,4x106 UFC/ mL que correspondió al punto máximo de crecimiento, se redujo notoriamente el día 3 y siguió disminuyendo hasta llegar a un recuento de 4,9x106 UFC/mL, con un promedio de 9,5x106 UFC/mL, mientras que C. neoformans mantuvo un crecimiento uniforme con un promedio de 47,6x106 UFC/mL. En este medio de cultivo el crecimiento de las dos especies presentó diferencias estadísticas significativas (P<0,001).
Tercera fase: extracto negativo sin solución amortiguadora
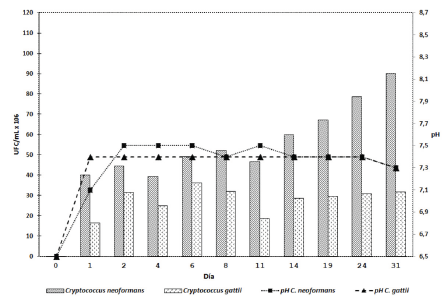
La Figura 4 muestra que el pH de este extracto se mantuvo estable con las dos especies y no presentó diferencias significativas. Los valores de pH estuvieron entre 7,1-7,5, con un promedio de 7,4 y una DE de 0,13.
Cryptococcus gattii alcanzó un crecimiento promedio de 28,0x106 UFC/mL y C. neoformans de 56,8x106 UFC/mL. No se presentaron diferencias significativas P = (0,056)
Cuarta fase: extracto negativo amortiguadora con solución
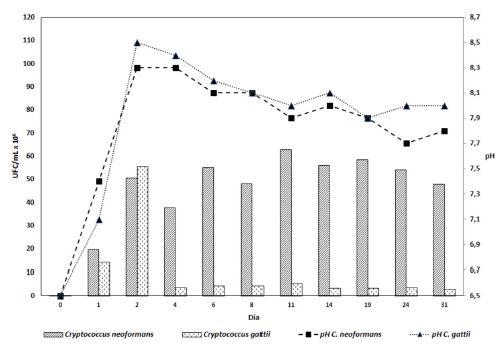
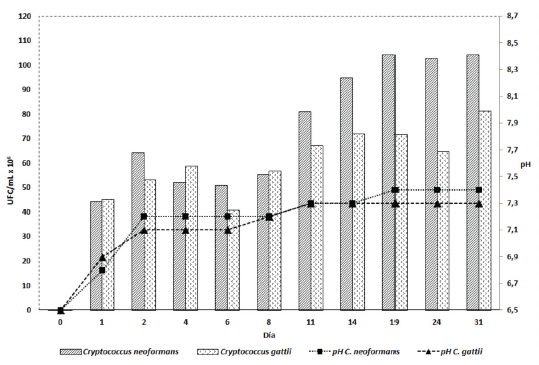
La Figura 5 muestra que el máximo valor de pH alcanzado se registró el día 19, con un rango a lo largo del proceso entre 6,8-7,2 y una DE de 0.08. No se presentaron diferencias significativas. Cryptococcus gattii, alcanzó un crecimiento promedio de 61,0x106 y C. neoformans de 75,3x106 UFC/ mL, sin presentar diferencias significativas P = (0,14).
Fuente: Los autores
Figura 5 Crecimiento de C. neoformans y C. gattii y cambios de pH en el extracto de heces de palomas negativos con solución amortiguadora.
Los frascos que contenían los extractos negativos con y sin solución amortiguadora presentaron un precipitado muy notorio que al observarse al microscopio correspondió a cristales de trifosfato de amonio.
Con relación a los datos de creatinina, ácido úrico y proteínas se observó que el comportamiento de los tres compuestos fue similar en los dos extractos; en la Tabla I se presentan para el día inicial y final de los diferentes ensayos, los resultados de estos tres compuestos relacionados con e pH y el crecimiento (UFC/mL) de las dos especies de Cryptococcus. Con estos datos no se logró establecer diferencias significativas entre las concentraciones de estos compuestos, el pH y el crecimiento de estas dos especies en excretas de palomas.
5. Discusión
El hábitat más importante y frecuente de C. neoformans son las excretas de palomas en especial las de C. livia, (Huamán, et al., 2018; Menezes et al., 2014; Canónico-González; et al.; Aréchiga-Carvajal, 2013), llama la atención que C. gattii solo en pocas ocasiones se ha aislado de forma natural en heces de otras especies de aves (Dongmo et al., 2016; Kangogo et al., 2014 y Abegg et al.,2006). En el presente estudio, los extractos de heces de paloma permitieron el desarrollo de las dos especies de Cryptococcus; no obstante, el crecimiento de C.gattiifue menor y su comportamiento fue diferente en los extractos positivos y negativos. En los extractos positivos las dos especies crecieron gradualmente y alcanzaron su máximo desarrollo entre los días 2 y 4, lo que coincidió con el aumento del pH. Luego, el crecimiento de C. neoformans se mantuvo constante a lo largo del estudio, mientras que el de C. gattii fue significativamente menor. Este patrón de crecimiento no se produjo en los extractos negativos, donde ambas especies crecieron bien y tuvieron recuentos de UFC /mL más altos. Una posible explicación podría ser el contenido nutricional de las excretas; Iyappan, Karthikeyan y Sekar, (2011) describieron que la composición de las excretas de aves cambia según la dieta y es importante destacar que los extractos positivos provenían de palomas alimentadas solo con maíz, mientras que las palomas de donde se obtuvieron los extractos negativos eran alimentadas con una variedad de granos. Nielsen, De Obaldia y Heitman, (2007) encontraron que C. neoformans crece mejor en el guano de paloma que en un medio de cultivo a base de levadura, lo que corrobora que la composición nutricional puede proporcionar un entorno favorable para el crecimiento de estos hongos.
En este estudio, se observó que un pH superior a 7,5 afectaba el crecimiento de C. gattii pero no el de C. neoformans. El estiércol de paloma es rico en compuestos nitrogenados como la creatinina; en ambas especies, la creatinina induce la síntesis de la enzima creatinina desaminasa, pero los mecanismos de regulación son diferentes (Polacheck y Kwong-Chung 1980). La creatinina desaminasa de C. neo-formans exhibe un mecanismo de regulación por producto, en este caso el ion amonio, que al alcanzar un cierto nivel, inhibe la síntesis de la enzima y detiene el catabolismo de la creatinina, mientras que la creatinina desaminasa de C. gattii no tiene mecanismos de regulación por producto, su síntesis en presencia de creatinina es constante, lo que permite una acumulación del ion amonio y un aumento de los valores de pH y se conoce que los iones de amonio pueden ser tóxicos para las células (Franco, Smith y Berry, 1984; Vidotto, Benech, Maina, Bruatto 1993; Lloyd, Kristensen y Degn, 1983). En los extractos de excretas negativos, la mayor cantidad de nutrientes (azúcares) puede haber influido en los valores de pH más bajos. Los estudios realizados por Polacheck y Kwong-Chung (1980), muestran que la producción de iones de amonio se inhibe en presencia de ciertos azúcares y que éstos pueden reaccionar con los fosfatos, produciendo pH neutros. En este estudio los valores de pH de las excretas negativas se mantuvieron muy homogéneos posiblemente por la formación de cristales de trifosfato de amonio que actuaron como un tampón natural y mantuvieron el pH entre 7,2 y 7,4.
Los valores anteriores contrastaron con lo que sucedió con los extractos positivos, donde posiblemente la concentración de azúcares y fosfatos fue baja y se encontraron los pH más altos, Burton (1980) describe que la dieta puede influir en el pH de la orina del animal y también en el contenido de nitrato en las excretas de las palomas (Sales y Janssens 2003a, 2003b). El menor crecimiento de C. gattiien excretas de palomas, podría indicar al igual que lo planteado por Nielsen, De Obaldia y Heitman (2007), que este sustrato es su nicho fundamental, mientras que para C. neoformans que creció muy bien, indicaría que este organismo está mejor adaptado y que es su nicho realizado.
Tabla 1 Relación de los compuestos nitrogenados con el crecimiento (UFC/mL) y pH encontrados en los extractos de excretas de paloma el día inicial y final de los ensayos.
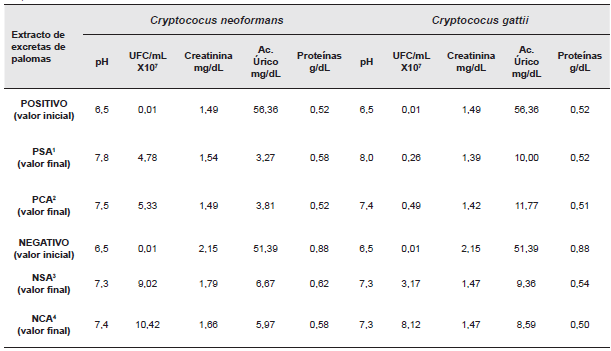
1 PSA: Extracto positivo sin amortiguador 2PCA: Extracto positivo con amortiguador 3NSA: Extracto negativo sin amortiguador 4NCA: Extracto negativo con amortiguador.
Fuente: Los autores
Aunque el extracto positivo permitió el crecimiento de C gattii, lo hizo de una manera muy restringida, mientras que en el extracto negativo el crecimiento de las dos cepas no mostró diferencias significativas. Este comportamiento similar en los extractos negativos podría explicarse por los valores de pH menores a 7,5 encontrados en este sustrato.
Los resultados del presente estudio muestran diferencias en el crecimiento de las dos especies en excretas de palomas, pero se necesitan estudios posteriores con ambas especies en estos extractos para poder analizar las interacciones entre ellas, así como determinar la influencia del pH en la presencia de diferentes concentraciones de compuestos nitrogenados y azúcares. Además, se debe establecer el efecto del ion amonio, dada su importancia en la regulación de los diferentes compuestos nitrogenados (Lee, Chow, Morrow, Djordjevic y Fraser, 2011; Baumgardner, 2009). También, se deben buscar posibles metabolitos liberados por C. neoformans que pueden ayudar a limitar el crecimiento de C. gattii.
6. Conclusiones
Cryptococcus gattiicrece en extractos de excretas de palomas (Columba livia), sin embargo, su crecimiento (UFC/ mL) se ve notoriamente disminuido cuando se compara con el desarrollo de C. neoformans, en los diferentes extractos empleados.
Los pH mayores de 7.5 y los extractos de excretas positivas para C. neoformans limitan el crecimiento de manera significativa el crecimiento de C gattii, pero no en los extractos de excretas negativos.
El presente estudio aporta nueva información sobre el desarrollo de C. neoformans y C. gattii, sin embargo es necesario realizar más investigaciones para aclarar las interacciones de estas especies en los extractos de excretas de palomas (Columba livia).