Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
CES Medicina Veterinaria y Zootecnia
versão On-line ISSN 1900-9607
Ces. Med. Vet. Zootec. vol.11 no.1 Medellín jan./jun. 2016
Artículos originales de investigación
Detection of Ptaquilosides in different phenologic stages of Bracken fern (Pteridium aquilinum) and analysis of mik samples in farms with hematuria in Tolima, Colombia¤
Detección de ptaquilósido en diferentes estados fenológicos de "helecho macho" (Pteridium aquilinum) y análisis de muestras de leche en granjas con hematuria en Tolima, Colombia
Detecção da ptaquilosida em diferentes estágios fenológicos da samambaia (Pteridiumaquilinum) e análise de amostras de leite em fazendas com hematúria em Tolima, Colômbia
Diego F. Rincón1*, MV; Gonzalo J.Díaz1, MV, MSc, PhD; Dale R. Gardner2, PhD.
¤Para citar este artículo: Rincón DF, Díaz GJ, Gardner DR. Detección de ptaquilósido en diferentes estados fenológicos de "helecho macho" (Pteridium aquilinum) y análisis de muestras de leche en granjas con hematuria en Tolima, Colombia. Rev. CES Med. Zootec. 2016; Vol 11 (1): 72-77..
*Autor para correspondencia: Gonzalo J. Díaz. gjdiazg@unal.edu.co
1 Laboratorio de Toxicología, Facultad de Medicina Veterinaria y de Zootecnia, Universidad Nacional de Colombia, Ciudad Universitaria, Bogotá, D.C., Colombia.
2 Poisonous Plant Research Laboratory, USDA, ARS, Logan, Utah, USA
(Recibido: 4 de mayo, 2015; aceptado: 15 de abril, 2016)
Abstract
Bracken fern or "Helecho Macho" (Pteridium aquilinum) is one of the most common weeds in the meadows of the mountain ranges of Colombia. Consumption of this palatable plant by bovines causes a disease known as bovine enzootic hematuria and esophageal neoplasia. The toxic effect of the plant in bovines is caused by the ptaquiloside, main carcinogenic toxin of this plant. In this study, eight samples of Bracken fern in different phenologic stages and 16 milk samples collected in two towns of Tolima, Líbano and Murillo, were analized. In both cases, Highperformance liquid cromatography (HPLC) coupled with Mass Spectrometry (MS) was used. In all Bracken fern samples analized, detectable levels of ptaquilosides were observed, ranging from 23 to 1194 µg/g, with a 342 µg/g mean. No detectable levels of ptaquilosides were found in the milk samples. The results show a great variation in the content of ptaquilosides depending on the phenologic stage and collection site of the plant. It is posible that the reported instability of the ptaquiloside and the processing given to the milk samples could have caused the lack of detection of the compound in milk
Key words:Helecho macho, milk, Pteridium aquilinum, ptaquiloside.
Resumen
El "helecho macho" (Pteridium aquilinum) es una de las malezas más comunes en praderas de la región de cordillera en Colombia. El consumo de esta planta palatable por parte de los bovinos causa una enfermedad conocida como hematuria enzoótica bovina y neoplasias de esófago. El efecto tóxico de la planta en los bovinos es causado por el ptaquilósido, principal toxina carcinogénica de esta planta. En el presente estudio se analizaron ocho muestras en diferentes estados fenológicos del helecho obtenidas en dos municipios del departamento del Tolima (Líbano y Murillo) y 16 muestras de leche de la misma zona. En ambos casos se utilizó como técnica analítica cromatografía líquida de alta eficiencia (HPLC) acoplada a espectrometría de masas (MS). En todas las muestras analizadas se observaron niveles detectables de ptaquilósido, con un rango de 23 a 1.194 µg/g y un promedio de 342 µg/g. No se encontraron niveles detectables de ptaquilósido en ninguna de las muestras de leche. Los resultados del estudio muestran la gran variación en el contenido de ptaquilósido dependiendo del estado fenológico de la planta y del sitio de colecta. Es posible que la reportada inestabilidad del ptaquilósido y el tipo de procesamiento dado a las muestras de leche haya ocasionado la no detección del compuesto en las mismas.
Palabras clave: Helecho macho, Pteridium aquilinum, ptaquilósido, leche.
Resumo
A samambaia (Pteridium aquilinum) é uma das ervas daninhas mais comuns nas pastagens na região de cordilheira na Colômbia. O consumo desta planta palatável para os bovinos, causa uma doença conhecida como hematúria enzoótica bovina e neoplasias de esôfago. O efeito tóxico da planta nos bovinos é causado pelo ptaquilosídeo, principal toxina carcinogênica desta planta. No presente estudo foram analisadas oito amostras em diferentes estágios fenológicos da samambaia e 16 amostras de leite obtidas em dois municípios do departamento de Tolima (Líbano e Murillo). Em ambos os casos foi utilizada como técnica analítica a cromatografia líquida de alta eficiência (HPLC) acoplada a espectrometria de massas (MS). Em todas as amostras analisadas foram observados níveis detectáveis de ptaquilosídeo, com um rango de 23 a 1.194 µg/g e uma média de 342 µg/g. Não foram encontrados níveis detectáveis de ptaquilosídeo em nenhuma das amostras de leite. Os resultados do estudo mostram a grande variação no conteúdo de ptaquilosídeo dependendo do estágio fenológico da planta e do local da coleta. É possível que a reportada instabilidade do ptaquilosídeo e o tipo de processamento dado às amostras de leite seja a causa da falta de detecção do composto nas amostras de leite analisadas.
Palabras-clave:Leite, ptaquilosida, Pteridium aquilinum, Samambaia.
Introducción
El "helecho macho" (Pteridium aquilinum) es una de las malezas más comunes en la región de cordillera en Colombia. El ptaquilósido es la principal toxina carcinogénica presente en Pteridium aquilinum. Químicamente este corresponde a un glucósido norsesquiterpenoide, inestable en condiciones tanto ácidas como alcalinas a temperatura ambiente, que sufre aromatización y deglucosilación formando pterosin B5,una dienona conjugada inestable, la cual ha demostrado ser un fuerte agente de alquilación del ADN5,14. A pH menor a 4 la vida media en solución acuosa es de horas a días y a pH mayor a 7 la vida media es de segundos a horas5. El ptaquilósido, se considera el responsable del cuadro clínico manifiesto en algunas especies domésticas, entre estas principalmente la hematuria vesical enzoótica bovina y la formación de carcinomas de células escamosas de faringe o de tracto digestivo alto en bovinos6. En equinos el consumo de helecho macho puede ocasionar una defiencia de tiamina debido a la presencia en la planta de una tiaminasa tipo 18. Animales de laboratorio pueden también desarrollar carcinomas. Pamucku et ál. (1978)12 alimentaron ratones con leche proveniente de vacas obligadas a consumir Pteridium aquilinum y observaron una mayor incidencia de neoplasias en los ratones expuestos comparados con los controles.
Varios estudios realizados en leche de vaca han reportado ptaquilósido mediante cromatografía liquida de alta eficiencia (HPLC) o cromatografía de gases/ espectrometría de masas (GS-MS)2,6. Recientemente en Ecuador se reportó la presencia de ptaquilósido en leche comercial, utilizando el método descrito por Alonso-Amelot et al. (1998) 2 mediante HPLC 7. La determinación de ptaquilósido ha generado interés en salud pública, debido a que estudios epidemiológicos han relacionado el aumento en la incidencia de cáncer de esófago y gástrico en humanos, con el consumo de leche proveniente de vacas que pastorean en zonas con presencia del Pteridium aquilinum 4,9.
En Colombia no se conoce si la leche producida en las zonas de helecho contiene ptaquilósido, no obstante, se conoce principalmente el cuadro clínico de la hematuria en distintas regiones, entre las cuales se destacan las regiones de la cordillera8,13. Previamente, la Agencia Internacional para la Investigación en Cáncer (IARC) en su sexto documento divulgativo de prioridades para futuras evaluaciones ubicó al ptaquilósido en el grupo 2B como "posiblemente carcinogénico", pero lo ubica junto al Pteridium aquilinum en prioridad alta en investigación 6,10
Los objetivos del presente estudio de carácter preliminar fueron determinar y cuantificar el ptaquilósido en distintos estados fenológicos de helecho macho recolectado en dos zonas del Tolima y determinar la posible presencia de la toxina en muestras de leche proveniente de zonas con alto grado de infestación de las praderas.
Materiales y métodos
Se realizó un estudio analítico a muestras tomadas en dos municipios del norte del departamento del Tolima, Colombia: el municipio de Líbano ubicado a 1.565 metros sobre el nivel del mar (msnm) y el de Murillo a 2.950 msnm. En estos dos municipios la planta es abundante en los potreros de pastoreo y se encuentran fincas con animales clínicamente afectados por hematuria en donde se observa que los animales consumen voluntariamente el helecho joven (Figura 1). Se recolectaron muestras de helecho clasificadas en cuatro distintos estados fenológicos y muestras de leche como se describe a continuación.
Método colecta de las plantas
Las muestras se colectaron en cada uno de los cuatro estados fenológicos del helecho (I, II, III y IV, Figura 2) provenientes de los dos municipios muestreados (n = 8) de acuerdo con lo reportado por Alonso-Amelot (1999)3. Las muestras se obtuvieron de dos granjas distintas de cada municipio, se agruparon de acuerdo a su estado fenológico y se mantuvieron refrigeradas a 4 °C hasta su secado a 45 °C durante 5 días. Posteriormente se trituraron en trozos menores a 2 mm para su posterior envío al laboratorio analítico.

Muestras de leche
Se tomaron 16 muestras de leche de 200 ml, de las cuales siete correspondían a centros de acopio. En el primero de estos, ubicado en Líbano, reciben leche de granjas comprendidas entre los 1.200 y 1.800 msnm. El segundo centro de acopio, ubicado en Murillo, recibe leche de granjas ubicadas entre 2.000 y 3.100 msnm.
Las otras nueve muestras de leche se tomaron directamente en granjas ubicadas en Líbano y Murillo en donde se encontraron animales afectados con hematuria y donde es alta la infestación de los potreros con Pteridium aquilinum. Las muestras se colectaron en frascos protegidos de la luz y se mantuvieron a 4 °C hasta su llegada al laboratorio en Bogotá (24 a 48 horas). Posteriormente las muestras fueron liofilizadas antes de su envío al laboratorio analítico. Para la liofilización cada muestra se llevó a congelación a -80 °C durante 12 horas luego de lo cual se introdujo en el liofilizador durante 24 horas. Se utilizó un liofilizador marca "CHRIST" modelo ALPHA 1-4 Plus (Osterode am Harz, Alemania).
Análisis de las muestras
Los análisis fueron realizados en el Laboratorio de Investigación de Plantas Tóxicas (Poisonous Plants Research Laboratory) del Departamento de Agricultura de los Estados Unidos en Logan, Utah.
Análisis del material vegetal. El material vegetal seco y molido (100 mg) fue extraído con 4,0 ml de agua destilada y 4,0 ml de diclorometano mediante agitación mecánica en un tubo de ensayo de 10 ml durante 2 horas. Las muestras fueron luego centrifugadas para ayudar a separar las capas de solventes y 1,0 ml de la solución acuosa superior fue transferido a un vial de automuestreador de 1.5 ml para su posterior análisis por cromatografía líquida de alta eficiencia acoplada a espectrometría de masas con fuente de ionización electrospray positiva [HPLC-esi(+)MS]. Los estándares de calibración se prepararon a partir de una solución madre de ptaquilósido puro (1.0 mg/ml) por diluciones seriadas para obtener concentraciones de 10, 5, 2,5, 1,25 y 0,625 µg/ml. Los estándares de calibración y los extractos de las plantas fueron luego analizados utilizando un espectrómetro de masas LCQ Advantage acoplado a una bomba Surveyor MS y un automuestreador (Thermo Scientific, USA) equipado con una fuente de ionización de electrospray (esi) en modo positivo y una columna Betasil C18 (100 x 2.1 mm). Las muestras (10 µl) se inyectaron y eluyeron a un flujo de 0.3 ml/min con gradiente de metanol (A) y acetato de amonio 20 mM (B) de la siguiente manera: 5% A (0-3 minutos); 5%-40% A (3-4 minutos); 40%-90% A (4-15 minutos); 90%-5% (15-16 minutos); y 5%A (16-21 minutos). El flujo de la columna se conectó a la fuente de ionización del espectrómetro de masas y se escaneó en el rango de masas de 100 a 800 uma. Para las mediciones cuantitativas se reconstruyeron los cromatogramas de ion m/z 421 del ptaquilósido.
Análisis de la leche
Las muestras liofilizadas de leche se extrajeron de manera similar al procedimiento recientemente descrito por Aranha et al. (2014)5. Una alícuota de 3 g de leche se reconstituyó con 30 ml de agua destilada y se agitó por rotación mecánica durante 2 horas. Las muestras fueron luego centrifugadas por 10 minutos para separar la capa de grasa. Una alícuota de 3 ml de la leche reconstituida y desengrasada se centrifugó luego a 13000 g por 15 minutos y luego 2 ml del sobrenadante se adicionaron a una columna de extracción en fase solida (SPE, Strata X 60 mg, Phenomenex, USA) previamente acondicionada con 2 ml de metanol y 2 ml de agua. La columna SPE fue luego lavada con 3 ml de agua y 3 ml de metanol al 20% en agua para finalmente eluir el ptaquilósido con 3 ml de metanol al 80% que fueron llevados a sequedad bajo vacio. La muestra seca se reconstituyó con 0.2 ml de metanol al 50% y se analizó por HPLC-esi(+)MS utilizando un espectrómetro de masas Velos Pro LTQ (Thermo Scientific, USA) acoplado a un cromatografo Agilent 1200 (Agilent Technologies, USA) con una columna Betasil C18 (100 x 2.1 mm). Las condiciones cromatográficas fueron iguales a las utilizadas para las muestras de material vegetal. Como control positivo, muestras blanco de leche liofilizada fueron adicionadas de ptaquilósido y sometidas al procedimiento analítico mostrando una recuperación del analito del 70%.
Resultados
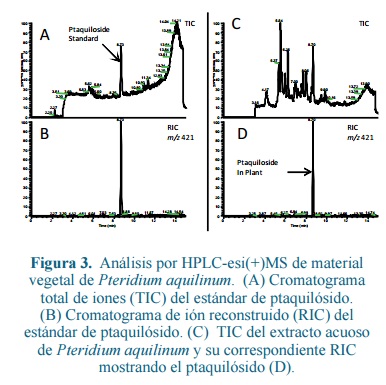
Todas las muestras de plantas mostraron niveles detectables de ptaquilósido. Los niveles de ptaquilósido en los diferentes estados fenológicos de las plantas recolectadas en los municipios de Líbano y Murillo se muestran en la tabla 1. La figura 3 muestra los cromatogramas correspondientes a un estándar de ptaquilósido y a una de las muestras de plantas. No se encontraron niveles detectables de ptaquilósido en ninguna de las muestras de leche analizadas.
Discusión
En general, los estados fenológicos iniciales o frondes (I y II) fueron los que presentaron mayores niveles de

ptaquilósido, resultados que concuerdan con estudios previos, en donde se reporta una correlación negativa en los niveles de ptaquilósido versus su estado de crecimiento1. Sin embargo, los niveles de ptaquilósido en los helechos colectados en Líbano, fueron mucho mayores que los encontrados en Murillo. Los valores de ptaquilósido en los helechos provenientes de Líbano fueron similares a los de Alonso Amelot et al. (1992) quienes encontraron que el ptaquilósido en la etapa de "báculo" tenía niveles de 1670 µg/g y se redujo a 113 µg/g en el fronde maduro, en muestras colectadas a 1850 msnm en Mérida, Venezuela 1.
Los niveles de ptaquilósido de las muestras de Murillo son más bajos con respecto a estudios previos. Estos resultados podrían estar asociados a condiciones específicas medio-ambientales, incluyendo la altura sobre el nivel de mar y condiciones nutricionales del suelo. Zaccone et al. (2014) encontraron un rango de 2 a 780 µg/g de ptaquilósido en siete muestras de Pteridium aquilinum y demostraron el efecto de los distintos tipos de suelo sobre la cantidad de ptaquilósido en los frondes16. Otro factor a considerar es la humedad del ambiente.
En un estudio realizado por Rasmussen et al. (2008) en Nueva Zelanda con otra especie de helecho (Pteridium esculetum), se encontró ptaquilósido en el 63% de 275 muestras con concentraciones que variaban de 280 a 13300 µg/g (promedio de 3800 µg/g), demostrando como la cantidad de ptaquilósido puede variar según la localización geográfica14. Es probable que las diferentes concentraciones y distribuciones del ptaquilósido en los genotipos de helecho pueda ser la razón de la localización geográfica de la hematuria enzoótica crónica15. Esto podría explicar el por qué en algunas zonas del país es baja la incidencia de hematuria enzoótica en bovinos, a pesar de la presencia de Pteridium aquilinum en los potreros. Adicionalmente, debe investigarse si hay diferencias importantes en el consumo de la planta, independientemente de su contenido de ptaquilósido.
Existen pocos estudios en los que se haya reportado presencia de ptaquilósido en leche en condiciones no experimentales. Bonadies et ál.6 encontraron únicamente en una muestra de cuatro presencia de ptaquilósido. En el presente estudio a pesar de haber encontrado ptaquilósido en el helecho consumido por las vacas muestreadas en fincas, no se encontraron niveles detectables de la toxina en la leche. Es posible que la no detección de la toxina en la leche se haya debido al carácter altamente inestable del ptaquilósido5,14 y al hecho de haber tenido que liofilizar y reconstituir las muestras días más tarde. Adicionalmente, la manipulación tradicional de la leche, las variaciones en el pH asociadas a contaminación bacteriana, el procesamiento industrial de la leche, el almacenamiento, la adición de aditivos químicos y probióticos, son algunas de las variables que posiblemente podrían afectar el ptaquilósido y ocasionar su degradación. En estas circunstancias, el mayor riesgo de exposición a ptaquilósido lo presentan aquellas personas que consumen leche fresca sin procesar o cruda en granjas o pequeños pueblos4.
Conclusiones
El presente estudio, de carácter preliminar, reporta por primera vez en Colombia niveles detectables y cuantificables de ptaquilósido en muestras de Pteridium aquilinum recolectadas en zonas en donde se presenta hematuria en bovinos. Los estados fenológicos más tempranos tendieron a presentar los mayores niveles de la toxina. Aunque no se detectó ptaquilósido en las muestras de leche analizadas, existe la posibilidad de que leches frescas, no procesadas, puedan contener la toxina y representar riesgo para la salud pública. Es indispensable realizar mayores estudios sobre contaminación con ptaquilósido en leche y en lo posible realizar los análisis en laboratorios locales con el fin de evitar la manipulación excesiva de las muestras y posible pérdida de la toxina.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Referencias
1. Alonso-Amelot ME, Perez-Mena M, Calcagno MP, Jaimes-Espinoza R. Castillo U. Ontogenic variation of biologically active metabolites of Pteridium aquilinum (L. KUHN), pterosins A and B, and ptaquiloside in a bracken population of the tropical Andes. J Chem Ecol 1992; 18: 1405-1420. [ Links ]
2. Alonso-Amelot ME, Castillo U, Smith BL, Lauren DR. Excretion, through milk, of ptaquiloside in bracken-fed cows. A quantitative assessment. Lait 1998; 78: 413-423. [ Links ]
3. Alonso-Amelot ME. Helecho macho, salud animal y salud humana. Rev Fac Agron (LUZ) 1999; 16: 528- 541. [ Links ]
4. Alonso-Amelot ME, Avendaño M. Possible association between gastric cancer and bracken fern in Venezuela: An epidemiologic study. Int J Cancer 2001; 91: 252-259. [ Links ]
5. Aranha PCR, Hansen HCB, Rasmussen LH, Stroble BW, Friis C. Determination of ptaquiloside and pterosin B derived from braken (Pteridium aquilinum) in cattle plasma, urine and milk. J Chromatogr B 2014; 951-952: 44-51. [ Links ]
6. Bonadies F, Berardi G, Nicoletti R, Romolo FS, De Giovanni F, et al. A new very sensitive method of assessment of ptaquiloside, the major bracken carcinogen in the milk of farm animals. Food Chem 2011; 124: 660-665. [ Links ]
7. Calderón A, Mancebo B, Sánchez LM, Chiriboga X, Lucero D, et al. Niveles de ptaquilósido en muestras de leche bovina en grajas de San Miguel de Bolívar, Provincia de Bolívar, Ecuador. Revista de Salud Animal 2013; 35: 109-115. [ Links ]
8. Díaz GJ. Plantas tóxicas de importancia en salud y producción animal en Colombia. 2010. Editorial Universidad Nacional de Colombia. [ Links ]
9. Gil Da Costa RM, Bastos MSM, Oliveira PA, Lopes C. Bracken-associated human and animal health hazards: chemical, biological and pathological evidence. J Hazard Mater 2012; 203-204: 1-12. [ Links ]
10. IARC. Statement in support of the IARC Monographs Program by members of the Sixth Advisory Group. 2003; (07 Septiembre de 2014) Accedido en: http://monographs.iarc.fr/ENG/Publications/internrep/03-001.pdf. [ Links ]
11. Øllgaard B, Tind K. Scandinavian Ferns. A natural history of the ferns, clubmosses, quillworts, and horsetails of Denmark, Norway and Sweden. Copenhagen: Rhodos, 1993. [ Links ]
12. Pamukcu AM, Ertürk E, Yalçiner S. Carcinogenic and mutagenic activities of milk from cows fed bracken fern (Pteridium aquilinum). Cancer Res 1978; 38: 1556-1560. [ Links ]
13. Pedraza C, Villafañe F, Torrenegra RD. Hematuria vesical bovina y su relación con algunas especies vegetales. Rev ACOVEZ 1983; 7: 11-19. [ Links ]
14. Rasmussen LH, Lauren DR, Smith BL, Hansen HCB. Variation in ptaquiloside content in bracken (Pteridium esculetum (Forst f.) cockayne) in New Zealand. New Zeal Vet J 2008; 56: 304-309. [ Links ]
15. Roperto S, Borzacchiello G, Brun R, Leonardi L, Maiolino P, et al. A review of bovine urothelial tumours and tumour-like lesions of the urinary bladder. J Comp Pathol 2010; 142: 95-108. [ Links ]
16. Zaccone C, Cavoski I, Costi R, Sarais G, Carboni P, et al. Ptaquiloside in Pteridium aquilinum subsp. aquilinum and corresponding soils from the south of Italy: Influence of physical and chemical features of soils on its occurrence. Sci Total Environ 2014; 496: 365-372. [ Links ]














