Introducción
Actualmente el consumo percapita de carne de cuy en la región andina a incrementado paulatinamente, considerando su alto valor nutricional, al contener un 20,3% de proteína y un 10% de grasa (Gil, 2007) ácidos grasos poliinsaturados de la familia omega 3 y 6, que ayudan a destruir los ateromas en personas con enfermedades cardiovasculares y problemas de obesidad (Fernández, Martin, & Apraez, 2016), y una enzima llamada asparginasa que interrumpe el crecimiento de tumores cancerígenos (Villanueva, 2018); sin embargo en el Ecuador los niveles de producción, según el INIAP con una población de 21 millones de cuyes y una producción de 14.300 toneladas de carne, no se cubre la demanda local (Cuzco, 2012), debido a que en el país no existen sistemas de producción tecnificados que permitan obtener rendimientos productivos aceptables (Castro, Narvaez , & Ortega, 2016); no obstante en la actualidad se han desarrollado varias estrategias enfocadas a mejorar las funciones del tracto gastrointestinal (TGI) en animales de producción comercial utilizando aditivos zootécnicos como: antibióticos promotores de crecimiento (APC), prebióticos, pro-bióticos, entre otros.
Está demostrado que la inclusión de APC en la dieta alimenticia de los animales otorga beneficios sobre la ganancia de peso y conversión alimenticia (Nakandakari & Vílchez, 2016); sin embargo su amplia utilización genera resistencia bacteriana a Enterococus faecium, E. coli, Campylobacter, Salmonella, entre otras bacterias patógenas (Cepero, 2006), incrementando patologías que alteran la salud y bienestar animal (Carro & Ranilla, 2002), y efectos negativos para el consumidor, por lo tanto la Unión Europea prohibió el uso de los mismos (Montoya, Vélez, & Gutiérrez, 2013), (Torres & Zarazaga, 2002).
Ante esta situación el empleo de probióticos y prebióticos ha surgido como una alternativa al reemplazo de antibióticos promotores de crecimiento, entre ellos Saccharomyces cerevisiae Sc7, la cual ha sido registrada en Japón, Estados Unidos, la Unión Europea y otros países, como un microorganismo seguro para la alimentación animal (López, Afanador, & Ariza, 2009), otorgándole la FDA (Food y Drug Administration) el grado GRAS (Seminario & Cuenca, 2018) (Medina, González, Daza, Restrepo, & Barahona, 2014); por esta razón la levadura ha sido ampliamente estudiada, comercializada y utilizada como aditivo en alimentación animal (Zhang, y otros, 2005), (Aghdamshahriar, Nazer, & Ahmadzadeh, 2006), demostrando resultados positivos sobre los parámetros productivos en monogástricos y rumiantes, por su alto contenido en proteínas (40-45%), vitaminas del complejo B como: biotina, niacina, ácido fólico, pantoténico, y tiamina (Linares, Peralta, Miazzo, & Nilson, 2009), fibra dietética, algunos minerales como el selenio (Medina, González, Daza, Restrepo, & Barahona, 2014), polisacáridos (80 a 85%), glucosa y manosa que actúan como inmuno estimuladores y colonizadores de la mucosa intestinal (Arce, Ávila, López, García, & García, 2005) y otros importantes cofactores que la hacen atractiva para su aplicación en la alimentación animal (Castro & Rodríguez, 2005), puesto que ha demostrado beneficios sobre la performance de varias especies incrementando la rentabilidad de los sistemas productivos.
Así (Chicaiza, 2015) evaluó la adición de S. cerevisiae al 3% en la alimentación de cobayos durante la fase de crecimiento y engorde logrando obtener resultados positivos sobre los parámetros productivos de los animales; por otra parte, (Narváez, 2014) investigó la adición de S. cerevisiae en la ración alimenticia de cobayos durante las etapas de gestación y recría, observando efecto positivo de la levadura sobre el incremento de peso y longitud en gazapos; por último, dentro de los beneficios que aportan las levaduras se puede mencionar que actúan como probióticos o prebióticos, producen minerales, mejoran la eficiencia alimenticia, absorción de nutrientes, promueven el crecimiento, estimulan la inmunidad intestinal, entre otros (Castro & Rodríguez, 2005) Por lo tanto, el objetivo del presente estudio se centró, a evaluar el efecto de la adición de levadura de cerveza Saccharomyces cerevisiae sobre parámetros productivos y calidad intestinal en cobayos.
Materiales y métodos
Localización y población de estudio
El estudio se llevó a cabo en la provincia del Azuay, cantón Oña, parroquia Susudel, ubicada a 2353 msnm, con una temperatura promedio anual de 18-22°C y una humedad atmosférica del 50-80%, siendo sus coordenadas UTM: 702986 Este, 9623729 Norte. Se emplearon 120 cuyes criollos mejorados con la línea Perú, machos de 21 días de edad, con un peso promedio de 280 gr, distribuidos al azar en tres tratamientos y cuatro repeticiones utilizando 10 unidades experimentales por cada repetición. Los tratamientos aplicados fueron: T1 alfalfa + concentrado (2 kg de S. cerevisiae/ Tn de balanceado); T2 alfalfa + concentrado (4 kg de S. cerevisiae/ Tn de alimento) y T0 alfalfa + concentrado (testigo). La dieta experimental fue a base de alfalfa y concentrado comercial, suministrada de acuerdo a los requerimientos nutricionales de cada etapa fisiológica, determinando un consumo del 10% de materia seca en base al peso vivo; el agua se ofreció a voluntad. La adición de S. cerevisiae fue dosificada para cada tratamiento en horas de la mañana. Los animales fueron manejados en pozas de 1,5 x m2, proporcionando similar manejo zootécnico de acuerdo a los parámetros de crianza establecidos.
Toma de muestras
Los datos de consumo de alimento, incremento peso, cálculo de conversión alimenticia y porcentaje de mortalidad se registraron semanalmente, mientras que para morfometría intestinal se sacarificaron cuatro animales por tratamiento a los 21, 65 y 95 días. Se ejecutó cortes histológicos del tracto digestivo de los cobayos (duodeno, yeyuno e íleon) a nivel de la parte medial de cada segmento, para realizar estudios de los siguientes indicadores: número de vellosidades intestinales/mm, altura y ancho de vellosidades intestinales (µm), número de criptas de Lieberkühn/mm, profundidad y ancho de criptas de Lieberkühn (µm), longitud del eje cripta-vellosidad (µm), y grosor de la pared intestinal (µm). Las muestras se fijaron en solución de formol al 10% y enviadas al laboratorio debidamente identificadas para su respectivo análisis; la técnica utilizada para medir el número de vellosidades intestinales y criptas fue la descrita por (Viguera, Rojas, Hernández, Reyes, & Alvarez, 1999); quienes plantean que se debe seleccionar mínimo 5 puntos al azar por corte y medir 1 mm de longitud en relación a la base de las vellosidades y proceder a contabilizar; mientras que para obtener la medida del eje de cripta-vellosidad, altura y ancho de vellosidad, profundidad y ancho de criptas se utilizó la técnica descrita por (Ríos, y otros, 2002), mismos que indican que se debe escoger aleatoriamente 10 ejes cripta-vellosidad por corte; por último, la medición de longitud del eje cripta- vellosidad se obtuvo midiendo la distancia entre el ápice de la vellosidad hasta la base de la cripta, técnica descrita por (Rodríguez, García, Valdés, & Hernández, 2011). La coloración utilizada fue hematoxilina-eosina, señalada por (Hermes, Azevedo, Araújo, & Sant'Ana, 2008).
Análisis estadístico
Para el análisis de los datos se utilizó un Diseño de Bloques Completos al Azar (DBCA) y como complemento la prueba de DUNCAN al 5 y 1 %, los cuales fueron interpretados mediante el programa estadístico SPSS, el modelo para el diseño en mención se detalla a continuación:
Yij = u+Ti+βj+εij
µ = Parámetro, efecto medio
Ti = Parámetro, tratamientos l
βj = Parámetro, sacrificios j
εij = Valor aleatorio, error experimental de la u.e.i, j
Yij= Observación de la unidad experimental.
Resultados
Consumo de alimento
La tabla 1 indica que el mayor consumo de alimento lo registro el tratamiento T0 (testigo) con 79,9 gr/cuy/día, en tanto que los tratamientos T1 (2 kg de S. cerevisiae / Tonelada de alimento) y T2 (4 kg de S. cerevisiae /Tonelada de alimento) consumieron 77,3 y 78,4 gr/cuy/día, respectivamente; no existiendo diferencia estadística significativa (p>0,05).
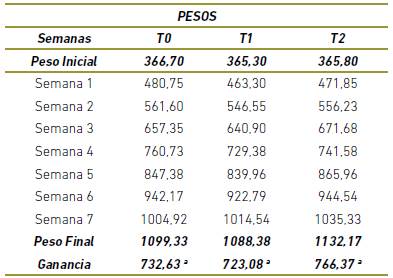
Ganancia de peso
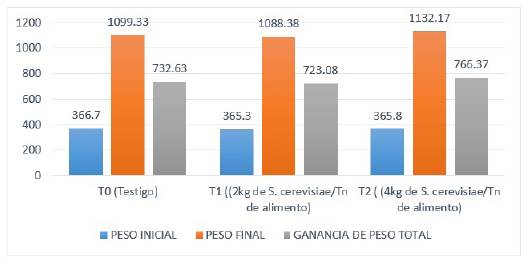
La tabla 2 indica que S. cerevisiae no ejerció efecto positivo sobre esta variable, puesto que no existe diferencia estadística significativa (p>0,05) = 0,846 entre tratamientos; sin embargo, el T2 logró el mayor peso promedio con 766,37 gr/animal; además se evidenció que las repeticiones fueron homogéneas; por otra parte, la figura 1 exhibe que todos los tratamientos se comportaron por igual respecto a esta variable.
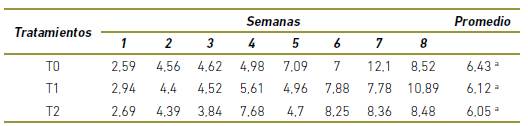
Conversión alimenticia
En la tabla 3 se observa que el tratamiento que obtuvo la mejor conversión alimenticia fue el T2 con un promedio de 6,5, seguido de los tratamientos T1 y T0 con 6,12 y 6,43 respectivamente, no evidenciando diferencia estadística significativa (p>0,05).
Mortalidad
El porcentaje de mortalidad más alto lo registro el T2 con el 5%, seguido de los tratamientos T1 y T0 con el 2,5%.
Parámetros de morfometría intestinal
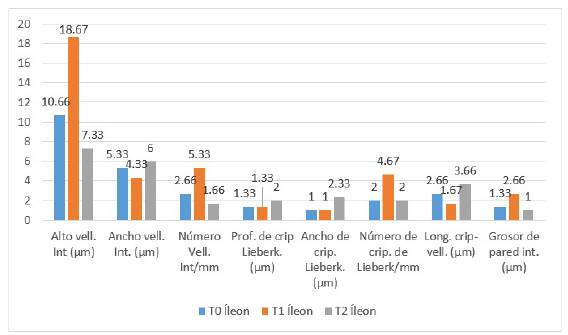
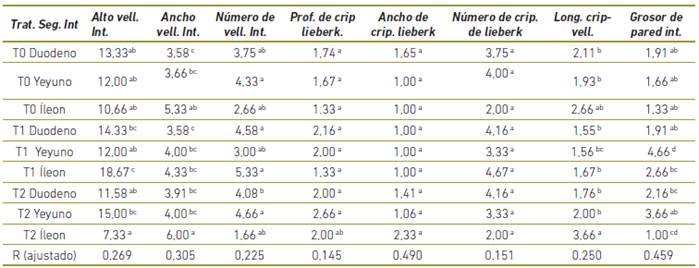
Luego de analizados los datos en cuanto a las variables de morfometria intestinal descritas: número de vellosidades intestinales/mm, altura y ancho de vellosidades intestinales (µm), número de criptas de Lieberkühn/mm, profundidad y ancho de criptas de Lieberkühn (µm), longitud del eje cripta-vellosidad (µm), y grosor de la pared intestinal (µm), se pudo determinar que la edad influye de forma significativa (p<0,05) en el número de criptas y longitud de las vellosidades, puesto que a mayor edad, estas dos variables incrementan; así mismo se observó que a nivel de íleon existe diferencia significativa (p<0,05) en el ancho de vellosidades, longitud cripta - vellosidad y grosor de la pared, variables que estuvieron influenciadas por el tratamiento, así, se registró que los tratamientos T1 y T2 obtuvieron valores superiores al testigo en la mayoría de variables evaluadas de morfometria intestinal a nivel dei íleon, datos que se exhiben en la tabla 4 y se resumen en la figura 2.
Tabla 4 Influencia dei tratamiento - jugar de la toma de la muestra con ias variables morfométricas.
Discusión
En el presente estudio la adición de S. cerevisiae en la alimentación de cuyes sobre los parámetros productivos permitió determinar que en cuanto a consumo de alimento en base a materia seca (MS), existió diferencia numérica, siendo el tratamiento testigo quien mostró un mayor consumo con 79,7 g/cuy/día de MS, resultado que es diferente al encontrado por (Castro, Narvaez , & Ortega, 2016) quien adiciono levadura de cerveza en la alimentación de cobayos durante las fases de gestación y recría de cobayos registrando que los animales que fueron suplementados consumieron mayor cantidad de ración alimenticia frente al resto de tratamientos, registrando un consumo de 25,32 g/cuy/día.
En lo referente a ganancia de peso el tratamiento 2 (4 kg S. cerevisiae/Tn de balanceado) obtuvo el mayor rendimiento con 766,4 g, dato que es superior al de (Chicaiza, 2015) y (Saravia, 2018) quienes incluyeron S. cerevisiae al 3% y 3 g en la dieta de cuyes en fase de crecimiento y engorde, registrando pesos de 623,7 g y 601,2 g respectivamente; y a los encontrados por (Narváez, 2014) que obtuvo pesos de 750,87 g en cuyes de recría y gestantes, incluyendo levadura y promotores de crecimiento.
La mejor conversión alimenticia (CA), la alcanzo el tratamiento 2 con 6.05; resultado que difiere al de (Saravia, 2018) quien obtuvo una conversión de 3,08 con la adición de 3 g de S. cerevisiae; así mismo (Narváez, 2014) registro una conversión de 3,08; mientras que (Chicaiza, 2015) y (Flores, 2014) reportan conversiones alimenticias de 3.25 y 3,9 respectivamente.
El porcentaje de mortalidad de los animales en este estudio fue de 2,5 y 5%; datos que son inferiores a los reportados por (Ordoñez, 2016) quien indicó una mortalidad del 5 y 10%; sin embargo los datos difieren de los señalados por (Chinguercela, 2014) que registró el 1,85% de mortalidad en cobayos durante la fase de crecimiento y engorde.
En cuanto a los indicadores de morfometría intestinal de duodeno y yeyuno no existió diferencia estadística significativa entre tratamientos y tiempo de toma de muestras, resultados que coinciden con los de (Puente, 2018) quien evaluó el efecto de diferentes niveles de probióticos sobre la histomorfometría intestinal y no encontró diferencia en cuanto al ancho y altura de vellosidad, longitud de eje cripta-vellosidad y profundidad de cripta; no obstante los datos difieren de los citados por (Leone, y otros, 2003) quien en su estudio de morfometría intestinal y a nivel de duodeno encontró diferencia estadística significativa en altura de vellosidad y longitud de eje-cripta cripta vellosidad; por otra parte (Viguera, Rojas, Hernández, Reyes, & Alvarez, 1999) demostró que las características histológicas de la mucosa intestinal (duodeno, yeyuno) en ratones disminuyen con el transcurso de la edad, mientras que el número de criptas incrementa dato que coincide con los encontrados por (Hiyagon, 2014) quien encontró un incremento en cobayos de 15 días de edad en mayor proporción a nivel de fundus.
A nivel de íleon se registró diferencia significativa con respecto al ancho de vellosidades y a longitud del eje cripta-vellosidad, datos que se contraponen con los resultados de (Puente, 2018) y, los cuales no reportan diferencias significativas. Por ultimo en cuanto al grosor de pared intestinal fue mayor para el tratamiento 2 con respecto al testigo por lo que se deduce que existió influencia de S. cerevisiae en la ración, concordando con (Trahair & Robinson, 1986) y (Checcnes, 2014) los cuales señalan que existe un incremento en el grosor de la pared intestinal en corderos y alpacas según corresponde.
Conclusión
Luego de realizado el análisis de los datos obtenidos en el estudio se concluye que la adición de Saccharomyces cerevisiae en la alimentación de cobayos a razón de 4 kg/tn de alimento, mejora los parámetros productivos de los cobayos de forma significativa en lo referente a ganancia y de peso y conversión alimenticia; sin embargo, en lo referente a morfometria intestinal de duodeno y yeyuno no demuestra diferencia estadística significativa en comparación con la no adición de la levadura; no obstante a nivel del íleon S. cerevisiae ejerce efecto positivo respecto al ancho de vellosidades y a longitud del eje cripta-vellosidad, así mismo se obtienen beneficios en cuanto al grosor de pared intestinal; por lo tanto se recomienda suplementar a los cobayos utilizando S. cervisiae a razón de 4 kg/tn de alimento, y realizar futuras investigaciones variando la dosis de la levadura.