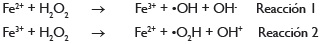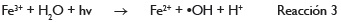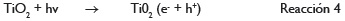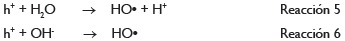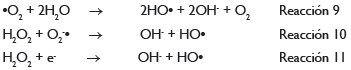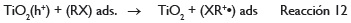Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Producción + Limpia
Print version ISSN 1909-0455
Rev. P+L vol.6 no.1 Caldas Jan./June 2011
1Derivado del proyecto de investigación: "FeCl3 and TiO2 interaction with H2O2 in the liquid waste treatment from the textile industry using artificial light trough factorial model", para optar al título de doctor of Sciences in Environmental Engineering. Financiado por el Fondo para el Desarrollo de la investigación de la Corporación Universitaria Lasallista.
2Ingeniero Sanitario. MSc. DSc. Director de Investigación, Corporación Universitaria Lasallista.
Correspondencia: Luis Fernando Garcés Giraldo, e-mail: lugarces@lasallista.edu.co
Artículo recibido: 17/10/2010; Artículo aprobación: 09/04/2011
Resumen
Introducción. Los colorantes textiles tienen gran persistencia en el ambiente, y los métodos de eliminación clásicos no son útiles debido a que oxidaciones o reducciones parciales pueden generar productos secundarios altamente tóxicos. Una gran proporción de los colorantes no son directamente tóxicos para los organismos vivos; sin embargo, la fuerte coloración que imparten a los medios de descarga puede llegar a suprimir los procesos fotosintéticos en los cursos de agua, por lo que su presencia debe ser controlada. Objetivo. Seleccionar la dosis óptima de fotosensibilizador y agente oxidante para la degradación del colorante azul novactive FHBRNS. Materiales y métodos. Se utilizó una muestra sintética con 300 mg/L del colorante azul novactive FHBRNS utilizado en la industria textil para el teñido de prendas. Esta concentración es la más común en los efluentes industriales textiles de las industrias que utilizan este colorante. En los experimentos se utilizó el TiO2 y el FeCl3 en concentraciones de 30 y 60 mg/L; y como agente oxidante el H2O2 en concentraciones que variaron entre 0.5, 1.0 y 1.5 mg/L. Resultados. El colorante degrada y mineraliza más rápidamente con el FeCl3; esto sucedió en el ensayo donde se utilizaron 60 mg/L FeCl3 y 1.0 mL/L de H2O2. Conclusión. Se obtuvieron porcentajes de degradación y mineralización de 97.3% y del 65.8%, respectivamente.
Palabras clave: fotodegradación, azul Novactive FHBRNS, agente oxidante, fotólisis, fotocatálisis.
Abstract
Introduction. Textile dyes are very persistent in the environment and the classic methods to eliminate them are not useful because partial oxidations or reductions can create very toxic secondary products. Many of the dyes are not directly toxic for living organisms, but the strong coloring they bring to the aquatic environment can suppress photosynthesis in watercourses so their presence must be controlled. Objective. To select the optimal dose of photo sensitizer and oxidation agent to degrade novactive blue FHBRNS. Materials and methods. A synthetic sample with 300mg/L of novactive blue FHBRNS dye used in textiles was used. This is the most common concentration in effluents from the textile industries that use this dye. In the experiments, TiO2 and FeCl3 were used in 30 and 60 mg/L concentrations and as an oxidation agent H2O2 was used in concentrations between 0.5, 1.0 and 1.5 mg/L. Results.The dye is fastly degraded and mineralized with FeCL3. This happened in the test in which 60mg/L FeCL3 and 10 mL/L of H2O2 were used. Conclusion. Degradation percentages of 97.3% and 65.8%, respectively, were obtained.
Key words: photo degradation, Novactive blue FHBRNS, oxidation agent, photolysis, photocatalysis.
Resumo
Introdução. Os corantes têxteis têm grande persistência no ambiente, e os métodos de eliminação clássicos não são úteis devido a que oxidações ou reduções parciais podem gerar produtos secundários altamente tóxicos. Uma grande proporção dos corantes não são diretamente tóxicos para os organismos vivos; no entanto, a forte coloração que dão aos meios de descarga pode chegar a suprimir os processos fotosintéticos nos cursos da água, pelo que sua presença deve ser controlada. Objetivo. Selecionar a dose ótima de fotosensibilizador e agente oxidante para a degradação do corante azul novactive FHBRNS. Materiais e métodos. Utilizou-se uma mostra sintética com 300 mg/L do corante azul novactive FHBRNS utilizado na indústria têxtil para o tingido de prendas. Esta concentração é a mais comum nos efluentes industriais têxteis das indústrias que utilizam este corante. Nos experimentos se utilizou o TiO2 e o FeCl3 em concentrações de 30 e 60 mg/L; e como agente oxidante o H2Ou2 em concentrações que variaram entre 0.5, 1.0 e 1.5 mg/L. Resultados. O corante degrada e mineraliza mais rapidamente com o FeCl3; isto sucedeu no ensaio onde se utilizaram 60 mg/L FeCl3 e 1.0 ML/L de H2Ou2 . Conclusão. Obtiveram-se percentagens de degradação e mineração de 97.3% e do 65.8%, respectivamente.
Palavras importantes: fotodegradação, azul Novactive FHBRNS, agente oxidante, fotólisis, fotocatálisis.
Introducción
La industria textilera genera residuos líquidos con cargas orgánicas manifestadas en DBO, DQO, y otros contaminantes que provienen de las secciones de tintorería, estampado, acabados y planta de agua, además de temperaturas mayores de 30°C y pH fuera de rango.
El colorante es un compuesto que al aplicarse a un sustrato en forma de dispersión o difusión le da un color permanente a la tela o al hilo. Tiene que interactuar con el sustrato y este tiene que ser capaz de absorberlo. Las condiciones que se deben cumplirson1: tener un fuerte poder colorante, es decir, con poca cantidad de sustancia se debe conseguir gran superficie coloreada; debe tener solidez, es decir, debe ser resistente a los agentes atmosféricos y la luz; se debe conseguir una buena adherencia al sustrato; se tiene que conseguir un buen nivelado, esto es, uniformidad de color en el proceso de teñido; tiene que tolerar otros colorantes que puedan mezclarse, y debe ser fácilmente aplicable.
Los colorantes son sustancias intensamente coloreadas que se usan en el teñido de diversos sustratos, que incluyen papel, cuero, cabello, alimentos, drogas, cosméticos, ceras, grasa, plásticos, textiles, etc. Estos sustratos los retienen por absorción física, formación de complejos con sales o metales, disolución, retención mecánica o por medio de la formación de enlaces químicos covalentes. Los métodos que se utilizan en la aplicación de colorantes a los sustratos difieren ampliamente, dependiendo del sustrato y de la clase de colorante2, 3.
Existen numerosos procesos utilizados en la actualidad para la degradación de sustancias presentes en el agua. Algunos de ellos son los recientemente aplicados procesos de oxidación avanzada, los cuales se constituirán, en un futuro próximo, en uno de los recursos tecnológicos más utilizados para el tratamiento de aguas contaminadas con productos orgánicos recalcitrantes industriales. Estos procesos implican la formación de radicales hidroxilo (•OH), altamente reactivos, que actúan como iniciadores de la oxidación. Entre estos procesos, los de mayor auge son la fotólisis y la fotocatálisis. La fotodegradación sensibilizada se ha usado para degradar y/o mineralizar una variedad de compuestos orgánicos, algunos de ellos, de gran uso industrial o agrícola4-6.
La investigación en tecnologías como la oxidación fotocatalítica, alternativa a procesos de oxidación tradicionales (ozono, peróxido de hidrógeno e hipoclorito), está plenamente justificada para estos fines. Los sistemas de oxidación avanzada, en los que se combina la energía radiante ultravioleta y un oxidante, como aire, en presencia de semiconductores estables, como el dióxido de titanio o el reactivo fenton, se presentan como una alternativa sencilla y económica para la mineralización completa de compuestos orgánicos, y para la adecuación de efluentes industriales a su vertido y posterior tratamiento de redes de saneamiento7.
El reactivo fentón o fotofenton (Fe3+)8,9
Uno de los métodos clásicos de producción de radicales hidroxilo consiste en la adición de sales de hierro como catalizador en presencia de peróxido de hidrógeno; esta adición es conocida como reactivo Fenton, y tiene como resultado uno de los agentes oxidantes más potentes a pH ácidos (pH 3-5). El hierro puede ser añadido como sal ferrosa o férrica como se muestra en las reacciones 1 y 2.
Estos radicales inician una cadena de reacciones para eliminar toda la materia oxidable. En concreto, los radicales hidroxilo reaccionan con compuestos orgánicos, generando radicales orgánicos (C-centrados) que aceleran el grado de oxidación. Aunque el reactivo Fenton es un potente e indiscriminado agente oxidante, existen especies resistentes al mismo como los alcanos clorados (tetracloroetano, tricloroetano, cloroformo,...), n-parafinas y ácidos carboxílicos de cadena corta (maleico, oxálico, acético, malónico).
Se ha comprobado que la radiación UV/visible acelera las reacciones Fenton (H2O2/Fe3+, Fe2+), y favorece así el grado de degradación de contaminantes orgánicos, incluidos los compuestos aromáticos y alifáticos. Este reactivo presenta una mayor efectividad a pH ácido, debido a la aparición de hidróxidos de hierro como precipitados coloidales a pH mayor de 3, lo cual hace necesaria su separación, mediante un proceso adicional de tipo coagulación, sedimentación o filtración. Además, algunos intermedios de reacción pueden alterar la reactividad del hierro debido a la formación de complejos.
En las reacciones de Fenton tradicional, el Fe2+ actúa como catalizador en la descomposición del H2O2 dando lugar a la formación de radicales °OH (reacción 1). En esta reacción, los iones Fe3+ se van acumulando a medida que el Fe2+ se consume y la reacción finalmente se detiene (reacción 2). En este proceso se intenta solucionar este problema, mediante la regeneración fotoquímica de los iones Fe2+ reduciendo el ión férrico según la reacción 3.
El dióxido de titanio (tiO2)4, 10, 11
En el caso de la fotocatálisis heterogénea, existen referencias12, 13 de aplicaciones con múltiples semiconductores como Al2O3, ZnO, Fe203 y TiO2. Sin embargo, el más ampliamente utilizado es el dióxido de titanio, ya que presenta una mayor actividad fotocatalítica, no es tóxico, es estable en soluciones acuosas y no es costoso; se han evaluado diferentes estructuras del mismo.
Al irradiar TiO2, en su forma anatasa, con una longitud de onda inferior a 400 nm, se genera un exceso de electrones (e-) en la banda de conducción y huecos positivos (h+) en la banda de valencia.
En la superficie del TiO2, los huecos reaccionan tanto con H2O absorbida como con grupos OH• para formar radicales hidroxilo (•OH):
Los electrones en exceso de la banda de conducción reaccionan con el oxígeno molecular para formar radicales superóxido y peróxido de hidrógeno:
Tanto el radical superóxido como el peróxido de hidrógeno generan más radicales hidroxilos así:
El radical hidroxilo (HO•) provoca la completa mineralización de muchas sustancias orgánicas. Dependiendo del equilibrio de adsorción/desorción para un contaminante dado, la oxidación fotocatalítica de un sustrato orgánico adsorbido podría iniciar la eficiencia de su degradación oxidativa:
Materiales y métodos
Se utilizó una muestra sintética con 300 mg/L del colorante azul novactive FHBRNS usado en la industria textil para el teñido de prendas. Esta concentración es la más común en los efluentes industriales textiles de las industrias que utilizan este colorante. En los experimentos se utilizaron el TiO2 y el FeCl3 en concentraciones de 30 y 60 mg/L; y como agente oxidante el H2O2 en concentraciones que variaron entre 0.5, 1.0 y 1.5 mg/L. La degradación del colorante se evaluó midiendo la concentración del contaminante por seguimiento del color (fotometría), y la mineralización, utilizando la técnica del carbono orgánico total (COT). Se realizó por triplicado cada uno de los experimentos para disminuir el error experimental. La duración de los ensayos fue de dos horas.
Para el procesamiento de la información se empleó el programa R 2.7.2 y los métodos utilizados fueron: análisis de varianza (ANOVA) de tres factores con un nivel de confianza del 95% y un nivel de potencia para detectar diferencias significativas del 100%, y análisis factorial 33 para optimizar las variables respuesta: porcentaje de degradación y porcentaje de mineralización.
Análisis de Varianza (ANOVA)
El modelo utilizado para el porcentaje de degradación y el porcentaje de mineralización como variables respuesta fue un modelo de tres factores, efectos fijos completamente aleatorizados, con tres réplicas; el nivel de confianza es del 95% y la potencia para detectar diferencias significativas es de 100%.
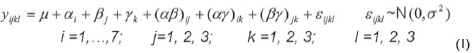
Donde:

Es importante anotar que αl,β¡,γk son los efectos principales; (αβ)ij;(βα)ji;(βγ)kj son los efectos de interacción de los factores. Estas son constantes y están sujetas a las siguientes restricciones:
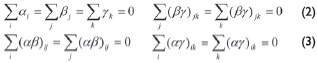
Las hipótesis con las que fue realizado el diseño experimental de tres factores de efectos fijos son las siguientes:
Factor: tiempo acumulado (minutos)
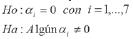
Factor: TIO2 ó FeCl3
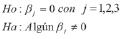
Factor: H2O2
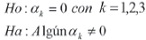
Interacción: Tiempo*TIO2 ó FeCl3
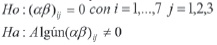
Interacción: Tiempo*H2O2
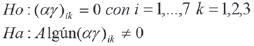
Interacción: H2O2*TIO2 ó FeCi2
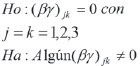
La regla de decisión para aceptar o rechazar la hipótesis nula Ho, se basa en el siguiente criterio: Si el Valorp≤ α = 0,05 se acepta H2, en caso contrario se rechaza.
Diseño factorial 33
Para optimizar las variables respuesta: porcentaje de degradación y porcentaje de mineralización, se corrió un diseño factorial 33 con las variables: tiempo acumulado, TiO2, ó FeCI2, y H2O2, cuyos niveles se presentan en la tabla 1.
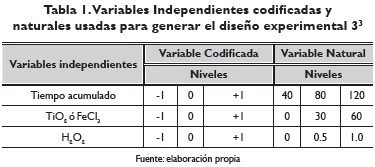
Resultados y discusión
Experimentación con FeCl3
Se obtuvo un valor p es (p = 0,0001 ≤α), para los efectos principales tiempo acumulado (minutos), cloruro férrico (mg/L), peróxido de hidrogeno (mL/L) y sus interacciones. Por lo tanto, rechazamos la hipótesis nula con un nivel de confianza del 95%, con lo cual se concluye que estos efectos y sus interacciones son significativos, o sea, que el cambio en el tiempo acumulado, la concentración de cloruro férrico (mg/L) y peróxido de hidrógeno (mL/L), así como sus interacciones, influye significativamente en el porcentaje de degradación y el porcentaje de mineralización. Como las interacciones son significativas no se pueden evaluar los efectos principales por separados; por lo tanto, en la figura 1 se presenta el análisis de las interacciones para cada variable respuesta.
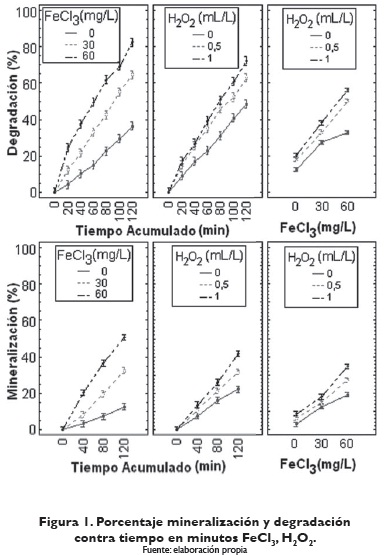
El R2 para los modelos porcentaje de mineralización y el porcentaje de degradación es R2=0.9933 y R2=0.9964 lo que indica que cada modelo explica un 99,33% y 99,64% los datos obtenidos; por tanto, el error absorbe un 0,67% y 0,36%, respectivamente, debido a factores incontrolables desconocidos. Lo anterior indica que los factores fueron bien seleccionados y controlados para el experimento. Como cada modelo cumplió con los supuestos (anexo A, figura 41) y, además, explica más del 90% de los datos obtenidos, concluimos que son adecuados para explicar el porcentaje de degradación y el porcentaje de mineralización del azul con FeCl3.
En la figura 1 se observa cómo el porcentaje de degradación aumenta durante el tiempo en minutos del experimento, con cualquier nivel de cloruro férrico y de peróxido de hidrógeno, pero es óptimo este aumento para 60 mg/L de FeCl3 y 1 mL/L de H2O2. Trabajar sin peróxido de hidrógeno y sin cloruro férrico proporciona la menor degradación. Se puede ver que las mayores degradaciones del colorante se obtienen cuando se combina 1 mL/L de peróxido de hidrogeno con 60 mg/L de cloruro férrico.
Cinética de degradación y mineralización
Para determinar si el orden de la reacción es uno, se representó gráficamente el logaritmo de la concentración residual del colorante contra el tiempo acumulado, para el porcentaje de degradación y porcentaje de mineralización (figura 2). Las reacciones fueron de primer orden (mayor valor en el coeficiente de correlación). La reacción de primer orden dependería de la constante de degradación del colorante. Los tiempos de vida media y las velocidades de reacción fueron calculados de acuerdo con los planteamientos realizados en la ecuación de orden de reacción 1.
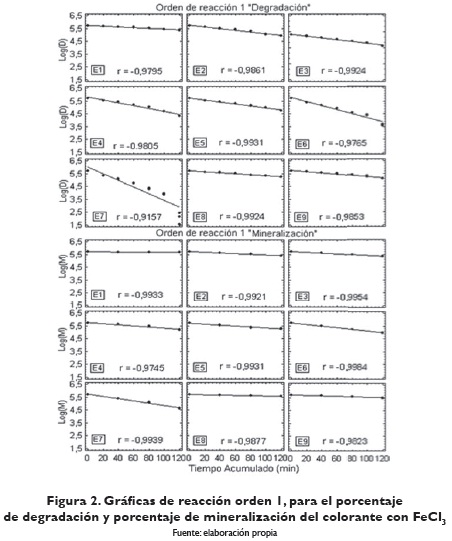
La figura 3 presenta el resumen del logaritmo de la concentración de degradación y logaritmo de la concentración de mineralización del colorante con FeCl3. En esta figura se puede observar que el ensayo 7 es el que presenta mayor pendiente en las líneas rectas.
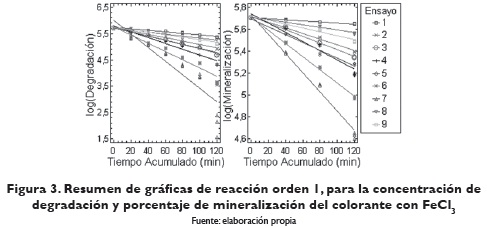
El orden de la reacción, la constante de velocidad y el tiempo de vida media para cada uno de los ensayos realizados en el porcentaje de degradación y porcentaje de mineralización del azul con FeCl3 se observan en la tabla 2. Según la constante de velocidad, la reacción de degradación y mineralización del azul con FeCl3 más rápida fue con el ensayo 7, con un tiempo de vida medio de 26.65 y 78.75 minutos, respectivamente.
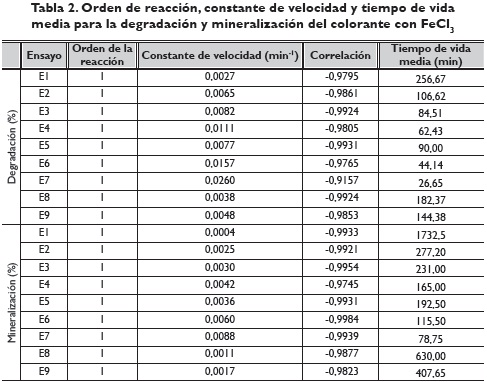
Diseño factorial 33 para optimizar las variables respuestas
Con la metodología de la pendiente ascendente se obtuvieron los valores de los factores que optimizan la variable respuesta en cada porcentaje desde 50 hasta 100%. La combinación de FeCl3, H2O2 y tiempo que generan el máximo de porcentaje de degradación y de mineralización se presenta en la tabla 3. La superficie de repuestas para las variables dependientes estudiadas se presenta en la figura 4.
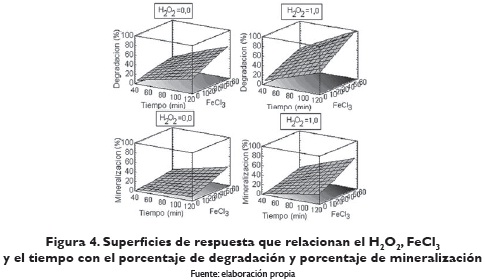
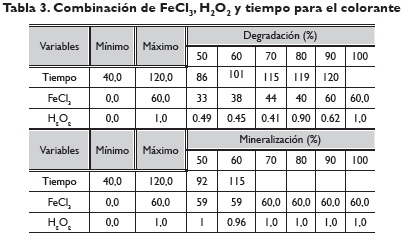
El máximo de porcentaje de degradación es estable en FeCl3, H2O2, y el tiempo permanece constante después de 80%; respecto al porcentaje de mineralización permanece constante en las variables FeCl3, H2O2, y tiempo constante desde 70% (tabla 3).
Con TiO2
Se encontró que el valor p es (p = 0,0001 ≤α), para los efectos principales "tiempo acumulado (minutos), dióxido de titanio (mg/L), peróxido de hidrogeno (mL/L)" y sus interacciones. Por lo tanto, rechazamos la hipótesis nula con un nivel de confianza del 95%, con lo cual se concluye que estos efectos y sus interacciones son significativos, o sea, que el cambio en el tiempo acumulado, la concentración de dióxido de titanio (mg/L) y peróxido de hidrógeno (mL/L), así como sus interacciones, influyen significativamente en el porcentaje de degradación y en el porcentaje de mineralización. Como las interacciones son significativas, no se pueden evaluar los efectos principales por separados; por lo tanto, en la figura 5 se presenta el análisis de las interacciones para cada variable respuesta.
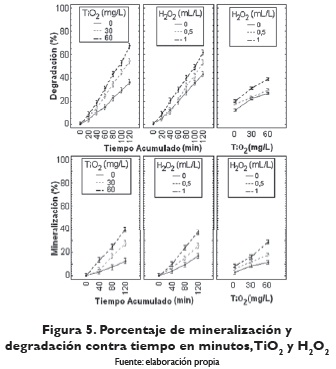
El R2 para los modelos porcentaje de mineralización y el porcentaje de degradación es R2=0.9847 y R2=0.9947, lo que indica que cada modelo explica un 98,47% y 99,47% los datos obtenidos; por tanto, el error absorbe un 1.53% y 0,53%, respectivamente, debido a factores incontrolables desconocidos. Lo anterior indica que los factores fueron bien seleccionados y controlados para el experimento. Como cada modelo cumplió con los supuestos y, además, explica más del 90% de los datos obtenidos, concluimos que son adecuados para explicar el porcentaje de degradación y el porcentaje de mineralización del colorante con TiO .
En la figura 5 se observa cómo el porcentaje de degradación aumenta durante el tiempo en minutos del experimento, con cualquier nivel de dióxido de titanio y de peróxido de hidrógeno, pero es óptimo este aumento para 60 mg/L de TiO2 y 1 mL/L de H2O2. Trabajar sin peróxido de hidrógeno y sin dióxido de titanio proporciona la menor degradación. Se puede ver que las mayores degradaciones del colorante se obtienen cuando se combina 1 mL/L de peróxido de hidrógeno con 60 mg/L de dióxido de titanio.
Cinética de degradación y mineralización
Para determinar si el orden de la reacción es uno, se representó gráficamente el logaritmo de la concentración residual del colorante, contra el tiempo acumulado, para el porcentaje de degradación y el porcentaje de mineralización (figura 6). Las reacciones fueron de primer orden (mayor valor en el coeficiente de correlación). La reacción de primer orden dependería de la constante de degradación del colorante. Los tiempos de vida media y las velocidades de reacción fueron calculados de acuerdo con los planteamientos realizados en la ecuación de orden de reacción 1.
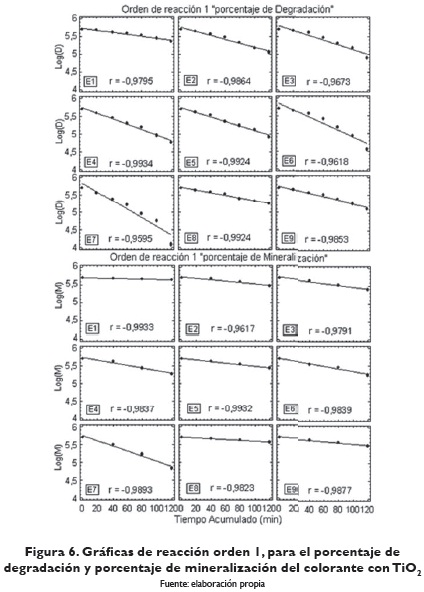
La figura 7 presenta el resumen del logaritmo de la concentración de degradación y logaritmo de la concentración de mineralización del amarillo con TiO2. En esta figura se puede observar cómo el ensayo 7 es el que presenta mayor pendiente en las líneas rectas.
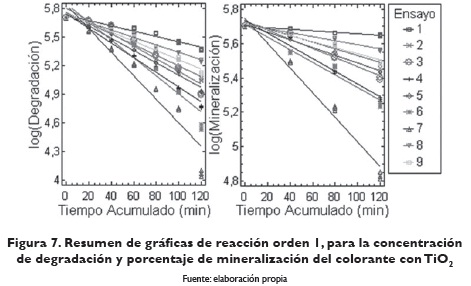
El orden de la reacción, la constante de velocidad y el tiempo de vida media para cada uno de los ensayos realizados en el porcentaje de degradación y porcentaje de mineralización del azul con TiO2, se observan en la tabla 4. Según la constante de velocidad, la reacción de degradación y mineralización del azul con TIO2 más rápida fue con el ensayo 7, con un tiempo de vida medio de 56.34 y 96.25 minutos, respectivamente.
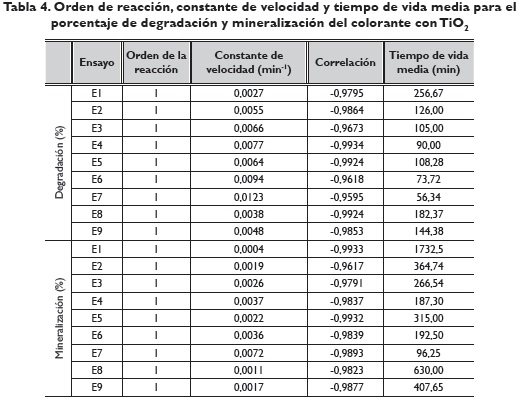
Diseño factorial 33 para optimizar las variables respuestas
Con la metodología de la pendiente ascendente se obtuvieron los valores de los factores que optimizan la variable respuesta en cada porcentaje desde 50 hasta 100%. La combinación de TiO2, H2O2 y tiempo que generan el máximo de porcentaje de degradación y de mineralización se presentan en la tabla 5. La superficie de repuestas para las variables dependientes estudiadas se presenta en la figura 8.
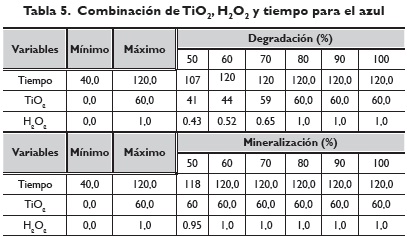
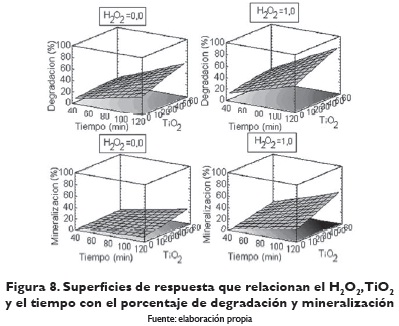
El máximo de porcentaje de degradación se estabiliza en TiO2, H2O2 y tiempo después de 70%, respecto al porcentaje de mineralización permanece constante en las variables TiO2, H2O2 y tiempo constante desde 60% de (tabla 5).
Conclusiones
Se utilizó la metodología de la pendiente ascendente para optimizar las variables respuesta, la cual es una técnica de optimización que tiene como objetivo encontrar el y/o los puntos que maximizan o minimizan la ecuación de superficie de respuesta. Este proceso permite recorrer secuencialmente la trayectoria de la máxima o la mínima pendiente que conduce a la dirección del máximo o del mínimo aumento de la respuesta.
En los ensayos del colorante azul novactive FHBRNS (FeCl3 y TiO2), se concluye que este degrada y mineraliza más rápidamente con el FeCl3; esto sucedió en el ensayo E7 (60 mg/L FeCl3 y 1.0 mL/L de H2O2), donde se obtuvo un porcentaje de degradación del 97.3% y un porcentaje de mineralización de 65.8%. En este mismo experimento fue donde se obtuvieron los mejores resultados para la degradación y mineralización del colorante con el TiO2.
Referencias
1. FRANCO C. Alexander y ORTIZ, Natalia. Manejo y tratamiento de los residuos líquidos de la facultad de ingenierías. Universidad de Antioquia. Departamento de Ingeniería Química, Medellín, 2000. 226 p. [ Links ]
2. ZHAO, Wei; et al. Photodegradation of Sulforhodanine-B dye in plantinizad titania dispersions under visible light irradiation: influence of platinium as a functional co-cotalyst. In: The journal of physicalchemistry. 2002. Vol 16, No. 16. p. 5022-5028. [ Links ]
3. NAOMI, L.; et al. Combinative sonolysis and photocatalysis for textile dye degradation. In: Environmental Sciencie-Technology. 2000. Vol. 34. p. 1747-1750. [ Links ]
4. GARCES G., Luis F. Fotocatálisis con TiO2 de los colorantes azul de metileno y naranja reactivo 84 utilizando colector solar. Tesis de Maestría. Medellín: Universidad de Antioquia - Facultad de ingeniería, 2003. [ Links ]
5. HERNANDEZ A., Marta Lucia y GARCES G., Luis F. Comparación de los tratamientos con TiO2 y FeCl3 para aguas residuales coloreadas textiles. En: Revista Lasallista de Investigación. Corporación Universitaria Lasallista. Jul-Dic. 2006. Vol. 3, No. 2. p. 25-33. [ Links ]
6. LITTER, Marta; et al. Tratamiento de residuos nucleares líquidos por fotocatálisis heterogénea. Comisión Nacional de Energía Atómica, Unidad de Actividad Química. 2003. [ Links ]
7. COZ, A. y VILLASEÑOR J. Tratamiento de efluentes fenólicos de la industria de la celulosa: procesos de oxidación avanzada. En: Ingeniería Química. Madrid. Ene. 2003. Vol. 35, No 397. p. 104-114. [ Links ]
8. ARROYAVE R. Joan; et al. Fotodegradación del pesticida mertect empleando fotofenton con lámpara de luz ultravioleta. En: Fotocatálisis y electrocoagulación para el tratamiento de aguas residuales: investigaciones y aplicaciones. Corporación Universitaria Lasallista. Caldas-Antioquia. 2007. [ Links ]
9. HERNANDEZ A., Marta Lucia y GARCES G., Luis F. Comparación de los tratamientos con TiO2 y FeCl3. En: Fotocatálisis y electrocoagulación para el tratamiento de aguas residuales: investigaciones y aplicaciones. Corporación Universitaria Lasallista. Caldas-Antioquia. 2007. [ Links ]
10. CHEN, Chuncheng; et al. Photocatalysis by Titanium Dioxide and Polyoxometalate/TiO2 Cocatalysts. Intermediates and Mechanistic Study. In: Enviromental Science & Technology. Ene. 2004. Vol. 38, No. 1, p. 329-337. [ Links ]
11. GELOVER, Silvia; MONDRAGÓN, Pedro y JIMÉNEZ, Antonio. Titanium Dioxide sol-Gel Deposited Over Glass and its Application as a Photocatalyst for Water Descontamination. In: Journal of Photochemistry and Photobiology A: Chem. 2004. Vol 165. No. 1-3. p. 241-246. [ Links ]
12. ARAÑA M. Javier; et al. Role of Fe3+/Fe2+ as TiO2 dopant ions in photocatalytic degradation of carboxylic acids. In: Journal of Molecular Catalysis A: Chemical. 2003. No. 197. p. 157-171. [ Links ]
13. _____. FTIR study of formica cid interaction with TiO2 and TiO2 doped with Pd and Cu in photocatalyticu processes. In: Applied Surface Science. 2004. No. 239. p. 60-71. [ Links ]