Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Producción + Limpia
Print version ISSN 1909-0455
Rev. P+L vol.10 no.1 Caldas Jan./June 2015
Valorización hidrometalúrgica de los materiales catódicos y anódicos de baterías recargables gastadas de tipo Ni-MH*
Hydrometallurgical valuing of cathodic and anodic materials of used rechargeable batteries from the Ni-MH Type
Valorização hidrometalúrgica dos materiais catódicos e anódicos de baterias recargáveis usadas de tipo Ni-MH
Antonio Zambrano Colmenares**, Carlos Humberto Romero Briceño***, Alberto Moccia Paradisi****, Raúl Evencio Orta Rodríguez*****, José Luis López Sanz******, Pedro Delvasto Angarita*******
* Artículo derivado del proyecto de investigación titulado "Diseño de una planta piloto con tecnología sencilla y apropiable para el procesamiento de pilas y baterías gastadas con el objeto de reciclar Ni, Cd y otros metales", desarrollado en la Universidad Simón Bolívar, Caracas, Venezuela y financiado por el Fondo Nacional de Ciencia, Tecnología e Innovación (FONACIT) bajo la subvención N.° 2011000401, Vigencia: Diciembre 2011 - Noviembre 2014.
** Ingeniero de Materiales, asistente de Investigación adscrito a la Unidad de Gestión en Materiales y Procesos Sustentables (UGEMAT). Fundación de Investigación y Desarrollo (FUNINDES), Universidad Simón Bolívar, Caracas, Venezuela.
*** Ingeniero químico, magíster en Ingeniería Química, profesor a dedicación exclusiva adscrito al Departamento de Termodinámica y Fenómenos de Transferencia Universidad Simón Bolívar. Caracas, Venezuela.
**** Ingeniero de Materiales, asistente de Investigación adscrito a la Unidad de Gestión en Materiales y Procesos Sustentables (UGEMAT). Fundación de Investigación y Desarrollo (FUNINDES), Universidad Simón Bolívar, Caracas, Venezuela.
***** Ingeniero de Materiales, asistente de Investigación adscrito a la Unidad de Gestión en Materiales y Procesos Sustentables (UGEMAT). Fundación de Investigación y Desarrollo (FUNINDES). Universidad Simón Bolívar, Caracas, Venezuela.
****** Ingeniero Metalúrgico, profesor a tiempo convencional adscrito al Departamento de Ciencia de los Materiales, Universidad Simón Bolívar, Caracas, Venezuela.
******* Ingeniero de Materiales, magíster en Ingeniería de Materiales, doctor en Ciencia y Tecnología de Materiales, profesor asociado adscrito a la Escuela de Ingeniería Metalúrgica y Ciencia de los Materiales, Facultad de Ingenierías Fisicoquímicas, Universidad Industrial de Santander, Bucaramanga, Colombia.
Correspondencia: Antonio Zambrano Colmenares, e-mail: chromero@usb.ve.
Artículo recibido:15/06/2014; Artículo aprobado: 11/05/2015
Resumen
Introducción. Las pilas y baterías gastadas pertenecen a un grupo de sustancias peligrosas denominadas residuos tecnológicos. Las mismas contienen metales pesados, que son perniciosos para los ecosistemas y la salud. En este trabajo se presenta una metodología para procesar mediante hidrometalurgia los materiales contenidos en pilas gastadas del tipo níquel hidruro metálico (Ni-MH). Objetivo. Valorizar los materiales catódicos y anódicos de baterías gastadas del tipo Ni-MH mediante procesos hidrometalúrgicos de lixiviación y precipitación de sales. Materiales y métodos. Se desensambló de manera manual un lote de 3,7 kg de este tipo de pilas y se analizaron químicamente los materiales anódicos y catódicos por separado. Los materiales fueron lixiviados con HCl al 14 %. Los licores preñados, en cada caso, se sometieron a un proceso de precipitación con NaHCO3, y se obtuvieron sales de los metales de interés. Resultados. Se encontró que el ánodo contiene principalmente níquel (50 % m/m), lantano (18 % m/m) y cobalto (6 % m/m), y que el cátodo, por su parte, contiene principalmente níquel (53 % m/m), cobalto (4 % m/m) y zinc (3 % m/m). Se encontró que la solución de HCl fue capaz de lixiviar aproximadamente 87 % y 91 % del Ni en el material anódico y catódico, respectivamente. Finalmente, se presentan los diagramas de flujo de proceso para establecer una ruta de procesamiento hidrometalúrgico para este tipo de residuos tecnológicos. Conclusión. Se encontró factible utilizar un proceso hidrometalúrgico de varias etapas para la valorización de los metales contenidos en los materiales electródicos de las pilas Ni-MH, y para obtener sales metálicas que pueden ser aprovechadas en diferentes procesos industriales.
Palabras clave: Reciclaje, baterías, níquel, tierras raras, hidrometalurgia.
Abstract
Introduction. Used batteries are considered as dangerous substances of the technological waste kind.They contain heavy metals, which are harmful for ecosystems and health. This paper introduces a technology to process, by means of hydrometallurgy, the materials contained in used batteries from the hydride metallic type (Ni-MH). Objective. Value the cathodic and anodic materials from used batteries from the (Ni-MH) type,by the use of hydrometallurgical lixiviation and salts precipitation processes. Materials and methods. A 3,7 kg batch of this kind of batteries was manually dissembled and the cathodic and anodic materials were separated and chemically analyzed. The materials were lixiviated with HCL at 14 %. The pregnant liquors, in each case, were subjected to a precipitation process with NaHCO3, obtaining salts from the metals of interest. Results. The anode mainly contains nickel (50 % m/m), lanthanum (18 % m/m) and cobalt (6 % m/m) and the cathode mainly contains nickel (53 % m/m), cobalt (4 % m/m) and zinc (3 % m/m). The HCL solution was able to lixiviate approximately 87 % and 91% of Ni in the anodic and the cathodic materials, respectively. Finally, the process flowcharts are showed in order to establish a hydrometallurgical process route for this type of technological waste. Conclusion. It is possible to use a metallurgical process with several stages to value the metals contained in the electrode materials from Ni-MH batteries, obtaining metallic salts that can be used in several industrial processes.
Key words: Recycling, batteries, nickel, Rare Earth Elements -REE-, hydrometallurgy.
Resumo
Introdução. As pilhas e bateristas usadas pertencem a um grupo de substâncias perigosas denominadas resíduos tecnológicos. As mesmas contêm metais pesados, que são perniciosos para os ecossistemas e a saúde. Neste trabalho se apresenta uma metodologia para processar mediante hidrometalurgia os materiais conteúdos em pilhas gastadas do tipo níquel hidreto metálico (Nem-MH). Objetivo. Valorizar os materiais catódicos e anódicos de bateristas usadas do tipo Ni-MH mediante processos hidrometalúrgicos de lixiviação e precipitação de sais. Materiais e métodos. Se desmontou de maneira manual um lote de 3,7 kg deste tipo de pilhas e se analisaram quimicamente os materiais anódicos e catódicos por separado. Os materiais foram lixiviados com HCl ao 14 %. Os licores carregados, em cada caso, submeteram-se a um processo de precipitação com NaHCO3, obtendo-se salgues dos metais de interesse. Resultados. Encontrou-se que o ânodo contém principalmente níquel (50 % m/m), lantânio (18 % m/m) e cobalto (6 % m/m) e que o cátodo, por sua vez, contém principalmente níquel (53 % m/m), cobalto (4 % m/m) e zinco (3 % m/m). Encontrou-se que a solução de HCl Valorización hidrometalúrgica de los materiales catódicos y anódicos de baterías recargables gastadas de tipo Ni-MH foi capaz de lixiviar aproximadamente 87 % e 91 % do Ni no material anódico e catódico, respectivamente. Finalmente, apresentam-se os diagramas de fluxo de processo para estabelecer uma rota de processamento hidrometalúrgico para este tipo de resíduos tecnológicos. Conclusão. Encontrou-se viável utilizar um processo hidrometalúrgico de várias etapas para a valorização dos metais contidos nos materiais eletródicos das pilhas Ni-MH obtendo sais metálicos que podem ser aproveitadas em diferentes processos industriais.
Palavras chaves: Reciclagem, Bateristas, Níquel, Terras Raras, hidrometalurgia.
Introducción
Las pilas y baterías son dispositivos de almacenamiento de energía eléctrica cuyo principio de funcionamiento se basa en una reacción electroquímica. Existen dos tipos: las primarias, que son de un solo uso, y las secundarias, también denominadas como recargables (Besenhard, 1999, 1). Las pilas o baterías recargables deben su característica a la reversibilidad de la reacción electroquímica. Existen varios tipos de pilas recargables para dispositivos electrónicos domésticos; las principales son: Níquelcadmio (Ni-Cd), níquel-hidruro metálico (Ni-MH), ión de litio (Li-Ion) o litio-polímero (Li-Po).Todos estos sistemas de almacenamiento de energía tienen en común que sus reacciones electroquímicas involucran la óxido-reducción de especies químicas que contienen iones metálicos, normalmente metales pesados (Linden y Reddy, 2002, 1.3 - 1.9).
En el caso particular de las pilas de Ni-MH, las mismas están conformadas por un electrodo positivo de hidróxido de níquel y, adicionalmente, una aleación de níquel y tierras raras como electrodo negativo, la cual permite absorber hidrógeno (Linden y Reddy, 2002, 29.2). La reacción global reversible que ocurre en la pila se muestra en la ecuación 1:
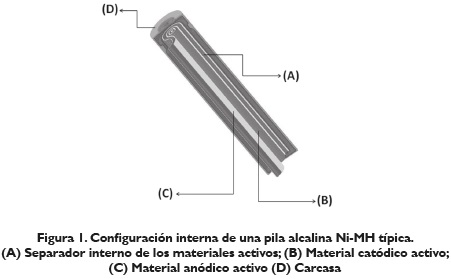
Donde M es el metal que absorbe hidrógeno y MH el hidruro metálico. En la figura 1 se observa la configuración interna de las pilas Ni-MH.
Una vez han cumplido su vida útil, las pilas y baterías gastadas deben someterse a un proceso de reciclaje, para prevenir que los metales pesados que contienen accedan a los ecosistemas y afecten la biota y, eventualmente la salud de los seres humanos. Es imperativo evitar que las pilas y baterías gastadas terminen su vida útil depositadas en basurales o vertederos poco controlados, en contacto directo con el agua y con los suelos, lo que facilitaría la migración de los metales pesados al medio natural (Bernard, 2011, 801). En este orden de ideas, son muchos los procesos planteados, sobre todo en países desarrollados, para tratar este tipo de desechos tecnológicos y extraer de manera factible los metales que contienen.
Existen dos grandes grupos de procesos recuperativos para extraer los metales contenidos en las pilas y baterías gastadas, a saber: procesos pirometalúrgicos y procesos hidrometalúrgicos. Los procesos pirometalúrgicos emplean altas temperaturas en reactores de gran escala, para extraer los metales contenidos a través de fusión o destilación. Los procesos patentados BATRECâ y CITRONâ son ejemplos de pirometalurgia aplicada para recuperación de zinc, presente en baterías gastadas por destilación. La destilación es también la base para la recuperación del cadmio; ejemplo de ello son los procesos patentados SNAM-SAVANâ, SAB-NIFEâ e INMETCOâ. Por su parte, los procesos basados en hidrometalurgia, tales como BATMIXâ, ZINCEXâ o RECUPYLâ, emplean soluciones de ácido sulfúrico como agente lixiviante, para recuperar los metales contenidos en las pilas y baterías gastadas (Nogueira y Margarido, 2007, 227; Fröhlich y Sewing, 1995, 27-30).
Todos estos procesos se encuentran instaurados en países industrializados, donde, además, existen políticas de retorno responsable y sistemas de gestión de residuos tecnológicos afianzados en la sociedad. En la actualidad, no obstante, la mayoría de los países latinoamericanos, incluyendo a Venezuela, no están en la misma situación, por lo que las pilas y baterías gastadas, así como muchos otros tipos de residuos electrónicos, no cuentan con una disposición final apropiada para prevenir la contaminación y mucho menos, para recuperar por medio de procesos de reciclaje los recursos metálicos que contienen. En el caso venezolano, resulta muy difícil establecer cuántas pilas se desechan por año. No obstante, estudios previos indican que de un lote de 2,5 toneladas de pilas gastadas recogidas entre 2011 y 2012 en la ciudad de Caracas las pilas del tipo Ni-MH constituyen el 2,7 % en peso. Dado su elevado contenido en metales valiosos, tales como níquel y tierras raras, resulta apropiado estudiar las posibilidades de recuperación metalúrgica de estos recursos (Moccia, 2013, 102; Zambrano, 2013, 101).
Con base en la realidad anterior, el presente trabajo tiene por finalidad caracterizar fisicoquímicamente los materiales activos de una muestra de 3,7 kg de pilas gastadas Ni-MH, de diferentes marcas y dimensiones, recopiladas en Venezuela. Los materiales activos (ánodo y cátodo) se sometieron luego a un proceso hidrometalúrgico de lixiviación con ácido clorhídrico al 14 %, con el fin de obtener un licor preñado en metales a partir del cual pudiesen precipitarse sales de níquel y tierras raras con potencial aplicabilidad industrial y, por tanto, con un mayor valor agregado. Finalmente, se presentan diagramas de flujo de proceso preliminares en los que se describen las diferentes etapas que involucraría el proceso semindustrial de valorización de este tipo de residuos tecnológicos.
Materiales y métodos
Caracterización de los materiales activos presentes en las pilas gastadas Ni-MH
Un lote de 3,7 kg de pilas Ni-MH desechadas fue desensamblado de manera manual, y todos sus componentes fueron pesados separadamente, para establecer, en promedio, el balance de masas de sus componentes. Los materiales activos, es decir, aquellos que están ubicados en el ánodo y el cátodo de las baterías, y que participan en las reacciones de óxido-reducción, se separaron manualmente y se secaron en estufa a 60 °C durante 24 horas. Posteriormente, dichos materiales se caracterizaron mediante análisis químico por espectrofotometría de absorción atómica (EAA) y determinación de fases cristalinas por medio de difracción de rayos X (DRX).
En el caso de EAA para la determinación de metales, los polvos anódicos o catódicos de las pilas (200 a 300 mg de muestra) se disolvieron en un beaker con una mezcla de 3 mL de HCl al 37 %, 3 mL de HNO3 al 65 % y 7 mL de agua destilada, calentada por 20 minutos a 50 °C, y dejada reposar hasta verificar la ausencia de sólidos en la digestión. En el caso del ánodo de las pilas, se debió realizar un filtrado para remover material carbonoso no disuelto. La solución se enrasó con agua destilada hasta 100 mL en un balón aforado, antes de efectuar el análisis de EAA con un equipo marca GBC modelo SAVANTAA. Para determinar el carbono presente en algunas de las muestras, se utilizó un carbonómetro LECO, modelo CS 600.
La técnica de DRX se empleó para la identificación cualitativa de las fases cristalográficas del material de trabajo anódico y catódico seco. El estudio se hizo siguiendo un barrido entre 2θ=10° hasta 2θ=90°. Se empleó la longitud de onda Kα del cobalto (1,78897 Å), un voltaje de 30 kV, una corriente de 22 mA y una velocidad de barrido 0,02° 2θ/s. Se empleó un difractómetro X Phillips PW1840. La caracterización se llevó a cabo por comparación con fichas del International Center of Difraction Data (ICDD).
Experimentos de valorización hidrometalúrgica de los materiales activos presentes en las pilas gastadas Ni-MH
Se pesaron 5,3 ± 0,1 g del material correspondiente (ánodo o cátodo) y dicha masa se agregó en un matraz de erlenmeyer de 250 mL con un volumen de solución lixiviante de 100 ± 1 mL ácido clorhídrico comercial con una concentración del 14 % m/m a temperatura ambiente, teniendo así una densidad de pulpa de 5 %. Posteriormente se procedió a colocar el matraz en agitación orbital constante a 230 RPM, usando un agitador orbital DigiSystem Laboratory Instruments Inc. modelo OS340C. La lixiviación de los materiales activos se efectuó durante 600 minutos, midiendo la cantidad de metales presentes en la disolución al final de dicho tiempo. Se cuantificó Ni, Co, Fe, Mn y Zn mediante EAA en los licores lixiviados, previa filtración de los contenidos del matraz.
Los licores preñados, obtenidos luego de 600 minutos de lixiviación, se trataron mediante precipitación con bicarbonato de sodio (NaHCO3), con el objetivo de obtener un lodo que contenga a los metales pesados presentes en el lixiviado. A tales fines, en un matraz erlenmeyer de 250 mL de capacidad cargado con 50 g de bicarbonato de sodio seco, se añadieron 100 mL de licor preñado a razón de 10 mL/minuto. El proceso de precipitación se llevó a cabo sobre una plancha calefactora, a 50 °C, bajo agitación magnética (200 RPM). Una vez añadido todo el licor preñado, se continuó la agitación durante 4 horas, luego de las cuales se centrifugó la muestra durante 10 minutos a 2500 RPM en una centrifugadora Eppendorf modelo 5430. Este procedimiento garantiza una fácil separación sólido-líquido, en la cual el sólido recolectado contiene todo el níquel inicialmente presente en el lixiviado, mientras que el líquido sobrenadante, luego de la centrifugación, se encuentra libre de níquel. El sólido recolectado no se sometió a lavado alguno y fue secado directamente durante 24 horas, a 100 °C, antes de someterlo a caracterización mediante EAA y DRX, de la misma manera como se describió en la sección 2.1.
Resultados
Caracterización de los materiales activos presentes en las pilas gastadas Ni-MH
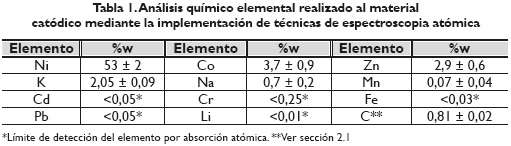
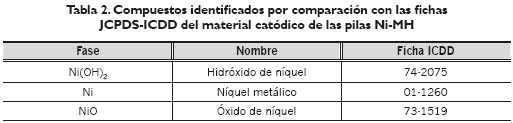
En esta sección se presentan los resultados obtenidos en el proceso de caracterización fisicoquímica de los materiales electródicos extraídos de las pilas Ni-MH estudiadas. En la tabla 1, se muestra el resumen de los análisis químicos cuantitativos elementales de los materiales catódicos procedentes de las pilas y baterías Ni-MH estudiadas. Los resultados están expresados en porcentaje en peso con respecto a la muestra analizada; para esta etapa de la caracterización se analizaron cinco sub-muestras. Por otra parte, en la tabla 2, se muestran los compuestos que fueron identificados por difracción de rayos X, mediante comparación con las fichas JCPDS-ICDD. Se destaca la presencia de compuestos de níquel, como es de esperarse. Cabe mencionar que los resultados obtenidos concuerdan con resultados expuestos por otros investigadores en trabajos similares (Assumpção et al, 2006, 1467).
Los materiales anódicos, por su parte, muestran un mayor contenido en metales, añadiendo a la presencia de níquel, metales estratégicos como el lantano y el cobalto, como se verifica en la tabla 3. Estos metales se encuentran formando aleaciones intermetálicas más o menos complejas, como lo atestigua el análisis de difracción de rayos x mostrado en la tabla 4. Se encuentra en estos materiales también la presencia de NaOH, que es el agente químico que conforma el electrolito de las baterías.
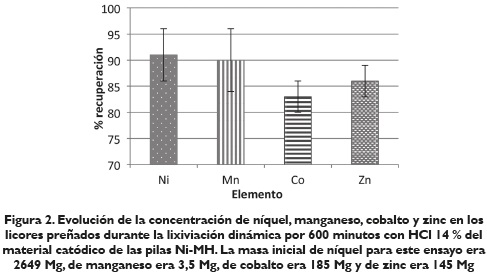
En la figura 2 se muestra que la lixiviación con HCl al 14 % permite extraer de los cátodos de las pilas Ni-MH más del 90 % del níquel contenido. Las recuperaciones de Mn, Co y Zn son, de igual manera, son elevadas, y superan, en todos los casos, el 80 %. En todo caso, debe considerarse que los cátodos de este tipo de pilas están conformados mayoritariamente por Ni, de forma que se corrobora que el procesamiento hidrometalúrgico genera licores muy ricos en Ni, de forma que la recuperación de este metal resulta interesante. Las elevadas recuperaciones de Ni están asociadas con la presencia en este electrodo de compuestos de Ni relativamente solubles en medio ácido, tales como óxido de níquel e hidróxido de níquel. En este medio, el Ni metálico es menos soluble; por tal razón, no todo el Ni se recupera con este proceso, en una primera lixiviación.
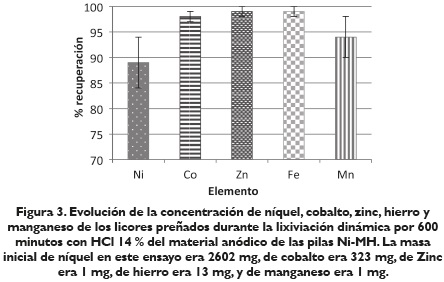
Por otro lado, en el procesamiento de los materiales anódicos, la figura 3 muestra que las recuperaciones de níquel son menores, debido a la presencia de una mayor cantidad de níquel en forma de aleaciones complejas, las cuales son más difíciles de disolver. Se recupera también la mayor parte del cobalto contenido en dichas pilas, el cual es considerado un metal de tipo estratégico, así como cantidades de hierro, zinc y manganeso, metales presentes de manera minoritaria en esta fracción de las pilas.
En la sección 3.3, se describirá el resultado de la precipitación de los metales a partir de las soluciones preñadas obtenidas en estos procesos.
Precipitación de los metales extraídos de las pilas y baterías gastadas Ni-MH luego de la lixiviación y caracterización de las sales precipitadas
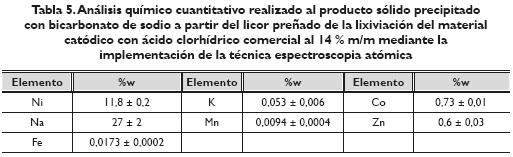
Para precipitar el licor extraído del proceso de lixiviación de los materiales electródicos con ácido clorhídrico al 14 % durante 600 minutos se utilizó bicarbonato de sodio (NaHCO3). Para un volumen de 100 mL de licor se utilizaron 50 g de bicarbonato de sodio para obtener una masa de sal metálica de aproximadamente 20 g en el caso del licor del material catódico, y de aproximadamente 28 g en el caso del licor del material anódico. Se realizó la caracterización mediante análisis químico por absorción atómica y difracción de rayos X de dichas sales. En la tabla 5 se muestran los resultados del análisis químico por absorción atómica de la sal precipitada a partir del licor obtenido de la lixiviación del material catódico; asimismo, en la tabla 6 se muestran los compuestos identificados a partir de difracción de rayos X.
Como se puede observar el elemento mayoritario de la sal precipitada en el proceso es el sodio, con 27 ± 2 % en peso. Dicho elemento está asociado al cloruro de sodio que se forma por la neutralización del ácido clorhídrico al añadir el bicarbonato. El producto tuvo, además, 11,8 ± 0,2 % en peso de níquel asociado, parcialmente, un carbonato de níquel y potasio hidratado. Los demás elementos estuvieron presentes en menos de 1 % en peso. No es descartable tampoco que parte del níquel y del resto de metales presentes en el lixiviado precipiten junto con el cloruro sódico, incorporándose a su red cristalina, bajo la forma de átomos sustitucionales. Debe destacarse que la técnica de difracción de rayos X tiene la limitación de que solo identifica fases cristalinas, de manera que cabe la posibilidad de que en el precipitado se encuentren presentes otras especies químicas amorfas o parcialmente amorfas, que no generen máximos de difracción y que, por tanto, no puedan ser plenamente identificadas. Esta posibilidad se ve corroborada por los análisis químicos presentados en la tabla 5, puesto que, si se realiza un balance estequiométrico de los metales presentes, atribuyéndolos, exclusivamente, a las fases identificadas, se concluye que no toda la muestra de sal precipitada puede estar formada, únicamente, por las fases que se lograron identificar en la tabla 6.
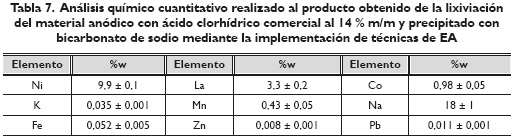
En las tablas 7 y 8 se encuentran los resultados del análisis químico por absorción atómica y los compuestos identificados por difracción de rayos X, respectivamente, del producto precipitado a partir del licor obtenido de la lixiviación del material anódico. Al igual que el producto caracterizado anteriormente, el elemento mayoritario es el sodio con 18 ± 1 % en peso asociado igualmente al cloruro de sodio proveniente de la reacción entre el bicarbonato de sodio y el ácido clorhídrico del licor. El níquel fue encontrado en un 9,9 ± 0,1 % en peso asociado a un carbonato de níquel y potasio hidratado, y se midió un 3,3 ± 0,2 % de lantano en la forma de hidroxicarbonato de lantano. Fue identificado hidroxicarbonato de cerio sin embargo no fue medido este elemento por absorción atómica, pues dicha técnica no es capaz de cuantificarlo. Los demás elementos medidos se encuentran en menos de 1 % en peso. En este caso, conviene también aclarar que es posible que la técnica de difracción de rayos x permita identificar todas las especies químicas presentes en la muestra, ya que sólo es posible detectar fases que se encuentren totalmente cristalizadas.
Discusión de resultados y propuesta de diagramas de flujo de procesos
Con base en los resultados presentados anteriormente, la vía de valorización hidrometalúrgica propuesta en este trabajo fue el tratamiento de los materiales electródicos con ácido muriático (ácido clorhídrico comercial al 14 % m/m) con una densidad de pulpa DE 5 % m/m, y posterior precipitación del licor preñado con bicarbonato de sodio comercial, con una relación 50 % m/v (g/mL). En las tablas 8 y 9, se resumen los compuestos determinados en los productos sólidos finales obtenidos a partir del material catódico y anódico, respectivamente, y sus posibles usos comerciales.
Finalmente uniendo posibles vías de comercialización para los compuestos presentados en las tablas 8 y 9, se debe tener especial atención a la industria cerámica y del vidrio como posibles lugares de colocación para este producto, debido a que son industrias donde compuestos similares tienen presencia; tampoco se debe descartar el mercado de los catalizadores donde se usan con frecuencia compuestos de níquel y lantano.
A continuación se hará un breve análisis sobre la posibilidad que tienen los compuestos sintetizados mediante la segunda vía de valorización, de tomar parte en el mercado de la industria del vidrio. La coloración tiene utilidad no solo en el aspecto estético, sino que también es fundamental en los vidrios o lentes polarizados y con protección UV. En el caso del níquel, la coloración que otorga al vidrio es influida por la alcalinidad del sistema. En el caso de los vidrios sódicos, toma un color gris con una tonalidad roja parduzca y los vidrios potásicos un color gris con tonalidades rojo azulado; igualmente este compuesto puede actuar como decolorante de otras tonalidades otorgadas por los iones ferrosos; para el caso de actuar como decolorante este se puede agregar en proporciones entre 0,0005 % a 0,0001 % en peso con respecto a la arena utilizada (Fernández, 2003, 302-309).
Para el caso de los elementos de tierras raras, estos también pueden actuar como decolorantes; en el caso del óxido de neodimio, este tiene la ventaja de actuar como decolorante pero no eliminar la transparencia del vidrio. Para el caso del cerio este posee múltiples aplicaciones en esta industria; quizá entre las de mayor importancia está su uso en la preparación de vidrios oftálmicos protectores de la radiación ultra violeta. El lantano aporta resistencia al vidrio por ataques de álkalis y se utiliza en vidrios especiales por sus propiedades de reflexión (Hammond, 2014, 4-20).
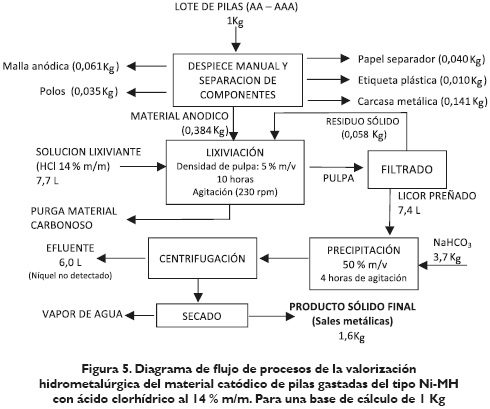
Para finalizar se presenta el diagrama de flujo de procesos, propuesto para la valorización de los materiales anódico y catódico; en primera instancia se presentará para el material anódico y luego para el material catódico. Esto se puede observar en las figuras 4 y 5, respectivamente.
Es importante aclarar que el residuo de la figura 4 está compuesto, principalmente, por carbón que no se disuelve durante la lixiviación, por lo cual, luego de extraer el resto de los metales allí contenidos, se debe retirar ese carbón del circuito (purga). En el caso de la figura 5, el material de residuo está compuesto principalmente por la malla catódica interna la cual no se disuelve durante el proceso de lixiviación, por lo cual se recomienda recircularla, aunque también puede ser interesante comercializarla por separado al ser una aleación compuesta principalmente por níquel. Con respecto al producto sólido final mostrado en la figura 4, el mismo está compuesto por los carbonatos y hidroxicarbonatos especificados en la tabla 9; de la misma manera, el producto sólido final mostrado en la figura 5 está compuesto por los carbonatos mostrados en la tabla 8.
Conclusiones
Con los resultados obtenidos en el presente trabajo se puede concluir que es posible utilizar un proceso hidrometalúrgico de varias etapas para la valorización de los metales contenidos en los materiales electródicos de las pilas Ni-MH, y obtener sales metálicas que pueden ser aprovechadas en otros procesos industriales. Esta vía presenta una manera de evitar el daño ambiental que implica desechar las pilas directamente en un depósito de basura municipal. Otra ventaja que presenta la utilización de usar esta vía de valorización es la posibilidad de tener una fuente alternativa de productos ricos en elementos como níquel y tierras raras, las cuales son de gran interés económico para ciertas industrias.
Agradecimientos
Este trabajo fue posible gracias al apoyo del Fondo Nacional de Ciencia, Tecnología e Innovación (FONACIT) de la República Bolivariana de Venezuela, mediante la subvención al proyecto número 2011000401 titulado: "Diseño de una planta piloto con tecnología sencilla y apropiable para el procesamiento de pilas y baterías gastadas con el objeto de reciclar Ni, Cd y otros metales".
Referencias bibliográficas
Assumpção, Daniel; Moura, Andrea; & Soares, Jorge. (2006). Spent NiMH Batteries: Characterization and Metal Recovery through Mechanical Processing. Journal of Power Sources, 160 (2), 1465-1470. [ Links ]
Bernard, Alfred. (2011). Renal and Neurological Effects Heavy Metals in the Environment, Universidad Católica de Lovaina. Bruselas. Bélgica. p.801. [ Links ]
Besenhard, Jürgen O. (1999). Handbook of Battery Materials. Alemania:Wiley-CVH. [ Links ]
Fernández, Jose María. (2003). El Vidrio. Madrid, España: Artegraf, S. A. [ Links ]
Fröhlich, Siegmund & Sewing, Dirk. (1995). The BATENUS Process for Recycling Mixed Battery Waste. Journal of Power Sources, 57 (1), 27-30. [ Links ]
Hammond, Charles R. (2014). Handbook of Chemistry and Physics. (95° Edición). USA: CRC press. [ Links ]
Linden, David; Reddy, & Thomas B. (2002). Handbook of Batteries. (3° Edición). USA: McGraw-Hill. [ Links ]
Moccia Paradisi, Alberto. (2013). Caracterización y Recuperación Sustentable de Materiales Contenidos en las Pilas Gastadas del Tipo Ni-Cd. Trabajo de Grado de la Universidad Simón Bolívar. Caracas; Venezuela. [ Links ]
Nogueira, Carlos A; & Margarido, Fernanda. (2012). Battery Recycling by Hydrometallurgy: Evaluation of Simultaneous Treatment of Several Cell Systems, en Energy Technology 2012: Carbon Dioxide Management and Other Technologies. USA: John Wiley & Sons, Inc. [ Links ]
Patnaik, Pradyot. (2002). Handbook of inorganic chemicals. USA: McGraw-Hill. [ Links ]
Zambrano Colmenares, Antonio. (2013). Caracterización y Valorización de los Metales Peligrosos Contenidos en los Materiales Electródicos de Pilas y Baterías Gastadas del Tipo Ni-MH, Trabajo de Grado de la Universidad Simón Bolívar. Caracas; Venezuela. [ Links ]