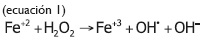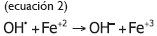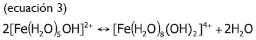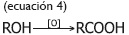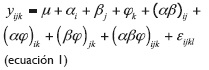Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Producción + Limpia
Print version ISSN 1909-0455
Rev. P+L vol.11 no.1 Caldas Jan./June 2016
Estudio preliminar de la cascarilla de arroz modificada y su efecto en la adsorción de Cr(VI) en solución*
Preliminary study of modified rice husk and its effect on the adsorption of Cr(VI) in solution
Estudo preliminar da casca de arroz modificada e seu efeito na adsorção de Cr(VI) em solução
Gloria María Doria Herrera**, Gloria Cristina Valencia Uribe***, Angelina Hormaza Anaguano****, Darío Gallego Suárez*****
* Artículo original derivado del proyecto de investigación "Apoyo para la dotación del Nuevo Laboratorio de Química Experimental de la Escuela de Química y su asociación con el Área de Espectroscopia Láser del Laboratorio de Óptica de la Escuela de Física, en la Facultad de Ciencias. (2008-2009). Dirección de Investigación de la Universidad Nacional, sede Medellín.
** Estudiante de Doctorado en Ingeniería Ambiental. Grupo GDCON. Universidad de Antioquia, Medellín, Colombia. E-mail: gloria.doria@udea.edu.co.
*** Doctora en Química, magister en Ciencias Químicas. Universidad Nacional de Colombia - Sede Medellín, Colombia - Facultad de Ciencias - Escuela de Química. GIAFOT gcvalenc@unal.edu.co.
**** Química, magister en Química Orgánica y doctora en Ciencias Químicas. Universidad Nacional de Colombia - Sede Medellín, Colombia - Facultad de Ciencias - Escuela de Química. SIRYTCOR. ahormaza@unal.edu.co.
***** Ingeniero Químico y magister en Ingeniería Ambiental. Universidad Nacional de Colombia - Sede Medellín, Colombia. Facultad de Minas - Escuela de Procesos. Medellín, Colombia. dgallego@unal.edu.co.
Autor correspondencia: Gloria María Doria Herrera E-mail: gloria.doria@udea.edu.co; gloria.doria83@gmail.com.
Artículo recibido: 26/01/2016; Artículo aprobado: 20/05/2016
Resumen
Introducción. Se ha reportado estudios que aseguran que la cascarilla de arroz tiene una buena capacidad adsortiva en solución acuosa para la remoción de Cr(VI). Por otro lado, el reactivo de Fenton conduce a la formación de radicales hidroxilos, considerados especies altamente oxidantes lo cual ha permitido su amplia aplicación para el tratamiento de aguas. En el caso de la cascarilla de arroz, desecho de la agroindustria, es considerado un problema medioambiental debido a su acumulación, sin embargo, estos residuos poseen grandes cantidades de lignina, celulosa, hemicelulosa y óxidos de silicio, por ello es considerado un adsorbente natural eficaz para la remoción de metales pesados. La modificación química de la superficie de estos materiales aumenta la capacidad adsortiva de metales en solución. Objetivo. Determinar las condiciones para la reacción de modificación de la cascarilla de arroz con el reactivo de Fenton y establecer el efecto sobre la remoción de Cr(VI) en solución acuosa previo y posterior a la modificación. Materiales y métodos. Se analizó el efecto de variables como el pH inicial, relación [Fe+2]/ [H2O2], y tiempo de los reaccionantes, para establecer las mejores condiciones para la modificación. Posteriormente, se realizó un análisis factorial 2k con las variables concentración inicial del metal (C), acidez del medio (pH) y dosificación del adsorbente (D) para establecer los cambios en términos de porcentaje de remoción. Resultados. Se evidenció que a menor dosis de contaminante utilizada (0.7 ppm) los porcentajes de remoción alcanzaron un 90 % tanto en la cascarilla modificada como en la nativa. Conclusiones. En esta investigación, se demostró la modificación estructural de la cascarilla de arroz con el reactivo de Fenton y al incrementar la dosis de Cr(VI) se reduce el porcentaje de remoción, encontrando que la concentración del Cr(VI) es una variable significativa en la remoción del metal en solución, contrario a ello, la dosificación del adsorbente en el rango utilizado, no es una variable significativa en el modelo obtenido.
Palabras clave: cascarilla de arroz, espectrofotometría UV-Visible, Fenton, modificación estructural, diseño factorial. 2k.
Abstract
Introduction. There are several studies that affirm that rice husk has a good adsorption capacity in an aqueous solution for removing Cr(VI). On the other hand, the Fenton reagent leads to the formation of hydroxyl radicals, considered as highly oxidant species, and this has brought their wide application in water treatments. Concerning the rice husk, a waste from agricultural industries, it is regarded as an environmental problem given its accumulation, but this waste contains a lot of lignin, cellulose, hemicellulose and silicon oxides and, therefore, it is an efficient natural adsorbent to remove heavy metals. The chemical modification of these materials´ surfaces increases the adsorption capacity of metals in solutions. Objective. Determine the conditions for the modification reaction of rice husk with the Fenton reagent and establish the effect on the removal of Cr(VI) in aqueous solution before and after the modification. Materials and methods. The effect of variables such as initial pH, [Fe+2]/[H2O2] ratio and time of the reactants were analyzed in order to establish the best conditions for the modification. Then, a 2k factorial analysis was performed with the initial metal concentration (C), acidity of the medium (pH) and adsorbent´s dosage (D) variables, in order to establish the changes in terms of removal percentages. Results. It was demonstrated that with a lower dose of the contaminant (0.7 ppm), the removal percentages reached 90% in both the modified and the native husks. Conclusions. This research work demonstrated the structural modification of rice husk and the Fenton reagent and also demonstrated that, as the Cr(VI) is increased, the removal percentage is lower. Therefore, the Cr(VI) concentration is a significant variable in the metals´ removal in a solution and, the other way around, the dose of the adsorbent in the ratio used is not a significant variable in the model obtained.
Key words: rice husk, spectrophotometry, UV-Visible, Fenton, structural modification, 2k, factorial design.
Resumo
Introdução. Se há reportado estudos que asseguram que a casca de arroz tem uma boa capacidade adsortiva em solução aquosa para a remoção de Cr(VI). Por outro lado, o reativo de Fenton conduz à formação de radicais hidroxilos, considerados espécies altamente oxidantes o qual há permitido sua amplia aplicação para o tratamento de águas. No caso da casca de arroz, resíduo da agroindústria, é considerado um problema meio-ambiental devido a sua acumulação, mas, estes resíduos possuem grandes quantidades de lignina, celulosa, hemicelulosa e óxidos de silício, por isto é considerado um adsorvente natural eficaz para a remoção de metais pesados. A modificação química da superfície destes materiais aumenta a capacidade adsortiva de metais em solução. Objetivo. Determinar as condições para a reação de modificação da casca de arroz com o reativo de Fenton e estabelecer o efeito sobre a remoção de Cr(VI) em solução aquosa prévio e posterior à modificação. Materiais e métodos. Se analisou o efeito de variáveis como o pH inicial, relação [Fe+2]/[H2O2], e tempo dos reagentes, para estabelecer as melhores condições para a modificação. Posteriormente, se realizou uma análise fatorial 2k com as variáveis concentração inicial do metal (C), acidez do meio (pH) e dose do adsorvente (D) para estabelecer as mudanças em termos de porcentagem de remoção. Resultados. Se evidenciou que a menor dose de contaminante utilizada (0.7 ppm) as porcentagens de remoção alcançaram um 90 % tanto na casca modificada como na nativa. Conclusões. Nesta investigação, se demostrou a modificação estrutural da casca de arroz com o reativo de Fenton e ao incrementar a dose de Cr(VI) se reduz a porcentagem de remoção, encontrando que a concentração do Cr(VI) é uma variável significativa na remoção do metal em solução, contrário a isto, a dose do adsorvente na faixa utilizada, não é uma variável significativa no modelo obtido.
Palavras chave: casca de arroz, espectrofotometria UV-Visível, Fenton, modificação estrutural, desenho fatorial. 2k.
Introducción
Frente a la problemática de contaminación de aguas superficiales con metales pesados se han diseñado metodologías de tratamiento, dentro de las que se destacan las fisicoquímicas y biológicas, sin embargo, éstas pueden presentar inconvenientes por generación de lodos activos, remociones incompletas y altos costos, entre otros (Wan Ngah y Hanafiah, 2008, Ma, Liu, Anderson y Chang, 2015, Gupta, Ali, 2004). Entre los métodos físicos en el tratamiento de aguas, la adsorción es una metodología efectiva por los resultados satisfactorios obtenidos, en el que se utiliza por ejemplo el carbón activado (Argun, Dursun, Ozdemir, y Karatas, 2007, Di Natale, Erto, Lancia y Musmarra, 2014), sin embargo, su costo elevado motiva la búsqueda de otro tipo de materiales que brinden propiedades adsortivas eficientes para la remoción de contaminantes. En este contexto, el radical hidroxilo, especie con potencial redox de 2.8 produciéndose tal como se explica a continuación (Ecuación 1) (Neyens y Baeyens, 2006, Asghar, Abdul Raman y Wan Daud, 2015):
Para que esta reacción ocurra eficientemente se debe realizar a pH ≤ 3.0, debido a que, a pH mayores, se da una oxidación del Fe(II) como se muestra en la Ecuación 3, formando complejos que no propician la oxidación. El radical hidroxilo (OH•) reacciona con la materia orgánica (asociada a la composición del residuo agroindustrial) provocando la oxidación progresiva y la formación de ácidos carboxílicos, tal como se muestra en las Ecuaciones 3 y 4:
Con el propósito de aprovechar los residuos agroindustriales, se han realizado estudios previos acerca de las propiedades de estos materiales como adsorbente de metales en solución (Wang, Li y Sun, 2008, Wong, Lee, Low y Haron, 2003, Wong et al., 2003; Kumar y Bandyopadhyay, 2006, Mohanty, Jha, Meikap y Biswas, 2005, Rangabhashiyam y Selvaraju, 2015a, Rangabhashiyam y Selvaraju, 2015b). Así mismo, un estudio reportado por Argun y Dursun, (2008) usando aserrín de pino modificado con reactivo de Fenton para la remoción de Cd(II) demostró que al realizar modificaciones estructurales se aumentaba la eficiencia hasta en un 97 %. En un estudio posterior se simuló un agua residual con Cd(II) y del Pb(II), se obtuvieron porcentajes de remoción con aserrín de 54 % y 60 %, y luego de la modificación alcanzaron porcentajes de remoción del 89 % y 91 % respectivamente (Argun y Dursun, 2008).
El estudio realizado por Bansal, Garg, Singh y Garg (2009) evaluó si el tratamiento químico (ebullición con formaldehido) de la cascarilla de arroz generaba mejoras como adsorbente en los porcentajes de remoción de Cr(VI), concluye que la cascarilla de forma natural es capaz de remover estos iones en solución gracias a la presencia de grandes cantidades de óxido de silicio y de lignina presentes en el material (Arcosa, Pintob, Enrique y Páeza, 2007) pero al tratar químicamente la cascarilla se obtuvieron mejoras en las remociones, pasando de un 71 % a un 76 % de remoción de Cr(VI) en solución.
En esta investigación, se planteó la hipótesis que, al modificar químicamente la superficie de la cascarilla de arroz como material adsorbente, se aumentaría la remoción de Cr(VI) presente en efluentes contaminados. Para comprobar esta hipótesis, se hizo un estudio preliminar para determinar las mejores condiciones que permiten la reacción de modificación, luego se establecieron las variables pH, concentración del contaminante y dosis del adsorbente apoyados en un diseño factorial 2k para determinar el efecto sobre la remoción, con miras a la disminución del número de experimentos manteniendo la validez estadística.
Materiales y métodos
Preparación del material adsorbente
Se realizó pretratamiento de la cascarilla de arroz proveniente de la región de Córdoba, que incluyó lavado con agua, secado, molienda y tamizado (Doria, Hormaza y Gallego, 2011) y de cuyo análisis preliminar se observó mejor absorción con tamaños de partícula < 500 µm. Este material se identifica como cascarilla natural.
Modificación química del material adsorbente
En la modificación con reactivo tipo Fenton se utilizó un pH de 3.0, como se recomienda en la literatura (Bansal et al., 2009). Se realizaron ensayos con diferentes proporciones [Fe+2]/ [H2O2], de 0.001, 0.005 y 0.01, respectivamente; para la proporción [Fe+2]/[H2O2]=0.01 se empleó una solución sulfato de hierro (II) de 10 ppm y una solución de peróxido de hidrogeno a 10.000 ppm. Para la segunda proporción de [Fe+2]/ [H2O2]=0.05 se preparó una solución de sulfato de hierro (II) a 50 ppm y solución de H2O2 a 10.000 ppm y finalmente, para la proporción de [Fe+2]/[H2O2]=0.1 se adicionó una solución de sulfato de hierro (II) a 100 ppm y una solución de H2O2 a la misma concentración anteriormente mencionada. Para la reacción de modificación, se adicionaron 2.5 g de cascarilla de arroz nativa a erlenmeyers que contenían 25 mL del reactivo de Fenton y se sometió a agitación continua (127 ppm), midiendo cada 120 min el cambio en el espectro de absorción UV-Vis (Espectrofotómetro Perkin Elmer Lambda 35), con el propósito de monitorear la modificación. Posteriormente, las muestras se filtraron por gravedad (con papel Whatman número 40) y se lavaron con agua destilada/desionizada cinco veces. Finalmente, el adsorbente transformado se sometió a secado a 85 °C por 24 horas para luego depositarse en frascos plásticos debidamente rotulados.
Test de adsorción
Entre los procedimientos estadísticos, el diseño factorial es empleado para reducir el número total de experimentos y lograr la mejor optimización del sistema; esta metodología permite el estudio simultáneo de los efectos de múltiples factores y brinda la optimización de un proceso particular. Además, determina qué condiciones tienen los efectos importantes en una superficie de respuesta, así como la influencia de un parámetro que varía con el nivel de los otros.Las herramientas estadísticas en las que se apoya este diseño incluyen el análisis de varianza, el cual sirve para comparar que tan significativa es la dispersión de un conjunto de datos numéricos con respecto a otro; el test t-Student; la regresión lineal y el test F, los cuales permiten definir la variable más influyente en la eficiencia de remoción del metal. En particular, para esta investigación, se escogió el diseño factorial 23 porque dentro de sus notables ventajas, es una metodología capaz de mostrar los cambios que le ocurren a todas las variables de interés al mismo tiempo; para dicho diseño se utilizó el paquete estadístico R para realizar el diseño se escogieron las variables pH inicial, dosificación de adsorbente, la concentración inicial del metal y como variable de respuesta la eficiencia del proceso de adsorción (porcentaje de remoción) bajo sistema discontinuo tanto para la cascarilla natural como la cascarilla modificada.
Luego de la obtención del material modificado, éste se utilizó para llevar a cabo ensayos previstos de remoción del Cr(VI), con el que se evaluó la influencia del pH, dosificación del adsorbente en concentración del metal, teniendo como variables fijas el volumen de solución de 25 mL, tamaño de partícula seleccionado fue de > 500µm, la temperatura a 21 °C y el tiempo de contacto a 6 horas, analizados a través de un diseño factorial 2k los tres factores con dos niveles (Argun y Dursun, 2008), se seleccionan tal como se evidencia en la Tabla 1:
Resultados
Efecto de la relación de [Fe+2]/[H2O2] , pH y tiempo de reacción
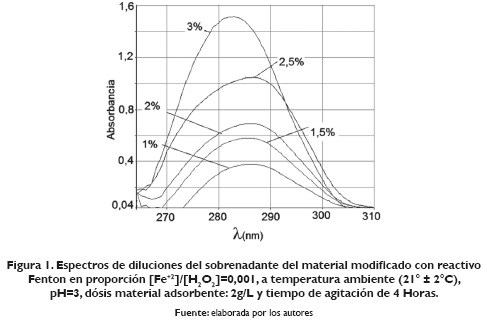
Debido a que el pH se ha reportado como una variable crítica en la reacción de Fenton, se procedió a fijar el pH en un valor de 3. Del análisis preliminar para determinar la relación de [Fe+2]/[H2O2], tomando como referencia valores menores a 0.1 (Neyens y Baeyens, 2006); por ello se utilizaron proporciones de 0.001, 0.005 y 0.01. En los tres casos se realiza seguimiento del cambio de absorción a 282 nm para el sobrenadante de la cascarilla modificada, para ello se realizaron curvas de calibración para determinar la absorbancia es proporcional al porcentaje de dilución. En la Figura 1 se muestra el espectro obtenido desde diferentes diluciones acuosas para uno de los experimentos.
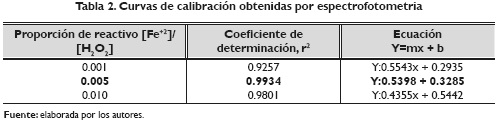
En la Tabla 2 se muestran las ecuaciones de las curvas de dilución obtenidas con el objeto de poder determinar una porción lineal susceptible a cuantificar el complejo formado, esta linealidad se obtuvo con factores de dilución hasta de un 3 % V/V demostrando un buen coeficiente de determinación.
Es oportuno mencionar que la selección del tamaño de partícula, se asocia a ensayos univariados. De igual forma se realizaron test de adsorción tal como se evidencia en la Tabla 3, los cuales permitieron escoger el tiempo de reacción, pH y proporción de los reactivos más favorable para la modificación.
Concentración= 3 mg/L; dosis= 0.1g/L; pH: 1; Velocidad de agitación: 127 rpm; temperatura 21° ± 2°C.; tiempo de agitación: 24 Horas
Propiedades del material modificado
Estudios reportados previamente y que incluyen análisis de espectroscopia infrarroja con reflectancia difusa (DRIFT), microscopia electrónica de barrido (SEM), análisis termogravimétrico (TGA), análisis bromatológico, permitieron evidenciar la modificación del material modificado tras el tratamiento con reactivo tipo Fenton (Doria, Hormaza y Gallego, 2013).
En el análisis espectroscópico, se observan cambios en la intensidad de algunas de las bandas principales en IR y que incluyen las vibraciones alrededor 3370 cm-1 correspondiente al enlace O-H, las del enlace C-H alifático entre 2.900 - 3.000 cm-1, las vibraciones asociadas al enlace C=C anillo aromático entre 1.490 y 1.617 cm-1, y finalmente, las bandas del enlace C-O alrededor de 1000 cm-1 y la banda del grupo C=O en 1.28 cm-1. Específicamente, se observó el aumento en la intensidad de la banda correspondiente al grupo C=O, luego de efectuada la modificación, así como su desplazamiento a un número de onda menor, después de efectuada la retención del Cr(VI), lo cual se asocia a la coordinación entre el oxígeno del carbonilo y el metal.
Ensayos de adsorción
Los ensayos de adsorción de metales como el Cr(VI), se han analizado aplicando el método univariado y el análisis de varianza (ANDEVA), los cuales pese a la posible aplicación de nuevos modelos estadísticos, siguen teniendo validez (Rocha, Zaia, Alfaya y Alfaya, 2009). No obstante, su principal falencia radica en la imposibilidad de determinar la interacción de las variables, así como definir cuál es la variable que genera mayores cambios. El diseño estadístico factorial, por el contrario, ofrece correlación de todas las variables de un experimento. Para el desarrollo de esta investigación se analiza el efecto de estos tres factores con dos niveles con relación al mejor porcentaje de remoción del metal en solución.
Los tres factores escogidos en la elaboración del diseño se muestran en la Tabla 1 pH del medio (x1), dosificación del adsorbente (x2) y concentración inicial del metal (x3). Los niveles seleccionados para el diseño van de la mano con los ensayos univariados realizados con anterioridad (Doria et al., 2011). En el caso particular del intervalo seleccionado para el factor x3, éste se realiza considerando el segmento lineal en las curvas de calibración, y está en consonancia con la Resolución 0631 del 2015 (Ministerio del Medio Ambiente, 2015), que establece como límite permisible para el vertimiento de cromo en aguas superficiales y a los sistemas de alcantarillado público con una concentración hasta de 0.50 ppm para el Cr(VI), por lo que este proceso de cuantificación puede ser aplicado. En el diseño 2k propuesto, se tomaron para cada una de los tres factores dos niveles.
En la Tabla 4 se presenta el porcentaje de remoción Cr(VI), cuyo seguimiento se realizó por espectrofotometría UV-Vis, a través de la absorbancia a 540 nm del complejo formado entre el Cr(VI) con 1,5-difenilcarbazida, como medida proporcional a la concentración del metal en solución (Doria, Hormaza y Paz, 2013). Se observa de forma general la mayor remoción en los experimentos 1, 2, 6 y 8, que tienen en común la menor concentración de Cr(VI) evaluada, de 0.7 ppm. En este grupo, a diferencia de la entrada 6 en la que se observó menor porcentaje de remoción del metal al utilizar la cascarilla modificada en la dosis inferior ensayada de 0,50 g/L, los otros tres experimentos presentan variaciones en los resultados entre la cascarilla nativa y la modificada, que no superan el 2 %. Por lo anterior, no sólo se evidencia en general una excelente capacidad de la cascarilla nativa de arroz para la remoción del Cr(VI) en concentraciones cercanas a los 0.7 ppm del metal, sino que también puede deducirse que el efecto de la modificación con el reactivo de Fenton no ofrece mejoras sustanciales de la capacidad adsortivas de este material.
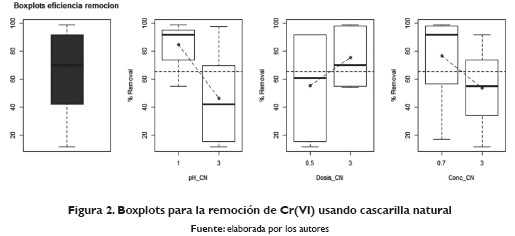
Al realizar el análisis descriptivo de los datos que se muestran en la Figura 2, específicamente los Boxplots del proceso de remoción de Cr(VI) usando la cascarilla natural, se evidencia que los valores con respecto a la mediana muestra una dispersión hacia valores más bajos de remoción, es decir, a más bajas concentraciones es donde evidencian que los datos están más dispersos con relación a la totalidad de los datos, destacando que los valores de forma preliminar muestran normalidad. Al analizar cada factor de forma individual se evidencia que para la cascarilla natural con respecto a la variable pH, teniendo mayor remoción a pH bajos, el incremento en la dosificación conduce a un aumento en la remoción y para la concentración inicial la remoción se ve ligeramente disminuida.
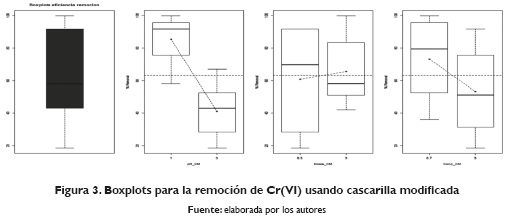
Por otro lado, para la cascarilla modificada el otro lado, al aumentar la dosificación, se aumenta Boxplots del experimento que se muestra en levemente la remoción y a mayor concentración la Figura 3, a nivel general indica que la mayor inicial, se disminuye la remoción. De forma inicial dispersión está a porcentajes de remoción más se muestra que la variable pH genera un efecto bajas, similar al comportamiento de la cascarilla significativo en la remoción de este metal en natural, la remoción aumenta a menor pH; por solución.
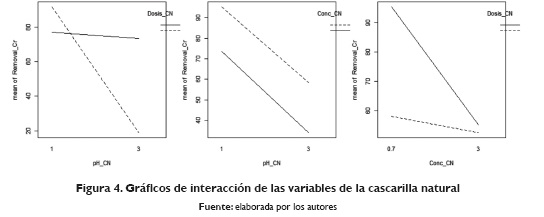
Otro aspecto significativo a analizar en el experimento son los gráficos de interacción, los cuales permiten mostrar la correlación entre las variables analizadas y la significancia evidente en el análisis de varianza a través del p-valor. Al realizar el análisis gráfico para la cascarilla natural mostrada en la Figura 4, la interacción entre el pH y la dosificación muestra una fuerte interacción, la cual no es tan evidente entre la concentración y la dosificación, aspectos que serán verificados al analizar y validar el modelo.
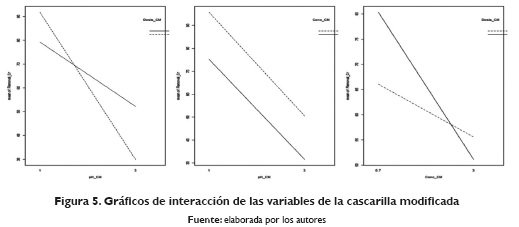
En el caso de las interacciones entre los factores para la cascarilla modificada, se indica en la Figura 5, un comportamiento similar al de la cascarilla natural, en el que el pH genera un efecto importante en la eficiencia de la remoción, evidente en la interacción con la dosificación de adsorbente, dado que al aumentar la dosificación y el pH se disminuye la eficiencia de la remoción. En el caso de la interacción entre la concentración inicial del metal y la dosificación del adsorbente, ocurre un efecto parecido, la eficiencia de la remoción disminuye. En ambos casos es coherente este comportamiento, en el caso del pH al acidificarse el medio, el adsorbente tiene más posibilidades de adsorber el metal y el caso del efecto asociado a la concentración con relación a la dosificación, al tener mayor cantidad del metal, los posibles sitios de adsorción se saturan por lo que la eficiencia disminuye.
El modelo matemático empleado para este experimento es la :
Donde

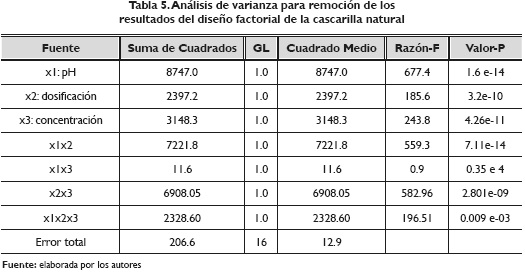
Para comprobar si lo planteado en el análisis preliminar en el que los datos poseen una normalidad e independencia en los errores y que además el modelo factorial si es adecuado para el experimento, se realiza un análisis de varianza (ANDEVA) para demostrar que las varianzas son homogéneas entre sí, apoyadas por el estadístico coeficiente de determinación (R2). El análisis de varianza (ANDEVA) para la cascarilla natural se reporta en la Tabla 5:
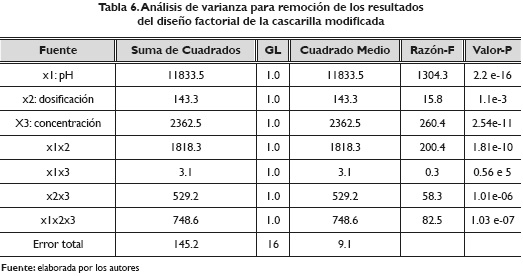
De igual forma se analizaron los datos para la cascarilla modificada, los que se reportan en la Tabla 6. Para la cascarilla natural como para la modificada, se evidencia que la interacción x 1 x 3 es decir pH: concentración con un valor p mayor de 0.05, demuestra que esta interacción en el modelo no es significativa, es decir, puede ser omitida dentro de la ecuación que describa el modelo, además el estadístico R2 ajustado para el modelo lineal es de 0.99 por lo que no es necesario aplicar nuevos procedimientos.
Los modelos de predicción para ambos experimentos son:
Para la cascarilla natural:
%R : 91.74 - 67.20 x1 + 6.813 x2 + 2.69 e-14 x3 + 60.81 x1 x2 - 43.04 x2 x3 + 17.15 x1 x2 x3
Para la cascarilla modificada:
% R: 91.74 - 51.37 x1 + 8.040 x2 + 1.42 e-14 x3 + 12.48 x1 x2 - 41.12 x2 x3 + 44.68 x1 x2 x3
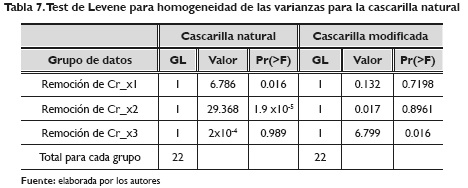
El ANDEVA conduce a la validación del modelo y al análisis de los supuestos, partiendo que los residuales poseen una distribución normal, para ello se aplica el test de shapiro wilks, para los experimentos de la cascarilla natural y la cascarilla modificada son en ambos casos w=0.7564 con un p–valor de 6.194 x 10-05 por lo que no se acepta que los residuales poseen normalidad, esto puede deberse a los puntos por fuera o también denominados "outliers" en el análisis, por lo que se puede plantear una transformación de potencia que no es el objetivo de esta investigación. En el caso de la homogeneidad de las varianzas se aplica el test de Levene, los resultados para la cascarilla natural son reportados en la Tabla 7, los cuales evidencian que los residuales poseen homogeneidad entre las varianzas.
Finalmente, para analizar la independencia de los errores, se acude al test de Durbin- Watson, con el cual se busca explicar que no haya errores asociados a la planeación y ejecución del experimento. En el caso de la cascarilla natural se obtuvo un DW = 2.3132, p-valor = 0.4104 y en el caso de la cascarilla modificada DW = 2.3415, p-valor = 0.4574, señalado que los errores poseen independencia.
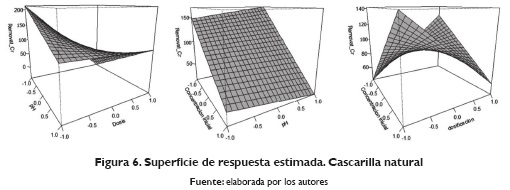
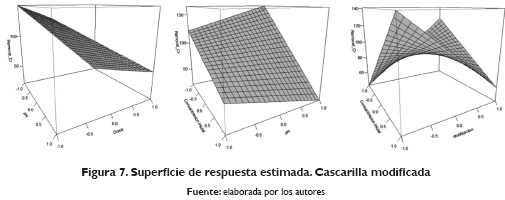
Para obtener los gráficos cúbicos de los modelos obtenidos para la cascarilla natural (Figura 6) y la cascarilla modificada (Figura 7) sí se observa un comportamiento hiperplanar por lo que es posible asegurar que el modelo factorial es útil para poder explicar el comportamiento del diseño. Al analizar el gráfico de la cascarilla natural, se muestran curvaturas en las interacciones dosis: pH y concentración inicial: dosificación de adsorbente; en el caso de la cascarilla modificada, se evidencia que, de las tres interacciones, solo la relación dosificación de adsorbente: concentración inicial, muestran una curvatura, por lo que es necesario ubicar más puntos dentro de las regiones experimentales para poder optimizar el diseño. Una de las estrategias más utilizadas en este tipo de experimentos es el diseño de superficie de respuesta, en el cual se puede aplicar el diseño de Box-Behnken o el diseño de composición central, siempre y cuando se asegure la toma de datos en las regiones curveadas y así proceder a optimizar (Gutiérrez y De la vara, 2012).
Conclusiones
El diseño factorial propuesto para la adsorción de Cr(VI) utilizando cascarilla de arroz nativa y modificada mostró que las variables evaluadas fueron significativas; en ambos diseños experimentales se evidenció que las interacciones pH: dosificación y dosis: concentración tienen una incidencia en el comportamiento del modelo.
Las mejores condiciones de adsorción para la cascarilla modificada fueron a pH 1, dosificación de 3.0 g/L y una concentración inicial de 0.7 ppm, alcanzando porcentajes de remoción hasta de un 99,7 % en un tiempo de 360 minutos, señalando que este es un material promisorio para el tratamiento de efluentes contaminados con metales. No obstante, al comparar ambos resultados se evidencia que no hay diferencias significativas entre la cascarilla natural y modificada, esto se justifica gracias a la capacidad que tiene el ion cromato de formar oxoaniones capaces de generar reacciones de oxolación en solución, las cuales dependen del pH y la temperatura, sin embargo, seria interesante conocer un poco más sobre el mecanismo de retención del metal en la superficie del material, para la generación de nuevas investigaciones con miras a la aplicación para la remoción de otros metales. Los modelos matemáticos planteados para ambos diseños fueron adecuados, sin embargo, es interesante revisar en futuras investigaciones la toma de más información de la región experimental, que permita obtener la superficie de respuesta optimizada.
Agradecimientos
Los autores extienden sus agradecimientos a la Universidad Nacional de Colombia - Sede Medellín por el apoyo a través de la infraestructura del Laboratorio de Química Experimental, así como a la Dirección de Investigación de la Sede Medellín, DIME, por el financiamiento del proyecto Código 201010011038 y por el apoyo financiero a través del Programa de Jóvenes Investigadores e Innovadores de Colciencias 2009.
Referencias bibliográficas
Arcosa, C.; Pintob, D.; Enrique, J. y Páeza, R. (2007). La cascarilla de arroz como fuente de SiO2 Husk of rice as source of SiO2. Scielo. Org.Co, 7-20. Retrieved from http://www.scielo.org.co/scielo.php?pid=S012062302007000300001&script=sci_arttext. [ Links ]
Argun, M. y Dursun, S. (2008). A new approach to modification of natural adsorbent for heavy metal adsorption. Bioresource Technology, 99(7), 2516-2527. http://doi.org/10.1016/j.biortech.2007.04.037. [ Links ]
Argun, M.; Dursun, S.; Ozdemir, C. y Karatas, M. (2007). Heavy metal adsorption by modified oak sawdust: Thermodynamics and kinetics. Journal of Hazardous Materials, 141(1), 77-85. http://doi.org/10.1016/j.jhazmat.2006.06.095. [ Links ]
Asghar, A.; Abdul, A. y Wan, W. (2015). Advanced oxidation processes for in-situ production of hydrogen peroxide/hydroxyl radical for textile wastewater treatment: a review. Journal of Cleaner Production, 87, 826-838. http://doi.org/10.1016/j.jclepro.2014.09.010. [ Links ]
Bansal, M.; Garg, U.; Singh, D. y Garg, V. (2009). Removal of Cr(VI) from aqueous solutions using preconsumer processing agricultural waste: A case study of rice husk. Journal of Hazardous Materials, 162(1), 312-320. http://doi.org/10.1016/j.jhazmat.2008.05.037. [ Links ]
Di Natale, F.; Erto, A.; Lancia, A. y Musmarra, D. (2014). Equilibrium and dynamic study on hexavalent chromium adsorption onto activated carbon. Journal of Hazardous Materials, 281, 47-55. http://doi.org/10.1016/j.jhazmat.2014.07.072. [ Links ]
Doria, G.; Hormaza, A. y Gallego, D. (2011). Cascarilla de arroz: material alternativo y de bajo costo. Gestion Y Ambiente, 14(1), 73-84. [ Links ]
Doria, G.; Hormaza, A. y Gallego, D. (2013). Structural characterization of the husks from modified rice as an alternative absorbant and effective for the removal of Cr(VI) in solution. Revista de Investigacion Agraria Y Ambiental, 4(1), 21-29. [ Links ]
Doria, G.; Hormaza, A. y Paz, P. (2013). Estandarización de la difenilcarbazida como indicador y acomplejante en la identificación de cromo hexavalente-Cr (VI). Producción Más Limpia, 8(2), 9-20. Retrieved from http://www.scielo.org.co/scielo.php?pid=S190904552013000200002&script=sci_arttext. [ Links ]
Gupta, V. K. y Ali, I. (2004). Removal of lead and chromium from wastewater using bagasse fly ash - A sugar industry waste. Journal of Colloid and Interface Science, 271(2), 321-328. http://doi.org/10.1016/j.jcis.2003.11.007. [ Links ]
Gutierrez, H. y De la vara, R. (2012). Analisis y diseño de experimentos. [ Links ]
Kumar, U. y Bandyopadhyay, M. (2006). Sorption of cadmium from aqueous solution using pretreated rice husk. Bioresource Technology, 97(1), 104-109. http://doi.org/10.1016/j.biortech.2005.02.027. [ Links ]
Ma, X.; Liu, X.; Anderson, D. y Chang, P. (2015). Modification of porous starch for the adsorption of heavy metal ions from aqueous solution. Food Chemistry, 181, 133-139. http://doi.org/10.1016/j.foodchem.2015.02.089. [ Links ]
Ministerio del Medio Ambiente. (2015). Resolución_0631_marzo_2015. pdf. [ Links ]
Mohanty, K.; Jha, M.; Meikap, B. y Biswas, M. (2005). Removal of chromium (VI) from dilute aqueous solutions by activated carbon developed from Terminalia arjuna nuts activated with zinc chloride. Chemical Engineering Science, 60(11), 3049-3059. http://doi.org/10.1016/j.ces.2004.12.049. [ Links ]
Neyens, E. y Baeyens, J. (2006). A review of classic Fenton's peroxidation as an advanced oxidation technique E. Journal of Hazardous Materials, 44(1), 66-74. http://doi.org/10.1016/j.jhazmat.2008.05.027. [ Links ]
Rangabhashiyam, S. y Selvaraju, N. (2015a). Adsorptive remediation of hexavalent chromium from synthetic wastewater by a natural and ZnCl2 activated Sterculia guttata shell. Journal of Molecular Liquids, 207, 39-49. http://doi.org/10.1016/j.molliq.2015.03.018. [ Links ]
Rangabhashiyam, S. y Selvaraju, N. (2015b). Efficacy of unmodified and chemically modified Swietenia mahagoni shells for the removal of hexavalent chromium from simulated wastewater. Journal of Molecular Liquids, 209, 487-497. http://doi.org/10.1016/j.molliq.2015.06.033. [ Links ]
Rocha, C.; Zaia, D.; Alfaya, R. y Alfaya, A. (2009). Use of rice straw as biosorbent for removal of Cu(II), Zn(II), Cd(II) and Hg(II) ions in industrial effluents. Journal of Hazardous Materials, 166(1), 383-388. http://doi.org/10.1016/j.jhazmat.2008.11.074. [ Links ]
Wan Ngah, W. S., & Hanafiah, M. a K. M. (2008). Removal of heavy metal ions from wastewater by chemically modified plant wastes as adsorbents: A review. Bioresource Technology, 99(10), 3935-3948. http://doi.org/10.1016/j.biortech.2007.06.011. [ Links ]
Wang, X. S., Li, Z. Z., & Sun, C. (2008). Removal of Cr(VI) from aqueous solutions by lowcost biosorbents: Marine macroalgae and agricultural by-products. Journal of Hazardous Materials, 153(3), 1176-1184. http://doi.org/10.1016/j.jhazmat.2007.09.079. [ Links ]
Wong, K., Lee, C., Low, K., & Haron, M. (2003). Removal of Cu and Pb by tartaric acid modified rice husk from aqueous solutions. Chemosphere, 50(1), 23-28. http://doi.org/10.1016/S0045-6535(02)00598-2. [ Links ]