Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Producción + Limpia
Print version ISSN 1909-0455
Rev. P+L vol.11 no.2 Caldas July/Dec. 2016
https://doi.org/10.22507/pml.v11n2a12
DOI: http://dx.doi.org/10.22507/pml.v11n2a12
La cascarilla de arroz como una alternativa en procesos de descontaminación*
Rice husk as an alternative in decontamination processes
A casca de arroz como uma alternativa em processos de descontaminação
Oriana Llanos Páez**, Andrea Ríos Navarro***, César Augusto Jaramillo Páez****, Luis Fernando Rodríguez Herrera*****
* Artículo derivado del proyecto de investigación titulado "Evaluación de la cascarilla de arroz bajo diferentes estados de calcinación como material para la remoción de metales pesados presentes en aguas residuales", financiado por la Oficina de Investigaciones de la Universidad del Tolima y ejecutado entre enero de 2014 y diciembre de 2015.
** Bióloga, Universidad del Tolima, Facultad de Ciencias. Colombia. ollanosp@ut.edu.co.
*** Bióloga, Universidad del Tolima, Facultad de Ciencias. Colombia. ariosn@ut.edu.co.
**** Magister en Química, Docente Universidad del Tolima. Colombia. cajaramillopa@ut.edu.co.
***** Magister en Química, Docente Universidad del Tolima. Colombia.
Autor para correspondencia: Luis Fernando Rodríguez Herrera, email: lfrodriguezh@ut.edu.co
Artículo recibido: 11/7/2016; Artículo aprobado: 30/11/2016.
RESUMEN
El desarrollo industrial trae consigo graves consecuencias para el ambiente y la salud, debido a la generación de desechos tóxicos como resultado de sus procesos; estos desechos incluyen metales pesados que se vierten indiscriminadamente en los afluentes. Una alternativa de descontaminación incluye la utilización de residuos como la cascarilla de arroz que, gracias a características fisicoquímicas, promete ser un buen adsorbente de metales pesados. Se han realizado diversos estudios de adsorción variando parámetros como tamaño de partícula, pH, tiempo de contacto y concentración inicial del metal. Estas variables se deben controlar para garantizar una mayor eficiencia en el proceso.
Palabras clave: cascarilla de arroz, metales pesados, adsorción, descontaminación.
ABSTRACT
The development of industries has brought serious harm to the environment and health, due to the generation of toxic waste as a result of those industries' processes. This waste includes heavy metals that are indiscriminately poured on water bodies. A decontamination alternative includes the use of remains, such as rice husk, that, thanks to its physical-chemical characteristics, looks like a good adsorbent of heavy metals. Several adsorption studies have been made, varying parameters such as particle size, pH, contact time and initial concentration of metals. These variables must be controlled in order to guarantee a higher efficiency in the process.
Key words: rice husk, heavy metals, adsorption, decontamination.RESUMO
O desenvolvimento industrial traz consigo graves consequências para o ambiente e a saúde, devido à geração de resíduos tóxicos como resultado dos seus processos; estes resíduos incluem metais pesados que se despejam indiscriminadamente nos afluentes. Uma alternativa de descontaminação inclui a utilização de resíduos como a casca de arroz que, graças a características físico-químicas, promete ser um bom adsorvente de metais pesados. Se há realizado diversos estudos de adsorção variando parâmetros como tamanho de partícula, pH, tempo de contato e concentração inicial do metal. Estas variáveis se devem controlar para garantir uma maior eficiência
no processo.
Palavras chave: casca de arroz, metais pesados, adsorção, descontaminação.
INTRODUCCIÓN
El desarrollo industrial ha traído consecuencias desfavorables para el ambiente, debido a que los procesos industriales generan grandes cantidades de desechos tóxicos, entre los que se encuentran los metales pesados, los cuales se vierten a los afluentes de forma indiscriminada; ello ha provocado que al nivel mundial exista una preocupación para controlar y reducir las concentraciones de estos (Khalid, Ahmad, Toheed y Ahmed, 2000).
Las fuentes de metales pesados que generan el mayor riesgo de contaminación ambiental son las industrias de pintura, metalúrgica, minería, curtido, agroindustria, textiles, las cuales en su mayoría vierten sus desechos en cuerpos de agua (Akhtar, Iqbal, Kausar, Bhanger y Shaheen, 2010). Los metales pesados no se degradan y tienden a acumularse en los organismos vivos pasando a través de la cadena trófica, y en pequeñas concentraciones pueden causar graves enfermedades y desórdenes en el organismo (Chuah, Jumasiah, Azni, Katayon y Choong, 2005; Kumar y Bandyopadhyay, 2006).
Se ha determinado que los metales pesados son peligrosos para la salud humana ya que pueden llegar a causar severos daños en los riñones, el sistema nervioso, el sistema reproductivo, el hígado y el cerebro (Karnib, Kabbani, Holail y Olama, 2014; Naiya, Bhattacharya, Mandal y Das, 2009); también pueden causar cáncer en el tracto digestivo y en los pulmones, epigastria, diarrea severa y hemorragia, entre otros (Bansal, Garg, Singh y Garg, 2009). Además de causar daños a la salud humana también se pueden generar graves daños en el ambiente, especialmente en la fauna presente en los ecosistemas acuáticos (Bohli, Ouederni, Fiol y Villaescusa, 2015; Rocha et al., 2012; Rocha, Dias, Boufleur y Santos, 2014).
Existen diferentes metodologías para la eliminación de los metales pesados (tabla 1) clasificadas en tres categorías principalmente; químicas como intercambio iónico, precipitación electroquímica, electroflotación, oxidación, precipitación química, coagulación y floculación (Balsamo et al., ). Estas metodologías tienen limitaciones que radican en su alto costo de operación y en la generación de subproductos como lodos contaminantes (Ali, 2013; El-Shafey, 2007); una segunda categoría son métodos físicos como filtración por membrana (nanofiltración, ósmosis reversa, electrodiálisis); su corto tiempo de vida útil los convierte en un proceso poco atractivo para ser utilizado a gran escala (Ahmaruzzaman, 2011); por último están los métodos biológicos como la utilización de microorganismos como algas, levaduras, bacterias y hongos los cuales sirven para acumular y degradar diferentes contaminantes; sin embargo, requieren de grandes áreas para su ejecución, y se ven limitados por variaciones ambientales (Ahmaruzzaman, 2011).
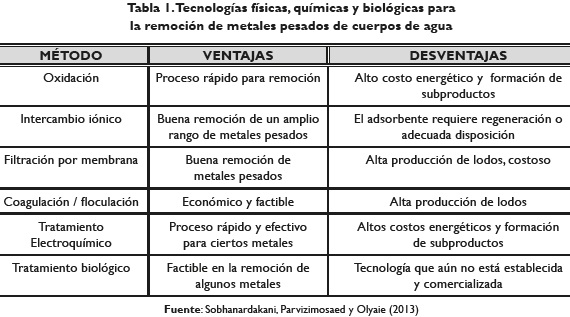
A partir de estos métodos, se han generado alternativas de bajo costo e impacto ambiental que reduzcan las concentraciones de metales pesados en los afluentes (Khan, Ibrahim y Subramaniam, 2004).
Tales alternativas involucran procesos de adsorción donde diversos materiales, producto de procesos agrícolas, han sido usados con el fin de remover contaminantes presentes en cuerpos de agua como bagazo de caña de azúcar (Ali, 2013; Mohan y Singh, 2002), cáscara de coco (Bhatnagar, Vilar, Botelho y Boaventura, 2010), aserrín (Yasemin y Zequi, 2007; Yu, Zhang, Shukla, Shukla y Dorris, 2000); unos de los más usados en remoción de metales pesados de cuerpos acuosos son los carbones activados (Bishnoi, Bajaj, Sharma y Gupta, 2004; Guo et al., 2003; Selvi, Pattabhi y Kadirvelu, 2001), que presentan dificultades para su preparación ya que requieren agentes que mejoren la remoción de material inorgánico, lo que puede aumentar su costo (Babel y Kurniawan, 2003); también hay residuos agrícolas que ofrecen un futuro prometedor en procesos de adsorción, como es el caso de la cascarilla de arroz que debido a sus propiedades fisicoquímicas se postula como un buen adsorbente de metales pesados (Wong, Lee, Low y Haron, 2003). Dentro de sus características se encuentra que cuenta con un área superficial de 270 m2/g aproximadamente (Malik, 2003); además, una vez calcinada presenta más del 90 % de óxido de silicio, el cual tiene tamaño fino y alta reactividad, compuesto al que se le atribuye gran capacidad de remoción de contaminantes, como metales pesados (Kurtis y Rodrígues, 2003).
Esta revisión pretende brindar un amplio panorama de la utilización de la cascarilla de arroz en procesos de remoción de metales pesados de cuerpos de agua contaminados por aquellos y los principales factores que intervienen en el proceso como pH, concentración de los metales, tiempo de contacto y tamaño de partícula del adsorbente, y así evidenciar una alternativa económica y de fácil aplicación para procesos de descontaminación.
CASCARILLA DE ARROZ
La producción mundial de arroz en el año 2015 ha sido aproximadamente 491 millones de toneladas, de las cuales la cascarilla representa entre 20 y 25 % de la producción total de arroz; se estima su cantidad en aproximadamente 123 millones de toneladas (FAO, 2016).
La producción de arroz mecanizado en Colombia es de aproximadamente 1.558.044 toneladas, de las cuales 389.511 corresponden a cascarilla (DANE, 2015); estas son cantidades apreciables de desechos que se producen a nivel nacional y que deben ser aprovechados eficientemente para reducir la contaminación por este residuo. Entre los usos que se le ha dado a la cascarilla se encuentran la producción de silicatos (Ahumada y Rodríguez-Páez, 2006; Arcos, Macíaz y Rodríguez-Páez, 2007) y biocombustibles (Álvarez, López, Amutio, Bilbao y Olazar, 2014), y como material para la producción de cemento puzolánico (Kurtis y Rodrígues, 2003; Romano y Rodrígues, 2008); otra alternativa es el uso como material adsorbente en procesos de remoción de contaminantes, con el fin de solucionar problemas de contaminación (Rodríguez, Salinas, Ríos y Vargas, 2012).
La cascarilla de arroz es un tejido vegetal lignocelulósico constituido por un 85 % de material orgánico, representado por celulosa, lignina, D-xilosa y pequeñas cantidades de D- galactosa (Krishnarao, Subrahmanyam y Kumar, 2001).
Cuando la cascarilla de arroz es sometida a altas temperaturas produce ceniza entre el 13 y 29 % del peso inicial, constituida principalmente por sílice entre un 87 y 97 % debido a que no se disocia al quemarse, y pequeñas cantidades de sales inorgánicas (Arcos et al., 2007; Valverde, Sarria y Monteagudo, 2007).
En un análisis próximo realizado en cuatro diferentes países y en diferentes variedades de arroz se evidencian valores similares para las características evaluadas (Carbón fijo, material volátil y ceniza) (Valverde et al.,2007).En promedio la cascarilla de arroz cuenta con un 64,30 % de material volátil, un 16,10 % de carbono fijo y un 19,54 % de ceniza; es en esta última donde se concentra el contenido de dióxido de sílice que supera el 90 %, y gracias a su fino tamaño y su alta reactividad ha sido utilizado en industrias como la del cemento (Kurtis y Rodrigues, 2003), como fuente para preparar compuestos a base de silicio (Krishnarao, Mahajan y Kumar, 1998) y zeolitas (Panpa y Jinawath, 2009); además, ha sido ampliamente utilizada en procesos de remoción de contaminantes como lo son los metales pesados y colorantes (Ajmal, Rao, Anwar, Ahmad y Ahmad, 2003; Bishnoi et al., 2004; Chandrasekhar y Pramada, 2006; Lakshmi, Srivastava, Mall y Lataye, 2009; Rodriguez et al., 2012).
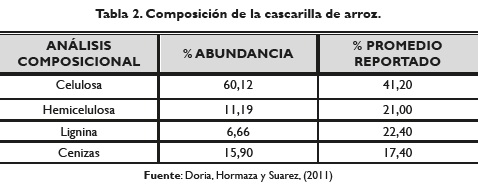
La tabla 2 muestra la composición general de la cascarilla de arroz, donde se evidencia una gran proporción de celulosa. Autores como Doria et al. (2011) le atribuyen la capacidad de adsorción de la cascarilla de arroz a los compuestos lignocelulósicos que posee.
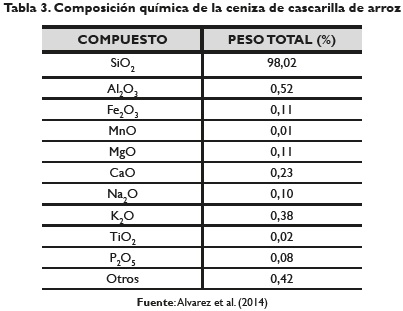
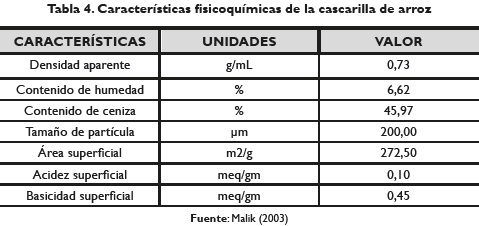
En el proceso de combustión, se genera una variedad de óxidos, dentro de los que se destaca el dióxido de silicio en una proporción del 98% (tabla 3). Adicionalmente la cascarilla tiene unas propiedades que le confieren su capacidad de adsorción como lo es su área superficial y el tamaño de partícula (tabla 4). Aprovechando y modificando estas características se podrían lograr altos porcentajes de remoción de metales pesados.
CASCARILLA DE ARROZ COMO MATERIAL ADSORBENTE DE METALES PESADOS
Debido a las características fisicoquímicas que presenta la cascarilla de arroz se ha postulado este residuo agroindustrial como un material viable y económico para la remoción de diferentes contaminantes como tintes y principalmente metales pesados (Khan et al., 2004; Akhtar, Bhanger, Iqbal y Hasany, 2006). El hecho de que sea un residuo de fácil manejo y acceso lo hace llamativo, puesto que usándolo en procesos de descontaminación se están solucionando dos problemas ambientales de forma directa, ya que se da uso y manejo a la cascarilla y se remueven contaminantes de gran impacto ambiental de los cuerpos de agua. Esto se evidencia en los múltiples estudios que se han desarrollado en este campo y con este material.
Debido a la alta toxicidad de los metales pesados, la investigación se ve enfocada en la remoción de estos, lo que ha sido demostrado en diferentes estudios, como el realizado por Bishnoi et al. (2004) sobre remoción de Cr (VI), usando cascarilla de arroz carbonizada a 300 °C y activada con alúmina; ellos encontraron que a pH ácidos (2-4) menor tamaño de partícula (0,30 mm), aumento en la dosis del adsorbente (0,60 -1,40 g/100 mL) y tiempo de contacto de 1 hora, se alcanzan porcentajes de remoción por encima del 95 %; en otro estudio para remover Cr (VI) realizado por Bansal et al. (2009) utilizando la cascarilla de arroz previamente hervida y tratada con formaldehido 1 %, tamaño de partícula de 0,30 mm, adsorbente de 0,20 g/100 mL, pH de 2-7, encontraron un porcentaje de remoción por encima del 70 %. En Colombia también se ha investigado acerca del uso de este material en remoción de Cr (VI) en sistemas acuosos; tal es el caso de Rodríguez et al. (2012), quienes prepararon tres diferentes materiales a partir de la cascarilla de arroz, los cuales consistieron en calcinar la cascarilla a 450 °C para obtener ceniza, cascarilla de arroz activada con H3PO4 y ceniza activada con NaOH; estos los usaron en una matriz real, obtuvieron resultados de 49,20, 54,50 y 72,80%, respectivamente, y encontraron la activación química con NaOH como el tratamiento más eficiente. En otro estudio realizado por Doria et al. (2011) donde no se le aplicó tratamiento a la cascarilla y usando un tamaño de partícula de 0,50 mm, rango de pH 1-/2, y concentración del metal de 3 mg/L, lograron una máxima remoción del 100 % a pH 1 con una dosificación de 3 g/L. Estos estudios comprueban que la cascarilla de arroz es un material capaz de adsorber de forma eficiente el cromo (VI). La cascarilla de arroz también ha sido probada como adsorbente en otros metales como el mercurio (II) el cual ha aumentado su presencia en los afluentes y de la misma manera su toxicidad en los seres vivos, al verse implicado en el avanzado desarrollo de las actividades mineras (Garay, 2013). Estudios como el realizado por Feng, Lin, Gong, Sugita y Shoya (2004), en donde la cascarilla fue lavada con HCl 1 N y llevada a cenizas a 700 °C por 4 horas, con tamaño de partícula de 43 a 175 µm, alcanzaron una remoción de 3,23 mg Hg/g C.A, demostrando una gran capacidad de adsorción. Autores como Rocha, López, Duarte y Pereira (2013) también han usado este residuo como alternativa para remover mercurio (II); ellos lavaron la cascarilla con agua destilada, la secaron a 60 °C y obtuvieron un tamaño de partícula de 500 |m; la máxima adsorción estuvo por encima del 90 % usando una concentración del metal de 500 jg/L.
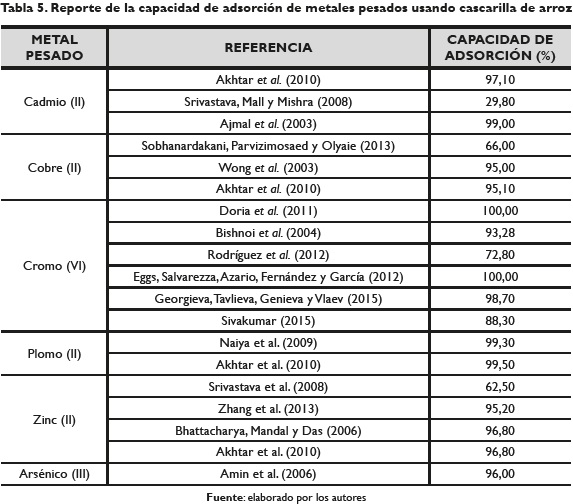
Este material residuo de actividades agrícolas ha sido usado en otros metales, donde ha demostrado ser un buen adsorbente (tabla 5).
VARIABLES DE ADSORCIÓN DE LA CASCARILLA DE ARROZ
Efecto de tiempo de contacto y de la concentración inicial del metal
En el proceso de adsorción de metales pesados se debe tener en cuenta la concentración inicial del metal a tratar y el tiempo que este dura en contacto con el material adsorbente (cascarilla de arroz). Estudios realizados por Zhang et al. (2013) donde trataron la cascarilla de arroz con NaOH 0,10 M para evaluar su efecto en la superficie del material, obtuvieron que con una concentración inicial del metal en solución a 25 mg/L, 0,10 g/L del adsorbente y con un tiempo de contacto máximo de 150 minutos, se logró evidenciar que en los primeros 10 minutos la remoción fue rápida, luego se mantuvo casi constante hasta alcanzar a remover hasta un 95,20 % del metal; por otro lado Bhattacharya et al. (2006) analizaron la remoción del mismo metal usando ceniza de cascarilla de arroz como adsorbente y encontraron que usando la misma concentración que en el estudio anterior el porcentaje de remoción de zinc (II) aumenta al incrementar el tiempo de contacto hasta 4 horas, pero disminuye cuando aumenta la concentración del metal logrando una remoción máxima del 96,80 %. También se han realizado estudios en otros metales como el plomo (II) en donde Naiya et al. (2009) trabajaron con ceniza de cascarilla de arroz y encontraron que el tiempo de equilibrio de adsorción se obtiene en 1 hora a una concentración de 10 mg/L; también se evidencia que a medida que aumenta la concentración del metal la adsorción disminuye, debido a que se saturan los sitios de enlace disponibles entre el metal y el adsorbente; el cromo (VI) ha sido ampliamente tratado debido a su gran toxicidad. Un ejemplo es el trabajo realizado por Bansal et al. (2009) donde modificaron la cascarilla de arroz en dos tratamientos; uno fue el adsorbente prehervido y el otro tratado con formaldehído; las concentraciones a evaluar fueron las mismas en cada tratamiento (10, 30, 50, 70 mg/L) y evidenciaron comportamientos de adsorción similares, pues en cada caso el porcentaje de adsorción es proporcional al tiempo de contacto hasta los 120 min donde se vuelve constante; similar a los otros casos demuestran que a medida que aumenta la concentración inicial del metal disminuye el porcentaje de adsorción, logrando a 10 mg/L un porcentaje de remoción por encima del 60 % en cada tratamiento. Se han realizado numerosos estudios de remoción de metales pesados con cascarilla de arroz y el porcentaje de remoción se comporta de una manera similar frente a la concentración inicial del metal y al tiempo de contacto (Ajmal et al., 2003; Srivastava et al., 2008; Taha, Kiat, Shaharun y Ramli, 2011).
Efecto de pH
A partir de la gran variedad de estudios realizados en procesos de adsorción de metales pesados se ha comprobado que el pH es una variable fundamental en este proceso en donde pequeñas variaciones pueden generar grandes cambios en la adsorción; además, puede variar según el metal con el que se efectúe el proceso; como lo describen Asadi, Shariatmadari y Mirghaffari (2008), esta variable es indispensable debido a que a pH altos aumentan los sitios de adsorción negativos y disminuye la competencia de los iones metálicos con los iones H+1 por los sitios de sorción; a pH bajos la formación de iones hidrolizados decrece y con eso la adsorción de los metales, además de que aumenta la competencia por sitios de sorción con los iones H+L.
Según Srivastava, Mall y Mishra (2009) el pH es la variable más importante, debido a que los iones H+1 son fuertes competidores por los sitios de adsorción, además de que esta variables influencia directamente en la especiación de los iones metálicos.
El pH varía según el ion metálico que se trabaje. Autores como Amin et al. (2006) reportaron que a un pH entre 6,50 y 8,00 se alcanzan los máximos porcentajes de adsorción para As (V) y As (III); por otro lado, Ahmed, Attar y Parande (2012) reportaron que para el Cr (VI) un porcentaje de adsorción de 96 % se alcanza a pH bajos con valores de 2; también estudios realizados con este metal y bajo diferentes condiciones de trabajo encuentran que generalmente a pH bajos la capacidad de adsorción es mayor ya que la superficie del material está protonada lo que favorece la adsorción de cromo (VI) en su forma aniónica (HCrO4); además, al aumentar el pH incrementa la competencia de iones CrO42-y OH- lo que reduce la eficiencia del proceso (Bansal et al., 2009), para el caso de níquel, Srivastava et al. (2009) reportaron que la máxima adsorción es alcanzada cuando los valores de pH son iguales o mayores a 6; El-Shafey (2007) en su trabajo realizado en la remoción de Se (IV) y Cd (II) encontró que la máxima adsorción de Se (IV) se presenta cuando los valores de pH son de 1,50 y para el caso de Cd (II) la máxima adsorción se presenta en pH en un rango de 3-7.
Efecto de tamaño de partícula
La velocidad de adsorción de los metales sobre la cascarilla de arroz depende en gran medida de fenómenos de superficie y, por tanto, del área superficial de la cascarilla en donde se va a dar la interacción del metal con la superficie de esta en el proceso de adsorción (Chuah et al., 2005); es por esto que la relación tamaño de partícula-área superficial se vuelve muy importante en estos procesos, tal y como lo reportan Feng et al. (2004) en la remoción del plomo y el mercurio en donde se evidencia que partículas menores a 43 μm poseen una mayor área superficial y, por tanto, generan un incremento en la capacidad de adsorción. Este parámetro sigue la misma tendencia incluso en el tratamiento con otro metales como el cobre, tal y como lo reportó Wong et al. (2003) en donde a menor tamaño de partícula aproximadamente de 105 μm mayor será la adsorción.
CONCLUSIONES
La cascarilla de arroz es un material ampliamente utilizado en procesos de remoción de metales pesados demostrando eficiencia y facilidad en su aplicación, lo que la perfila como una alternativa viable, económica y de fácil acceso para solucionar problemas de contaminación de afluentes por metales pesados.
En procesos de adsorción usando residuos agroindustriales como materiales adsorbentes se debe tener en cuenta el control de las variables como pH, concentración inicial y tiempo de contacto, entre otras, puesto que estas varían según el metal y de ellas depende en gran medida el éxito del tratamiento.
REFERENCIAS BIBLIOGRÁFICAS
Ahmaruzzaman, M. (2011). Industrial wastes as low-cost potential adsorbents for the treatment of wastewater laden with heavy metals. Advances in Colloid and Interface Science, 166(1-2), 36-59. [ Links ]
Ahmed, I.; Attar, S. J. & Parande, M. G. (2012). Removal of Hexavalent Chromium (Cr (VI)) from Industrial Wastewater by Using Biomass Adsorbent (Rice Husk Carbone). International Journal of Advanced Engineering Research and Studies, 1(2), 92-94. [ Links ]
Ahumada, L. M. & Rodríguez-Páez, J. E. (2006). Uso del SiO2 obtenido de la cascarilla de arroz en la síntesis de silicato de calcio. Revista Acad. Coloma. Cien, 30 (117), 581-594. [ Links ]
Ajmal, M.; Rao, R. A. K.; Anwar, S.; Ahmad, J. & Ahmad, R. (2003). Adsorption studies on rice husk: removal and recovery of Cd(II) from wastewater. Bioresource Technology, 86(2), 147-9. [ Links ]
Akhtar, M.; Bhanger, M. I.; Iqbal, S. & Hasany, S. M. (2006) . Sorption potential of rice husk for the removal of 2,4-dichlorophenol from aqueous solutions: Kinetic and thermodynamic investigations. Journal of hazardous materials, 128 (1), 44-52. [ Links ]
Akhtar, M.; Iqbal, S.; Kausar, A.; Bhanger, M. I. & Shaheen, M. A. (2010). An economically viable method for the removal of selected divalent metal ions from aqueous solutions using activated rice husk. Colloids and Surfaces. B, Biointerfaces, 75(1), 149-55. [ Links ]
Ali, N. A. (2013). Removal of heavy metals from drainage waters using sugar cane bagasse. Egy J aquac, 3(4), 39-53. [ Links ]
Álvarez, J.; López, G.; Amutio, M.; Bilbao, J. & Olazar, M. (2014). Bio-oil production from rice husk fast pyrolysis in a conical spouted bed reactor. Fuel, 128, 162-169. [ Links ]
Amin, M. N.; Kaneco, S.; Kitagawa, T.; Begum, A.; Katsumata, H.; Suzuki, T. & Ohta, K. (2006). Removal of Arsenic in Aqueous Solutions by Adsorption onto Waste Rice Husk. Industrial & Engineering Chemistry Research, 45(24), 8105-8110. [ Links ]
Arcos, C. A.; Macías, P. D. & Rodríguez-Páez, J. E. (2007). La cascarilla de arroz como fuente de SiO2. Revista Facultad de Ingeniería Universidad de Antioquia, 1 (41), 7-20. [ Links ]
Asadi, F.; Shariatmadari, H. & Mirghaffari, N. (2008). Modification of rice hull and sawdust sorptive characteristics for remove heavy metals from synthetic solutions and wastewater. Journal of Hazardous Materials, 154(1-3), 451-8. [ Links ]
Babel, S. & Kurniawan, T. A. (2003). Low-cost adsorbents for heavy metals uptake from contaminated water: a review.Journal of hazardous materials, 97(1), 219-243. [ Links ]
Balsamo, M.; Di Natale, F.; Erto, A.; Lancia, A.; Montagnaro, F. & Santoro, L. (2011). Cadmium adsorption by coal combustion ashes-based sorbents-Relationship between sorbent properties and adsorption capacity. Journal of Hazardous Materials, 187(1-3), 371-378. [ Links ]
Bansal, M.; Garg, U.; Singh, D. & Garg, V. K. (2009). Removal of Cr(VI) from aqueous solutions using pre-consumer processing agricultural waste: a case study of rice husk. Journal of Hazardous Materials, 162(1), 312-20. [ Links ]
Bhatnagar, A.; Vilar,V. J. P.; Botelho, C. M. S. & Boaventura, R. a R. (2010). Coconut-based biosorbents for water treatment-- a review of the recent literature. Advances in Colloid and Interface Science, 160(1-2), 1-15. [ Links ]
Bhattacharya, A. K.; Mandal, S. N. & Das, S. K. (2006). Adsorption of Zn(II) from aqueous solution by using different adsorbents. Chemical Engineering Journal, 123(1-2), 43-51. [ Links ]
Bishnoi, N. R.; Bajaj, M.; Sharma, N. & Gupta, A. (2004). Adsorption of Cr(VI) on activated rice husk carbon and activated alumina. Bioresource Technology, 91(3), 305-307. [ Links ]
Bohli, T.; Ouederni, A.; Fiol, N. & Villaescusa, I. (2015). Evaluation of an activated carbon from olive stones used as an adsorbent for heavy metal removal from aqueous phases. Comptes Rendus Chimie, 18(1), 88-99. [ Links ]
Chandrasekhar, S. & Pramada, P. N. (2006). Rice husk ash as an adsorbent for methylene blue- effect of ashing temperature. Adsorption, 12(1), 27-43. [ Links ]
Chuah, T. G.; Jumasiah, A.; Azni, I.; Katayon, S. & Choong, S.Y. (2005). Rice husk as a potentially low-cost biosorbent for heavy metal and dye removal: an overview. Desalination, 175(3), 305-316. [ Links ]
DANE (2015). Encuesta Nacional de Arroz Mecanizado II Semestre de 2015. Recuperado de http://www.dane.gov.co/index.php/agropecuario-alias/estadisticas-de-arroz-mecanizado-enam. [ Links ]
Doria, M.; Hormaza, A. & Suarez, D. (2011). Cascarilla de arroz: material alternativo y de bajo costo para el tratamiento de aguas contaminadas con cromo (VI). Gestión y Ambiente, 14(1), 73. [ Links ]
El-Shafey, E. I. (2007). Sorption of Cd (II) and Se (IV) from aqueous solution using modified rice husk. Journal of Hazardous Materials, 147(1-2), 546-55. [ Links ]
Eggs, N.; Salvarezza, S.; Azario, R.; Fernández, N. & García, M. D. (2012). Adsorción de cromo hexavalente en la cáscara de arroz modificada químicamente. Avances en Ciencias e Ingeniería, 3 (3), 141-151. [ Links ]
Feng, Q.; Lin, Q.; Gong, F.; Sugita, S. & Shoya, M. (2004). Adsorption of lead and mercury by rice husk ash. Journal of Colloid and Interface Science, 278(1), 1-8. [ Links ]
Garay, S. L. (2013). Minería en Colombia: Institucionalidad y territorio, paradojas y conflictos. Bogotá: Contraloría General de la República. [ Links ]
Georgieva, V. G.; Tavlieva, M. P.; Genieva, S. D. & Vlaev, L. T. (2015). Adsorption kinetics of Cr (VI) ions from aqueous solutions onto black rice husk ash. Journal of Molecular Liquids, 208, 219-226. [ Links ]
Guo, Y.; Qi, J.; Yang, S.; Yu, K.; Wang, Z. & Xu, H. (2003). Adsorption of Cr (VI) on micro-and mesoporous rice husk-based active carbon. Materials Chemistry and Physics, 78(1), 132-137. [ Links ]
FAO (2016). Nota informativa de la FAO sobre la oferta y la demanda de cereales. Recuperado de: http://www.fao.org/worldfoodsituation/csdb/es/. [ Links ]
Karnib, M.; Kabbani, A.; Holail, H. & Olama, Z. (2014). Heavy metals removal using activated carbon, silica and silica activated carbon composite. Energy Procedia, 50(1), 113-120. [ Links ]
Khalid, N.; Ahmad, S.; Toheed, A. & Ahmed, J. (2000). Potential of rice husks for antimony removal. Applied Radiation and Isotopes, 52(1), 31-8. [ Links ]
Khan, N. A.; Ibrahim, S. & Subramaniam, P. (2004). Elimination of Heavy Metals from Wastewater Using Agricultural Wastes as Adsorbents. Malaysian Journal of Science, 23(1), 43-51. [ Links ]
Krishnarao, R. V.; Mahajan, Y. R. & Kumar, T. J. (1998). Conversion of raw rice husks to SiC by pyrolysis in nitrogen atmosphere. Journal of the European Ceramic Society, 18(2), 147-152. [ Links ]
Krishnarao, R.V.; Subrahmanyam, J. & Kumar,T. J. (2001). Studies on the formation of black particles in rice husk silica ash. Journal of the European Ceramic Society, 21 (1), 99-104. [ Links ]
Kumar, U. & Bandyopadhyay, M. (2006). Sorption of cadmium from aqueous solution using pretreated rice husk. Bioresource Technology, 97(1), 104-9. [ Links ]
Kurtis, K. E. & Rodrigues, F. A. (2003). Early age hydration of rice hull ash cement examined by transmission soft X-ray microscopy. Cement and Concrete Research, 33(4), 509-515. [ Links ]
Lakshmi, U. R.; Srivastava,V. C.; Mall, I. D. & Lataye, D. H. (2009). Rice husk ash as an effective adsorbent: evaluation of adsorptive characteristics for Indigo Carmine dye. Journal of Environmental Management, 90(2), 710-20. [ Links ]
Malik, P. K. (2003). Use of activated carbons prepared from sawdust and rice-husk for adsorption of acid dyes: a case study of Acid Yellow 36. Dyes and Pigments, 56(3), 239-249. [ Links ]
Mohan, D. & Singh, K. P. (2002). Single- and multi-component adsorption of cadmium and zinc using activated carbon derived from bagasse- an agricultural waste. Water Research, 36(9), 2304-2318. [ Links ]
Naiya, T. K.; Bhattacharya, A. K.; Mandal, S. & Das, S. K. (2009). The sorption of lead(II) ions on rice husk ash. Journal of Hazardous Materials, 163(2-3), 1254-64. [ Links ]
Panpa, W. & Jinawath, S. (2009). Synthesis of ZSM-5 zeolite and silicalite from rice husk ash. Applied Catalysis B: Environmental, 90(3-4), 389-394. [ Links ]
Rocha, J. B. T.; Aschner, M.; Dórea, J. G.; Ceccatelli, S.; Farina, M. & Silveira, L. C. L. (2012). Mercury toxicity. Journal of Biomedicine & Biotechnology. 1-2 [ Links ]
Rocha, M. L. F.; Dias, J. F.; Boufleur, L. A. & Santos, C. E. I. (2014). Metal concentration in muscle of two species of flatfish from Santos Bay, Southeastern Brazilian coast. Nuclear Instruments and Methods in Physics Research, Section B: Beam Interactions with Materials and Atoms, 318(1), 88-93. [ Links ]
Rocha, L. S.; Lopes, C. B.; Duarte, A. C. & Pereira, E. (2013). A cost - effective and eco-friendly treatment technology to remove realistic levels of mercury by means of the unmodified rice husk. E3S Web of Conferences, 1 (25002). 1-4. [ Links ]
Rodríguez, Y. M.; Salinas, L. P.; Ríos, A. & Vargas, L. U. (2012). Rice husk-based adsorbents in the removal of chromium from tanning industry efluents. Biotecnología en el Sector Agropecuario y Agroindustrial, 10(1), 146-156. [ Links ]
Romano, J. S. & Rodríguez, F. A. (2008). Cements obtained from rice hull: Encapsulation of heavy metals. Journal of hazardous materials, 154(1), 1075-1080. [ Links ]
Selvi, K.; Pattabhi, S. & Kadirvelu, K. (2001). Removal of Cr (VI) from aqueous solution by adsorption onto activated carbon. Bioresource technology, 80(1), 87-89. [ Links ]
Sivakumar, D. (2015). Hexavalent chromium removal in a tannery industry wastewater using rice husk silica. Global Journal of Environmental Science and Management, 1(1), 27-40. [ Links ]
Sobhanardakani, S.; Parvizimosaed, H. & Olyaie, E. (2013). Heavy metals removal from wastewaters using organic solid waste - rice husk. Environmental Science and Pollution Research, 20(8), 5265-5271. [ Links ]
Srivastava, V. C.; Mall, I. D. & Mishra, I. M. (2008). Removal of cadmium(II) and zinc(II) metal ions from binary aqueous solution by rice husk ash. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 312(2-3), 172-184. [ Links ]
Srivastava, V. C.; Mall, I. D. & Mishra, I. M. (2009). Competitive adsorption of cadmium(II) and nickel(II) metal ions from aqueous solution onto rice husk ash. Chemical Engineering and Processing: Process Intensification, 48(1), 370-379. [ Links ]
Taha, M. F.; Kiat, C. F.; Shaharun, M. S. & Ramli, A. (2011). Removal of Ni (II), Zn (II) and Pb (II) ions from Single Metal Aqueous Solution using Activated Carbon Prepared from Rice Husk. World Academy of Science, Engineering and Technology,5(12), 1473-1478. [ Links ]
Valverde, A.; Sarria, B. & Monteagudo, J. (2007). Análisis comparativo de las características fisicoquímicas de la cascarilla de arroz. Scientia et Technica, 5(37), 255-260. [ Links ]
Wong, K. K.; Lee, C. K.; Low, K. S. & Haron, M. J. (2003). Removal of Cu and Pb by tartaric acid modified rice husk from aqueous solutions. Chemosphere, 50(1), 23-8. [ Links ]
Yasemin, B. & Zequi, T. (2007). Removal of heavy metals from aqueous solution by sawdust adsorption. Journal of Environmental Sciences, 19(2), 160-166. [ Links ]
Yu, B.; Zhang, Y.; Shukla, A.; Shukla, S. S. & Dorris, K. L. (2000). The removal of heavy metal from aqueous solutions by sawdust adsorption - removal of copper. Journal of Hazardous Materials, 80(1-3), 33-42. [ Links ]
Zhang, Y.; Zheng, R.; Zhao, J.; Zhang, Y.; Wong, P.; Ma, F. & Studies, C. (2013). Biosorption of Zinc from Aqueous Solution Using Chemically Treated Rice Husk. BioMed research international, 1-7. [ Links ]














