Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Luna Azul
versión impresa ISSN 1909-2474
Luna Azul no.38 Manizales ene./jun. 2014
THE RELATIONSHIP BETWEEN PELTIGERA SP. AND RHIZOPHORA MANGLE IN ARROYO DE PLATA (BOLIVAR), COLOMBIAN CARIBBEAN REGION
Darío Avendaño-Remolina2
Adolfo M. Sanjuan-Muñoz3
1 Fundación Verdes Horizontes. Manizales (Caldas) Colombia, ricardoalvarezleon@gmail.com
2 Oficina de la Naciones Unidas Contra la Droga y el Delito UNODC, Santa Marta (Mag.) Colombia, darioavendano@gmail.com
3 Universidad de Bogotá "Jorge Tadeo Lozano". Santa Marta (Mag.) Colombia, adolfo.sanjuan@utadeo.com
Objetivo: determinar la distribución y el estado de los rodales de manglar en Arroyo de Plata (Departamento de Bolívar). Metodología: se realizaron labores de campo a través del arbolado, mediante el muestreo biológico de la flora y de los parámetros físicos y químicos del agua y de los suelos a lo largo de transectos dentro del bosque. Resultados: la composición del rodal incluye cinco especies, Rhizophora mangle (mangle rojo, colorao o colorado), Avicennia germinans (mangle salado, prieto, negro o iguanero), Laguncularia racemosa (mangle blanco, amarillo o bobo), Conocarpus erecta (mangle zaragoza) y Pelliciera rhizophorae (mangle piñuelo). Asociado a la especie pionera (R. mangle) se encontró el líquen (Peltigera sp.), cuya relación se lleva a cabo solo cuando el mangle está en estado de degradación y los parámetros fisicoquímicos de las aguas y los suelos, son extremos. Conclusión: Los manglares mostraron características mixtas, tipo maduro ribereño y de cuenca, donde la especie invasora P. rhizophorae presenta el mayor IVI, debido a su alta densidad. El registro de los líquenes Peltigera sp. y su presencia en los manglares del Caribe colombiano no solo es el primero para esta Región, su distribución puede estar restringida a la zona costera, es incidental, y demuestra su gran capacidad de adaptación a los cambios ambientales, y puede ser considerada entre los en bio-indicadores de las características ambientales, especialmente de las alteraciones actuales de los suelos y las aguas.
PALABRAS CLAVEPeltigera, líquenes, Rhizophora, manglares, Caribe, Colombia.
ABSTRACTObjective: To determine the distribution and status of mangrove stands in Arroyo de Plata (Department of Bolívar). Methodology: Field work was conducted through woodland, using biological sampling of the flora and the physical and chemical parameters of water and soil along transects within the forest. Results: The composition of the stand includes five species, Rhizophoramangle (red, colorao or colorado mangrove), Avicenniagerminans (salty, dark color, black or iguanero mangle) Laguncularia racemosa (white, yellow or bobo mangrove), Conocarpus erecta (zaragoza mangle) and Pelliciera rhizophorae (tea mangrove). The lichen (Peltigera sp), was found associated with the pioneer species (R. mangrove) whose relationship is carried out only when the mangrove is in a state of degradation and the physical-chemical parameters of water and soil, are extreme. Conclusion: Mangroves showed mature coastal basin type mixed characteristics, where the invasive species P. rhizophorae has the highest IVI due to its high density. Registration of Peltigera sp lichens and its presence of the Colombian Caribbean mangrove is not only the first for this region, its distribution may be restricted to the coastal zone, it is incidental and demonstrates its ability to adapt to environmental changes, and can be considered between the bio-indicators of environmental characteristics, especially of the the current alterations of soil and water.
KEY WORDSPeltigera, lichens, Rhizophora, mangroves, Caribbean, Colombia.
INTRODUCCIÓN
Manglares. Los ecosistemas de manglar en el departamento de Bolívar, se extienden en forma discontinua a lo largo de la línea de costa entre los límites de los departamentos de Sucre y del Atlántico. La zona costera del departamento de Bolívar se encuentra delimitada al norte por las Salinas de Galerazamba (10º58' N y 75º12' W) en el municipio de Santa Catalina en límites con el departamento del Atlántico, y al sur por Boca Flamenquito (10º35' N y 75º21' W) en el Distrito Turístico y Cultural de Cartagena de Indias en límites con el departamento de Sucre; e incluye el Parque Nacional Natural Corales del Rosario e Islas de San Bernardo (CIOH/CARDIQUE, 1997; Sánchez-Páez et al., 1997). Presenta un clima con déficit hídrico considerable, con dos estaciones lluviosas y dos secas definidas por la zona de confluencia intertropical, en la cual la temperatura media anual es de 27,6ºC con máximos y mínimos anuales de 23,1 y 32,9ºC respectivamente, y una pluviosidad promedio de 1160 mm. La evaporación es igual o, en la mayoría de los casos, superior a la precipitación esbozando una deficiencia hídrica que influye notablemente en el desarrollo estructural de los bosques de manglar del departamento.
Las formaciones de manglar están conformadas por cinco especies: Rhizophora mangle (mangle rojo, coloraoo, colorado), Avicennia germinans (mangle salado, prieto, negro o iguanero), Laguncularia racemosa (mangle blanco, amarillo o bobo), Conocarpus erecta (mangle zaragoza) y Pelliciera rhizophorae (mangle piñuelo), que son la totalidad de las especies encontradas en el Caribe colombiano (Sánchez-Páez et al., 1997). Estas especies se encuentran habitualmente mezcladas formando bosques mixtos sin mostrar un patrón de distribución definido, en donde A. germinans es generalmente la especie dominante en la parte interior de la floresta, mientras que R. mangle predomina en los sectores marginales limitando, en la gran mayoría de los casos, con los cuerpos de agua (Pino-Renjifo et al., 1999; Agudelo-Ramírez, 2000).
A nivel general, en el departamento, el manglar se caracteriza por presentar un alto grado de intervención urbanística e industrial que se traduce en la degradación y pérdida continua de extensiones representativas de bosque y de suelo, siendo aprovechada por los nativos de la región en forma artesanal tan solo una pequeña parte del recurso forestal (Pino-Renjifo et al., 1999).El grado de desarrollo estructural alcanzado por los bosques es variable y está determinado por factores físicos como el tipo de suelo, la climatología local, las energías de subsidio y los tensores o presiones que los afectan sean de tipo natural o antropogénico (Sánchez-Páez et al., 1997).
Líquenes asociados. Según Hawksworth et al. (2005):Los líquenes tienen un importante papel como bioindicadores de lectura inmediata de la contaminación medioambiental, de los cambios climáticos y de la estabilización del suelo. Se han realizado muchos trabajos acerca de este tema en regiones templadas, pero tan solo en algunos pocos casos las técnicas empleadas en este tipo de estudios han sido utilizadas en los trópicos (p. 71).
La mayor parte de las investigaciones realizadas en los trópicos hasta la fecha, se relacionan con la contaminación ambiental y perturbaciones forestales, pero estas han sido ejecutadas solo en algunos pocos lugares, y permanecen aún sin realizar en la mayoría de las regiones tropicales. Las ventajas que poseen los líquenes para ser utilizados como bio-indicadores de lectura inmediata en los trópicos, se basan en que los trabajos pueden ser realizados sin la identificación total de las especies involucradas, y en el hecho de que son perennes y fácilmente discernibles a simple vista o con la ayuda de una lupa decampo. Esto último constituye un factor importante, ya que la falta de entrenamiento para la identificación es el principal problema en la realización de este tipo de investigaciones; a su vez, Wolf (1993) reconoce los patrones de biomasa y diversidad de las briófitas y líquenes en los diferentes gradientes altitudinales en el norte de los Andestropicales; además, Sipman et al. (2008) confirman que en Colombia existen 1444 especies de hongos liquenizados, pero que su número puede ascender a 3000-4000 especies.
Según Martínez (1999), la forma de crecimiento foliácea pertenece al género Peltigera, cuyas especies están asociadas con cianobacterias como fotobiontes, y muchas de sus especies son consideradas indicadoras de madurez forestal. Martínez et al. (2003) discuten sobre la distribución del género y resaltan el número de especies, así como su dificultad para determinar las especies.
De acuerdo con Miadlikowska y Lutzoni (2000), Peltigera (Peltigerineae, liquenizados Ascomycota) es uno de los géneros de líquenes más extendidos, con incorporación de asociaciones bilaterales y trilaterales, que involucran hongos, algas verdes (cf. Coccomyxa), y las cianobacterias (cf. Nostoc). Se presenta en este género una amplia gama de caracteres morfológicos y químicos (compuestos secundarios) y la variación involucra niveles tanto intraespecíficos como interespecíficos. En comparación con muchos otros géneros de macro-líquenes, su taxonomía, incluyendo quimio-taxonomía, todavía sigue siendo poco conocida. Las clasificaciones de infragenéricos Peltigera son casi exclusivamente con base en la composición fotobionte del talo. Estas clasificaciones suponen que cada biytritaxones, tienen diferentes entidades monofiléticas. El género Peltigera nunca ha sido el centro de un amplio estudio filogenético. La subdivisión más reciente y de amplia aceptación del género en siete grupos, se basa principalmente en los caracteres morfológicos y químicos. Las relaciones entre las especies de Peltigera se han investigado sobre sus componentes químicos, morfológicos y subunidad grande de ADN nuclear ribosomal (LSU nrDNA) de datos.
Vitikainen (1998), reconoce tres tipos principales de estructura del género Peltigera en Suramérica, donde se han identificado con base en estudios avanzados de bioquímica: P. laciniata (G. Merr. ex Riddle) Gyeln. Ecuador, Kalb 511 (H), en P. pulverulenta (Tayl.) Nyl. 1. Venezuela, Ahti 37205 (H) y P. pulverulenta 2. Ecuador, Ardvisson 4627 (H).
Van Duunné y Wolf (s.f.), trabajaron intensamente en briófitos y líquenes epilíticos de las plantaciones de café, encontrando una diversidad muy alta. También a nivel nacional, Aguirre-Ceballos (2006, 2008), estudio la diversidad de los musgos y los líquenes de Colombia, evaluando y promoviendo su conservación. Posteriormente Aguirre-Ceballos y Rangel-Churio (2007), analizaron las amenazas a la conservación de las especies de musgos y líquenes en el país, y reconocen las especies amenazadas de la familia Peltigeraceae y el género Peltigera (P. collina, P. fibrilloides, P.membranacea, P. mexicana y P. microdactyla).
Sipman (2008), enfatiza que Peltigera dolichorhiza (Nyl.) Nyl. - Nylander (1860: 327 sub Peltigera polydactylavar. dolichorhiza), Nylander (1874: 71), Galloway (1985: 364), Vitikainen (1998: 136) Typus: Bogotá, 2600-2700 m, 1860 (?), Lindig 2519 p.p. (H-NYL 33203, Lectotipus) y Peltigera laciniata var. Irregularis Gyelnik - Gyelnik (1932: 40), son las más conocidas y estudiadas.
Recientemente Coca y Sanín (2010), describen 8 especies del género Coccocarpia Coccocarpiaceae), colectados también en el PNN Tatamá, de las cuales 7 (C. domingensis, C. erythroxy, C. filiformis, C. palmicola, C. pellita, C. prostrata, C. stellata) son novedades corológicas para el PNN Tatamá y una (C. microphyllina) para Colombia. Los géneros son novedades corológicas tanto para Tatamá, como para Colombia, siendo Sticta el género más rico.
Pérez-Quintero y Watteijne-Cerón (2010), analizaron la estructura de una comunidad de líquenes y en especial la morfología del género folioso Sticta Stictaceae) en un gradiente altitudinal. La comunidad de líquenes epifitos esta distribuida en un gradiente altitudinal (2000-2600 m) también del PNN Tatamá. Se encontró que con el aumento en altura hay una disminución en riqueza y diversidad, lo cual se desvía del patrón encontrado generalmente en otros trabajos sobre líquenes y gradientes altitudinales. La comunidad a bajas alturas se compone principalmente de líquenes fruticosos (cobertura de 30% a 2070 m y 0% a 2560 m) y a mayores alturas de líquenes foliosos (cobertura de 15% a 2070 m y 43% a 2560 m). La altura, además de influenciar la estructura de la comunidad de los líquenes, puede afectar el desarrollo y la morfología de estos. En Sticta se presentaron variaciones intraespecíficas en la densidad de cifelas (órganos de intercambio gaseoso) asociadas a la altura, encontrándose un efecto significativo de la altura sobre la densidad de cifelas en las especies S. andensis y S. gyalocarpa (con un valor de ANOVA, de P= 0,008 y 0,05 respectivamente). Esto muestra un mecanismo de adaptación a los cambios ambientales que se dan con la altura.
Rincón-Espitia (2011) documenta la composición de la flora liquénica corticícola en algunas localidades de las planicies y los macizos montañosos de la región Caribe. Se encontraron 348 especies de líquenes corticícolas, representadas en 950 ejemplares provenientes de cinco localidades, que corresponden a tres tipos de vegetación: bosque húmedo, bosque semihúmedo y bosque seco. Se describieron dos especies como nuevas para la ciencia y se encontraron 116 nuevos registros para Colombia, la mayoría de especies son nuevos registros para las áreas de estudio y algunos nuevos registros para el Neotrópico.
Soto-Medina (2011) registra géneros para ocho municipios del Valle del Cauca (Cali, Buenaventura, Cerrito, Dapa, Jamundí, Restrepo, Roldanillo y Trujillo) y tres del Cauca (Caloto, Guapi y Coconuco). Las zonas de vida visitadas incluyeron bosque húmedo tropical, bosque seco tropical, bosque muy seco tropical, bosque premontano y subpáramo. Se encontraron 510 especímenes incluidos en aproximadamente 230 morfoespecies de líquenes, de los cuales 190 fueron identificados incluido Peltigera sp. y los restantes no se han trabajado a nivel de especie dada la complejidad y el escaso conocimiento taxonómico de los géneros.
Coca et al. (2012), confirman que los Peltigerales están segregados del Orden Lecanorales, que contiene la mayor riqueza de cianolíquenes con aproximadamente 1700 especies distribuidas en todo el mundo. En el PNN Tatamá, entre los 2400 y los 3000 m con especies epifitas, foliícolas y terrícolas, la mayor diversidad se encontró a los 2600 m, especialmente en las familias Coccocarpiaceae, Loariaceae y Pannariaceae. Peltigera sp. solo se encontró en Santuario, Loc. Planes de San Rafael (entre Monte Zancudo y El Fracaso, 2800-3000 m). Ofrecen una clave para el reconocimiento del Orden Peltigerales:
2. Ascocarpos como peritecios o lirelas ........... Varios órdenes (Ascomicetes).
2. Ascocarpos como apotecios............................................................. 3.
3. Ascas bitunicadas ......................................................... ARTHONIALES.
3. Ascas unitunicadas ........................................................................ 4.
4. Apotecioshemiangiocárpicos ............................................. OSTROPALES.
4. Apotecios gymnocárpicos ................................................................ 5.
5. Fotobiontechlorococcoide (en su mayoría Trebouxia) ........... LECANORALES.
5. Fotobionte cianobacterias (Nostoc o Scytonema), raramente algas verdes (solo en Lobariaceae y Peltigeraceae) ................... PELTIGERALES. (Coca et al., 2012).
Así como una clave para la identificación del género de Fotobionte [Peltigera, según Bungartz (2002), in Nash III et al.(2002)]:
Apotecios pardos, situados en la cara superior del extremo de los lóbulos, en ocasiones éstos se pliegan en forma de silla de montar elevándose sobre el resto del talo. Cara inferior no corticada, pero surcada por venas de distintos tipos: desde finas, claras, bifurcadas hasta oscuras, anchas, planas y de aspecto reticulado, por lo que sólo se ve la médula inferior blanca en algunas pequeñas zonas ovaladas. Rizinas abundantes de muy diversos tipos. Talos grandes, algunos >30 cm, con lóbulos anchos >1 cm [talo con tomento homogéneo en la cara ventral, con venas y generalmente terrestre, Coca et al.(2012)]... Peltigera. (Barreno y Pérez-Ortega, 2003, p. 156).
MATERIALES Y MÉTODOSArroyo de Plata se encuentra ubicado en el sector de la Bahía de Barbacoas, la cual está localizada al noroeste del departamento de Bolívar, entre los 10º08'09'' y 10º14'56'' N y los 75º31'21'' y los 75º40'17'' W, abarcando una superficie de 140 km² (Hinestrosa y Viña, 1986). En ella desembocan los caños Lequerica y Matunilla que se originan del Canal del Dique, los cuales son producto de la canalización del canal realizada en el siglo XVII, direccionando aguas a la Bahía de Barbacoas (Alvarado-Ortega, 2001).Los aportes continuos e importantes de agua dulce provenientes del Canal del Dique y que aportan sedimentos a la bahía por los caños Lequerica y Matunilla que con su dinámica deltaica originan la formación de "bancos" en sus desembocaduras, permiten la colonización por manglar. De acuerdo a lo anterior, el desarrollo de los bosques se divide en dos etapas: la primera etapa, se caracteriza por un rápido crecimiento y un buen desarrollo del manglar gracias a la presencia de aguas dulces, que aportan nutrientes y disminuyen la salinidad hasta niveles adecuados para el desarrollo del manglar. La segunda etapa, presenta una degradación del manglar debido a la saturación por sedimentos, que llegan a modificar los flujos hídricos del sistema provocando el estancamiento de las aguas, que al evaporarse aumentan los niveles de salinidad y la temperatura alterando progresivamente las condiciones descritas en la primera etapa.
La estación muestreada en Arroyo de Plata se ubica a los 10º08'06,5" N y 75º32'35,8" W. En ella se delimitó una parcela perpendicular a la línea de costa, utilizando un cinta metrada de 120 m, sobre la cual se establecieron subparcelas de 100 m² (10 x 10 m), usando cuatro tubos de PVC unidos por un cabo, abarcando 5 m a lado y lado de la línea direccional, y prolongado 10 m de longitud hacia el fondo o parte interna del bosque. En cada parcela se identificaron y marcaron todos los árboles de mangle para evitar el reconteo. A cada uno se le midió la altura total utilizando como referencia tubos de PVC de 2 m de largo y la circunferencia a la altura del pecho (CAP) a 1,3 m con una cinta métrica. Para la medición de la CAP se tuvo en cuenta lo sugerido por Schaeffer-Novelli y Cintrón-Morelo (1986).
Con el fin de determinar los niveles de intervención o los factores estresantes, se realizaron anotaciones del estado de salud de cada árbol, indicando los vivos, muertos, talados y aquellos que tenían algún signo de deterioro o presencia de hormigas y termitas (Schaeffer-Novelli y Cintrón-Morelo, 1986).
Para determinar el reclutamiento en los bosques de mangle de las estaciones de muestreo, en cada subparcela de 100 m² se lanzaron al azar tres cuadrantes de 1 m². En los 30 cuadrantes se identificaron y contaron todas las propágulos y plántulas de mangle.
A partir de las medidas tomadas en campo (número de árboles vivos registrados en cada estación, especie y CAP), se calculó el diámetro a la altura del pecho (DAP = CAP/p) y los atributos estructurales del bosque de manglar: densidad, área basal y diámetro de área basal promedio (Schaeffer-Novelli y Cintrón-Molero, 1986), además del índice de valor de importancia (IVI) (Matteucci y Colma, 1982).
Para la determinación de variables físicas y químicas del agua intersticial y suelos, se ubicaron tres puntos (inicial, intermedio y final correspondientes a las abscisas k0+00, k0+050 y k0+100). Se midieron in situ pH, salinidad, oxígeno disuelto, conductividad y temperatura con una sonda multi-paramétrica. Para las variables a determinar en el laboratorio (turbidez, oxígeno disuelto, nitrógeno amoniacal, nitritos, nitratos, nitrógeno total, fósforo total, fosfatos, sodio, potasio, calcio, magnesio, cloruros, sulfatos, sulfuros y sólidos totales). Para la recolecta de muestras de agua y suelo, se cavaron agujeros de 50 cm de profundidad por debajo del nivel freático. Las perforaciones se realizaron de acuerdo al orden de ingreso al bosque desde la parte externa -colindando con el agua- hacia el interior, de esta forma el agua intersticial iba brotando, alcanzando el nivel freático para luego decantarse. Las muestras de agua y suelo fueron recolectadas, almacenadas y preservadas siguiendo lo enunciado por Clesceri et al. (1998).
Finalmente, se llevaron a cabo recorridos errantes en las florestas, tanto dentro como fuera de las parcelas, anotando los organismos asociados a los árboles de mangle y haciendo el respectivo registro fotográfico para la confirmación de la asociación incidental; posteriormente, se procedió a colectar manual y cuidadosamente los individuos, y a la identificación de los especímenes de líquenes, utilizando las claves especializadas (Bungartz, 2002; Barreno y Pérez-Ortega, 2003; Coca et al., 2012).
RESULTADOSEl bosque es maduro ribereño y de cuenca, de composición mixta que supera los 10 m de altura en algunos puntos, compuesto por R. mangle, A. germinas, L. racemosa y P. rhizophorae. El dosel es cerrado en los primeros metros y luego se abre en la medida en que la floresta se va degradando y las condiciones físico-químicas se hacen extremas.
En la primera franja (de 20 m aproximadamente) se establece una mezcla de R. mangle y P. rhizophorae, en cuyas raíces se advierte colonización de bálanos, ostras, algas y esponjas. El suelo, en este segmento, presenta abundante hojarasca y numerosos embriones de R. mangle pequeños que en varios casos tienen adherido aún el collar epi-cotiledonear. En esta franja la regeneración natural es representativa.
A partir de los 20 m se observa una mezcla de A. germinans, L. racemosa, R. mangle y P. rhizophorae. Las hojas de L. racemosa son pequeñas y los fustes presentan signos de defoliación, mientras que las de A. germinans presentan hongos "carbones" y blanqueamiento, evidenciando un estado fitosanitario deficiente. El suelo en este sector evidencia sequedad, desnudez y alcanza altas temperaturas haciendo más difícil el proceso de recuperación del bosque (Figura 1).
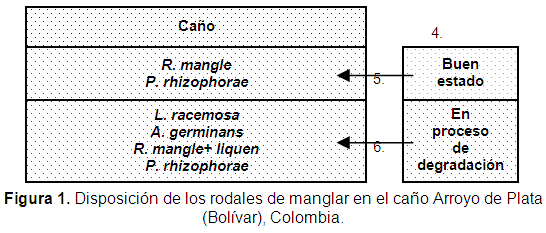
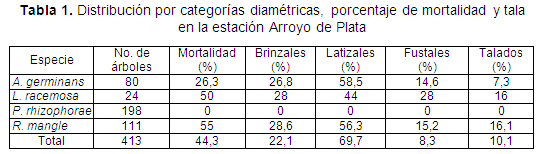
Entre los tensores que afectan al rodal cabe mencionar la tala de L. racemosa (16,0%), y R. mangle (16,1%) y la salinización del suelo, factor que está causando una degradación progresiva de la floresta a la cual puede deberse el 54,4% de mortalidad. Los efectos generados por la salinización del suelo se notan principalmente en los troncos (agrietados, con putrefacción en la parte basal y manchas amarillas en todo su contorno), las raíces (lenticelas expandidas) y en las hojas (pequeñas) (Tabla 1).Otros signos de este proceso se fundamentan en la presencia de hormigas y restos vegetales en forma desbordante.
Asociada exclusivamente a R. mangle y solamente en aquellas plantas deterioradas de esta especie, se advirtió la presencia del liquen Peltigera sp., epífito de color verde claro, elongado y con desarrollo dicotómico (Figuras 1, 2, 3). En este punto es evidente el proceso de degradación de la floresta, la cual se asienta sobre un suelo arenoso, compacto y con costras de sal (Avendaño-Remolina et al., 2000).
En la zona es muy frecuente encontrar "tapetes" de neumatóforos de L. racemosa que alcanzan alturas de hasta 15 cm ubicados alrededor de los fustes, mientras que los de A. germinans sobrepasan los 30 cm.
En la parte media del rodal, entre los 80 y 100 m, la tala es más significativa. La salinización de suelos y aguas es causada por el rompimiento del flujo hídrico derivado del taponamiento de los canales de irrigación natural que aprovisionan el área (Figura 2).
Hacia la parte final, el bosque recupera su vigor lo cual parece estar asociado a la cercanía de un cuerpo de agua. En este punto es R. mangle la especie que empieza a dominar y sus fustes superan los 10 m, el bosque sigue siendo abierto y el suelo despliega mayor cobertura vegetal, pues la cantidad de hojarasca aumenta (Figura 2).

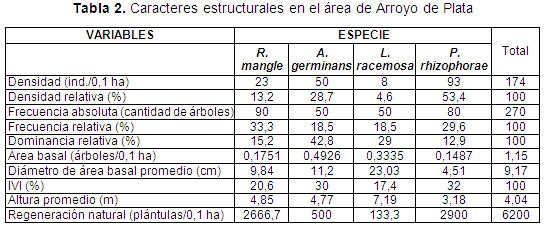
El mayor IVI lo presentó P. rhizophorae, seguida en importancia por A. germinans, R. mangle y por último L. racemosa.
La mayor importancia de P. rhizophorae se debe principalmente a la cantidad de troncos presentes (216), lo cual influyó en una alta densidad relativa y alta frecuencia, no obstante su dominancia relativa fue la menor de todas las especies debido a su baja área basal producto de sus reducidos diámetros (4,51 cm en promedio) y la ausencia de fustales.
Por su parte, A. germinans presenta la mayor área basal y por tanto la mayor dominancia relativa, pero la densidad relativa es muy inferior a la de P. rhizophorae. La distribución de R. mangle es homogénea en el bosque por lo que registró la mayor frecuencia relativa, su área basal fue muy pequeña lo que influyó en su baja dominancia a pesar de tener el mayor número de fustales en la estación.
L. racemosa, a pesar de presentar los mayores diámetros (23,03 cm), lo cual influiría en una alta área basal, presentó la más baja densidad relativa con la presencia de tan solo 18 individuos entre latizales y fustales.
En cuanto a la regeneración natural se presentan en altas proporciones P. rhizophorae (2900 ind./0,1 ha) y R. mangle (2666,7 ind./0,1 ha), mientras que A. germinans y L. racemosa presentaron valores muy bajos, 500 y 133,3ind./0,1 ha, respectivamente. Se trata de un bosque joven y en crecimiento, con una gran cantidad de latizales que no alcanzan los 6 m de altura, el porcentaje de mortandad total es alto (44,3%), este aspecto y un porcentaje de tala del 10% han permitido el acceso de luz al sotobosque y con esto una alta regeneración natural (Tabla 2).
El punto inicial corresponde a la orilla del caño (Arroyo de Plata), el punto medio se encuentra a 50 m del punto inicial y el punto final está a 100 m del punto inicial, siendo este punto final el que corresponde al área donde se encontraron los líquenes sobre plantas de R. mangle con abundantes líquenes costrosos y estructuras degradadas o en proceso de degradación (hojas amarillentas, tallo descascarado).
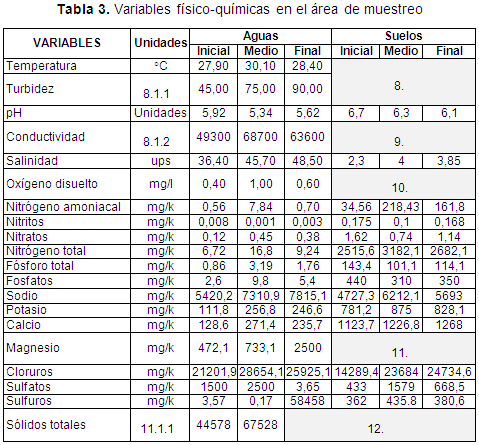
Peltigera sp., se halló en un área caracterizada por parámetros físico-químicos extremos en alguna medida, tanto de las aguas como de los suelos (aguas con temperatura de 28,4ºC, pH de 6,1,oxígeno disuelto de 0,60 mg/l, nitrógeno amoniacal de 0,70 mg/k, nitritos de 0,003 mg/k, nitratos 0,38 mg/k, nitrógeno total 9,24 mg/k, fósforo total 1,76 mg/k, fosfatos 5,4 mg/k, sodio 7815,1 mg/k, potasio 246,6 mg/k, calcio 235,7 mg/k, magnesio 2500,0 mg/k, cloruros 25925,1 mg/k, sulfatos 3,65 mg/k, sulfuros 0,17 mg/k, sólidos totales 67528,0 mg/k, y suelos con pH de 6,1-6,7, nitrógeno amoniacal de 161,8 mg/k, nitritos de 0,168 mg/k, nitratos 1,14 mg/k, nitrógeno total 2682,1 mg/k, fósforo total 114,1 mg/k, fosfatos 350,0 mg/k, sodio 5693 mg/k, potasio 828,1 mg/k, calcio 1268,0 mg/k, cloruros 24734,6 mg/k, sulfatos 668,5 mg/k, sulfuros 380,6 mg/k).

CONCLUSIONES
Los manglares de Arroyo de Plata presentan unas características mixtas, tipo maduro ribereño y de cuenca, conformado por individuos de R. mangle, A. germinans, L. racemosa y P. rhizophorae. Con la particularidad de que la especie invasora entre los manglares, P. rhizophorae, presenta el mayor IVI, debido a su alta densidad. Inicialmente el dosel es cerrado y posteriormente se abre a medida que se presenta degradación de la floresta y las condiciones físico-químicas son menos favorables.
El registro de los líquenes Peltigera sp. (Avendaño-Remolina et al., 2000), y su presencia en los manglares del Caribe colombiano, si bien es cierto es incidental, demuestra que gracias a su gran capacidad de adaptación a los cambios ambientales, bien pueden constituirse en bio-indicadores de las características ambientales y de las alteraciones actuales en Arroyo de Plata, cuya existencia se ve reforzada en el hecho de los manglares sobre los cuales se encontró el liquen, así como de los suelos poco estabilizados.
Entre otrasventajas que poseen los líquenes para ser utilizados como bioindicadores de lectura inmediata en los trópicos es que los trabajos pueden ser realizados sin la identificación total de las especies involucradas, y en el hecho de que son perennes y fácilmente determinados a simple vista o con la ayuda de una lupa de campo (Hawksworth et al., 2005, p. 71).
Los trabajos de Sipman (1984), Aguirre-Ceballos y Avendaño-Torres (2008), Avendaño-Torres y Aguirre-Ceballos (2009), Rincón-Espitia (2011),Rincón-Espitia et al. (2011),no citan a Peltigera sp., lo que ratifica que su hallazgo no solo es el primero para la Región del Caribe colombiano, sino que su distribución puede estar restringida a la zona costera del Caribe colombiano. En la Región Pacífico colombiano (Cordillera occidental-PNN Tatamá), Coca et al. (2012) la encontraron y manifiestan que en general la riqueza de especies de líquenes es similar a otros ecosistemas andinos (Sierra Nevada de Santa Marta-Buritaca-La Cumbre), obviamente todo podrá aclararse cuando se determinen los epítetos específicos.
AGRADECIMIENTOSQueremos agradecer a Eugenio Escobar-Manrique, profesor de la Universidad Nacional de Colombia sede Palmira, por la reconfirmación de la identidad de los ejemplares; y al Herbario José Cuatrecasas Arumí, donde se encuentran los ejemplares registrados en Arroyo de Plata (Bolívar) Colombia.
REFERENCIAS
• Agudelo-Ramírez, C. (2000). Estructura de los bosques de manglar del Departamento de Bolívar y su relación con algunos parámetros abióticos (Tesis Profesional). Fac. de Biología Marina, Univ.de Bogotá Jorge Tadeo Lozano. 318p. [ Links ]
• Aguirre-Ceballos, J. (2006). Diversidad de los musgos (Bryophyta) y líquenes de Colombia-Una evaluación con propósitos de conservación (Tesis Doctoral). Universidad Nacional de Colombia, Facultad de Ciencias, Instituto de Ciencias Naturales. 542p. [ Links ]
• ________. (2008). Diversidad y riqueza de líquenes en Colombia. En Rangel-Churio, J.O. (ed.), Colombia - Diversidad Biótica VI - Riqueza y diversidad de los musgos y líquenes en Colombia (pp. 1-18). Bogotá D.C.: Universidad Nacional de Colombia. 598 p. [ Links ]
• Aguirre-Ceballos, J. y Avendaño-Torres, K. (2008). Líquenes de la Región Caribe. En Rangel-Churio, J.O. (ed.), Colombia - Diversidad Biótica VI - Riqueza y diversidad de los musgos y líquenes en Colombia (pp. 383-387). Bogotá D.C.: Universidad Nacional de Colombia. 598 p. [ Links ]
• Aguirre-Ceballos, J. y Rangel-Churio, J.O. (2007). Amenazas a la conservación de las especies de musgos y líquenes en Colombia - Una aproximación. Caldasia, 29(2), 235-262. [ Links ]
• Alvarado-Ortega, M. (ed.). (2001). Canal del Dique. Plan de Restauración Ambiental, 1ª Etapa. Barranquilla: Ediciones Uninorte. 328 p. [ Links ]
• Avendaño-Remolina, D.; Sanjuán-Muñoz, A. y Álvarez-León, R. (2000). New lichen in the mangrove swamps of the Colombian Caribbean. UCR-Rev. Biol. Trop., 48(2/3), 719-724. [ Links ]
• Avendaño-Torres, K. y Aguirre-Ceballos, J. (2009). Estudio preliminar de los líquenes de la Serranía de Perijá. En Rangel-Churio, J.O. (ed.), Colombia -Diversidad Biótica VIII - Media y baja montaña de la Serranía del Perijá (pp. 223-228). Bogotá D.C.: Universidad Nacional de Colombia. [ Links ]
• Barreno, E. y Pérez-Ortega, S. (2003). Clave para la identificación de los Géneros + de Fotobiontes (según F. Bungartz, 2002, in Nash III et al., 2002) + de Líquenes (Gelatinosos, Fruticulosos, Foliáceos, Crustáceos, Escuamulosos, Dimórficos, Talos Leprarioides o Estériles) + Especies. Consejería del Medio Ambiente. Ordenación del Territorio e Infraestructuras del Principado de Asturias y KRK Ediciones. 133-429 p. [ Links ]
• Barreno, E. y Pérez-Ortega, S. 2003. Líquenes de la Reserva Integral de Muniellos Asturias. Oviedo (España). Cuad. Medio Amb. Serie Naturaleza 5. [ Links ]
• Bungartz, F. (2002). The chemistry of lichens: Emphasizing unique features a bit of history. Lecture for PLB 400 - Lichenology. Arizona State University. Natural History Collections. Arizona (Az) USA. [ Links ]
• CIOH/CARDIQUE. (1997). Caracterización y diagnóstico integral de la zona costeras comprendida entre Galerazamba y Bahía de Barbacoas (Tomo I y II). Dirección General Marítima. Centro de Investigaciones Oceanográficas/Hidrográficas (Corporación Autónoma Regional del Canal del Dique). Convenio de Cooperación CIOH /CARDIQUE. 694 p. [ Links ]
• Clesceri, L.S.; Greenberg, A.E. y Eaton, A.D. (1998). Standard methods for the examination of water and wastewater (20th edition) (Tomos I y II). Washington D.C.: APHA. 1983 p. [ Links ]
• Coca, L.F. y Sanín, D. (2010). Coccocarpia Pers. (Ascomicetes Liquenizados- Peltigerales) en Colombia. Trop. Bryo., 32, 19-38. [ Links ]
• Coca, L.F.; Sanín, D.; Posada-Herrera, J.M. y Sierra-Giraldo, J.A. (2012). Peltigerales (AscomycetesLiquenizados) del bosque alto andino del Parque Nacional Natural Tatamá, Colombia. Bol. Cient. Mus. Hist. Nat., 16(1), 60-72. [ Links ]
• Hawksworth, D.L.; Iturriaga, T. y Crespo, A. (2005). Líquenes como bioindicadores inmediatos de contaminación y cambios medio-ambientales en los trópicos. Rev. Iberoam. Micol., 22, 71-82. [ Links ]
• Hinestrosa, R. y Viña, G. (1986). Efectos del dragado de zonas de manglar y geomorfología deltaica y desarrollo en el Canal Lequerica, Bahía de Barbacoas (Tesis Profesional). Fac. de Biología Marina, Univ. de Bogotá Jorge Tadeo Lozano. [ Links ]
• Martínez, I. (1999). Taxonomía del género Peltigera Willd. (Ascomycetes liquenizados) en la Península Ibérica y estudio de sus hongos liquenícolas. Ruizia, 15, 1-200. [ Links ]
• Martínez, I.; Burgaz, A.R.; Vitikainen, O. y Escudero, A. (2003). Distribution patterns in the genus Peltigera Willd. Lichenologist, 35, 301-323. [ Links ]
• Matteucci, S. y Colma, A. (1982). Metodología para el estudio de la vegetación. OEA. Monografía No. 22 Serie Biología. Programa Regional de Desarrollo Científico y Tecnológico. Washington D.C. 168 p. [ Links ]
• Miadlikowska, J. y Lutzoni, F. (2000). Phylogenetic revision of the genus Peltigera (lichen-forming Ascomycota) based on morphological, chemical, and large subunit nuclear ribosomal DNA data. Int. J. Plant Sci., 161(6), 925-958. [ Links ]
• Nash III, T.H.; Ryan, B.D.; Gries, C. y Bungarts, F. (eds.). (2002). Lichen Flora of the Greater Sonoran Desert Region (Vol. I). Lichens Unlimited, Arizona State University. Tempe, Arizona (USA). 532 p. [ Links ]
• Pérez-Quintero, A.L. y Watteijne-Cerón, B. (2010). Estructura de una comunidad de líquenes y morfología del género Sticta (Stictaceae) en un gradiente altitudinal. Acta Biológica Colombiana, 14(3), 157-170. [ Links ]
• Pino-Renjifo, J.C.; Sanjuán-Muñoz, A. y Avendaño-Remolina, D. (1999). Diagnóstico y zonificación de las áreas de manglar del Departamento de Bolívar. Corporación Autónoma Regional del Canal del Dique (CARDIQUE). Informe Final. Cartagena de Indias (Bol.). 375 p. [ Links ]
• Rincón-Espitia, A.J. (2011). Composición de la flora de líquenes corticícolas en el Caribe colombiano (Tesis de Maestría). Fac. de Ciencias, Departamento de Biología, Univ. Nacional de Colombia. 180 p. [ Links ]
• Rincón-Espitia, A.J.; Aguirre, J. y Lücking, R. (2011). Líquenes corticícolas en el Caribe colombiano. Caldasia, 33(2), 331-347. [ Links ]
• Sánchez-Páez, H.; Álvarez-León, R.; Pinto-Nolla, F.; Sánchez-Alférez, A.; Pino-Renjifo, J.C.; García-Hansen, I. y Acosta-Peñalosa, M. (1997). Diagnóstico y zonificación preliminar de los manglares del Caribe de Colombia. Proyecto MMA-OIMT. Santa Fe de Bogotá, D.C. 509 p. [ Links ]
• Schaeffer-Novelli, Y. y Cintrón-Morelo, G. (1986). Guia para estudo de áreas de manguezal. Estrutura, função e flora. São Pablo: Caribbean Ecological Research. 25 p. [ Links ]
• Sipman, H.J.M. (1984). Líquenes del transecto Buritaca-La Cumbre. La Sierra Nevada de Santa Marta, Colombia. En Van der Hammen, T. y Ruiz, P.M. (eds.), Studies on Tropical Andean Ecosystems, 2 (pp. 185-188). J. Cramer. Berlin: J. Cramer. 603 p. [ Links ]
• Sipman, H.J.M. (2008). Checklist of lichens and lichenicolous fungi of Colombia, H. Sipman (Berlin) is working on a checklist of Colombian lichens. Disponible en: http://www.biologie.uni-hamburg.de [ Links ]
• Sipman, H.J.M.; Hekking, W. y Aguirre, J. (2008). Checklist lichenized and lichenicolous fungi of Colombia. Biblioteca José Jerónimo Triana, 20, 1-242. [ Links ]
• Soto-Medina, E. (2011). Contribución al conocimiento de los líquenes del Valle del Cauca y Cauca (Colombia). En Resúmenes. VI Congreso Colombiano de Botánica. II Simposio Colombiano de Liquenología. Biodiversidad, Desarrollo y Cultura: Una Visión Integradora. Cali (Valle) Agosto 11-15, 2011 (p. 103). 621 p. [ Links ]
• Van Duunné, H.J.F. y Wolf, J.H.D. (s.f.). Development of ephylitic and bryophyte and lichen vegetation on plantation coffee tree. pp. 95-111 Chapter 6. University of Amsterdam. [ Links ]
• Vitikainen, O. (1998). Taxonomic notes on neotropical species of Peltigera. En Marcelli, M.P. y Seaward, M.R.D. (eds.) Lichenology in Latin America: History, Current Knowledge and Applications (pp. 135-139). São Paulo: CETESB. [ Links ]
• Wolf, J. (1993). Diversity patterns and biomass of epiphytic bryophytes and lichens along an altitudinal gradient in the northern Andes. Ann. Mo. Bot. Gard., 80, 928-960. [ Links ]
Para citar este artículo: Álvarez-León, R., Avendaño-Remolina, D. & Sanjuán-Muñoz, A. M. (2014). La relación entre Peltigera sp. y Rhizophora mangle en Arroyo de Plata (Bolívar), Caribe colombiano. Revista Luna Azul, 38, 105-121. Recuperado de http://lunazul.ucaldas.edu.co/index.php?option=content&task=view&id=896













