1 | INTRODUCCIÓN
Como resultado del incremento en el consumo de biodiesel a escala mundial hay sobreoferta de glicerina, la cual se genera como subproducto en relación de 10% en peso con respecto a la producción de biodiesel [1][2].
La glicerina que se sale directamente del proceso está contaminada con agua, metanol, trazas de jabones, sales orgánicas e inorgánicas y color, por este motivo se le denomina Glicerina Cruda (GC) [3]. Las impurezas de GC no permiten su utilización directa como materia prima debido a la toxicidad implícita y bajo rendimiento en procesos químicos.
La GC se purifica para obtener GT con el fin de valorizarla como precursor químico para producir derivados como 1,3-propanodiol [4], ácido succínico, glicerina carbonatada [5], acetinas [6][7], biopolímeros [8][9], gas de síntesis, hidrógeno [10], entre otros [11][5]. El proceso convencional para purificar la GC consta de varias etapas: A) Neutralización con ácidos inorgánicos como sulfúrico o fosfórico para remover jabones. B) Evaporación al vacío para retirar metanol. C) Lavado con agua y D) Destilación para retirar el exceso de humedad. E), Filtración con carbón activado para retirar color. Con los métodos recientemente descritos se obtiene GT que tiene aproximadamente 97.5% de pureza [12][13][14].
Existen otros procesos de purificación los cuales se pueden combinar para purificar la glicerina para llevarla hasta grado USP (99,7% pureza) tales como destilación a alto vacío, ultrafiltración con membranas, separación de trazas indeseables con resinas de intercambio iónico sin embargo estas operaciones aún son muy costosas [15][16]. Se han desarrollado estrategias para tratar de disminuir los costos de purificación combinando varios métodos de purificación [17][18][19].
Uno de los procesos importantes de trasformación química de glicerina es la acetilación con anhídrido acético o AA para producir mezclas de mono, di, tri acetil gliceroles (MDTAG) [20][21][22]. Mono acetil glicerol (MAG) y diacetil glicerol (DAG) y triacetil glicerol (TAG) se usan como aditivos oxigenantes para combustibles, precursores en síntesis de biopolímeros, plastificantes, alimentos y cosméticos [2][6][7][23]. MDTAG, se caracterizan por tener puntos de fusión muy bajos: -30 °C (DAG) [24], -78 °C (MAG, TAG) [25][26] y elevados puntos de ebullición: 280 °C (DAG) [24], 258259 °C (MAG, TAG) [25][26]. MDTAG también se denominan: mono, di, tri acetinas.
En el pasado la reacción de acetilación se realizaba con catálisis homogénea, empleando ácidos fuertes inorgánicos como el ácido sulfúrico [27][28], sin embargo esta técnica ha sido abandonada gradualmente debido a los riesgos asociados con el manejo de este tipo de sustancias. Actualmente el proceso químico se lleva a cabo en presencia de catalizadores heterogéneos que son resinas de intercambio iónico, estos materiales intercambian iones con el medio reaccionante, generalmente están compuestas de una matriz polimérica insoluble (copolímeros de poliestireno-divinilbenceno) [11][29][30][31]. Comercialmente las resinas Amberlyst 15® y Amberlyst 35® son catalizadores eficientes en las reacciones de acetilación [32]. A nivel industrial se preiere la esteriicación de la glicerina con AA en lugar del anhídrido acético, por facilidad en el control de la reacción, el ácido tiene menor reactividad con respecto al anhídrido, además no es tóxico [33].
El mecanismo de la esterificación con AA ha sido ampliamente estudiado, como regla general las reacciones se llevan a cabo con exceso de ácido. Se acepta que inicialmente ocurre una protonación promovida por el catalizador sobre el oxígeno electrónico par del AA, seguido por una sucesión de ataques nucleofílicos sobre el grupo OH del glicerol para producir MAG y agua. MAG en una segunda etapa puede reaccionar con una nueva molécula electrofílica de AA para producir DAG y agua [34][35]. DAG también puede reaccionar con otra molécula de AA para producir TAG [32][36]. En general el avance de la reacción esta gobernado por la temperatura y tiempo de reacción [20]. El mecanismo de reacción está fuertemente influenciado por el tipo de catalizador [37][38] y la estequiometría, por ejemplo, una relación molar (glicerol: AA, 1:4) produce principalmente MAG y DAG, mientras que (glicerol: AA, 1:9) es selectiva hacia TAG [28].
En este estudio se sintetizará a escala de laboratorio MDTAG a partir de la reacción de acetilación entre glicerina grado técnico proveniente de la industria del biodiesel y ácido acético en presencia de catalizador heterogéneo. MDTAG serán caracterizados por medio de espectroscopia de infrarrojo y se evaluarán las propiedades térmicas por medio de calorimetría diferencial de barrido.
2 |MATERIALES
2.1 Materiales
GT (pureza 97,5%, Cereus Advanced Chemistry®, MonterreyMéxico); AA (pureza 99%, Sucroal® S.A., Palmira-Colombia), Resina de intercambio iónico Amberlyst 15® (Sigma Aldrich®, St. LouisUSA), tolueno (pureza 99%, Shell Chemicals®, HoustonUSA), agua desionizada (Albor Químicos®, BogotáColombia)
2.2 | Síntesis de MDTAG
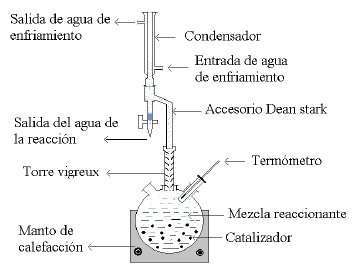
La reacción de acetilación se realizó en un reactor de vidrio de 500 cm3, equipado con manta de calentamiento y agitación magnética, baño térmico en aceite mineral, termómetro, torre de fraccionamiento vigreux, accesorio dean stark, condensador con agua de enfriamiento (Ver Fig. 1). Se usó la relación molar (GT:AA, 1:6), el volúmen de la mezcla de reactivos fue 137,7 cm3; se añadieron 163,8 cm3 de tolueno al sistema. Cuando la mezcla reaccionante alcanzó la temperatura de 95 °C, se adicionaron 2,5 gramos de Amberlyst®15, dando inicio a la reacción, la cual duró 4,5 horas, la máxima temperatura alcanzada fue 110 °C.
Durante el desarrollo de la reacción, se retiró periodicamente el agua producida, usando el tolueno como agente de arraste, el agua salió a través del accesorio dean stark. MDTAG se llevaron a un equipo de destilacion a vacío para eliminar el exceso de AA, posteriormente fueron lavados con agua desionizada y finalmente MDTAG se sometieron a roto-evaporación durante 2 horas a 60 °C y presión 15 mmHg, para eliminar humedad y trazas de AA.
2.3 | Espectroscopia de infrarrojo
El análisis por espectroscopia de MDTAG se realizó por medio de infrarrojo con transformada de Fourier (FT-IR) en un espectrómetro Nicolet® iS10 (Thermo Fisher Scientific®). Con la técnica de muestreo de reflectancia total atenuada horizontal (HATR), las muestras se colocaron en contacto directo sobre el accesorio Smart ARK® a 23 °C. Los espectros FT-IR fueron adquiridos con una resolución de 4 cm-1, número de scans de 32 y rango espectral de 4000-650 cm-1.
2.4 | Calorimetría diferencial de barrido (DSC)
El análisis térmico se hizo en un calorímetro DSC Serie Q20 de TA Instruments®. Se pesaron 10-12 mg de MDTAG en un crisol de aluminio abierto, éste se colocó en la celda DSC Tzero® con un crisol vacío como referencia. Para estudiar el comportamiento a temperaturas bajas, las muestras se purgaron con un flujo de nitrógeno (N2) de 50 ml/min y se llevaron rápidamente a 50 °C, luego se mantuvieron en condiciones isotérmicas durante 10 min. Posteriormente, el sistema se enfrió a -50 °C a una velocidad de 10 °C/min. Cuando las muestras alcanzaron los -50 °C, inmediatamente se realizó el proceso de calentamiento llevando el sistema hasta 50 °C con una velocidad de 10 °C/min. Los datos se analizaron con el software Universal Analysis 2000®, versión 4.5A (TA Instruments®).
3 | RESULTS AND DISCUSSION
3.0.1 | Análisis espectral de MDTAG
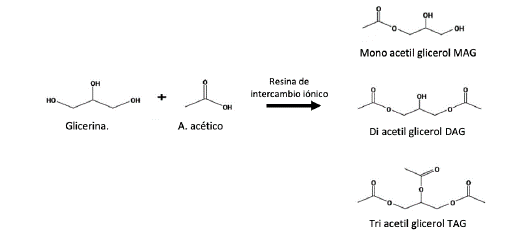
La Fig. 2 muestra el esquema básico de la reacción de acetilación. y son ésteres que tienen dos y un grupo (-OH) respectivamente, TAG no posee (-OH).
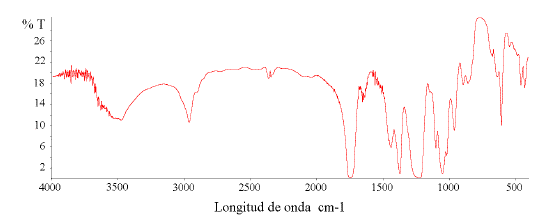
La Fig. 3 muestra el espectro FT-IR de MDTAG. Se observa con claridad las tres (3) bandas representativas de compuestos tipo éster: a) La vibración tipo stretch (fuerte y alargada) ubicada en 1750 cm-1 corresponde al enlace (C=O) [39]. b) La segunda banda característica se encuentra según la literatura en la longitud de onda: 1250cm-1. corresponde a la vibracion stretch del enlace C-O [39], en la Fig. 3 se observa claramente esta banda en 1225cm-1. c) La tercera banda importante del enlace C-O también corresponde a la vibración stretch, la cual se observa en 1055cm-1 [39].
La presencia de MAG y DAG se verifica por la presencia de la banda de absorción característica del enlace (O-H) en la región de 3450cm-1. La baja intensidad de esta banda también proporciona información acerca de la presencia de TAG. La banda correspondiente al enlace saturado del carbono unido al hidrógeno (C-H) se ubica en la región de 2900-3000 cm-1 [39], en la Fig. 3 se observa este pico en 2950cm-1.
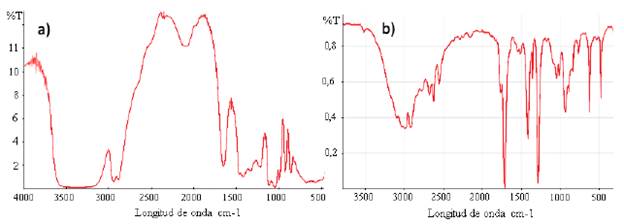
El espectro de MDTAG obtenido experimentalmente no presenta la banda de absorción en 1150cm3 la cual es característica de la glicerina, confirmando el avance de 100 % de la reaccion (la glicerina es el reactivo limitante, su espectro IR se muestra en la Fig. 4-a). El espectro MDTAG tampoco presenta una banda en 1330cm-1 la cual corresponde al ácido acético (Ver Fig. 4-b), indicando que la etapa de purificación fue eficiente.
3.0.2 | Comportamiento a baja temperatura de MDTAG
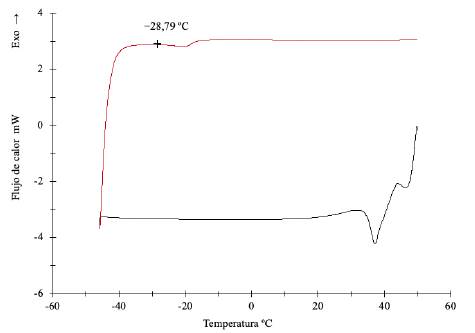
La Fig. 5 muestra las curvas de enfriamiento desde 50 hasta -50 °C y calentamiento (-50 hasta 50 °C) de MDTAG.
Curva de Enfriamiento: Nose observa la formación de algún pico de cristalización en temepraturas cercanas a 30 °C, el cual podría indicar formación de cristales de DAG. Los picos de MAG y TAG no se observan debido a que el punto de fusión de estas sustancias es 78 °C [25][26]. Curva de calentamiento: Se observa el inicio de la formacion de un pico suave de tipo endotérmico en 28,79 °C el cual podría tener relación con la fusión de DAG, cuya temperatura reportada en la literatura es 30 °C [24]. La ausencia de picos fuertes o agudos de cristalización y fusión indican que la mezcla de MDTAG son candidatos potenciales para considerarlos como aditivos para mejorar el desempeño a baja temperatura de biolubricantes.
4 | CONCLUSIONES
Se logró sintetizar una mezcla de mono, di, tri acetil gliceroles a partir de la esterificación de glicerina grado técnico con acido acético. Por esta via se puede lograr una valorización del glicerol proveniente de la producción de biodiesel. MDTAG presentaron excelente desempeño a baja temperatura desde el punto de vista de fluidez debido a que no presentaron cambio hacia la fase sólida (ausencia de cristalización). MDTAG podrian ser considerados como aditivos para mejorar la fluidez a baja temperatura de bases lubricantes derivadas de aceites vegetales.