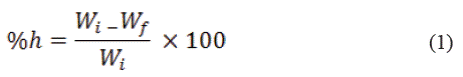I. NOMENCLATURA
Aw: Actividad de agua
TGA: Termogravimetría
IR FT: Infrarrojo con transformada de Fourier
DNS: Determinación de azúcares reductores por el método del ácido 3,5-dinitrosalicílico.
°Brix: Grados Brix
NTC: Norma técnica colombiana.
II. INTRODUCCIÓN
En los últimos años se ha incrementado la producción y comercialización de productos, como los edulcorantes naturales y artificiales catalogados como no calóricos, en contraste con la reducción del consumo de azúcares simples o concentrados como la glucosa, fructosa y sacarosa, debido a las necesidades del mercado, que busca productos funcionales, es decir con valor nutricional, pero con poder edulcorante similar a la sacarosa, bajo aporte calórico y disponibilidad a bajo costo [1].
A nivel industrial deben cumplir con ciertas condiciones para ser catalogados como edulcorantes, entre las que se encuentran, la inocuidad, las características organolépticas que le permitan ser percibido inmediatamente, que pueda degradarse rápidamente, ser lo más parecido al azúcar en cuanto al sabor, pero con menor aporte calórico y como consecuencia menos problemas de salud en términos de obesidad, diabetes y caries dental, debe ser termoestable y tener la capacidad de combinación con otros alimentos sin perder sus propiedades fisicoquímicas [2].
Bajo ésta premisa, día a día ganan un importante espacio en el mercado mundial los polioles, cuya característica más importante es que se comportan como el azúcar, pero con menor aporte calórico, tal como lo muestra la Tabla I.
TABLA I EDULCORANTES BAJOS EN CALORÍAS[2].
| Edulcorante Bajo en Calorías | Valor Calórico | Valor Calórico en relación al Azúcar | Dulzor en relación al Azúcar |
| Calorías/gramo | % | % | |
| POLIOLES | |||
| Eritritol | 0,2 | 5 | 70-80 |
| Isomalt | 2,0 | 50 | 45-65 |
| Lactitol | 2,0-2,4 | 50-60 | 40 |
| Maltitol | 2,1 | 52 | 90 |
| Manitol | 1,6 | 40 | 50 |
| Sorbitol | 2,4-2,6 | 60-65 | 60 |
| Xilitol | 2,4 | 60 | 100 |
| Otros | |||
| Tagatosa | 1,5 | 38 | 90-100 |
| Trehalosa | 3,6 | 90 | 50 |
Dentro de los edulcorantes naturales bajos en calorías, se destaca el xilitol, cuya tasa de producción anual se estima en 200000 Ton, según datos del International Starch Institute [3]. El xilitol es un poliol pentahidroxilado de fórmula molecular C5H12O5, que ha atraído el interés de muchos investigadores gracias a sus propiedades fisicoquímicas que lo hacen apto para ser usado en la industria farmacéutica, alimenticia, higiene oral, entre otras [4].
Presenta una elevada estabilidad química y microbiológica que le permite actuar como preservante en alimentos, no sufre pardeamiento de Maillard, genera un efecto refrescante en la boca por su calor de disolución endotérmico (34,8cal/g), tiene un poder edulcorante similar a la sacarosa, pero con menor aporte calórico, que lo convierten en una sustancia química ideal para ser utilizada por personas con problemas de obesidad y diabetes, ya que su metabolismo es independiente de la insulina, es anticariogénico, convirtiéndolo en materia prima importante en la fabricación de diversos productos de higiene oral y gomas de mascar.
La literatura reporta aplicaciones en el campo de la salud como prevención de la osteoporosis, la otitis media en los niños, los procesos inflamatorios y las infecciones respiratorias [5].
Se encuentra de forma natural en algunas frutas y verduras, pero su extracción es poco rentable por las bajas concentraciones (900mg/100g) [6].
Es producido industrialmente por hidrogenación química de la D-xilosa, en presencia de un catalizador como el níquel, a altas temperaturas y presiones, convirtiéndolo en un producto costoso debido a las etapas de separación y purificación. Como alternativa han surgido en los últimos años los procesos biotecnológicos (enzimático y microbiano), que podrían ser atractivos en la generación de un producto de alta calidad, bajo costo, ahorro energético y ante todo amigable con el medio ambiente en términos de reducción de contaminantes propios del proceso químico [7].
En cuanto al uso del ultrasonido como pretratamiento para mejorar la disponibilidad de azucares fermentables en la producción de xilitol, la elección obedece a reportes en la literatura [8] que describen la técnica como:
Amigable con el medio ambiente, ya que no genera subproductos contaminantes y difíciles de eliminar, como el furfural y el hidroximetil-furfural, generados en otros pretratamientos.
El consumo de energía es menor en comparación con otros, puesto que no se requieren altas temperaturas y presiones.
Los costos de producción son bajos por la no utilización de catalizadores que son de alto costo en el mercado como el níquel Raney.
Sus aplicaciones en diferentes áreas de la ciencia avalan la técnica.
Los parámetros fisicoquímicos de la biomasa de un material vegetal como éste, es promisorio para la obtención del xilitol, ya que es un proceso biotecnológico de bajo costo y alta productividad. El presente trabajo tiene como objetivo, determinar parámetros fisicoquímicos en las hojas de Eucalipto camaldulensis y su hidrolizado, en la producción de xilitol vía fermentativa, utilizando cepas del género candida, reconocidas en este campo como la tropicalis y la guilliermondii.
III. MATERIALES Y MÉTODOS
A. Desarrollo experimental
1. Materiales y métodos
El estudio parte de la selección del material vegetal, tomando muestras de hojas de eucalipto de la finca el progreso, ubicada en la intersección Circasia I, a 12 Kilómetros de la capital del departamento del Quindío y temperatura promedio de 18oC.
El material fue llevado al CIBUQ (Centro de Investigaciones Biológicas de la Universidad del Quindío), para la caracterización taxonómica correspondiente.
2. Preparación de la muestra
El material vegetal fue sometido a una serie de pretratamientos físicos y químicos necesarios en la obtención de un sustrato óptimo para desarrollar procesos fermentativos.
3. Análisis físico
Las hojas de Eucalipto camaldulensis fueron retiradas de las ramas, para determinar su masa en balanza analítica (Mettler Toledo P8602-S), luego sometidas a un proceso de secado en un horno de recirculación de aire a temperatura de 40oC, a diferentes tiempos, 24, 48 y 72h, hasta tener masa constante, según la norma NTC 1495.
El material seco se sometió a trituración y molienda (molino eléctrico siemens, 1725 rpm); posteriormente se utilizó un tamiz eléctrico marca Gilson, modelo SS-15 con tamaño de poro de 0,2mm, para obtener un tamaño de partícula que favoreciera los análisis posteriores.
3.1 Análisis químico
Con el material vegetal preparado, se procedió a determinar los parámetros fisicoquímicos, antes y después de hidrolizar por ultrasonido y por hidrólisis ácida, en los laboratorios de diseño de nuevos productos, plaguicidas y análisis instrumental de la Universidad del Quindío.
3.2. Caracterización fisicoquímica del material vegetal
Los parámetros fisicoquímicos determinados fueron: sólidos solubles totales, por refractometría (Mettler Toledo 30PX, intervalo de 0-85 °Brix), por conversión de índice de refracción a °Brix, según la norma NTC 4624; actividad de agua (Aw) con 4 repeticiones, en un higrómetro de punto de rocío (AquaLab serie 3 TE, marca Decagón, con punto de sensibilidad de 0,001); infrarrojo (FT IR) en equipo (Thermo Nicolet, Avatar 370), a la muestra vegetal pulverizada antes de la hidrólisis, y después al bagazo producto del filtrado; Termogravimetría (TGA), en analizador termogravimétrico (Netzsch, modelo TG 209 F1).
3.3 Hidrólisis del sustrato
Permite remover la lignina y la hemicelulosa, disminuyendo la cristalinidad de la celulosa y aumentando la porosidad del material, lo que conlleva a la exposición de azúcares fermentables disponibles para los microorganismos en procesos fermentativos.
En el presente estudio se efectuaron dos tipos de hidrólisis que permitieron establecer las mejores condiciones para el sustrato a fermentar.
En la hidrólisis ácida se utilizó como catalizador H2SO4 buscando romper las cadenas de polisacáridos (celulosa y hemicelulosa), que forman las paredes de las hojas en el Eucalipto camaldulensis en sus monómeros elementales, según la metodología reportada por I.S.M. Rafiqul et al, 2013.
Se utilizaron 20g de material vegetal en 100mL de solución al 2% (v/v) de H2SO4 con reflujo por 1h y 30min a 120oC, se dejó enfriar a temperatura ambiente, se añadió CaCO3 ajustando el pH a 5, se filtró y centrifugó para eliminar residuos tóxicos y precipitar sólidos, en un equipo Indulab Ref. 035 y 3000rpm.
El hidrolizado centrifugado se detoxificó adicionando 2g de carbón activado por cada 100mL de hidrolizado por 20min a 30oC, tomando una muestra para cuantificar azúcares reductores y sólidos solubles.
La hidrólisis por ultrasonido se efectuó en un equipo Branson, modelo 3510R-MT, utilizando 2 muestras diferentes de material vegetal, evaluando condiciones de pH y °Brix en función del tiempo.
Se utilizaron 20g de cada muestra en 100mL de agua desionizada, las muestras se sonicaron por 30min y 60min respectivamente, se filtraron y fueron sometidas al análisis fisicoquímico correspondiente.
3.4 Caracterización fisicoquímica del hidrolizado
Se hicieron análisis de pH por potenciometría, según la NTC 4592; acidez titulable con solución patrón de NaOH 0,1N según la NTC 4623; azúcares reductores por DNS y absorbancia a 540nm en espectrofotómetro UV VIS (Hewlett packard, modelo 8453); sólidos solubles totales por refractometría en un equipo (Mettler Toledo 30PX, intervalo de 0-85 °Brix), según la NTC 4624.
IV. RESULTADOS Y DISCUSIÓN
A. Tratamiento del material vegetal
1. Porcentaje De Humedad (%h)
Es un parámetro muy importante en caracterización de material vegetal, porque permite determinar la cantidad de agua en una muestra vegetal y con ello predecir la actividad microbiana [9].
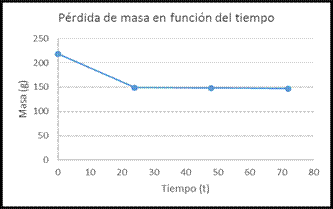
Los valores de humedad se determinaron por pérdida de masa en la muestra en horno de recirculación de aire a 40 oC, por tiempos de 24, 48 y 72 horas, obteniendo los siguientes resultados, ver Tabla II.
TABLA II MASA EN FUNCIÓN DEL TIEMPO.
| Tiempo de secado en horas | Masa (g) |
|---|---|
| 0 | 218,52 |
| 24 | 148,92 |
| 48 | 147,94 |
| 72 | 147,16 |
La Fig. 1 muestra que la cantidad de masa no presentó variaciones significativas entre las 24 y 72 horas, lo que se traduce en que la pérdida de masa en la muestra es mínima en este tiempo, concluyendo que con 24 horas de secado de la muestra vegetal se logra la remoción completa del agua libre, quedando un porcentaje de humedad correspondiente al agua ligada que hace parte de los compuestos estructurales.
El porcentaje de humedad en la muestra de eucalipto se determinó utilizando la siguiente expresión matemática reportada en la literatura [10,11].
Donde: h es la humedad, Wi el peso inicial y Wf es el peso final.
Se determinó que el porcentaje de agua en la muestra vegetal fue de 32,65%, demostrando que es apto como sustrato en la producción de xilitol, sin verse afectado por la actividad microbiana antes de la fermentación [12].
2. Caracterización fisicoquímica del material vegetal
2.1 Actividad de agua (Aw)
Corresponde al agua disponible para que los microorganismos desarrollen las actividades metabólicas; la escala que permite establecer este parámetro se encuentra entre 0 y 1; valores por debajo de 0,6 son indicativos de la no contaminación de la muestra por microorganismos [13].
En el laboratorio de investigación y diseño de nuevos productos de la Universidad del Quindío y utilizando un higrómetro de punto de rocío a 24°C, se realizó el análisis correspondiente, obteniendo un valor promedio de 0,518, con una desviación estándar de 1,29*10-3 y coeficiente de variación de 0,24, que demuestra poca variabilidad en los datos; el valor promedio indica que la muestra vegetal es apta para análisis posteriores sin verse afectada por la actividad microbiana, ver Tabla III.
TABLA III VALORES DE ACTIVIDAD DE AGUA DE LA MUESTRA VEGETAL
| Análisis | Actividad de agua (Aw) | Temperatura (°C) |
|---|---|---|
| 1 | 0,518 | 24,8 |
| 2 | 0,517 | 24,8 |
| 3 | 0,518 | 25,0 |
| 4 | 0.520 | 25,0 |
| Promedio | 0,518 | |
| D. estándar | 1,29*10 -3 |
2.2 Grados Brix (°Brix)
Los grados Brix indican la cantidad de sólidos solubles en una muestra vegetal, que permiten determinar la viabilidad del sustrato como materia prima en procesos fermentativos con microorganismos.
Los análisis se llevaron a cabo utilizando un refractómetro portátil, con 4 repeticiones, como lo muestra la Tabla IV.
TABLA IV GRADOS BRIX EN EUCALIPTO CAMALDULENSIS.
| Análisis | Índice De Refracción | Grados Brix |
|---|---|---|
| 1 | 1,338 | 4,00 |
| 2 | 1,337 | 3,00 |
| 3 | 1,338 | 4,00 |
| 4 | 1,338 | 4,00 |
| Promedio | 3,75 |
De acuerdo con los datos obtenidos se determinó en promedio un 3,75% de sólidos solubles totales por cada 100g de muestra, esto quiere decir que hay 3,75g de azúcares por 96,25g de agua.
Con el análisis realizado se determina que es necesario llevar a cabo un pretratamiento buscando mejorar la cantidad de sólidos disueltos por la disponibilidad de los azúcares en el medio.
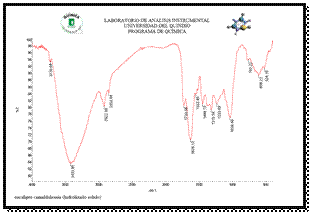
2.3 Infrarrojo (IR-FT)
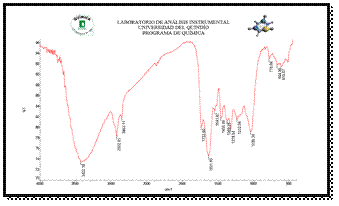
Una vez aislada y purificada la sustancia, se midió el espectro infrarrojo en un equipo (FT IR) hermo Nicolet, Avatar 370), tal como se muestra en la Fig. 2,
El espectro de infrarrojo muestra a los 3422 cm-1 una banda ancha propia de grupos hidroxilo (-OH), que exhiben absorción en infrarrojo (vibración por alargamiento en 3000 - 3700 cm-1) [7].
2.4 Termogravimetría (TGA).
El análisis termogravimétrico del Eucalipto camaldulensis se hizo buscando determinar el comportamiento de la masa en función del tiempo y la temperatura.
La curva primaria de la Fig. 3 representa el cambio porcentual de masa del material vegetal, con relación al aumento en la temperatura.
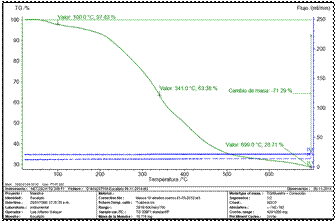
Fig. 3 Análisis termogravimétrico (TGA) del Eucalipto camaldulensis (masa en función de la temperatura).
Se observa que a 100oC todavía se mantiene un 97,83% de muestra, hasta ese momento la pérdida de masa corresponde al agua libre que contiene; a 341oC se mantiene un 63,38% de masa y a 699 oC un 28,71% de masa, demostrando ser un material estable térmicamente para ser usado a nivel de laboratorio y como materia prima en procesos industriales.
3. Caracterización Fisicoquímica de los Hidrolizados
De acuerdo con los datos obtenidos en la caracterización fisicoquímica del material vegetal, se hizo necesaria la aplicación de pretratamientos, buscando romper la pared vegetal de la muestra dejando expuestos los azúcares fermentables.
Los hidrolizados obtenidos por ultrasonido y por hidrólisis ácida se sometieron a análisis fisicoquímicos, que permitieron evaluar cuál de los dos procedimientos es el más adecuado para la conversión de D-xilosa en xilitol por fermentación.
3.1. Acidez Titulable y pH.
La acidez titulable corresponde a la cantidad de ácido presente en una solución determinada, para la titulación se utilizó una solución patrón de hidróxido de sodio 0,1 N, de acuerdo con la siguiente expresión:
Dónde: C1 y C2 corresponden a la concentración inicial y final respectivamente, en # equivalentes/litro, V1 y V2 corresponden al volumen inicial y final respectivamente en litros.
Se efectuaron 3 ensayos con 3 ml de muestra y se procedió a titular con hidróxido de sodio 0.1 N hasta alcanzar el punto de neutralización, utilizando como instrumento el potenciómetro.
El procedimiento se efectuó tanto en el hidrolizado por ultrasonido como en el realizado por vía ácida; para medir el pH de cada uno de los hidrolizados se hizo directamente con el pH-metro y se registraron los valores.
3.2 Acidez titulable y pH del hidrolizado por ultrasonido
La acidez titulable fue de 0.0166N, teniendo en cuenta la concentración del ácido en el punto de neutralización.
Utilizando el pH-metro se obtuvo un pH de 5.07 en el hidrolizado, que indica que es un medio adecuado para el crecimiento y desarrollo metabólico de las levaduras [12-14].
Acidez titulable y pH del hidrolizado vía ácida, ver Tabla V.
TABLA V ACIDEZ TITULABLE POR HIDRÓLISIS ÁCIDA.
| Solución | mL de NaOH adicionados | pH | Concentración (N) |
|---|---|---|---|
| 1 | 8,2 | 8,81 | 0,2733 |
| 2 | 8,0 | 7,10 | 0,2666 |
| 3 | 7,9 | 7,04 | 0,2633 |
La acidez titulable fue de 0,2633N, teniendo en cuenta la concentración del ácido en el punto de neutralización.
El pH del hidrolizado fue de 1,38, demostrando ser un medio poco apto para el desarrollo metabólico de los microorganismos a utilizar en la fermentación.
De los resultados anteriores se concluye sobre la importancia de detoxificar y clarificar el sustrato cuando se aplica hidrólisis ácida, ya que el pH tan bajo puede estar relacionado con la presencia de contaminantes en el medio propios de la reacción.
Comparando los valores obtenidos en términos de acidez y pH en ambos hidrolizados, se concluye que la hidrólisis por ultrasonido es un pretratamiento adecuado para ser usado en la producción de xilitol vía fermentativa, en comparación con la hidrólisis ácida que necesita de procedimientos como detoxificación y clarificación adicional para mejorar las condiciones y volverlo apto, lo que conlleva a contaminación por subproductos, gasto de energía, tiempo y reactivos.
3.3. Grados Brix
La determinación de sólidos solubles se efectuó tanto al hidrolizado por ultrasonido como al hidrolizado vía ácida, obteniendo los resultados que a continuación se relacionan en la Tabla VI.
TABLA VI SÓLIDOS SOLUBLES PARA LOS HIDROLIZADOS DE EUCALIPTO CAMALDULENSIS.
| Determinación de sólidos solubles ( o Brix) | ||||
|---|---|---|---|---|
| Ensayos | Hidrolizado por ultrasonido | Hidrolizado vía ácida | ||
| 30 min | 60 min | |||
| 1 | 5,1 | 5,1 | 7,5 | |
| 2 | 5,3 | 5,4 | 5,9 | |
| 3 | 6,0 | 5,9 | 5,2 | |
| Promedio | 5,5 | 5,5 | 6,2 | |
Teniendo en cuenta que los sólidos solubles se determinaron para el hidrolizado por ultrasonido a los 30min y a los 60min, buscando determinar la influencia del tiempo en el procedimiento, se puede observar que dicha variable no es determinante en la obtención de azúcares fermentables, ya que no hay diferencias en los valores promedio obtenidos, consistente con los resultados reportados por Kim, J.H., et al. 2002 [15].
Aunque los resultados obtenidos para el hidrolizado vía ácida son superiores a los obtenidos en el hidrolizado por ultrasonido, estos caen drásticamente al realizar el proceso de detoxificación, centrifugación y clarificación, llegando a un valor de 3,5, que es muy pequeño si se compara con la hidrólisis por ultrasonido.
4. Determinación de azúcares reductores (DNS)
Método que se basa en la oxidación del grupo aldehído o cetona presente en carbohidratos, para el caso específico la D-xilosa, y la respectiva reducción del DNS a ácido 3-amino-5-nitrosalisílico.
Ambos hidrolizados fueron sometidos a determinación de azucares reductores utilizando el método de DNS con 5 repeticiones, obteniendo en promedio los valores que aparecen en la Tabla VII.
TABLA VII CONCENTRACIÓN DE AZÚCARES REDUCTORES EN HIDROLIZADOS.
| Muestra | Concentración de azúcares reductores (mg/mL) |
|---|---|
| Hidrolizado por ultrasonido | 1054,42 |
| Hidrolizado vía ácida | 305,67 |
El análisis de azúcares reductores muestra que la hidrólisis por ultrasonido es un método apto para obtener azúcares fermentables, en comparación con la hidrólisis ácida, en donde la concentración de azúcares se ve claramente afectada por la presencia de contaminantes, haciéndose necesarios procesos adicionales para buscar mejorar el rendimiento.
A diferentes concentraciones los azúcares reductores presentes en los hidrolizados, presentan la mayor actividad óptica en una longitud de onda de 540 nm estando acorde con los datos suministrados por la literatura.
Con el método de DNS se puede determinar la concentración de azucares reductores a partir de una curva de calibración elaborada con una solución patrón de D-xilosa.
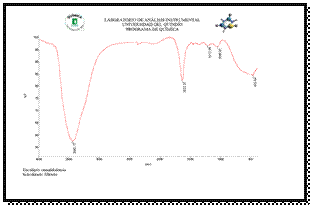
4.1 Espectro infrarrojo de los hidrolizados
Los espectros de la Fig. 4 y Fig. 5, muestran que el proceso de hidrólisis ya sea ácida o por ultrasonido, no afectan la presencia de grupos hidroxilo propio de azúcares, generando una banda ancha de absorción en los 3400 cm-1 aproximadamente. Cabe mencionar que también absorbe el enlace H-O del agua dado que es un hidrolizado, en la cual la muestra preparada para el IR, cumplió con condiciones que eliminan las interferencias por humedad.
De acuerdo con los resultados se puede observar que el ultrasonido es una técnica adecuada para hidrolizar el material lignocelulósico (Eucalipto camaldulensis), puesto que, la presencia de sólidos disueltos es mayor que en la hidrolisis ácida, que se ve afectada por procesos de purificación de subproductos propios de la reacción, que podrían inhibir el proceso metabólico de los microorganismos durante la fermentación [16].
Inicialmente la hidrólisis ácida generó mejores resultados en este parámetro, como se observa en la tabla correspondiente, pero al realizar el proceso de detoxificación y clarificación, el valor de grados Brix cae drásticamente, permitiendo determinar la influencia negativa de los procesos de purificación y clarificación en cuanto a la disponibilidad de sólidos disueltos.
La determinación de azucares reductores (DNS) para los dos tratamientos no muestra diferencias significativas, ya que en ambos casos se muestra actividad óptica a 540nm, que es indicativo de presencia de azúcares.
El espectro de infrarrojo, antes y después de la hidrólisis, no muestra diferencias significativas en cuanto a las bandas de absorción, lo que significa que ninguno de los dos tratamientos afecta la presencia de grupos hidroxilo (OH), que son propios de azúcares.
El valor de pH en la hidrólisis por ultrasonido se ajusta a los valores óptimos para que los microorganismos puedan desarrollar de la mejor manera sus procesos metabólicos a lo largo de la fermentación.
En la hidrólisis ácida se ve claramente la influencia negativa de los subproductos generados durante la reacción en términos de pH; haciendo indispensable la etapa de purificación, buscando eliminar contaminantes y con ello ajustando el pH a valores adecuados para la fermentación.
V. CONCLUSIONES
La determinación de parámetros fisicoquímicos como sólidos solubles y azúcares reductores es fundamental en la valoración del sustrato como materia prima en procesos biotecnológicos.
El ultrasonido es una técnica novedosa en este campo, que se puede utilizar como pretratamiento en la producción de xilitol a partir de material lignocelulósico.
La actividad de agua registrada por el material vegetal, muestra que es un sustrato apto para procesos químicos y biológicos, por su estabilidad microbiológica.
El porcentaje de humedad final se logra a las 24 horas a una temperatura de 40°C, permitiendo ahorrar tiempo y energía, valiosos en procesos investigativos.
La muestra de Eucalipto camaldulensis demostró ser termoestable por análisis termogravimétrico, favoreciendo su uso en la industria.
La hidrólisis por ultrasonido mostró efectividad utilizando 30 minutos, ya que, a tiempos mayores, las diferencias en cuanto a caracterización fisicoquímica no son significativas, permitiendo menos gasto energético y agilidad en los procesos.
En la búsqueda de desarrollar procesos físicos, químicos y/o biológicos amigables con el medio ambiente, el ultrasonido se convierte en una buena alternativa por la no utilización de sustancias tóxicas generadoras de contaminantes difíciles de extraer, convirtiéndose en determinantes en el éxito de la fermentación por microorganismos.