Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Ingeniería Biomédica
versão impressa ISSN 1909-9762
Rev. ing. biomed. vol.5 no.9 Medellín jan./jun. 2011
GUÍA PARA LA IMPLEMENTACIÓN DEL PROGRAMA NACIONAL DE TECNOVIGILANCIA EN EL HOSPITAL GENERAL DE MEDELLÍN
GUIDE FOR THE IMPLEMENTATION OF THE NATIONAL TECHNO-SURVEILLANCE PROGRAM AT THE MEDELLÍN GENERAL HOSPITAL
Catalina Vásquez Franco1, Mauricio Pérez Trujillo2
1 Programa de Ingeniería Biomédica. Escuela de Ingeniería de Antioquia - Universidad CES. cavafra@eia.edu.co.
2 Área de Ingeniería y Mantenimiento. Hospital General de Medellín Luz Castro de Gutiérrez.
Recibido 16 de diciembre de 2010, Aceptado 02 de Junio de 2011
RESUMEN
Este caso de estudio propone una guía al Hospital General de Medellín (HGM) para dar cumplimiento al Programa Nacional de Tecnovigilancia. Este programa fue diseñado por el Ministerio de la Protección Social, con al apoyo del Instituto Nacional de Vigilancia de Medicamentos y Alimentos (INVIMA), está reglamentado por la Resolución 4816 de 2008 y tiene un enfoque centrado principalmente en la Seguridad del Paciente. Para el desarrollo de este proyecto, se efectuaron visitas de referenciación a diferentes instituciones del sector salud de Medellín. Durante estas, se realizó una consulta guiada acerca de la tecnovigilancia en Colombia y el mundo y el marco normativo que encierra este programa en el país. A partir de esta información y del Sistema de Gestión Integral de la Calidad del HGM, se realizó un diagnóstico de la situación del Hospital frente al programa de Tecnovigilancia. Además, se diseñó un plan de mejoramiento con estrategias, acciones y herramientas que le permitieran impulsar el programa interno, direccionado al mejoramiento continuo de la calidad de sus servicios y a la seguridad de los pacientes.
PALABRAS CLAVE: Hospital General de Medellín, Institución Prestadora de Servicios de Salud, Programa Nacional de Tecnovigilancia.
ABSTRACT
This case of study offers to Medellín General Hospital (MGH) a guide to comply with the National Techno-Surveillance Program. The Ministry of Social Protection with the support of the National Drug and Food Surveillance Institute (INVIMA) designed this program. It is regulated by the 4816 Resolution of 2008 and its mainly focused on patient safety. For the development of this project, reference visits at different health institutions in the city of Medellín-Colombia were made. During these, a guided consultation was carried out to establish the current state of techno- surveillance programs and regulatory schemes in Colombia and the world. Using this information and the institutional quality management system at the MGH, the authors performed an analysis of the hospital techno- surveillance situation. Further, it was possible to design an improvement plan with strategies, actions and tools that are to be taken into account by the MGH to implement the planned institutional program and that are expected to improve their health care quality services and strengthen patient safety.
KEY WORDS: Hospital General de Medellín, Healthcare Services Institute, National Techno-Surveillance Program.
I. INTRODUCCIÓN
A medida que la humanidad ha evolucionado, han surgido tecnologías en salud cada vez mejores y novedosas. Por medio de éstas, se ha intentado mejorar la calidad de vida de las personas a través de la creación, adaptación y mejoramiento de herramientas que facilitan el diagnóstico, prevención, tratamiento o alivio de enfermedades, lesiones o deficiencias que afectan al ser humano. Día a día son mayores los avances en estas tecnologías, pero los riesgos asociados a estas siguen siendo inevitables. Por más que las condiciones de seguridad actuales sean mucho mayores que las de décadas anteriores, la utilización de toda tecnología tiene un riesgo implícito.
Según un informe de la Organización Mundial de la Salud y la Organización Panamericana de la Salud [1] todos los dispositivos médicos poseen un cierto grado de riesgo el cual podría causar problemas en circunstancias específicas. Los riesgos de salud pública derivados de la aplicación de las tecnologías en salud, han despertado el interés mundial por vigilar y controlar todos aquellos factores que impliquen una amenaza para la seguridad y bienestar de los seres humanos. Muestra de ello fue la conformación de la Alianza Mundial de la Salud en octubre de 2004 cuyo objetivo es facilitar el desarrollo de las políticas y de las prácticas de seguridad del paciente de los Estados Miembros [2].
Además, existen numerosas agencias y entidades reguladoras internacionales que vigilan y controlan las tecnologías biomédicas entre las que se encuentran los dispositivos médicos. Entre las agencias de referencia a nivel internacional se encuentran: FDA [3], ECRI [4] y GHTF [5] en EE.UU, AFSSAPS[6] en Francia, Health Canadá [7] en Canadá, ANMAT [8] en Argentina, ANVISA [9] en Brasil, entre otras.
Colombia impulsa una Política de Seguridad del Paciente liderada por el Sistema Obligatorio de Garantía de Calidad de la Atención en Salud (SOGCS) en la cual, uno de sus ocho objetivos, está centrado en prevenir la ocurrencia de situaciones que afecten la seguridad del paciente, reducir y, de ser posible, eliminar la ocurrencia de eventos adversos para contar con instituciones seguras y competitivas internacionalmente [10].
El Programa Nacional de Tecnovigilancia nació en Colombia como una estrategia de apoyo a las políticas de seguridad del paciente definidas por el Ministerio de la Protección Social, en la cual la vigilancia sanitaria de dispositivos médicos se articula con la prestación de servicios de salud. Este programa desarrolla un conjunto de actividades dirigidas a la obtención de información sobre incidentes y eventos adversos asociados a dispositivos médicos, y busca generar estrategias para reducir los riesgos y problemas de seguridad que puedan implicar daños al paciente, a los usuarios y demás personas que se relacionan directa o indirectamente con el uso de estas tecnologías biomédicas.
El Ministerio de la Protección Social con el apoyo del Instituto Nacional de Vigilancia de Medicamentos y Alimentos- INVIMA- diseñó el Programa Nacional de Tecnovigilancia, el cual se reglamenta por medio de la Resolución 4816 del 2008. A través de ésta, se definen los actores a nivel nacional, departamental y local, se establecen sus responsabilidades y se describe la gestión de reporte de eventos e incidentes adversos [11].
El Hospital General de Medellín Luz Castro de Gutiérrez (HGM), como Institución Prestadora de Servicios de Salud (IPS) e integrante del nivel local de operación del Programa de Tecnovigilancia, no está ajeno a estas normas y debe tenerlas en cuenta, no sólo por su obligatoriedad, sino como aporte a su Sistema de Gestión Integral de Calidad en el cual la seguridad del paciente juega un papel muy importante. El HGM es una entidad de tercer nivel de atención, fundada en 1942, con una categoría especial de entidad pública descentralizada de propiedad del Municipio de Medellín, con personería jurídica, patrimonio propio y autonomía administrativa [12].
El HGM tiene como misión "prestar servicios de salud hasta la alta complejidad, centrados en la seguridad del paciente, brindando afecto, confianza, satisfacción y promoviendo buenas prácticas ambientales y calidad". El mejoramiento en la calidad es un proceso continuo dentro de las actividades que se realizan a diario en el Hospital. Muestra de ello es que hoy el Hospital está posicionado en el segundo ciclo de Acreditación, con aval Internacional de ISqua, convirtiéndose en el primer Hospital público del país en ser evaluado y certificado en Acreditación en Salud por el Ministerio de la Protección Social y el Icontec. Además, ha sido reconocido como el mejor hospital público en Latinoamérica según la revista América Economía que realizó por segunda vez el estudio sobre la calidad de clínicas y hospitales en América Latina y elaboró el ranking de las 35 mejores de la región ocupando, el HGM, el puesto número 22 [13].
Para el HGM es importante trabajar la seguridad del paciente, que además de ser una fuerte tendencia mundial en salud, es una orientación filosófica de la institución que se centra en la satisfacción de los pacientes, de sus familias y de los demás usuarios. Igualmente, en la medida que todos los funcionarios y colaboradores de la institución se comprometen con la seguridad del paciente, se consigue que reconozcan al Hospital como una institución de salud segura, se logra una mayor competitividad en el medio, se cumple con la misión del Hospital, y se llega a ser referente en el sector salud y a generar confiabilidad para que la comunidad acuda al Hospital en busca de mejorar su calidad de vida [14].
Por lo anterior, se decidió adelantar el proyecto institucional "Guía para la implementación del Programa Nacional de Tecnovigilancia en el Hospital General de Medellín" con el cual se proponía brindar a la institución unas pautas a seguir para el cumplimiento de la Resolución 4816 del 2008 y contribuir en su constante búsqueda por el mejoramiento de la calidad y seguridad en la prestación de servicios de salud.
El desarrollo de este proyecto buscaba aportar principalmente un enfoque de interdisciplinariedad dentro de la institución en relación a Tecnovigilancia, direccionar procesos que se adelantaban desde diferentes áreas, como farmacia e ingeniería, para conformar un grupo de trabajo que proyectara sus actividades hacia este programa y profundizaran en aspectos por mejorar o por implementar.
Este caso de estudio, además, podría ser un punto de referencia para entidades del sector salud y la comunidad académica, en relación al enfoque y experiencia de implementación del Programa Nacional de Tecnovigilancia en una IPS.
II. MÉTODOS
Para la realización de este caso de estudio se desarrollaron tres objetivos específicos:
- Establecer que aspectos de la normatividad colombiana están relacionados con la Tecnovigilancia y cómo se les debe dar cumplimiento a esta.
- Determinar el nivel de cumplimiento del Programa Nacional de Tecnovigilancia en el HGM.
- Elaborar una guía que permita abordar y reforzar todos los aspectos del Programa Nacional de Tecnovigilancia dentro del HGM, que se adecué a sus necesidades y que le permita cumplir con las normas vigentes en Tecnovigilancia.
2.1 Tecnovigilancia en Medellín, Colombia y el mundo
2.1.1 Tecnovigilancia en el mundo
Como parte de la revisión bibliográfica de la Tecnovigilancia a nivel mundial, se consultó acerca de algunas de las agencias internacionales que ejercen acciones de inspección, vigilancia y control sobre los productos de uso en humanos entre los que se encuentran los dispositivos médicos. Estas agencias, en general, se preocupan por mejorar la calidad de vida de las personas y la seguridad de los pacientes por medio de labores de seguimiento a los productos y actividades que podrían causar algún daño al ser humano. Además, propenden por la promoción de las buenas prácticas clínicas y la comunicación constante con organizaciones y personas acerca de peligros potenciales, recomendaciones y posibles acciones de mejora ante problemas de seguridad que están relacionados con la utilización de dispositivos médicos. La Tabla 1 resume algunas de las agencias internacionales relacionadas con la Tecnovigilancia.
2.1.2 Tecnovigilancia en Colombia
Para enmarcar el contexto en el cual se desarrolla este programa a nivel nacional, se realizó una recopilación de la normatividad vigente en Colombia sobre Tecnovigilancia. En la Tabla 2 se sintetizan algunas de las leyes, decretos y resoluciones del Sistema Obligatorio de Garantía de calidad en salud que tienen alguna relación con Tecnovigilancia.
Adicionalmente, se realizó una búsqueda, asesorada por expertos en el tema, de las estrategias y/o actividades que se han realizado hasta ahora en el país para promover y fomentar el desarrollo del Programa Nacional de Tecnovigilancia. Dentro de estas estrategias se incluyeron los foros, eventos, páginas de Internet, formatos y guías que el INVIMA y demás actores del Programa Nacional de Tecnovigilancia han utilizado para promocionar este programa a nivel nacional.
La página Web del INVIMA es una fuente donde se suministra información completa y actualizada sobre el Programa Nacional de Tecnovigilancia, los conceptos generales de todo lo que se encierra dentro de la Tecnovigilancia, información sobre alertas nacionales e internacionales relacionadas con problemas de seguridad de dispositivos médicos e información proveniente de eventos de Tecnovigilancia.
De igual manera, la implementación de este programa ha permitido a instituciones de salud del país tener una base para evaluar sus procesos y tomar acciones correctivas y planes de mejoramiento enfocados a la seguridad del paciente, con base a las causas más frecuentes de generación de estos eventos e incidentes adversos asociados a dispositivos médicos [15].
Actualmente, la Secretaria Seccional de Salud y Protección Social de Antioquia (SSA), que hace parte también de los participantes del Programa Nacional de Tecnovigilancia, ha trabajado en la difusión y promoción del programa en el departamento de Antioquia por medio de charlas informativas a las diferentes instituciones de servicios de salud. La información sobre estas capacitaciones es publicada a través de la red seccional de Tecnovigilancia. Igualmente, en la página Web de la SSA se puede encontrar información sobre estos eventos.
2.1.3 Tecnovigilancia en Medellín
Se realizó referencia con algunas de las instituciones de la ciudad de Medellín que actualmente están trabajando con sus programas institucionales de Tecnovigilancia. Dentro de éstas se incluyeron tres Instituciones Prestadoras de Servicios de Salud (IPS) de alto nivel de complejidad, llamadas IPS(A), IPS(B) e IPS(C). La estrategia utilizada para esta referencia fue la realización de entrevistas dirigidas a personas de estas entidades que están involucradas directamente con los programas internos de Tecnovigilancia. Las preguntas fueron elaboradas en relación al proceso de implementación, difusión y gestión de todas las actividades del Programa Nacional de Tecnovigilancia que las IPS deben tener en cuenta de acuerdo a la Resolución 4816 del 2008. La Tabla 3 resume las principales características de los programas de Tecnovigilancia de las instituciones consideradas.
2.2 Diagnóstico de Tecnovigilancia en el HGM
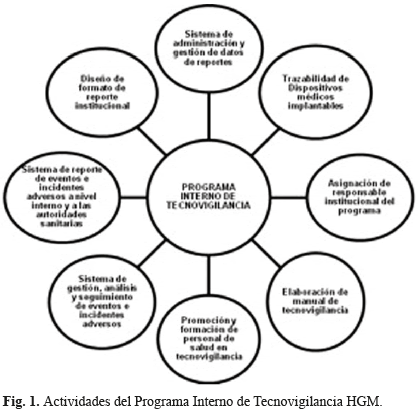
A partir del marco conceptual y normativo consultado y de las experiencias de algunos hospitales de la ciudad de Medellín, se elaboró una lista de chequeo para evaluar cuáles de las actividades del Programa Nacional de Tecnovigilancia se realizan dentro del Hospital General de Medellín y cuál es su grado de cumplimiento. Esta lista de chequeo está basada en los artículos de la Resolución 4816 que se relacionan directamente con las responsabilidades de una IPS dentro del programa. En total, se incluyeron 22 actividades en esta lista que se detalla en la Tabla 4. Estas actividades resumen lo que una IPS debe tener en cuenta para implementar un programa interno de Tecnovigilancia. Las actividades se resumen en Fig. 1.
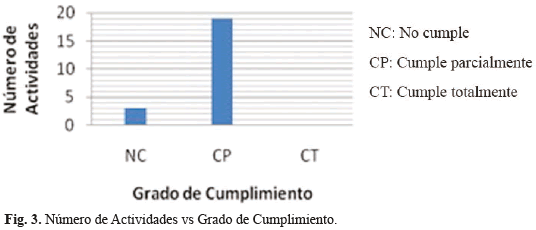
La lista de chequeo consiste en una tabla con las 22 actividades, su nivel de cumplimiento y cómo se abordan estas actividades en el HGM, según fuera el caso. El grado de cumplimiento se representó por medio de una ponderación "P" en porcentajes. Para una ponderación de 0% se consideró como "No se cumple" (NC). Una ponderación mayor al 0% se consideró como "Se cumple parcialmente" (CP). Si la actividad se calificaba al 100%, se consideraba como "Se cumple totalmente" (CT). Es de aclarar, que los resultados allí mostrados corresponden a la fecha de aplicación de esta herramienta y no es un referente de la situación actual del HGM.
2.3 Guía para la implementación: Plan de Mejoramiento
La lista de chequeo se revisó con algunos de los funcionarios del HGM que están relacionados con los procesos de Tecnovigilancia (jefe de calidad y planeación, líder de ingeniería y mantenimiento, líder de farmacia, química farmacéutica-integrante del grupo de farmacovigilancia, enfermera profesional-integrante del Comité de Seguridad del Paciente y una estudiante de ingeniería biomédica). De las actividades que resultaron pendientes por revisión o por implementación, se generaron tareas y compromisos. Las actividades que requerían de seguimiento y control se incluyeron en el plan de mejoramiento, que es una herramienta que se utiliza en el HGM, la cual contiene las acciones de mejora y los mecanismos para lograrlo. En este plan de mejoramiento se registran los siguientes conceptos:
- Oportunidad de mejora: dar cumplimiento a la Resolución 4816 del 2008 por la cual se reglamenta el Programa Nacional de Tecnovigilancia.
- Qué actividades se deben realizar para mejorar la situación: las Actividades que requieren seguimiento de acuerdo a los resultados de la lista de chequeo.
- Quién es el responsable.
- Por qué: el propósito de la actividad.
- Cuándo se va a realizar.
- Dónde se realizará la actividad.
- Cómo: estrategias o pautas para la realización de la actividad.
- Meta: puede ser de forma numérica o cualitativa.
- Indicador: forma cómo se mide el cumplimiento de la meta propuesta [16].
Este plan de mejoramiento constituye la guía de implementación del programa ya que incluye todas las actividades que el HGM debe realizar para lograr un objetivo que, en este caso, es dar cumplimiento total al Programa Nacional de Tecnovigilancia en la Institución y, además, plantea algunas estrategias o acciones que podrían contribuir al alcance de las metas planteadas. La Tabla 5 es un esquema que relaciona y sintetiza los aspectos más importantes de este plan de mejoramiento y los más pertinentes al proyecto expuesto.
III. RESULTADOS
El Hospital ya posee un sistema de reporte de eventos e incidentes adversos (casi eventos) en el cual se tiene en cuenta todos los hechos que afectan la seguridad del paciente. Dentro de su sistema de reportes se incluye los casos que involucraran la utilización de dispositivos médicos. La gestión de eventos adversos en el HGM se describe en la Fig. 2.
Adicional a este sistema de gestión de eventos y casi eventos adversos liderado por el Comité de Seguridad del Paciente del HGM, el Hospital ha implementado estrategias, acciones y herramientas para la atención segura desde la parte asistencial y administrativa, las cuales están incluidas dentro del Sistema de Gestión Integral de Calidad de la Institución.
A partir de los datos arrojados por la herramienta de diagnóstico y evaluación (lista de chequeo) de las actividades que se deben desarrollar en el HGM como actor del Programa Nacional de Tecnovigilancia y de la situación actual del Hospital frente a la seguridad del paciente y la Tecnovigilancia, se arrojan los siguientes resultados:
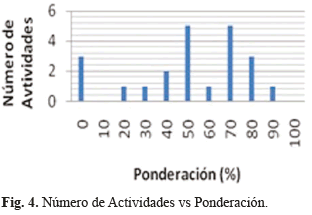
- La mayoría de las actividades establecidas como fundamentales dentro de la Resolución 4816 del 2008 para Instituciones Prestadoras de Servicios de Salud, se cumplen parcialmente en el HGM (ver Tabla 4, Fig.3 y Fig.4). El hecho de que se cumplan parcialmente no es un indicativo de que algo falta o esté mal enfocado. La primera actividad descrita en la lista de chequeo, estar atentos y vigilantes del desempeño, calidad y seguridad de los dispositivos médicos previos a su uso, por ejemplo, obtuvo una puntación de 90%, evidenciando que la vigilancia activa y la gestión de riesgos son procesos que continuamente se están mejorando y reevaluando para cumplir con estándares de calidad y seguridad cada vez más altos.
- Informar, divulgar y aplicar las prácticas adecuadas de utilización de dispositivos médicos. Al igual que ocurrió con la primera actividad, se evaluó su cumplimiento como parcial, debido a que es una actividad que se debe realizar continuamente en el HGM. A medida que nuevas tecnologías se adquieren y a medida que nuevo personal ingresa a la institución, se deben brindar capacitaciones acerca de cómo manejar los dispositivos médicos de manera óptima y segura. De igual manera se debe garantizar que exista una adecuada adherencia de la información brindada y las prácticas clínicas que involucren la utilización de dispositivos médicos con el fin de reducir la ocurrencia e incidencia de efectos indeseados.
- Desarrollar actividades de promoción y formación con los profesionales de la salud de la institución, en relación al desarrollo e implementación del Programa Nacional de Tecnovigilancia y la gestión de eventos o incidentes adversos con dispositivos médicos es la actividad número 8 de la lista de chequeo. Esta actividad es un pilar fundamental dentro del Programa Nacional de Tecnovigilancia, ya que de ésta depende que el potencial personal reportante tenga conocimiento de qué es la Tecnovigilancia, qué es reportar, cómo se debe reportar y cuál es su importancia dentro de la seguridad del paciente, de los usuarios y del entorno. También es primordial para que conozcan cómo integrar y articular los procesos y las políticas que ya se manejan dentro de la institución y la Tecnovigilancia. Como se comentó anteriormente, el HGM maneja un sistema de reporte voluntario de eventos e incidentes adversos (o casi eventos) en el que se incluyen los efectos indeseados por el uso de dispositivos médicos. Este es un indicador de que ya existe una cultura del reporte en la institución; sin embargo este debe ser un proceso continuo, debido a que la mentalidad "punitiva" sigue siendo un obstáculo a la hora de reportar y, muchas veces, el desconocimiento del programa por parte del personal de la salud evita que el sistema de reportes se aplique correctamente.
- En cuanto a la actividad número 14, la elaboración de un Manual de Tecnovigilancia, en el momento de la revisión de la lista de chequeo en la reunión, no se le asignó una calificación alta debido a que el manual debía incluir el proceso como tal de Tecnovigilancia en el HGM y cuáles serían las actividades que se realizarían para la identificación, reporte, análisis y seguimiento de los eventos e incidentes adversos por dispositivos médicos. Como en ese momento el programa institucional de Tecnovigilancia en el HGM estaba en una etapa de conformación total, se decidió que una vez aclarados los mecanismos, acciones y actividades que se incluirían dentro del programa, se elaboraría el manual y se finalizaría esta actividad.
- En total, tres actividades obtuvieron una puntuación de 0%, debido a que éstas se relacionan directamente con el reporte de eventos e incidentes adversos relacionados con el uso de dispositivos médicos al INVIMA o a las Secretarías Departamentales y Distritales de Salud. El incumplimiento de esta actividad no está directamente relacionada con la no ocurrencia de eventos e incidentes adversos a dispositivos médicos en el HGM. Se debe aclarar que la institución cuenta con un proceso de Gestión de Eventos Adversos liderado por el Comité de Seguridad del Paciente, y que, al igual que en cualquier IPS, los riesgos asociados al uso de dispositivos médicos siempre existirán. Los eventos e incidentes adversos, aunque se deben minimizar y evitar, ocurren, y en el HGM se reportan a nivel interno, pero al momento del diagnóstico, aún no se había finalizado el proceso de reporte de éstos a las autoridades sanitarias direccionadas en la Resolución 4816 del 2008, por medio de inscripción al INVIMA o a las Secretarías Departamentales y Distritales de Salud. Sin embargo, la institución sí está cumpliendo con lo normalizado por entidades gubernamentales como el Ministerio de la Protección Social, Supersalud y Dirección Seccional de Salud y Protección Social de Antioquia (DS y PSA), en acatamiento de los requerimientos del Sistema de Información para la Calidad (SIC). Quedó claro que esta es una actividad que requiere una atención especial, no sólo por el cumplimiento de la norma, sino también para contribuir en el "mejoramiento de los sistemas de información en salud en el país referentes a la vigilancia epidemiológica, para obtener información para la evaluación de los riesgos asociados con el uso de dispositivos médicos y para tomar acciones necesarias para la reducción o eliminación del riesgo de generación de eventos e incidentes adversos" [17].
IV. DISCUSIÓN
La revisión realizada acerca de las agencias internacionales brinda un espectro de lo que actualmente se adelanta a nivel mundial en pro del mejoramiento de la seguridad del paciente, y más específicamente, las labores de inspección, vigilancia y control que se llevan a cabo a las tocologías en salud. El marco normativo colombiano consultado dio una visión general de lo que a nivel nacional se legisla en relación a la Tecnovigilancia y qué papel debe jugar el HGM dentro del SOGCS como IPS. En relación a la referencia efectuada con las otras instituciones de la ciudad de Medellín, se puede extraer que cada entidad tiene una forma distinta de abarcar un programa institucional de Tecnovigilancia. La elección del responsable y la conformación del comité son, por la estructura interna de cada institución, diferentes pero tienen finalidades y roles similares dentro del programa. Igual ocurre con el sistema de gestión de eventos adversos: en procedimiento son diferentes pero tienen como objetivo final el reporte a las autoridades sanitarias y evaluación de estos a nivel organizacional. Los puntos más similares se enfocan en las herramientas usadas para el reporte interno (software) y los medios empleados para la formación del personal acerca del programa.
Todas las experiencias, al ser satisfactorias, pueden ser muy útiles para tomar ideas constructivas para otras instituciones que apenas están comenzando a implementar sus programas. El Sistema de Gestión integral de Calidad del HGM que abarca todos los procesos que se adelantan en la institución, tanto en el área administrativa como asistencial, ha sido una base fundamental en la gestión de riesgos asociados al uso de tecnologías en salud. Este sistema de calidad se ha venido fortaleciendo a medida que los estándares de habilitación y de acreditación (tanto nacionales como internacionales) van evolucionando y se van haciendo más exigentes. Todo esto se refleja en los resultados obtenidos de este análisis, que aunque muestra que hay aspectos por mejorar, en la institución se cuenta con las herramientas para lograr que las actividades a desarrollar dentro del Programa Nacional de Tecnovigilancia se cumplan, se mantengan y se mejoren.
Los resultados allí obtenidos sólo reflejan lo que era el estado actual del HGM frente al Programa Nacional de Tecnovigilancia en el momento de la revisión de la lista de chequeo y, por lo tanto, no es un diagnóstico a largo plazo. A medida que las actividades que se incluyeron en el plan de mejoramiento vayan siendo desarrolladas, se podrán ver los resultados del proceso de implementación de Tecnovigilancia en el Hospital.
El plan de mejoramiento es una herramienta guía para el cumplimiento de las actividades y las acciones de mejora que, en este caso, están enfocadas en la Tecnovigilancia dentro del HGM. Sin embargo, ésta no deja de ser una propuesta que está sujeta a modificaciones de acuerdo a las necesidades que vayan surgiendo en la institución y de las nuevas políticas que se generen a nivel nacional e institucional.
De igual manera, se debe resaltar que este plan de mejoramiento se aplica exclusivamente al HGM porque, como se mencionó anteriormente, las actividades que se incluyeron fueron determinadas en base al diagnóstico que se hizo de la situación del Hospital frente a la Tecnovigilancia empleando la lista de chequeo.
V. CONCLUSIÓN
El desarrollo de este caso de estudio permitió alcanzar los objetivos propuestos, y además, ayudó a fortalecer el trabajo interdisciplinario en el Hospital centrado en el cumplimento de un objetivo institucional, es decir, la implementación de un programa interno de Tecnovigilancia de acuerdo a lo reglamentado en la Resolución 4816 del 2008 y a los procesos y políticas que se enmarcan dentro del Sistema de Gestión Integral de Calidad de la institución. La información consultada sobre la Tecnovigilancia a nivel mundial, nacional, local e institucional, fueron el punto de partida para generar la herramienta de diagnóstico del HGM frente a la Tecnovigilancia. A partir de esto, se pudo determinar los aspectos por reforzar o implementar para cumplir con los requisitos del Programa Nacional de Tecnovigilancia.
Las herramientas utilizadas (lista de chequeo y plan de mejoramiento) son las que se emplean en las labores diarias del HGM dentro de su Sistema de Gestión Integral de Calidad, y han sido apropiadas para el diagnóstico que se requería. Fueron de gran utilidad para comenzar a impulsar la Tecnovigilancia en el Hospital liderado por un grupo de funcionarios competentes en este tema, y según lo establecido normativamente.
Es de destacar que el Sistema de Gestión Integral de Calidad del HGM y el trabajo en equipo serán grandes impulsores de la Tecnovigilancia en el Hospital así como lo han demostrado con todas sus labores. Esto ha convertido a la Institución en acreedora de grandes reconocimientos a nivel nacional e internacional por demostrar su alto grado de cumplimiento de estándares de calidad y su constante búsqueda por el mejoramiento de la atención en salud y la seguridad del paciente. Queda como meta propuesta para el HGM continuar con sus labores centradas en la seguridad del paciente y la calidad en la prestación de servicios de salud. Así mismo seguir fortaleciendo y evaluando las experiencias administrativas, organizacionales e ingenieriles en la implementación del programa de Tecnovigilancia.
REFERENCIAS
[1]. República de Colombia. Instituto Nacional de Vigilancia de Medicamentos y Alimentos (INVIMA). Guía de reporte eventos adversos a dispositivos médicos. Consultado el 2 de agosto de 2010 en: http://www.invima.gov.co/INVIMA/tecnovigilancia/docs_programanacional/guiareporte_eventosadversosdispositivos.pdf. [ Links ]
[2]. Villarreal Cantillo E. Seguridad de los pacientes, un compromiso de todos para un cuidado de calidad. Revista Salud Uninorte, 23(1): 112-119, 2007. [ Links ]
[3]. FDA (The United States Food and Drug Administration). About FDA, FDA organization. Consultado el 5 de agosto de 2010 en: http://www.fda.gov/AboutFDA/CentersOffices/default.htm. [ Links ]
[4]. ECRI (Emergency Care and Research Institute). Acerca de ECRI Institute. Consultado el 5 de agosto de 2010 en: https://www.ecri.org/ES/Pages/About.aspx. [ Links ]
[5]. GHTF (Global Harmonization Task Force). About GHTF, Overview and Mission. Consultado el 7 de agosto de 2010 en: http://www.ghtf.org/about/overview.html. [ Links ]
[6]. AFSSAPS (Agence Francaise de Securite Sanitaire des Produits de Sante). L'AFSSAPS, Qui sommesnous. Consultado el 6 de agosto de 2010 en: http://www.afssaps.fr/L-Afssaps/Qui-sommes-nous. [ Links ]
[7]. Health Canada. Home, About Health Canada. Consultado el 6 de agosto de 2010 en: http://www.hc-sc.gc.ca/ahc-asc/index-eng.php. [ Links ]
[8]. ANMAT (Administración Nacional de Medicamentos, Alimentos y Tecnología Médica). Institucional, qué es ANMAT. Consultado el 7 de agosto de 2010 en: http://www.anmat.gov.ar/webanmat/institucional/que_es_la_ANMAT.asp. [ Links ]
[9]. ANVISA (Agencia Nacional de Vigilancia Sanitaria). Institucional, Presentación. Consultado el 7 de agosto de 2010 en: http://www.anvisa.gov.br/esp/instituicion/presentacion.htm. [ Links ]
[10]. República de Colombia. Ministerio de la Protección Social. Lineamientos para la Implementación de la Política de Seguridad del Paciente. Bogotá: El Ministerio. Consultado el 13 de Septiembre de 2010 en: http://www.ocsav.info/ocs_contenidos/LINEAMIENTOSSP.pdf. [ Links ]
[11]. República de Colombia. Ministerio de la Protección Social. Decreto 4816 de 2008. Bogotá: El Ministerio. 2008. Consultado el 3 de agosto de 2010 en: http://web.invima.gov.co/portal/documents/portal/documents/root//resolucion_004816nov2008.pdf. [ Links ]
[12]. HGM (Hospital General de Medellín). El Hospital, Reseña Histórica. Consultado el 15 de Septiembre de 2010. Disponible en: http://www.hgm.gov.co/es/hospital/historia/. [ Links ]
[13]. América Economía. Ranking 2010 Hospitales y Clínicas. Consultado el 30 de septiembre de 2010 en: http://rankings.americaeconomia.com/2010/clinicas/. [ Links ]
[14]. Hospital General de Medellín. Seguridad del Paciente. Volantes del Sistema de Gestión Integral de Calidad. Medellín. 2010. [ Links ]
[15]. Alfonso L., Salazar C., Astolfo L. Incidencia de eventos adversos asociados a dispositivos médicos en una institución de salud en Colombia. Revista Ingeniería Biomédica, 4(8): 71-84, 2010. [ Links ]
[16]. Hospital General de Medellín. Formato de Plan de Mejoramiento por Procesos. Gestión Integral de Calidad, Gestión de Procesos Corporativos. Medellín. 2009. [ Links ]
[17]. República de Colombia. Instituto Nacional de Vigilancia de Medicamentos y Alimentos (INVIMA). Inspección, Vigilancia y Control, Preguntas frecuentes sobre el reporte de eventos adversos. Consultado el 13 de agosto de 2010 en: http://web.invima.gov.co/portal/faces/index.jsp?id=5081. [ Links ]
[18]. AEMPS (Agencia Española de Medicamentos y Productos Sanitarios). Misión de la AEMPS. Consultado el 6 de agosto de 2010 en: http://www.aemps.es/actividad/nosotros/mision/home.htm. [ Links ]
[19]. HMA (Heads of Medicines Agencies). HMA joint: About HMA. Consultado el 8 de agosto de 2010 en: http://www.hma.eu/267.html. [ Links ]
[20]. The Joint Commission. About the Joint Commission. Consultado el 6 de agosto de 2010 en: http://www.jointcommission.org/AboutUs/. [ Links ]
[21]. MHRA (Medicines and healthcare products regulatory agency). MHRA about us, who we are.Consultado el 5 de agosto de 2010 en: http://www.mhra.gov.uk/Aboutus/Whoweare/index.htm. [ Links ]