Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Ingeniería Biomédica
versão impressa ISSN 1909-9762
Rev. ing. biomed. vol.5 no.10 Medellín jul./dez. 2011
DETECCIÓN IN SILICO DE SEGUNDOS USOS DE MEDICAMENTOS CON POTENCIAL ACCIÓN LEISHMANICIDA
DETECTION IN SILICO OF SECOND USE DRUGS WITH POTENTIAL ANTI-LEISHMANIA ACTIVITY
Rodrigo Ochoa1,3, Andrés Flórez1, Carlos Muskus, MS1,2
1 Programa de Estudio y Control de Enfermedades Tropicales, PECET, Universidad de Antioquia, Medellín, Colombia.
2 Autor para Correspondencia: carmusk@yahoo.com.
3 Bioingeniería, Universidad de Antioquia, Medellín, Colombia.
Recibido 03 de noviembre de 2011. Aceptado 14 de diciembre de 2011
RESUMEN
Actualmente las enfermedades tropicales son objeto de importantes investigaciones en las ciencias biomédicas, debido al impacto global que causa en poblaciones vulnerables. Sin embargo son comúnmente ignoradas por la industria farmacéutica debido a su bajo potencial de rentabilidad económica. Por esta razón, la búsqueda de nuevos tratamientos terapéuticos por medios costo-efectivos es esencial para la lucha contra parásitos tropicales como Leishmania spp. En este trabajo se hizo una búsqueda y selección de medicamentos depositados en bases de datos públicas, y cuyo blanco de acción demostrado son proteínas conocidas. Con estas proteínas blanco de medicamentos, se hizo una búsqueda de ortólogos en el proteoma de Leishmania, con el fin de identificar rápidamente medicamentos que pudieran tener acción también contra este parásito, implementando herramientas in silico, basadas en la Bioinformática. También en el caso de poseer la estructura de las proteínas de interés, se realizó análisis de docking para corroborar la interacción con el medicamento. Empleando esta estrategia, se identificaron y seleccionaron 10 medicamentos que son evaluados actualmente en ensayos in vitro.
PALABRAS CLAVE: Bioinformática, Blancos moleculares, Medicamentos, Leishmaniasis, Segundos usos.
ABSTRACT
Currently, tropical diseases are a major subject of research in biomedical sciences due to its global impact on vulnerable populations. However, these diseases are normally ignored by pharmaceutical companies due to low profitability potential. For that reason, the search of new therapeutic treatments, that are cost-effective, is essential to fight against tropical parasites as Leishmania spp. In this work, a search and selection of drugs with known protein targets, which were deposited in public databases, was conducted. With these target proteins, a search for orthologs in the Leishmania proteome was carried out in order to identify drugs that could also have anti-leishmanial activity. For this purpose bioinformatics tools were implemented. In addition, in the case that Leishmania proteins have its tridimensional structure reported, docking analysis were simulated to corroborate interaction with the drug. At the end, a selection of 10 drugs was identified and is currently being evaluated in in vitro test.
KEY WORDS: Bioinformatics, Drugs, Leishmaniasis, Molecular Targets, Second use.
I. INTRODUCCIÓN
La leishmaniasis es una enfermedad parasitaria causada por diferentes especies del género Leishmania y transmitida por insectos vectores del género Lutzomyia en el Nuevo Mundo y Phlebotomus en el Viejo Mundo. La enfermedad constituye un serio problema de salud pública en 98 países alrededor del mundo y en países reconocidos como no endémicos, debido a un incremento del número de casos importados como consecuencia del turismo a países endémicos de la enfermedad [1-6]. En Latinoamérica el número anual de casos de Leishmania se ha incrementado notoriamente. Brasil y Colombia ocupan los dos primeros lugares respecto a los casos de leishmaniasis en América Latina [7].
Una de las medidas para el control de una enfermedad, en término costo-beneficio, es contar con una vacuna o desarrollarla. Sin embargo, la disponibilidad de una vacuna efectiva y segura para proteger a la población expuesta a Leishmania es incierta actualmente, a pesar de que varias iniciativas están en curso [8-12]. Por la carencia de una vacuna, el control de la enfermedad recae primariamente en la quimioterapia y en medidas encaminadas al control de los vectores. Los medicamentos usados actualmente presentan varios problemas, incluyendo fenómenos de toxicidad y efectos adversos severos, los cuales conllevan a los pacientes a suspender el tratamiento, favoreciendo la generación de resistencia. Además, el desarrollo de medicamentos de novo es un proceso costoso y laborioso que requiere un número de pruebas hasta llegar finalmente al mercado. En el proceso de descubrimiento de medicamentos, una de las primeras fases está orientada a la selección de un blanco molecular, es decir la molécula que ha de ser inhibida, en este caso en el parásito, con el objetivo de ocasionar la muerte de éste sin ocasionar daños secundarios en el huésped, o si los hay, que estos sean mínimos o leves. Diversas aproximaciones metodológicas han sido empleadas en la búsqueda de blancos moleculares en microorganismos de importancia médica. Sin embargo, algunas de ellas se han basado en premisas un tanto intuitivas que no tienen en cuenta la complejidad de los sistemas biológicos como el nivel de expresión de la molécula, su participación en un proceso metabólico esencial para el microorganismo, la localización en la célula, etc. Adicionalmente, las estrategias experimentales para evaluar esencialidad mediante deleción homóloga de genes, resultan costosos, consumen mucho tiempo y en algunos casos muy difíciles de llevar a cabo debido a limitaciones técnicas y experimentales [13]. En contraste, la disponibilidad actual de genomas secuenciados de una gran variedad de microorganismos, y los ensayos de expresión evaluando RNAm o la proteína a gran escala, constituyen una fuente importante de información que permitirá la comprensión de nuevos mecanismos moleculares, y constituye una oportunidad sin precedentes en la búsqueda de nuevos blancos terapéuticos. No obstante, la manipulación y extracción de conocimiento útil de estas grandes cantidades de datos requiere del uso de herramientas bioinformáticas y computacionales, que permitan diseñar estrategias novedosas para el desarrollo racional y más efectivo de fármacos anti-Leishmania.
La Bioinformática junto con la Biología de Sistemas son disciplinas bastante prometedoras en el proceso de descubrimiento de nuevos medicamentos o segundos usos de medicamentos actuales. Estas permiten el análisis masivo y riguroso de procesos celulares realizados por un microorganismo, generando predicciones sobre posibles eventos moleculares con un mayor grado de confiabilidad que lo proveniente por la intuición. Incluso, permiten predecir genes esenciales en todo el genoma de un organismo favoreciendo la selección de aquellas moléculas que puedan ser blanco de la acción de medicamentos [14], para posteriormente ser evaluadas experimentalmente in vitro e in vivo [15]. Estas estrategias quizás permitan mayores tasas de éxito que lo realizado en tamizajes al azar, y por ende la disminución de tiempo y costos en esta fase del proceso de descubrimiento o desarrollo de medicamentos.
En este trabajo se utilizó una estrategia computacional, la cual parte de implementar la información relacionada de aquellos medicamentos con blancos proteicos reconocidos, para luego buscar ortólogos de estas proteínas blanco de medicamentos en el proteoma de Leishmania spp. En los casos donde las proteínas blanco posean estructura tridimensional resuelta, estas serán analizadas complementariamente mediante docking molecular.
II. MATERIALES Y MÉTODOS
2.1 Obtención de las secuencias proteicas a analizar
Como modelo se implementó la información relacionada con el proteoma de los parásitos Leishmania major, Leishmania infantum y Leishmania braziliensis. Leishmania major es una especie presente exclusivamente en el Viejo Mundo, Leishmania braziliensis es exclusiva del Nuevo Mundo, mientras que Leishmania infantum está presente en ambas regiones, y es causante de leishmaniasis visceral a diferencia de las dos primeras que están más asociadas con casos cutáneos. Las secuencias proteicas de Leishmania se obtuvieron de la base de datos TriTrypDB [16], como parte del consorcio de proyectos genoma de parásitos.
2.2 Filtración de Homología con el proteoma del humano
Para la selección adecuada de posibles blancos moleculares en Leishmania, se seleccionaron proteínas que no presentaran homología con proteínas del hospedero humano, con el fin de evitar efectos secundarios del potencial medicamento. Para filtrar las proteínas presentes en el proteoma de Leishmania spp. y no en el humano se utilizó el algoritmo PSI-BLAST [17] de la versión de BLAST 2.2.23, utilizando como fuente de información el proteoma del humano presente en la base de datos UniProt [18].
2.3 Análisis de homología entre blancos proteicos moleculares reportados en la base de datos DrugBank y ChEMBL y proteínas de Leishmania
Para la implementación de técnicas comparativas y detección de ortólogos, se obtuvieron las secuencias proteicas de blancos moleculares, que a partir de información de ensayos experimentales reportados en la literatura, se comprueba que son inhibidos o seriamente afectados por medicamentos existentes, tanto comerciales como experimentales. Las proteínas a comparar se descargaron de las bases de datos de medicamentos DrugBank [19] o compuestos ChEMBL [20]. Después de tener como fuente de información la base de datos filtrada de proteínas de L. major, L. infantum y L. braziliensis, y los blancos de medicamentos reportados en Drugbank y ChEMBL, se utilizó el algoritmo PSI-BLAST entre el proteoma de cada especie de Leishmania descargados de la base de datos TriTrypDB contra las dos bases de datos de medicamentos o compuestos. En la ejecución de cada alineamiento, se controlaron parámetros de salida que filtrarán automáticamente los resultados que contuvieran un valor estadístico (E-value) menor de 10-5, para generar un umbral apropiado de selección de homólogos entre Leishmania spp. y los blancos reportados en las bases de datos de medicamentos.
2.4 Extracción de datos adicionales de las bases de datos Drugbank y ChEMBL
Para extraer información de la base de datos Drugbank, se accedió al Data Extractor, la cual es una herramienta disponible por DrugBank para realizar minería de datos. Se recuperó por cada medicamento reportado (4800 aproximadamente) datos para la clasificación, entre los que se encuentran el nombre del medicamento (químico o comercial), el valor de hidrofobicidad del compuesto (logP), experimental y predicho por medios in silico; el valor de permeabilidad Caco2, y las estructuras secundarias en formato de texto plano (SMILES). De esta información, se extrajeron solamente los compuestos que actúan sobre blancos moleculares que tuvieran homología con proteínas de Leishmania spp. por medio del resultado del algoritmo PSI-BLAST. Además, se realizó un filtro de las drogas nutracéuticas, las cuales no tienen un valor significativo de inhibición contra posibles blancos.
Respecto a la base de datos ChEMBL, se descargó la información de los compuestos reportados (680.000 compuestos aproximadamente), en formato SQL. De este se extrajeron campos determinantes para la clasificación de las drogas como los obtenidos a través de DrugBank. Adicionalmente, se realizó un nuevo filtro contra la base de datos RefSEQ, debido a la gran cantidad de medicamentos presentes en la base de datos.
2.5 Análisis cuantitativo de toxicidad
Para anotar la toxicidad de los compuestos, se utilizó el software libre ToxTree [21], que se basa en reglas estadísticas como Árboles de Decisión. Este permite, a partir de la estructura secundaria, predecir la toxicidad en 3 niveles (1,2,3), siendo el primero el de más baja toxicidad, aumentando a medida que crece el nivel. El dato cuantitativo de toxicidad fue tenido en cuenta a la hora de discriminar cuáles podrían ser los medicamentos óptimos para un posible tratamiento de la leishmaniasis.
2.6 Construcción de la red de interacción Medicamento-Blancos de Leishmania spp
A partir de los datos extraídos y tabulados de los medicamentos con sus putativos blancos en Leishmania spp., se creó una red de interacción haciendo uso del programa Cytoscape [22]. Esta estrategia permitió visualizar las interacciones existentes, y permitió realizar un ordenamiento de los compuestos por diversas características. Un ejemplo es el grado de conectividad entre el compuesto y múltiples blancos, o entre el blanco y múltiples compuestos, entre más grande sea el valor de conectividad, mejor para la respectiva selección, debido a que puede tratarse de un compuesto con potencial actividad en varios blancos al mismo tiempo, o en varias especies de Leishmania. Respecto a la toxicidad, se buscó filtrar los compuestos que arrojaran del paquete ToxTree un valor de toxicidad bajo o intermedio. Para el valor de Hidrofobicidad (logP), se tuvo en cuenta valores moderados (entre 0 y 4.0, según el formato de medida estándar), aunque para medicamentos de uso tópico, se pueden presentar valores de logP mayores a la media estándar. En el caso que existieran datos experimentales, estos serán prioritarios frente a los datos predichos computacionalmente. Todos estos parámetros son ingresados a la red como atributos de los nodos generados.
2.7 Extracción de putativos medicamentos con posible actividad en Leishmania spp
Como paso final, se seleccionó un grupo de medicamentos que presentan en sus atributos, características ideales para el tratamiento de la leishmaniasis, como baja toxicidad, capacidad de difusión por el torrente sanguíneo, número de blancos que podrían afectar en las tres especies de Leishmania, entre otras, para posteriormente poder ser evaluadas in vitro, y para validar la predicción bioinformática.
2.8 Análisis de Docking para proteínas de Leishmania spp. con estructura tridimensional resuelta
Con el fin de validar las interacciones medicamentoblanco, 2 proteínas de Leishmania homólogas a proteínas blanco de un medicamento que poseen estructura tridimensional resuelta por medios experimentales, y que están depositadas en el Protein Data Bank (PDB), se analizaron por Docking Molecular empleando el programa AutoDock Vina [23], con el fin de validar por otro método computacional, si este medicamento podría interactuar con la proteína de Leishmania predicha por homología.
III. RESULTADOS Y DISCUSIÓN
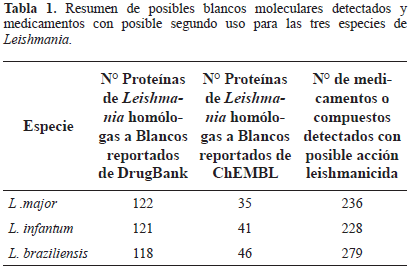
Análisis por PSI-BLAST de las proteínas blanco de acción de medicamentos depositadas en DrugBank y ChEMBL contra cada uno de los proteomas de Leishmania, permitió detectar proteínas homólogas en L. major, L. infantum y L. braziliensis, permitiendo a su vez identificar cuántos medicamentos o compuestos en total presentaban putativa acción leishmanicida contra uno o más blancos proteicos de las especies de Leishmania analizadas. Esto se realizó con el fin de construir por cada especie redes de interacción medicamento-proteína basadas en la hipótesis de que si dos proteínas son homólogas entre ellas, posiblemente un medicamento que reporte actividad inhibitoria sobre una de las proteínas, pueda tener actividad también sobre la que se detectó por homología (Tabla 1).
Además, 147 medicamentos mostraron relación con alguna proteína en las tres especies de Leishmania, y en algunos casos se reportaron como compuestos relevantes debido a su alta conectividad con múltiples blancos en el proteoma de Leishmania. Las redes fueron visualizadas con el programa Cytoscape, donde se anotó por medicamento los diferentes atributos mencionados en la metodología. Esta permitió visualizar relaciones especiales donde un blanco podría ser inhibido por varios medicamentos, o un medicamento podría tener acción sobre varios blancos al tiempo (Fig.1).
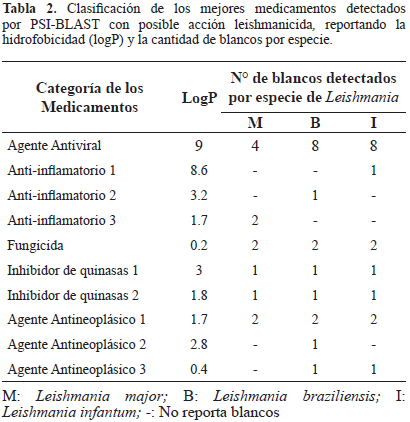
La red construida de medicamentos y putativos blancos de las especies sirvió como referente para encontrar medicamentos aprobados y/o experimentales, reportados en bases de datos oficiales que posiblemente interactúen con proteínas de novo. Esto permitió en primera instancia hacer una selección general de 10 medicamentos que por sus características como su toxicidad, hidrofobicidad y cantidad de blancos reportados, son viables para la realización de ensayos biológicos contra el parásito de Leishmania (Tabla 2). La evaluación de los resultados obtenidos empleando la base de medicamentos Drugbank, permitió la selección de un agente antiviral de uso tópico, el cual es un ácido graso saturado que se usa para el tratamiento de una virosis. Además arrojó otros valores adecuados de permeabilidad y toxicidad que lo inclinan como un posible agente en contra de la leishmaniasis cutánea. Es más, el análisis predijo acción inhibitoria en varios blancos moleculares de las tres especies estudiadas, 4 blancos en L. major, 8 en L. braziliensis y 8 en L. infantum; sin embargo dichos blancos son reportados como proteínas hipotéticas aunque conservadas en las especies de Leishmania y Trypanosoma.
En la lista de elegibles, se detectó otro agente dermatológico, el cual al ser suministrado de forma tópica en crema al 20%, actúa sobre diversas condiciones patológicas de la piel, entre ellas el acné, por lo cual puede ser importante para el tratamiento de la úlcera dejada por la forma cutánea de la enfermedad. Se predice que la bioactividad de este compuesto podría ser contra blancos presentes en las tres especies de Leishmania, específicamente sobre endonucleasas y deshidrogenasas. Se extrajeron también de la red tres agentes antineoplásicos que actúan posiblemente en Leishmania braziliensis. Su principal propiedad es la de funcionar como inhibidores de metástasis, entre ellos quinasas dependientes de ciclina, las cuales juegan un papel importante en la regulación de las fases del ciclo celular. También se seleccionó un medicamento con actividad fungicida, y que actualmente se implementa contra Trypanosoma, a través de la inhibición de la acción de la peroxidasa. Este compuesto en especial se seleccionó debido a uno de los casos exitosos de segundos usos de medicamentos contra Leishmania, como sucede con el antifúngico Anfotericina B, el cual funciona afectando la membrana del parásito, permitiendo la salida de fluidos y, por ende, desestabilizando al parásito llevándolo a su muerte [24]. Otros medicamentos interesantes, son dos inhibidores de quinasas, los cuales se consideran de gran importancia, gracias al papel que se le está asignando a las quinasas de Leishmania como un conjunto de blancos terapéuticos importantes, debido a su alta especificidad en el organismo, y además sus importantes funciones en los mecanismos de regulación génica [25]. Adicionalmente, se detectó un medicamento en fase experimental, cuya importancia radica en que podría actuar contra múltiples blancos moleculares en las tres especies de Leishmania evaluadas.
De la red generada a partir de la base de datos ChEMBL, se encontró también un buen número de medicamentos experimentales que inhiben a un grupo reducido de blancos moleculares en las tres especies de Leishmania. Se resaltan entre los posibles blancos, la Glutationil espermidina sintetasa (LmjF25.2380) y la Tripanotión sintetasa (LmjF27.1870). Ambas enzimas están involucradas en la catalización de la reacción química del glutatión, obteniendo como productos ADP y fosfatos. Estas enzimas se encuentran específicamente en especies de Trypanosoma y Leishmania, las cuales presentan alto porcentaje de conservación entre ellas. Respecto a los otros compuestos, la gran mayoría se reportaron como inhibidores potenciales de proteínas en el humano, hecho que podría generar efectos secundarios indeseados de toxicidad en el hospedero. Además, por tratarse en un buen porcentaje de drogas experimentales, es necesario determinar el índice de selectividad in vitro e in vivo de tal manera que permita identificar el potencial de toxicidad en el hospedero al momento de evaluarse como un medicamento putativo contra la leishmaniasis.
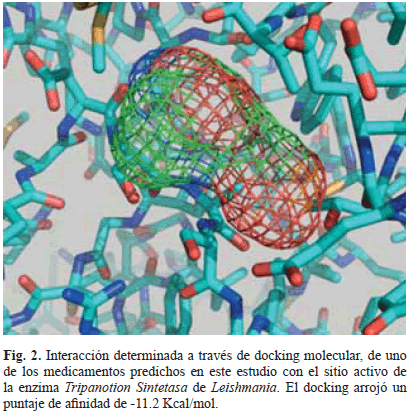
Al tener la Glutationil espermidina sintetasa y la Tripanotión sintetasa con estructura tridimensional resuelta, se procedió a realizar análisis de Docking entre los compuestos identificados y las dos proteínas de Leishmania. Se implementó el software Autodock Vina el cual es de libre distribución y es de amplio uso a nivel mundial. Al ejecutar el protocolo de acoplamiento, de un total de 5 compuestos contra las dos enzimas seleccionadas, uno de ellos arrojó un valor de energía libre considerable (-11.2 kcal/mol), que permite dar indicios de una posible acción inhibitoria del medicamento experimental contra el parásito de Leishmania spp (Fig. 2).
Este tipo de estrategias se han aplicado en otras enfermedades como la malaria a través de análisis estructural de sus proteínas y putativos ligandos por medio de docking, y a través de técnicas que permiten evaluar globalmente homología entre proteínas del parásito y blancos reportados de medicamentos existentes [26-27]. Estas estrategias se han implementado también con algunos tripanosomátidos como Trypanosoma cruzi [28], permitiendo restringir notablemente el espacio de búsqueda de medicamentos a la hora de ser evaluados experimentalmente. En Leishmania se han utilizado metodologías de búsqueda de blancos a través de homología, pero solo en proteínas específicas y no de manera global como se plantea en este proyecto [29-30].
3.1 Limitaciones
Un primer aspecto a tener en cuenta, es que el proyecto inicialmente está planteado in silico, por lo cual es importante validar posteriormente las predicciones a través de experimentos in vitro e in vivo, como se está haciendo con el primer grupo de medicamentos elegido. Otra limitación es que este tipo de protocolos es dependiente de información publicada. Analizando la información arrojada por las bases de datos, la mayoría de medicamentos seleccionados fueron de la base de datos DrugBank, la cual a pesar de tener menos compuestos reportados, contiene información de medicamentos que en su mayoría son aceptados y de uso comercial, poseen información amplia sobre sus atributos, incluyendo información respecto a efectos adversos que causan en el hospedero, en este caso el humano. La base de datos ChEMBL, permitió referenciar principalmente medicamentos en fase aún de experimentación, pero que por su condición, podrían en un futuro emplearse para el tratamiento efectivo de la leishmaniasis.
IV. CONCLUSIÓN
Empleando protocolos exclusivamente bioinformáticos es posible identificar segundos usos de medicamentos existentes contra proteínas de Leishmania spp. y que anteriormente quizás no se vislumbraban como blancos terapéuticos promisorios. Esta estrategia global de identificación de segundos usos de medicamentos en las tres especies de Leishmania evaluadas es novedosa, y permitió obtener una lista preliminar de medicamentos de uso comercial que puedan ser evaluados experimentalmente, con altas expectativas de arrojar resultados positivos en su potencial actividad contra el parásito.
Inicialmente se eligió un primer conjunto de 10 medicamentos; sin embargo está pendiente seguir evaluando más medicamentos que también puedan ser detectados por otros protocolos computacionales enfocados en la detección de nuevos blancos moleculares y segundos usos de medicamentos existentes. De los medicamentos elegidos, algunos de ellos están siendo evaluados en modelos in vitro y quizás algunos se conviertan en promisorios candidatos a ser evaluados en fases clínicas en el humano, con el fin de encontrar nuevas alternativas terapéuticas que permitan combatir una enfermedad de alto impacto en la salud pública. Finalmente, esta estrategia puede ser fácilmente aplicada a cualquier microorganismo que tenga su genoma secuenciado y sus proteínas anotadas.
AGRADECIMIENTO
Este trabajo fue financiado por Colciencias, código 111549326124 y con contrato No 538.
REFERENCIAS
[1]. Herwaldt, B. Leishmaniasis. Lancet Infectious Diseases, 354, 1191-1199, 1999. [ Links ]
[2]. Murray H. Treatment of visceral leishmaniasis (kala-azar): a decade of progress and future approaches. International Journal of Infectious Diseases, 4(3), 158-177, 2000. [ Links ]
[3]. Guerin P., Olliaro P., Sundar S., Boelaert M., Croft S., Desjeux P., Wasunna M., Bryceson A. Visceral leishmaniasis: current status of control, diagnosis, and treatment, and a proposed research and development agenda. Lancet Infectious Diseases, 2(8), 494-501, 2002. [ Links ]
[4]. Lawn S., Whetham J, Chiodini P., Kanagalingam J., Watson J., Behrens R., Lockwood D. New world mucosal and cutaneous leishmaniasis: an emerging health problem among British travellers. QJM, 97(12), 781-788, 2004. [ Links ]
[5]. Lawn S., Armstrong M., Chilton D., Whitty C. Electrocardiographic and biochemical adverse effects of sodium stibogluconate during treatment of cutaneous and mucosal leishmaniasis among returned travellers. Royal Society of Tropical Medicine and Hygiene, 100(3), 264-269, 2006. [ Links ]
[6]. Antinori S., Gianelli E., Calattini S., Longhi E., Gramiccia M., Corbellino M. Cutaneous leishmaniasis: an increasing threat for travellers. Clinical Microbiology and Infectious, 11(5), 343-346, 2005. [ Links ]
[7]. Kedzierski L., Zhu Y., Handman E. Leishmania vaccines: progress and problems. Parasitology, 133(Suppl.), 87-112, 2006. [ Links ]
[8]. Davies C., Kaye P., Croft S., Sundar S. Leishmaniasis: new approaches to disease control. BMJ, 326, 377-382, 2003. [ Links ]
[9]. Launois P., Tacchini-Cottier F., Kieny M. Cutaneous leishmaniasis: progress towards a vaccine. Expert Review of Vaccines, 8, 1277-1287, 2008. [ Links ]
[10]. Noazin S., Modabber F., Khamesipour A., Smith P., Moulton L., Nasseri K., Sharifi I., Khalil E., Bernal I., Antunes C., Kieny M., Tanner M. First generation leishmaniasis vaccines: a review of field efficacy trials. Vaccine, 26(52), 6759-6767, 2008. [ Links ]
[11]. Bhowmick S., Ali N. Identification of novel Leishmania donovani antigens that help define correlates of vaccine-mediated protection in visceral leishmaniasis. PLoS One, 4(6), 5820-5828, 2009. [ Links ]
[12]. Palatnik-de-Sousa CB. Vaccines for leishmaniasis in the fore coming 25 years. Vaccine, 26 1709-1724, 2008. [ Links ]
[13]. Chen Y., Xu D. Computational analyses of high-throughput protein-protein interaction data. Current Protein and Peptide Science, 4(3), 159-181, 2003. [ Links ]
[14]. Roberts S., Mazurie A., Buck G. Integrating genome-scale data for gene essentiality prediction. Chemistry and Biodiversity, 4(11), 2618-2630, 2007. [ Links ]
[15]. Fatumo S., Plaimas K., Mallm J., Schramm G., Adebiyi E., Oswald M., Eils R., König R. Estimating novel potential drug targets of Plasmodium falciparum by analysing the metabolic network of knock-out strains in silico. Infection, Genetics and Evolution, 9(3), 351-358, 2009. [ Links ]
[16]. Aslett M., Aurrecoechea C., Berriman M., Brestelli J., Brunk B., Carrington M. TriTrypDB: a functional genomic resource for the Trypanosomatidae. Nucleic Acids Research, 38(Suppl 1), 2010. [ Links ]
[17]. Stephen A., Thomas M., Alejandro S., Jinghui Z., Zheng Z., Webb M., David L. Gapped BLAST and PSI-BLAST: a new generation of protein database search programs. Nucleic Acids Research, 25(17), 3389-3402, 1997. [ Links ]
[18]. Bairoch A., Apweiler R., Wu C., Barker W., Boeckmann B., Ferro S., Gasteiger E., Huang H., López R., Magrane M., Martin M., Natale D., O'Donovan C., Redaschi N., Yeh L. The Universal Protein Resource (UniProt). Nucleic Acids Research, 33(suppl 1), D154-D159, 2005. [ Links ]
[19]. David W., Craig K., An C., Savita S., Murtaza H., Paul S., Zhan C., Jennifer W. DrugBank: a comprehensive resource for in silico drug discovery and exploration. Nucleic Acids Research, 34(suppl 1), D668-D672, 2006. [ Links ]
[20]. Paula M., Rafael A., Adriano D., Marcus E., Janna H., Kenneth H., Inmaculada S., Steve T., Christoph S. Chemical Entities of Biological Interest: an update. Nucleic Acids Research, 38(suppl 1), D249-D254, 2010. [ Links ]
[21]. Patlewicz G. An evaluation of the implementation of the Cramer classification scheme in the Toxtree software. SAR and QSAR in Environmental Research, 19, 495-524, 2008. [ Links ]
[22]. Shannon, P., Markiel A., Ozier O., Baliga N., Wang J., Ramage D., Amin N. Cytoscape: a software environment for integrated models of biomolecular interaction networks. Genome Research, 13(11), 2498-2504, 2003. [ Links ]
[23]. Trott O., Olson A. AutoDock Vina: Improving the speed and accuracy of docking with a new scoring function, efficient optimization, and multithreading. Journal of Computational Chemistry, 31(2), 455-461, 2010. [ Links ]
[24]. Davidson R. Short-Course Treatment of Visceral Leishmaniasis with Liposomal Amphotericin B (AmBisome). Clinical Infectious Diseases, 22(6), 938-943, 1996. [ Links ]
[25]. Neil P. Overriding Imatinib Resistance with a Novel ABL Kinase Inhibitor. Science, 305(5682), 399-401, 2004. [ Links ]
[26]. Joubert F., Harrison C., Koegelenberg R., Odendaal C., de Beer T. Discovery: an interactive resource for the rational selection and comparison of putative drug target proteins in malaria. Malaria Journal, 8, 178-186, 2009. [ Links ]
[27]. de Beer T., Wells G., Burger P., Joubert F., Marechal E., Birkholtz L., Louw A. Antimalarial Drug Discovery: In Silico Structural Biology and Rational Drug Design. Infectious Disorders - Drug Targets, 9(3) 304-318, 2009. [ Links ]
[28]. Bhatia V., Sinha M., Luxon B., Garg N. Utility of the Trypanosoma cruzi Sequence Database for Identification of Potential Vaccine Candidates by In Silico and In Vitro Screening. Infect. Immun, 72(11), 6245-6254, 2004. [ Links ]
[29]. Ben Khalaf N., De Muylder G., Louzir H., McKerrow J., Chenik M. Leishmania major protein disulfide isomerase as a drug target. Parasitology Research, 1-7, 2011. [ Links ]
[30]. Kaur J., Tiwari R., Kumar A., Singh N. Bioinformatic Analysis of Leishmania donovani Long-Chain Fatty Acid-CoA Ligase as a Novel Drug Target. Molecular Biology International, 1-14, 2011. [ Links ]