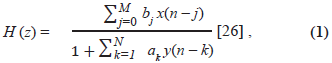Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Ingeniería Biomédica
versión impresa ISSN 1909-9762
Rev. ing. biomed. vol.9 no.17 Medellín ene./jun. 2015
MÉTODO ALTERNATIVO DE CONTROL DE INTENSIDAD LUMÍNICA PARA PULSIOXIMETRÍA EN TIEMPO REAL
AN ALTERNATIVE METHOD FOR POWER CONTROL OF LUMINICINTENSITY IN PULSEOXIMETRY ON REAL TIME
MÉTODO ALTERNATIVO DE CONTROLE DE INTENSIDADE DALUZ PARÁGRAFO OXIMETRIATEMPO REAL
R. P. Pérez1, Jairo. J. Pérez1, M. J. Betancur2, J. Bustamante1
1 Grupo de Dinámica Cardiovascular, Centro de Bioingeniería. Dirección para correspondencia (Perez R. P.): roxana.perez@alfa.upb.edu.co.
2 Grupo de Automática y Diseño; Universidad Pontificia Bolivariana, Medellín, Colombia.
RESUMEN
El pulsioxímetro es una herramienta no invasiva esencial para el monitoreo de la saturación arterial de oxígeno. Utiliza la espectrofotometría para detectar sobre la piel dos intensidades de luz (600 y 900 nm) que proporcionan información de la perfusión tisular y cantidad de oxígeno transportada. Depende de un circuito de manipulación de corriente, dos diferentes fuentes emisoras de luz, un foto-detector y una unidad de procesamiento que permiten ajustar las intensidades de luz ante tejidos de diferentes características. En el presente trabajo, se propone un método de modulación por ancho de pulso alternativo para el control de la intensidad lumínica media, cuyo principio es la conmutación on/off de la corriente aplicada a los LEDs en la etapa de emisión. Este sistema permite modificar tanto el nivel de CD como la amplitud de la señal de CA de la onda fotopletismográfica e implica la reducción del número de componentes analógicos y consumo de energía. La metodología presentada permite regular la resolución de la señal muestreada y ofrece disminuciones del 21 % y 40 % en potencia comparado con los esquemáticos propuestos por Freescale Semiconductor, Inc. y Texas Instruments Incorporated respectivamente. El uso de señales sincronizadas moduladas en ancho de pulso con frecuencias por encima de 333 kHz y pasos de 50 ns para emitir luz, permitió una reducción 41% de potencia, respecto al sistema con modulación analógica del módulo MDK pulse oximeter.
PALABRAS CLAVE: Control de LED; procesamiento de señales; señal fotopletismográfica; pulsioxímetro.
ABSTRACT
Pulse oximetry is an essential optical based non-invasive tool for monitoring blood oxygen saturation. It uses spectrophotometry to detect two light intensities (600 and 900 nm) through the skin; it provides information on tissue perfusion and quantity of transported oxygen. The process relies on a current control circuit, two light emitting sources, a photodetector, and a digital signal processor that adjusts the light intensities for different tissue characteristics. This paper proposes an alternative method of pulse width modulation for controlling the mean light intensity level, whose principle is a pulse width nodulation of the current applied to the LEDs in the emitting stage. This system allows modifying the DC level and the amplitude of the AC signal of the photopletismographic wave. The results is the reduction of the number of analog components and power consumption. The methodology presented, it allows adjusting the definition of the sample signal and offers power reductions of 21% and 40% compared to schematics given by Freescale Semiconductor, Inc. and Texas Instruments Incorporated, respectively. Thus, by using synchronized signal pulse width modulation to emit light, with frequencies above 333 kHz and steps of 50 ns, it will allow power reductions of 41%, compared to the conventional analog modulation module MDK pulse oximeter.
KEYWORDS: LED Drive; Signal Processing; Photoplethysmography Signal; Pulse Oximeter.
RESUMO
O oxímetro de pulso é uma ferramenta não invasiva essencial para o monitoramento da saturação de oxigênio no sangue. Usa espectrofotometria para detectar a pele duas intensidades de luz (600 nm e 900) para fornecer informações de perfusão tecidual ea quantidade de oxigênio transportado. Depende de manuseamento corrente do circuito, duas fontes diferentes emissores de luz, um fotodetector e uma unidade de processamento para ajustar a intensidade da luz nos tecidos com características diferentes. Neste trabalho, um método de modulação de largura de pulso alternativa para controlar a intensidade de luz média, o princípio é o de ligar/desligar da corrente aplicada aos LEDs no palco questão é proposto. Este sistema permite modificar tanto o nível DC e a amplitude do sinal AC da forma de onda fotoplestimográfico e envolve a redução do número de componentes analógicos e consumo de energia. A metodologia apresentada permite ajustar a resolução do sinal de amostragem e oferece reduções de 21% e 40% da potência em comparação com o esquema proposto pela Freescale Semicondutor, Inc. e Texas Instruments Incorporated, respectivamente. Sinais sincronizados usando freqüências moduladas por largura de pulso acima de 333 kHz e 50 ns passos para emitir luz, permitiu uma redução de 41% de energia em comparação com módulo de oxímetro de pulso MDK sistema de modulação analógica.
PALAVRAS-CHAVE: Controle LED; processamento de sinais; sinal fotoplestimográfico; oxímetro.
I. INTRODUCCIÓN
En Colombia, durante el año 2010, el Sistema de Vigilancia de Salud Pública (Silvigila) reportó 5 150 671 casos de infección respiratoria aguda, de los cuales 878 768 casos fueron en Antioquia [1]. Según el Departamento Administrativo Nacional de Estadísticas (DANE), la tasa de mortalidad por enfermedades respiratorias agudas fue 23,47 % en 2011 [2], mientras que en el mundo fue de 17,3 %, siendo este uno de los agentes con mayor impacto sobre los índices de morbimortalidad cada año [3]. Un adecuado tratamiento de esta condición, requiere de información clínica que facilite la interpretación de las señales fisiológicas y la selección acertada de los procedimientos terapéuticos.
El monitoreo de pacientes con enfermedades respiratorias está ligado al uso de pulsioxímetros. Estos sistemas ofrecen información sobre la frecuencia de pulsación y la saturación de oxígeno en sangre periférica (SpO2) [4-6]. Los dispositivos comerciales utilizan un método óptico de emisión de dos haces de luz, uno entre 630-660 nm y otro entre 820-940 nm, que inciden a través de la piel en los vasos subdérmicos, proporcionando los datos suficientes para estimar la cantidad de oxígeno transportado a partir los cambios de la absorción de luz de la oxihemoglobina y la desoxihemoglobina [4-7].
En la detección de señales, un fotodiodo adquiere las intensidades lumínicas reflejadas o transmitidas y la traza registrada es la señal fotopletismográfica (PPG, del inglés PhotoPlethysmoGraphy) [8-11]. De este modo, el funcionamiento de las etapas electrónicas depende de la sincronización de la emisión con la detección, y los mecanismos de adquisición para obtener información coherente.
La pulsioximetría se ha introducido en la práctica médica como un método no invasivo útil, fiable y sencillo que obtiene la estimación de la saturación de oxígeno en la sangre arterial. Es frecuente su utilización en la evaluación de estados respiratorios, esto incluye valoración de la efectividad de medicamentos, y el seguimiento de pacientes bajo ventilación asistida, cuidados intensivos, procedimientos clínicos, la unidad de neonatos, monitoreo de problemas cardíacos, estudios de sueño, durante anestesia y post-anestesia, sedación, cirugía, cuidados en casa o rehabilitación, entre otras [12-15].
Durante los últimos años la pulsioximetría convencional ha mostrado avances importantes en la extracción de artefactos, falsas alarmas por baja perfusión (baja amplitud de la señal), interferencias de luz y consumo energético. Más de 100 estudios clínicos independientes han demostrado numerosas ventajas de sistemas como Masimo, GE y Nellcor, que utilizan procesamiento en paralelo y filtrados especiales para proporcionar la fidelidad, especificidad y sensibilidad bajo diferentes condiciones de monitorización requeridas por el personal asistencial [16].
Numerosos sistemas se han propuesto para monitorizar los cambios en la SpO2, algunos basados en flip-flops, amplificadores operacionales, arreglos de transistores, conmutadores controlados, y compuertas lógicas, entre otras [17]. Varios sistemas comerciales han adoptado el uso de modulación analógica por amplitud con conversores digitales análogos (DAC, por sus siglas en inglés), modulación por frecuencia con convertidores de frecuencia a voltaje y trenes de pulso constantes en el tiempo para el control de la intensidad lumínica; no obstante, estos métodos requieren de consumo de potencia permanente, lo que implica un alto gasto energético [18-21].
En el presente trabajo se propone un mecanismo alternativo de regulación de potencia basado en modulación por el ancho de pulso, que emplea menor número de elementos considerando que otros utilizan amplificadores operacionales o DACs para regular la corriente de los LEDs. Las comparaciones de consumo base fueron realizadas con el módulo MED-SPO2 de Freescale Semiconductor® (FS), Inc. y MDK Pulse Oximeter de Texas Instruments Incorporated® (TI). El sistema de adquisición desarrollado permite obtener las características de onda necesarias para el cálculo del pulso arterial y la SpO2 en el paciente. Además, se consideran los elementos electrónicos, las estrategias de acondicionamiento, procesamiento y métodos computacionales utilizadas para obtener información confiable.
II. MATERIALES Y MÉTODOS
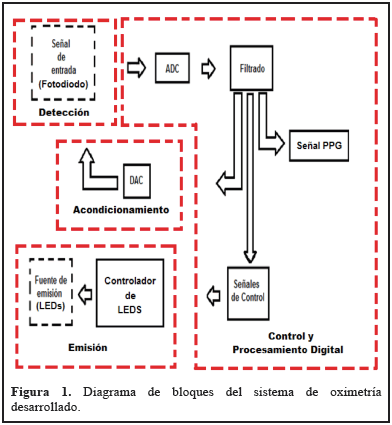
El núcleo principal de la técnica desarrollada es el subsistema de emisión de luz. Se acompaña de otros subsistemas como: detección, acondicionamiento, control y procesamiento digital, como se muestra en la Figura 1.
Los componentes utilizados fueron seleccionados para conmutar a frecuencias de hasta 500 MHz, operar con densidad de ruido de voltaje menor a 5 nV/ 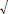 Hz, ancho de banda mayor a 1 MHz y limitar a 1 mV las pérdidas de voltaje debido a conexiones.
Hz, ancho de banda mayor a 1 MHz y limitar a 1 mV las pérdidas de voltaje debido a conexiones.
2.1. Emisión
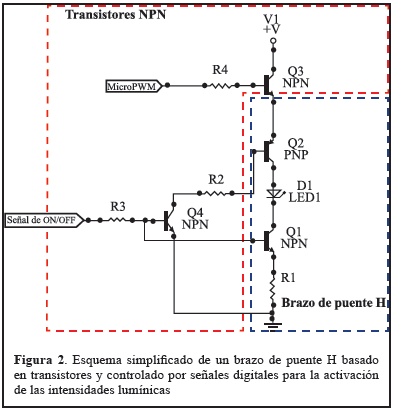
Se utilizó una sonda Durasensor DS-100A para adultos [22]. La potencia para activar los LEDs en la sonda es suministrada a través de una red de transistores en configuración de puente H (Controlador de LEDs), como se muestra en la Figura 2.
Los transistores del arreglo funcionan como interruptores que permiten la circulación de la corriente en sentidos opuestos. Se seleccionó un integrado 340S14_U dado que contiene cuatro transistores: 2 NPN y 2 PNP; todos ellos excitables a frecuencias de conmutación máxima de 350 MHz, pérdidas de conmutación de 0,5 mV y densidad de ruido de voltaje de 0,75 nV/ 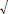 Hz [23].
Hz [23].
Adicionalmente, se utilizaron tres transistores 2N3904 (NPN) que proporcionan estabilidad al circuito y mantienen el voltaje asignado en la fuente y la base de cada brazo del puente H a frecuencias de conmutación de hasta 350 MHz.
El microcontrolador se seleccionó teniendo en cuenta su capacidad para proporcionar señales digitales de alta frecuencia (> 100 MHz), controlar y caracterizar las variables intermedias del sistema, consumo de corriente (< 1 uV) y alto rendimiento para el procesamiento de señales. Así, se utilizó un microcontrolador K53DN512ZCEQ10 de la familia Kinetis de FS, fabricado para aplicaciones médicas, que cuenta con alto desempeño computacional y bajo consumo de energía [24]. Este dispositivo cumple funciones como: digitalización de la señal PPG, procesamiento digital y control de comunicaciones.
2.2. Detección
Un fotodiodo de silicona ubicado en la sonda convierte la señal óptica que atraviesa la piel en valores proporcionales de corriente del orden de los nA.
Se seleccionó un amplificador de transimpedancia OPA380 de alta velocidad (ancho de banda de 90 MHz) y precisión (offset de voltaje de 25 µV, offset drift de 0,1 µV/°C, y corriente de bias de 50 pA), que atenúa el efecto de capacitancias parásitas, amplifica la señal, detecta cambios de corriente en el orden de 1 nA, presenta 80 V/µs de velocidad de respuesta y minimiza el ruido del fotodetector [25].
El principio de operación del sistema de detección depende de la constante de tiempo RC. Que responde a la ecuación τ = RC. El tiempo de estabilización o tiempo de carga se considera debe ser como mínimo 5 veces la constante de tiempo, es decir TC = 5τ. Para obtener el valor del condensador, el tiempo de carga fue 130 µs. De este modo la constante de tiempo es 26 µs. Se supuso una resistencia de retroalimentación de 2,7 MΩ, el valor del condensador sería entonces C = 9,62 pF ≈ 10 pF. Donde la ganancia del sistema es igual a la resistencia R, y la minimización de picos de voltaje y disminución del rizado de alta frecuencia son limitados por el condensador C. Así, el sistema de realimentación es capaz de entregar la proporción de la conversión adecuada y distinguir los cambios de absorción de luz de los tejidos.
La corriente del fotodetector se considera no debe exceder 1,04 µA puesto que satura al amplificador debido a la ganancia configurada. Es necesario bloquear factores externos perturbadores como luces de xenón, luces quirúrgicas o luz brillante del sol puesto que inciden directamente sobre la sonda causando distorsión en la medida.
2.3. Acondicionamiento de señal
Una señal PPG, por cada intensidad lumínica, contiene una componente de corriente alterna (CA) que corresponde al 2 % en amplitud, y una componente de corriente directa (CD) restante. Las diferentes características de la piel no permiten que todos los pacientes absorban la misma la cantidad de luz. Para no saturar al detector, se implementó un algoritmo de control cuyo propósito es mantener el nivel de CD a un valor programado y aproximar la amplitud CA a un valor constante para mantener la señal resultante en el área de muestra deseada.
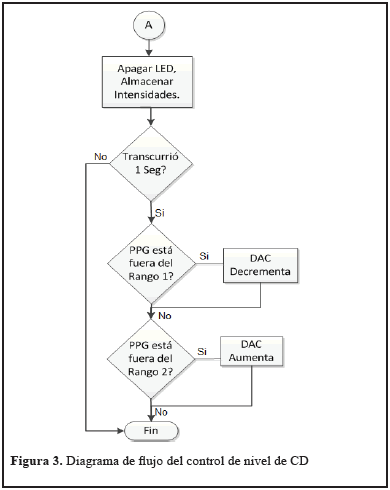
En la Figura 3 se visualiza el diagrama de flujo del control implementado para regular el nivel de CD. Tras capturar los valores de la intensidad lumínica por el microcontrolador se almacenan los datos, se filtran y se evalúa el tiempo transcurrido para analizar el nivel de CD de una sección de la señal PPG. Si la señal PPG capturada no está dentro de los rangos acordados, el microcontrolador disminuye o aumenta el valor del nivel de CD que se realiza a través de la variación de los rangos de salida del DAC.
La salida del algoritmo de control de CD es reproducida en un DAC de 12 bits embebido en el microcontrolador conectado a un amplificador de instrumentación INA326 que se encarga de eliminar el nivel de DC de la señal roja y la infrarroja. Dicho amplificador cuenta con una resistencia de 1010 Ω y capacitancia 2 pF a la entrada, pérdidas inferiores a 20 uV, rechazo de modo común 114 dB y precisión Rail to Rail de entrada y salida.
A través del INA326, se aplica una ganancia de valor 2 (dos) a la señal que posteriormente ingresa a un amplificador operacional interno del microcontrolador, para controlar la ganancia total en caso de ser requerido. El resultado obtenido es enviado a través de conexión interna a un canal del Conversor Analógico Digital (ADC, por sus siglas en inglés) configurado en el microcontrolador. Este es programado con una resolución de 16 bits y adquiere muestras consecutivas de la señal análoga a una frecuencia de muestreo de 2 kHz.
2.4. Procesamiento digital
Se compone de tareas como la conversión analógica-digital, filtrado, control de intensidad de los LED y nivel de CD.
La activación de los LEDs, dispuestos en contra paralelo de la sonda, es comandada por señales digitales sincronizadas para encender y apagar en los tiempos programados.
El microcontrolador, programado con un algoritmo de control habilita el paso de corriente que circula a través de los LEDs al variar el ciclo útil de la fuente a diferencia de los sistemas tradicionales que hacen uso de señales ON/OFF y modulaciones por amplitud de pulso para el control de intensidad lumínica.
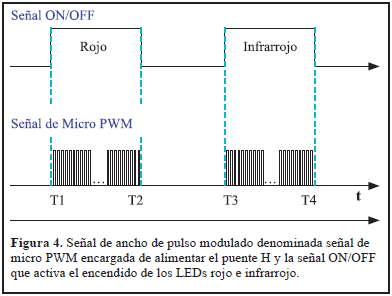
En la Figura 4 se ilustran las señales de control entregadas por el microcontrolador, las cuales corresponden a una señal de modulación de ancho de pulso (PWM, por sus siglas en inglés) como alimentación, denominada señal de micro PWM, y una señal ON/OFF. Estas son utilizadas como entradas para activar los LEDs, donde T3 - T1 = 0,50 ms y T2 - T1 = 0,22 ms.
Ambas señales son habilitadas simultáneamente cuando el temporizador cumple con el tiempo de espera definido para activar cada LED, de este modo solo se permite alimentar de energía al puente H en el momento indicado (T2 - T1 y T4 - T3). La señal ON/OFF conmuta a los transistores para cada LED, mientras que el ciclo útil de la señal de micro PWM varía la energía de la fuente y permite el ahorro de energía. Estas señales son generadas al implementar interrupciones anidadas, las cuales relacionan un número menor de instrucciones, reducen el costo computacional, activan el procesamiento de los datos y ejecutan procesos simultáneos cuando sea necesario para priorizar a las actividades críticas del sistema, lo que implica un incremento en el desempeño en tiempo real. La misma señal ON/OFF generada tiene periodo de 1 ms por canal y un ciclo útil constante del 22 %, mientras que la señal de micro PWM tiene una base de tiempo de 3 µs, seleccionada de alta frecuencia para que el detector no perciba los cambios de la conmutación de los LEDs. Su ciclo útil es modificado de acuerdo a la amplitud de la señal de CA a través de un algoritmo de control auxiliar que aumenta o disminuye el promedio de la señal total.
Los datos entregados por el detector están contaminados por diferentes tipos de ruido (artefactos, interferencia de luz, ondas electromagnéticas, etc.), por lo que se aplican filtros digitales lineales tipo Chebyshev 2 para limitar la señal PPG en frecuencia y atenuar características no deseadas. Se realizaron diferentes diseños de filtros IIR y FIR evaluando los cambios de ganancia en la banda de transición, el rizado en la banda de stop, número de coeficientes, tiempo de estabilización retardo de grupo, retardo temporal y tiempo de procesamiento.
Se seleccionaron filtros IIR, ya que un número menor de coeficientes proporcionan un menor tiempo de cálculo y una banda de transición con mayor inclinación en comparación con un filtro convencional FIR.
La ecuación general de la función de transferencia de los filtros IIR que se implementó para su ejecución en el microcontrolador es
donde ak y bj son los coeficientes de los filtros diseñados.
Las frecuencias fundamentales de la señal de PPG se encuentran en el espectro entre 0,5 Hz y 3 Hz, pero por su segundo y tercer armónico, el ancho de banda del filtro aplicado está limitado entre 0,5 Hz y 9 Hz; de esta forma es importante valorar qué tipo de morfología de la señal puede verse afectada por la variación de la potencia de los armónicos. De igual manera, se implementó un filtro pasa bajos Butterworth con frecuencia de corte en 0,3 Hz, encargado de extraer el nivel de CD característico de cada paciente que es utilizado en el algoritmo de control.
Los datos fueron graficados en Matlab®, mientras que el consumo estático de los sistemas fue calculado determinando el consumo individual de cada componente sin encender el sistema de emisión. Se emplearon los sistemas de entrenamiento MED-SPO2 fabricado por FS y MDK Pulse Oximeter de la compañía TI dado que disponen también de una sonda DS-100A para obtener la señal PPG.
La comparación entre el sistema de emisión propuesto y el de TI se realizó calculando el promedio y la desviación estándar. Se diseñó una prueba de 6 niveles modificando el ciclo útil del circuito propuesto y la amplitud de voltaje en el circuito de TI. Se repitió la prueba 20 veces utilizando personas adultas sanas voluntarias con un peso promedio de 63,6 kg y edad promedio de 33 años. Las señales fueron adquiridas en ambientes interiores con iluminación de lámparas de neón y tomadas en el dedo índice.
III. RESULTADOS Y DISCUSIÓN
Se fabricó una tarjeta electrónica para el procesamiento de señales PPG con dimensiones de 69 mm (L) por 50 mm (A), como se muestra en la Figura 5. Los componentes ensamblados presentaron un consumo energético base de 268 mW, lo que representa una disminución del 21 % y 40 % comparado con los esquemáticos de los circuitos propuestos por FS y TI.
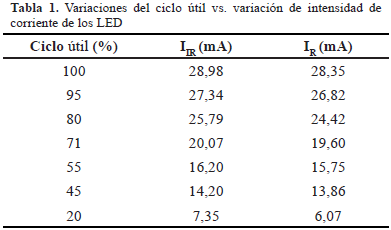
En la Tabla 1 se presenta la equivalencia entre las variaciones del micro PWM y la corriente que circula a través de los LEDs, lo cual se reproduce en variaciones de intensidad lumínica. Donde IR e IIR son la corriente del LED rojo y la corriente del LED infrarrojo respectivamente.
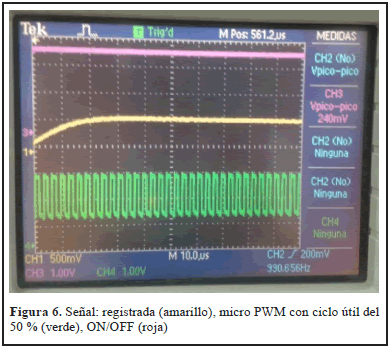
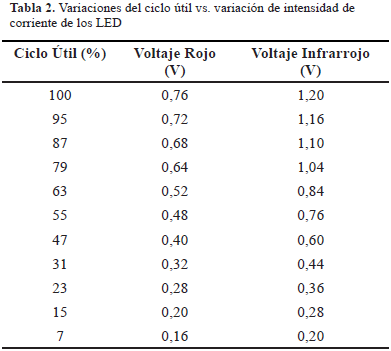
Estas variaciones de intensidad lumínica provocadas por los cambios del ciclo útil del micro PWM son identificadas por el sistema de detección que convierte las señales de corrientes entregadas por el detector en voltajes equivalentes. En la Tabla 2 se presenta las variaciones de voltaje respecto al porcentaje de variación del ciclo útil del micro PWM en la emisión. Las señales registradas en el sistema de detección no presentaron oscilaciones mayores a 0,6 uV, ver Figura 6, favoreciendo la captura de los datos de la señal pulsátil pues las variaciones son despreciables.
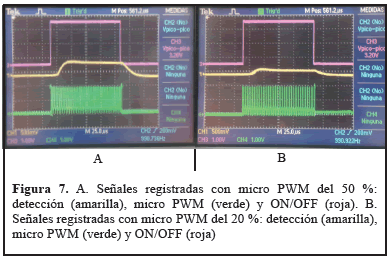
Las señales ON/OFF, micro PWM y la capturada por el detector, en la Figura 7, muestran que al variar el ciclo útil de la señal de micro PWM es posible variar la intensidad efectiva de los LED sin deformar la señal monitoreada. Luego de analizar los resultados en Matlab®, se seleccionó un filtro IIR Chebyshev 2 pasa bajo de orden 4 y un filtro IIR Chebyshev 2 pasa altos de orden 1,488.
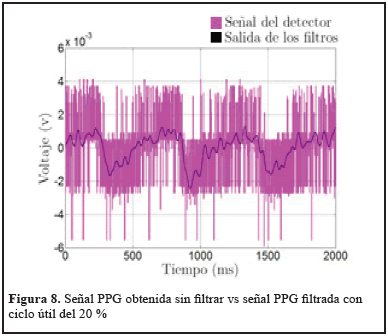
En la Figura 8 se ilustran los datos adquiridos aplicando un ciclo útil de 20 %, el cual es insuficiente para procesar la señal de información.
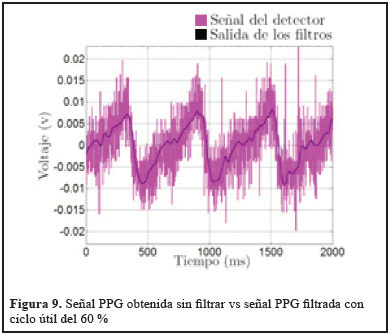
La misma prueba fue realizada, pero con un porcentaje del 60 %, lo que permitió observar un aumento en amplitud controlado para mejorar la calidad de la señal PPG capturada, ver Figura 9.
Se determinó que el ahorro energético está limitado por reducciones del ciclo útil de 50 % para garantizar una relación señal a ruido coherente. De este modo se asegura que tanto la morfología como la tendencia de la señal se conservan al aplicar el filtrado.
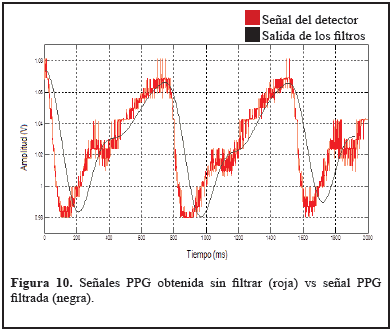
En la Figura 10 se presenta una señal registrada al utilizar un ciclo útil de micro PWM del 90 %. El retardo temporal que se observa en todos los casos es causado por los efectos el filtro. El retardo temporal registrado es de 18 ms y el retardo angular es de φ = 6,48°.
Los resultados de las pruebas con pacientes son presentados en la Tabla 3, donde se observa en todos los casos que las potencias promedio del sistema de la TI ( TI) son significativamente mayores que las del propuesto (
TI) son significativamente mayores que las del propuesto ( D), (p < 0,01). Se presentó un desplazamiento de 11 mW de
D), (p < 0,01). Se presentó un desplazamiento de 11 mW de  TI en el ensayo 1, que no corresponde al desplazamiento presentado en
TI en el ensayo 1, que no corresponde al desplazamiento presentado en  D,esto significa que aunque se utilicen ciclos útiles de 100 % en ambos sistemas, el modelo propuesto consume menos potencia que el de la referencia. Se identificó que el ahorro promedio de todos los ensayos fue 20,06 mW demostrando que bajo el esquema propuesto se logra un ahorro energético total de 41,06 mW respecto a TI.
D,esto significa que aunque se utilicen ciclos útiles de 100 % en ambos sistemas, el modelo propuesto consume menos potencia que el de la referencia. Se identificó que el ahorro promedio de todos los ensayos fue 20,06 mW demostrando que bajo el esquema propuesto se logra un ahorro energético total de 41,06 mW respecto a TI.
IV. CONCLUSIÓN
El sistema de control de intensidades lumínicas desarrollado permitió capturar señales PPG que proporcionan la información a monitorear en tiempo real. Al utilizar arquitecturas de alto desempeño energético, se refleja en una disminución en el número de componentes y el tamaño de la tarjeta electrónica pues en los casos comparados se desprecia el uso de convertidores digitales análogos y amplificadores operacionales.
El estudio con la muestra poblacional seleccionada permitió validar que existen diferencias irrelevantes para el ahorro de energía cuando se cambia de un paciente a otro. Cuando se requirió mayor resolución de la señal PPG, fueron necesarios aumentos en el ciclo útil que implicaron incrementos del consumo de potencia; aún así, el consumo registrado con el método desarrollado es menor que los utilizados convencionalmente.
El presente trabajo permitió determinar que los esquemas que utilizan modulación analógica presentan una desventaja en potencia respecto a los de modulación por ancho de pulso, obteniendo un ahorro promedio de 40 %. Por ello, la metodología presentada resulta ser apropiada en sistemas portables ya que se incrementa el tiempo de operación del dispositivo, permitiendo períodos prolongados de monitoreo.
Los resultados experimentales en la etapa de detección, reflejan que la señal de micro PWM utilizada en el circuito desarrollado permite regular la resolución de la señal muestreada. Este cambio dinámico es útil para aquellos casos donde se requiera monitorizar a pacientes con baja perfusión de oxígeno a través de la variación de la amplitud de la señal de CA en la onda PPG.
Si bien la información adquirida con el sistema implementado presenta variaciones instantáneas de amplitud provocadas por la emisión, los datos adquiridos contienen la información necesaria para obtener índices confiables como SpO2 y frecuencia de pulsación, con lo que se abren diferentes perspectivas que podrían aportar a trabajos futuros.
Las potencias de consumo promedio de los sistemas de emisión permitieron identificar, a través de sus desplazamientos, que bajo las mismas condiciones el sistema propuesto presentó un ahorro de energía significativo respecto al de referencia, ocasionado por los componentes y el sistema de control de iluminación implementados.
AGRADECIMIENTOS
A Colciencias por el apoyo brindado a esta investigación a través de la Convocatoria 566 del año 2012. Así mismo al diseñador industrial Camilo Páramo quien apoyó el proyecto en las etapas de diseño.
REFERENCIAS
[1]. Castillo Rodríguez L. Comportamiento de la Infección Respiratoria Aguda, Colombia, 2010. Inf. Quinc. epidemiológico Nac. (IQUEN, Colomb.), 16(23), 302-316, Dec. 2011. [ Links ]
[2]. Ministerio de Salud y Protección Social. Indicadores Básicos en Salud. 2011. [ Links ]
[3]. World Health Organization. Death rates: WORLD By cause. 2011. [ Links ]
[4]. Karlen W., Lim J., Ansermino J. M., Dumont G., Scheffer C. Design challenges for camera oximetry on a mobile phone. Engineering in Medicine and Biology Society (EMBC), Annual International Conference of the IEEE, 2448-2451, 2012. [ Links ]
[5]. Kyriacou P. A., Shafqat K., Pal S. K. Pilot investigation of photoplethysmographic signals and blood oxygen saturation values during blood pressure cuff-induced hypoperfusiono. Measurement, 42(7), 1001-1005, 2009. [ Links ]
[6]. Patterson J. A. C., Yang G.-Z. Ratiometric Artefact Reduction in Low Power, Discrete-Time, Reflective Photoplethysmography. Body Sensor Networks (BSN), 2010 International Conference, 174-179, 2010. [ Links ]
[7]. Ross E. M., Matteucci M. J., Shepherd M., Barker M., Orr L. Measuring Arterial Oxygenation in a High Altitude Field Environment: Comparing Portable Pulse Oximetry With Blood Gas Analysis. Wilderness Environ. Med., 24(2), 112-117, 2013. [ Links ]
[8]. Patterson J. A. C., Yang G.-Z. Ratiometric Artifact Reduction in Low Power Reflective Photoplethysmography. Biomed. Circuits Syst. IEEE Trans., 5(4), 330-338, 2011. [ Links ]
[9]. Raghuram M., Madhav K. V., Krishna E. H., Reddy K. A. On the Performance of Wavelets in Reducing Motion Artifacts from Photoplethysmographic Signals. Bioinformatics and Biomedical Engineering (iCBBE), 2010 4th International Conference, 1-4, 2010. [ Links ]
[10]. Tavakoli M., Turicchia L., Sarpeshkar R. An Ultra-Low-Power Pulse Oximeter Implemented With an Energy-Efficient Transimpedance Amplifier. Biomed. Circuits Syst. IEEE Trans., 4(1), 27-38, 2010. [ Links ]
[11]. Bustamante J., Pérez J., Crispín A. Sistema de telemonitoreo de oximetría en tiempo real (OXYS). Rev. Argentina Bioingeniería, 17(1), 3-11, 2011. [ Links ]
[12]. Fouzas S., Priftis K. N., Anthracopoulos M. B. Pulse oximetry in pediatric practice. Pediatrics, 128(4), 740-752, 2011. [ Links ]
[13]. Chan E. D., Chan M. M., Chan M. M. Pulse oximetry: Understanding its basic principles facilitates appreciation of its limitations. Respir. Med., 107(6), 789-799, 2013. [ Links ]
[14]. DeMeulenaere S. Pulse Oximetry: Uses and Limitations. J. Nurse Pract., 3(5), 312-317, 2007. [ Links ]
[15]. Hall M. W., Jensen A. M. The role of pulse oximetry in chiropractic practice: a rationale for its use. J. Chiropr. Med., 11(2), 127-133, 2012. [ Links ]
[16]. Masimo. What's the Difference? 2014. En: http://www.masimo.com/whymasimo/clinical-studies.htm. [ Links ]
[17]. Hood R. W. Pulse oximeter sensor control system. 4848901. Critikon, Inc., Tampa, Jul-1989. [ Links ]
[18]. Tian M., Liu W., Zhong Z., Pan Y. Design and research on the hardware of wireless oxygen saturation detection based on ARM. Intelligent Control and Information Processing (ICICIP), 2010 International Conference, 707-710. 2010. [ Links ]
[19]. Yongqing W., Zhipeng Z., Hongrui W., Xiuling L., Rongxia S. A design of noninvasive tester of human arterial oxygen saturation. Biomedical Engineering and Informatics (BMEI), 2010 3rd International Conference, 4, 1376-1380, 2010. [ Links ]
[20]. Markandey V. Pulse Oximeter Implementation on the TMS320C5515 DSP Medical Development Kit (MDK). Jun-2010. [ Links ]
[21]. Sueppel B. E. Mortara D. W. Low power pulse oximeter. 6,697,655 B2. Mortara Instruments, Inc, Feb-2004. [ Links ]
[22]. Nellcor. OxiMax. DS-100A Durasensor. Sensor de oxígeno para adultos. 2005. [ Links ]
[23]. THAT. Low-Noise Matched Transistor Array ICs. THAT 300 Series. 2010. [ Links ]
[24]. Freescale. K53 Sub-Family Reference Manual. Supports: MK53DN512CLQ10, MK53DN512CMD10, MK53DX256CLQ10, MK53DX256CMD10. Jun-2012. [ Links ]
[25]. Texas Instruments Incorporated. Precision, High-Speed Transimpedance Amplifier OPA380. 2007. [ Links ]
[26]. Begg R., Lai D. T. H., Palaniswami M. Computatio. [ Links ]