Introducción
Se estima que el déficit de hierro se encuentra presente en un tercio de la población mundial (1). Este se ha relacionado con múltiples afectaciones en todos los sistemas, con un número no despreciable de artículos que muestran las diversas complicaciones, síntomas y afecciones de la calidad de vida en pacientes con enfermedades digestivas, hematológicas, renales, entre otras. En un estudio realizado en Holanda, con personas sanas, donantes de sangre sin anemia, se tomó como medida indicadora de déficit de hierro concentraciones de protoporfirina > 100 μmol/mol y se halló que de 5280 personas, en el 6,9 % de los hombres y el 9,8 % de las mujeres se presentaba ferropenia sin anemia (2). En el presente artículo se busca caracterizar las afectaciones, el impacto, el mecanismo, el abordaje y el tratamiento de las diferentes complicaciones derivadas del déficit de hierro sin evidencia de anemia.
Metodología
Se realizó una búsqueda completa y actualizada de la literatura científica, en Medline, OVID, Lilacs, SciELO, EMBASE utilizando una estrategia definida con términos MeSH y no MeSH, en español e inglés, sin límite de año, en la cual participaron 5 investigadores. Se construyó una base de datos con los artículos que abarcaran la temática propuesta y que relacionaran la ferropenia sin anemia con cada una de las enfermedades seleccionadas por cada sistema. Estas enfermedades se escogieron basándose en la importancia en la práctica clínica, la cantidad y la calidad de la evidencia disponible para cada patología.
Hallazgos en laboratorio
Los depósitos de hierro se pueden evaluar tanto con métodos directos como indirectos, no excluyéndose los unos de los otros, dado que el adecuado abordaje de la homeostasis del hierro se da mediante la combinación de hallazgos de laboratorio y no de un único resultado (3). Los métodos directos, en su mayoría, son sensibles y específicos para evaluar el estado de hierro en el cuerpo (dentro de estos encontramos: la biopsia y el aspirado de médula ósea) y por medio de estos se obtiene una evaluación semicuantitativa de los depósitos de hierro a través de la tinción de la hemosiderina de los macrófagos con Azul de Prusia.
Así se determina la proporción y la morfología de sideroblastos, que se correlacionan con el aporte de hierro a la médula ósea y con las características generales de la hematopoyesis (3). No obstante, este es un método que en la práctica clínica tiene poca utilidad para evaluar la homeostasis del hierro, dado que es invasivo; de igual manera, en cuanto a los fines investigativos, el estudio de la médula ósea no es reproducible, dada la variabilidad entre observadores, las muestras inadecuadas y la poca correlación con la respuesta a la terapia con hierro (4,5). Todo esto, junto a que no hay una indicación de realizar estos métodos diagnósticos con solo tener hipoferritinemia o sospecha de ferropenia explica los pocos estudios realizados con estos métodos diagnósticos y por qué no se encuentran estudios que evalúen el estado de hierro en pacientes sin anemia con estas estrategias.
Por otro lado, los métodos indirectos son menos sensibles y específicos, aparte de que son alterados por enfermedades infecciosas e inflamatorias crónicas por medio de la hepcidina; pero, por no ser invasivos y más fáciles de interpretar en comparación con los métodos directos, son los más utilizados (figura 1).
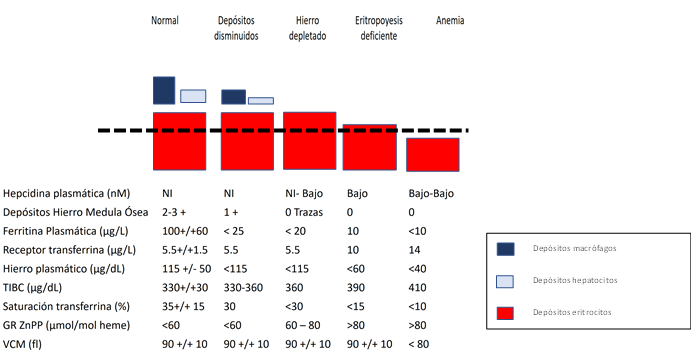
Fuente: imagen realizada por Daniel Martin et al., basada en Brittenham GM. Disorders of iron homeostasis [internet]. En Hematology: Basic Principles and Practice. 7th ed. Philadelphia: Elsevier; 2013. p. 437-49.
Figura 1 Hallazgos paraclínicos directos e indirectos
Antes de la aparición de la anemia franca (Hb < 12 g/L o 13g/L en mujeres y hombres, respectivamente), suceden una serie de alteraciones en los depósitos y en las células hematopoyéticas, comenzando con la disminución de la ferritina, la cual es la manifestación más temprana de este déficit. Si persiste el bajo aporte o absorción, se reduce la entrega de este a los tejidos y aumenta la protoporfirina de zinc, así como el receptor de transferrina, ya que la síntesis de receptores de transferrina aumentan de forma inversamente proporcional a la magnitud del déficit de hierro. En este punto, los valores de hemoglobina, volumen corpuscular medio (VCM) y hemoglobina corpuscular media (HCM) continúan dentro de límites normales, lo cual se ha denominado deficiencia de hierro sin anemia (6). También se puede encontrar disminución de la concentración de hemoglobina y reducción del contenido de la hemoglobina media. Si persiste la deficiencia de hierro, el VCM y la HCM empiezan a disminuir progresivamente, y a esta fase en la cual se ve afectada la hematopoyesis se le conoce como deficiencia de hierro con microcitosis o hipocromía (6). El paso siguiente es la anemia por déficit de hierro, en la cual se encuentran afectadas las cantidades de hemoglobina.
La ferritina es las más estudiada y usada en la práctica clínica, dada su sensibilidad y especificidad. Fue descubierta en 1936 por M. V. Laufberger, científico francés que aisló esta proteína en el bazo de un caballo. Esta proteína la componen dos tipos de subunidades, una H y otra L. Aunque el rol de la ferritina más estudiado es el del depósito de hierro, se sabe que está involucrada en el transporte de hierro, posee un mecanismo antiinmune mediado principalmente por la ferritina H y el receptor de células T con dominios de mucina e inmunoglobulina 2 (TIM-2), está relacionado con un cininógeno de alto peso molecular (HK) con el cual interacciona y desencadena vías que promueven la vasodilatación y liberación de moléculas proangiogénicas, así como otros mecanismos que desempeñan un papel importante en el cáncer, respuesta inflamatoria sistémica, entre otros (7).
En cuanto a la relación entre la ferritina y el déficit de hierro, como se puede evidenciar en la figura 1, incluso antes del desarrollo de la anemia ya hay cambios importantes en los niveles de ferritina. La medición en sangre es muy específica cuando no se mide en pacientes con enfermedades inflamatorias crónicas (8), y es el parámetro más fuerte y útil para evaluar el déficit de hierro. Se ha propuesto hablar de déficit de hierro cuando la ferritina se encuentra por debajo de 30 ng/ml; no obstante, aunque se obtenga una sensibilidad y especificidad del 92 % y del 98 %, respectivamente, no es un punto de cohorte que haya sido adoptado mundialmente, no se ha evaluado en paciente ancianos, con múltiples comorbilidades o enfermedades inflamatorias, por lo que se debe ser cauteloso en la interpretación de estos valores (9).
Los reticulocitos, al igual que la ferritina, presentan alteraciones mucho antes a la disminución de VCM, HCM y hemoglobina de los eritrocitos (10). Cambios en la coloración de los reticulocitos son una forma rápida de detectar la deficiencia de hierro subclínico en pacientes no anémicas premenopáusicas. Dentro de los parámetros evaluados se encuentra el contenido de hemoglobina reticulocitario, el cual es el producto entre la concentración de hemoglobina y el tamaño celular. Se ha demostrado que este parámetro de laboratorio está alterado desde estadios tempranos, principalmente desde la deficiencia de hierro latente (ferritina < 30 ng/ml, aumento del receptor soluble de transferrina > 8,3 μg/ml y TIBC > 390 μg/dL; p < 0,001) (11).
En este estudio también se evidenció una diferencia significativa entre los pacientes normales y aquellos con deficiencia de hierro prelatente (ferritina < 30 ng/ml) p < 0,05; así como una diferencia estadísticamente significativa entre ambos estadios (11). Sin embargo, la mejor sensibilidad y especificidad fue de tan solo 73,9 % y 73,3 %, respectivamente; estos datos se tomaron de una población en la cual se excluían los pacientes con una VCM mayor o igual de 100 fL, ya que la sensibilidad llega a disminuir hasta 60,7 %, abarcando a los pacientes con este VCM (9). Hay que tener en cuenta que la población evaluada era joven con una media de edad de 16,9 ± 1,8, atletas, sanos, lo cual no es el común denominador (11).
Sistema cardiovascular
Se ha estudiado ampliamente la anemia en falla cardiaca (FC) y se ha demostrado que aumenta la mortalidad dos veces en comparación con los pacientes sin anemia (figura 2). Sin embargo, a diferencia de la anemia, la relación entre el déficit de hierro y la FC es un tema relativamente nuevo y del cual en la última década se ha profundizado en los mecanismos fisiopatológicos, consecuencias y tratamiento de estos pacientes. Aproximadamente, el 20 % de los pacientes con FC presenta déficit de hierro (12,13). En un estudio realizado con 955 pacientes con FC y fracción de eyección reducida (< 45 %) se encontró que el 15 % de los pacientes sin anemia tenían algún test positivo para el déficit de hierro (14).
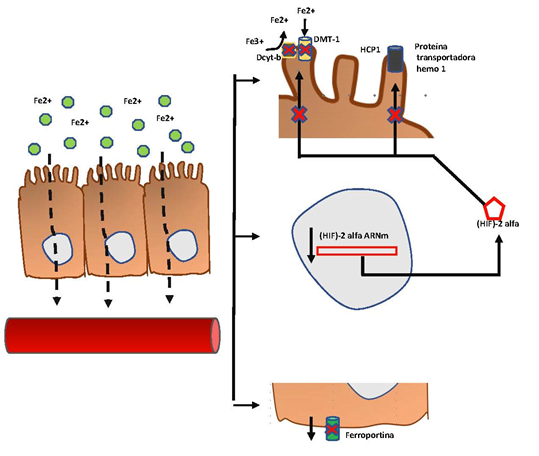
Figura 2 Déficit de hierro en falla cardiaca. La disminución en la expresión del factor intestinal inducido por hipoxia (HIF)-2 se relaciona con la disminución en la expresión del citocromo duodenal b (Dcyt-b) y el transportador divalente de metales 1 (DMT1), lo cual se asocia con la disminución en la captación de hierro. También se evidencia una disminución de la ferroportina que no se vincula directamente con la hepcidina
De igual manera, en otro estudio (15) realizado en Polonia en 544 pacientes con FC sistólica y fracción de eyección reducida estable, en el cual se definía deficiencia de hierro como ferritina < 100 mg/L o ferritina ≥ 100 mg/L, pero ≤ 300 mg/L con saturación de transferrina < 20 %, la prevalencia de déficit de hierro sin anemia fue de 32 ± 4 %. Se sabe que el déficit de hierro está relacionado con aumento del riesgo, empeoramiento de los síntomas e incluso la mortalidad en algunas enfermedades cardiovasculares, dentro de las que se encuentra la enfermedad coronaria y la FC. De igual modo, tiene un impacto negativo en los pacientes con cirugías cardiacas (trasplante cardiaco y otro tipo de cirugía cardiaca).
Enfermedad coronaria
Existe una relación proporcional entre las bajas concentraciones de transferrina y ferritina con un aumento en el riesgo de presentar enfermedad coronaria, aun cuando este es independiente a la presencia de anemia (16). Existen dos estudios en los cuales se demuestra una alta prevalencia de cardiopatía isquémica en los pacientes con déficit de hierro: el primero realizado por Jankowska et al. (15), en el cual se reportaba una prevalencia del 48 % en pacientes con enfermedad coronaria estable que iban a ser llevados a cirugía cardiaca, y el segundo realizado por Oona Meroño et al. (17), quienes reportaban una prevalencia del 61 %. No obstante, el último estudio definió el déficit de hierro como ferritina < 100 ng/mL o ferritina < 800 ng/mL más transferrina < 20 %, lo cual no está acorde con las definiciones de déficit de hierro utilizadas en la mayoría de estudios (ferritina < 100 mg/L o ferritina ≥ 100 mg/L, pero ≤ 300 mg/L con saturación de transferrina < 20 %).
No se conoce hasta el momento el mecanismo fisiopatológico que explique la relación entre ferropenia y enfermedad coronaria. Oona Meroño et al. (17) encontraron dos aspectos que pueden plantear un mecanismo inflamatorio como el causante de desarrollo de enfermedad coronaria: el primero es la diferencia significativa que existe entre los pacientes con déficit de hierro y el grupo placebo, dado que en el primer grupo hay un mayor número de pacientes con diabetes, hipertensión y tabaquismo, todos estos relacionados con un componente inflamatorio ya estudiado ampliamente, y el segundo, la correlación entre inflamación y ferropenia, donde se muestran cómo hay una relación significativa entre los niveles de interleucina 6 (IL-6), proteína C reactiva y niveles bajos de hierro sérico.
Esto último también fue evidenciado por Ching-Hui Huang et al. (18), quienes investigaron el valor pronóstico de la concentración de hierro sérico en relación con la fracción de eyección del ventrículo izquierdo y el puntaje de riesgo TIMI en pacientes posinfarto agudo de miocardio. Fue importante la relación significativa entre los niveles bajos de hierro sérico y un mayor riesgo de infarto agudo de miocardio, así como un menor porcentaje de recuperación (< 10 %) de la fracción de eyección del ventrículo izquierdo tras la angioplastia. Adicionalmente, fue significativa la relación entre hierro disminuido y concentraciones altas de IL-6 en pacientes con infarto agudo de miocardio con elevación del ST (segmento ST), así como una relación inversamente proporcional entre el hierro sérico y el puntaje TIMI (p = 0,002).
Por último, se destacan los resultados del estudio realizado por Ewa A. Jankowska et al. (19), en el cual se utilizó el aspirado de médula ósea para evaluar el déficit de hierro en personas con EC estable. Se encontró que el receptor soluble de transferrina, la transferrina y el receptor de eritropoyetina se correlacionaban con déficit de hierro, a diferencia de la ferritina sérica. De ahí que sea el receptor soluble de transferrina el de más fuerte asociación (área bajo la curva = 0,876 ± 0,048, siendo el punto más eficaz ≥ 1,32 mg/l, con una sensibilidad del 67 % y una especificidad del 97 %). Así mismo, encontraron que el 43 % de los diagnosticados con déficit de hierro no cursaban con anemia.
Falla cardiaca
Al usar los criterios de deficiencia de hierro absoluto y relativa (ferritina < 100 μg/L y ferritina 100-299 μg/L más transferrina < 20 %, respectivamente) de 546 pacientes con falla cardiaca, el 32 % presentaba ferropenia sin anemia, siendo el déficit de hierro un desenlace negativo independiente a la presencia de anemia (15). En un estudio prospectivo-observacional, realizado por Inês Rangel et al. (20), se incluyeron pacientes con falla cardiaca estable con fracción de eyección del ventrículo izquierdo reducida (< 45 %) y cuyo desenlace compuesto primario fue mortalidad total y eventos no fatales cardiovasculares, de 127 pacientes con déficit de hierro, el 74 % no presentó anemia y durante un periodo de 225 días el 24 % de los pacientes con déficit de hierro desarrolló el desenlace compuesto primario; mientras que solo el 5 % en aquellos sin déficit de hierro (21).
Hasta el momento no existe un mecanismo fisiopatológico que explique completamente la anemia en falla cardiaca. Se sabe que es multifactorial, pero hay contradicciones entre distintos artículos sobre cuál es el mecanismo más frecuente. Por ejemplo, Nanas et al. (22) estudiaron pacientes con anemia y falla cardiaca en estadio final y documentaron la presencia de anemia por déficit de hierro en el 73 % de los casos.
El déficit de hierro puede ser absoluto, cuando los depósitos están agotados, o puede ser funcional, cuando hay una alteración en el metabolismo del hierro, incluyendo los procesos inflamatorios (23). En un estudio realizado en ratones se buscó evaluar los mecanismos fisiopatológicos que llevaban al desarrollo de ferropenia. Se encontró que la expresión del factor intestinal inducido por hipoxia-2, encargado de la regulación del citocromo duodenal b y el transportador divalente de metales 1 se encontraba disminuida en los pacientes con falla cardiaca, e interesantemente, a pesar de que los niveles de hepcidina fueran bajos, había una disminución en la expresión de la ferroportina, lo cual se correlacionaría con una alteración generalizada de los sistemas reguladores del hierro. Se cree que el factor gatillo de esta teoría es el estrés oxidativo, el cual disminuye la expresión de factor intestinal inducido por hipoxia-2 alfa (24). Otro hallazgo llamativo es la relación entre caquexia y el desarrollo de ferropenia, pues se sabe que la caquexia es un indicador de inflamación, y en estos animales la presencia de esta se correlacionaba con ferritina baja, hierro disminuido y baja capacidad total de fijación del hierro, lo cual se encuentra a favor de que todo lo anterior esté mediado por un mecanismo inflamatorio.
La administración de hierro en pacientes con falla cardiaca e inicio conjunto con eritropoyetina en pacientes con anemia (25,26,27,28,29,30,31) no mostró ningún beneficio con el suministro de darbepoetina alfa vs. placebo, tanto en los desenlaces primarios (muerte por cualquier causa u hospitalización por empeoramiento de la falla cardiaca) como en los secundarios; por el contrario, aumentó la tasa de eventos tromboembólicos y el riesgo de accidente cerebrovascular isquémico. De igual manera, distintos estudios en pacientes con anemia sin el uso de eritropoyetina mostraron que hubo mejoría en los niveles de hemoglobina, clase funcional y calidad de vida (32).
Desde el estudio FERRIC-HF (33) se evaluó el beneficio de la aplicación intravenosa de hierro, incluyendo pacientes no anémicos (n = 17) con déficit de hierro (ferritina < 100 g/L o entre 100 g/L y 300 g/L con transferrina < 20 %), quienes encontraron una mejoría en la duración del ejercicio, transferrina, ferritina y clase funcional. Si bien el grupo con anemia evidenciaba parámetros similares a los pacientes no anémicos, los primeros mostraron mejoría en el consumo pico de oxígeno y hemoglobina, lo cual sugiere que el principal efecto del hierro en pacientes sin anemia es sobre la calidad de vida.
De forma similar, el estudio CONFIRM-HF (6) evaluó el suministro de hierro carboximaltosa vs. placebo en pacientes con falla cardiaca con fracción de eyección reducida, clase funcional NYHA II-III y hemoglobina < 15 g/dL. Se encontró una mejoría en la prueba de caminata de 6 min a la semana 24 e incluso a la semana 52, así como una disminución en el riesgo de hospitalización por descompensación de falla cardiaca en el grupo de pacientes que recibieron hierro.
El estudio EFFECT-HF (34), con una metodología similar a los anteriores, comparó la administración de hierro carboximaltosa vs . placebo en 174 pacientes con falla cardiaca con fracción de eyección reducida, estables, NYHA II-III con péptido cerebral natriurético o porción amino-terminal del propéptido natriurético tipo B > 100 pg/mL o > 400 pg/mL, respectivamente, y déficit de hierro con hemoglobina < 15 sin necesidad de transfusión inmediata. El desenlace primario fue el cambio de pico de oxígeno desde el inicio hasta la semana 24.
Respecto al desenlace primario, se evidenció una mejoría significativa en el grupo de hierro (p = 0,02), así como en la calidad de vida y clase funcional. Por el contrario, en los desenlaces secundarios no se encontró una diferencia significativa en cuanto a ventilación minuto/pendiente de producción de dióxido de carbono y la tasa de trabajo máximo. En este momento se encuentra en curso un estudio aleatorizado, doble ciego controlado, en pacientes con falla cardiaca aguda en que se compara el uso de hierro carboximaltosa vs. placebo (AFIRM-AHF-NCT02937454). En cuanto al uso de hierro oral, en el estudio IRONOUT HF (35) se comparó hierro polisacárido vs. placebo en 225 pacientes con falla cardiaca con fracción de eyección reducida y déficit de hierro, en el cual no se encontró mejoría en el pico de oxígeno ni prueba de caminata de 6 min.
Sistema respiratorio: enfermedad pulmonar obstructiva crónica
La enfermedad pulmonar obstructiva crónica (EPOC) constituye la cuarta causa de muerte en todo el mundo; pero se estima que para el 2020 se va a convertir en la tercera causa de muerte. Es una enfermedad frecuente, prevenible, tratable y se caracteriza por síntomas respiratorios y limitación al flujo aéreo persistente, lo cual es secundario a alteraciones en las vías respiratorias y alvéolos tras la exposición de gases o partículas nocivas (36). En el estudio de Barberan et al. (37), en el cual se buscaba evaluar el impacto de la ferropenia sin anemia en pacientes EPOC en la capacidad aeróbica, definiendo ferropenia como una ferritina < 100 g/dL, se encontró una prevalencia del 48 %, lo cual es un valor alto y que no tiene en cuenta aquellos pacientes con ferritina entre 100 y 300 g/dL con transferrina < 20 %, pues ello implicaría una mayor prevalencia.
Se cree que la ferropenia podría influir negativamente en el pronóstico del paciente a través de la alteración en la producción y función de las coenzimas que contienen hierro, lo cual implicaría una alteración en la función normal de los músculos respiratorios (38). En el estudio prospectivo publicado en el 2015 por Barberan et al. (37) se buscaba evaluar la relación entre la ferropenia sin anemia y la capacidad aeróbica en los pacientes con EPOC antes de un programa de alta intensidad y después de este. Se incluyeron 110 pacientes con EPOC, de los cuales 70 hicieron parte de la evaluación final, en la cual se constató una prevalencia del 48 %, una mayor tasa inicial de fumadores activos, disminución de la capacidad de difusión del dióxido de carbono y el tiempo de resistencia en el grupo de ferropenia en comparación con el grupo de hierro normal.
Adicionalmente, se evidenció una mejoría en la capacidad aeróbica solo en pacientes con hierro normal, lo cual indica una disminución en la respuesta al entrenamiento y terapia de rehabilitación en pacientes con ferropenia sin anemia (37). De forma contraria, en un estudio en el cual se tomaron datos clínicos de 107 pacientes con EPOC, solo un paciente (0,9 %) presentaba ferropenia sin anemia (39). En este último estudio, el segundo objetivo era evaluar el impacto en los parámetros hematológicos, así como en la percepción de la disnea tras la administración de eritropoyetina e hierro endovenoso (hierro sacarosa), y aunque el único paciente con ferropenia sin anemia no hizo parte de esta evaluación, cabe mencionar que en el grupo intervención hubo una mejoría en la hemoglobina y en la calidad de vida. Esto último nos hace cuestionarnos si la relación entre deficiencia de hierro y EPOC tendrá el mismo curso de la falla cardiaca, donde los estudios comenzaron de forma similar (39).
Se sabe que el hierro tiene una relación con el volumen espiratorio forzado en la fracción de eyección del ventrículo izquierdo, siendo menor este volumen en pacientes con hierro bajo (40). Se cree que el mecanismo fisiopatológico puede estar relacionado con la afectación muscular derivada del déficit de hierro; sin embargo, al igual que en la fisiopatología de la ferropenia en la EPOC, aún no están claros todos los mecanismos que llevan al compromiso de la funcionalidad del pulmón por déficit de hierro ni por qué se provoca este último. Dentro de las teorías planteadas hasta el momento, la que tiene más fuerza es la inflamación crónica, donde la hepcidina producida en los hepatocitos y macrófagos alveolares ejerce un papel importante (41). Se ha demostrado cómo por medio de la IL-6 y el interferón gamma se desencadena la producción de hepcidina desde los dos tipos de células anteriormente nombradas; de igual manera, el cigarrillo y la EPOC per se aumentan la permeabilidad capilar y permiten la distribución sistémica de los mediadores inflamatorios, lo cual estaría relacionado con el aumento de los niveles de hepcidina (figura 3).
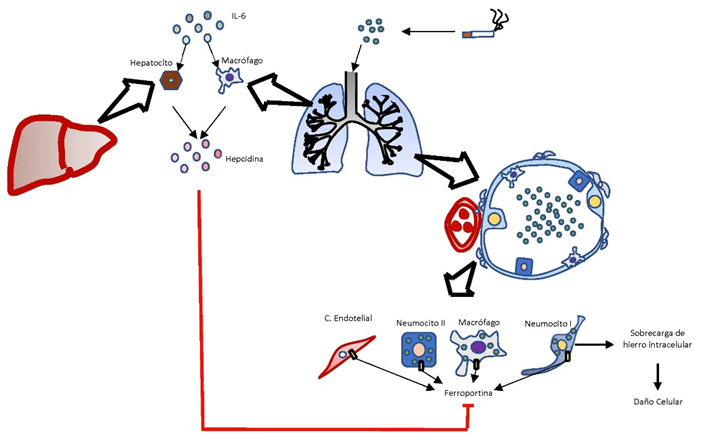
Fuente: imagen realizada por Daniel Martín et al., basada en González Alayón C, Pedrajas Crespo C, Marín Pedrosa S, Benítez JM, Iglesias Flores E, Salgueiro Rodríguez I, et al. Prevalencia de déficit de hierro sin anemia en la enfermedad inflamatoria intestinal y su impacto en la calidad de vida. Gastroenterol Hepatol. 2017 Sep;41(1):22-9.
Figura 3 Fisiopatología déficit de hierro en la EPOC: la hepcidina no solo inhibe la acción de la ferroportina en el intestino, como lo muestra la figura, sino que las células que se encuentran en el espacio alveolar y su alrededor también son afectadas por la acción de esta hormona.
Sistema digestivo
La anemia asociada con patología gastrointestinal ha sido ampliamente estudiada, considerándose la complicación extraintestinal más frecuente en patologías como la enfermedad inflamatoria intestinal (42,43,44,45). En cuanto a la ferropenia sin anemia o deficiencia de hierro sin anemia y la afectación que esta produce a la calidad de vida de pacientes con patología gastrointestinal, es muy reducida. La prevalencia oscila entre 13y 90 % en enfermedad inflamatoria intestinal (42), un rango muy amplio, ya que los estudios suelen usar criterios para anemia, mas no para deficiencia de hierro sin anemia, y en la práctica clínica no suele investigarse esta última con parámetros de hemoglobina o hematocrito normales. Otros estudios muestran que la prevalencia de anemia está entre 36 y 76 %, asociada a ferropenia en la mayoría de casos (42,43).
Existen múltiples mecanismos fisiopatológicos que explican ferropenia y posterior anemia: sangrados crónicos, malabsorción e inflamación (43,46). Los sangrados crónicos pueden ser provocados por úlceras o várices causadas por diferentes patologías en el tubo digestivo; así mismo, trastornos en la absorción, donde cobra mayor relevancia la infección por Helicobacter pylori, donde variables como el pH y el ácido ascórbico afectan la absorción de hierro. La infección por este microrganismo produce cambios histopatológicos inflamatorios en la mucosa gástrica y duodenal, inactivación del ácido ascórbico, que disminuyen su biodisponibilidad a través de receptores de membrana de lactoferrina. Adicionalmente, aumenta la concentración de hepcidina, lo cual disminuye la absorción del hierro (47,48).
La enfermedad inflamatoria intestinal es parte de un grupo de patologías con etiología multifactorial, de componente autoinmune, donde existe una respuesta inflamatoria en la mucosa intestinal que la erosiona y la destruye. Los sangrados producidos por estas lesiones, los trastornos en la absorción dada la inflamación crónica, la alteración de la absorción por los procedimientos quirúrgicos que se evidencian con mayor frecuencia en la enfermedad de Crohn (43,45,47) son los principales responsables de que sea mayor la prevalencia de la deficiencia de hierro sin anemia. En un estudio realizado con 111 pacientes con enfermedad de Crohn (61,4 %) o colitis ulcerativa (38,6 %) sin anemia se encontraron 47 (37 %) pacientes con alteraciones en la ferritina y la transferrina, siendo la presencia de actividad de la enfermedad la de mayor correlación (OR = 9,4; 2,5-35,9; IC 95 %; p = 0,001).
Sistema nervioso central
Proliferación y diferenciación neuronal
El papel del hierro en el desarrollo cerebral ha sido un tema de interés durante los últimos 25 años. Múltiples estudios han identificado cómo la deficiencia de hierro ha llevado a la formación de procesos patológicos y a la alteración de los procesos de desarrollo. Se han identificado diversas regiones afectadas como lo son el eje hipotálamo-pituitaria-adrenal, el estriado y el hipocampo. Así mismo, hay diferentes procesos bioquímicos afectados, como la fosforilación oxidativa, la producción dopaminérgica, el metabolismo de los ácidos grasos y la síntesis de nucleótidos.
Un estudio en modelos animales demostró que la deficiencia de hierro sin anemia tiene efectos en las neuronas hipocampales, por ejemplo, anormalidades moleculares, bioquímicas, estructurales y comportamentales. Las concentraciones de hierro regulan la formación de glutamato y su secreción. Esto es de particular importancia, pues los niveles de glutamato normales y el metabolismo energético son críticos para la morfogénesis de dendritas y la formación de sinapsis, particularmente en el hipocampo (49). El hipocampo es central para el procesamiento de la memoria de reconocimiento, particularmente el hipocampo doral, incluyendo áreas extensas de CA1 (cornu ammonis), que son importantes en los cambios estructurales y bioquímicos involucrados en la codificación de los eventos de memoria declarativa en humanos.
Mielinización
En cuanto a su rol en la mielinización, varios estudios lo han demostrado en la síntesis de lípidos de la mielina y fosfolípidos. También se postulan mecanismos adicionales como lo son cambios en los preoligodendrocitos tempranos y oligodendocritos, y alteraciones en la captación de hierro por los oligodendocritos por la transferrina (50). La deficiencia de hierro en etapas cruciales y la duración de esta deficiencia son factores clave para determinar las consecuencias cerebrales. La mielinización alterada puede llevar a daños en el desarrollo de los infantes (2). El periodo más alto de captación de hierro en el sistema nervioso central coincide con el pico de mielinización (50). El tiempo de aporte de hierro a los oligodendocritos durante el desarrollo es importante, pues la hipomielinización y las secuelas neurológicas subsecuentes persisten posterior a la corrección de la deficiencia (51).
Arborización dendrítica
La deficiencia de hierro temprana en neuronas, mediante la alteración de la función mitocondrial y el metabolismo energético de las neuronas, es responsable de defectos en la maduración sináptica y dendrítica de las neuronas. En modelos de cultivos celulares embrionarios de neuronas hipocampales expuestos a un agente quelante de hierro se evidenció que el número de dendritas era menor, al igual que su longitud, y así mismo había disminución de las ramificaciones secundarias y terciarias comparados con el control. Las neuronas con déficit de hierro permanecen anormales durante el periodo de desarrollo con campos dendríticos obtusos y expresión anormal de genes involucrados en el neurodesarrollo (49,52).
Síndrome de piernas inquietas
El síndrome de piernas inquietas, también conocido como la enfermedad de Willis-Ekborn, es una enfermedad neurológica común. El 7,2 % de los adultos norteamericanos y europeos reporta haber experimentado los síntomas del síndrome de piernas inquietas en algún punto durante un periodo de un año, y el 5 % reporta experimentar los síntomas de forma semanal. Este síndrome se caracteriza por la aparición de urgencia irresistible de mover las piernas, acompañado de síntomas desagradables, la presentación o el empeoramiento de estos síntomas durante el sueño, el reposo o la inactividad, la mejoría total o parcial moviendo las piernas y el empeoramiento o su aparecimiento al atardecer o durante la noche (53,54).
La deficiencia de hierro con anemia y sin esta se reconoce actualmente como un mecanismo fisiopatológico inicial en el desarrollo de esta entidad. La relación entre el nivel de hierro y el síndrome de piernas inquietas se examinó en 18 ancianos con esta enfermedad y 18 sujetos control. Calificaron en una escala con un puntaje máximo de 10 la severidad de la enfermedad y evaluaron los niveles de ferritina séricos. Se encontró que los niveles de ferritina estuvieron disminuidos en los pacientes con síndrome de piernas inquietas, comparados con los sujetos control, y como hallazgo relevante los niveles de hemoglobina no cambiaron entre los dos grupos (55). Los estudios más tempranos sobre síndrome de piernas inquietas revelaron que cerca del 25 % de los pacientes tiene deficiencia de hierro (56). Modelos animales también han establecido la relación entre la deficiencia de hierro cerebral y la función dopaminérgica alterada en el síndrome de piernas inquietas, sobre todo con la disminución de la densidad de receptores D2 en el estriado y con aumento en la actividad de la tirosina hidroxilasa en el mesencéfalo (57,58).
Adicionalmente, la síntesis de mielina depende del hierro, y la deficiencia del hierro en modelos animales reduce las proteínas, los lípidos y el colesterol de la mielina. La deficiencia de hierro cerebral en el síndrome de piernas inquietas es capaz de producir un déficit significativo de mielina, confirmado por estudios de imagen que demuestran una disminución significativa de la sustancia blanca en el cuerpo calloso, el cíngulo anterior y el giro precentral. La disminución de la mielinización contribuye a los síntomas de la enfermedad en relación con la integración sensorimotora que tiene una señalización tiempo dependiente (58).
Los niveles de ferritina en el líquido cefalorraquídeo son menores en los casos de síndrome de piernas inquietas, comparado con controles, y los estudios avanzados con resonancia magnética demuestran depósitos de hierro menores en el estriado, el tálamo y el núcleo rojo. Adicionalmente, la deficiencia de hierro en diferentes regiones cerebrales en el síndrome de piernas inquietas involucra una falla para proveer un transporte adecuado de hierro a través de la barrera hematoencefálica, llevando a una falla regional para importar hierro en neuronas críticas como lo son las células de neuromelanina en la sustancia nigra (59,60).
Con base en este papel relevante de la deficiencia de hierro se han planteado diferentes estrategias terapéuticas. En el estudio previamente mencionado, 15 de los pacientes ancianos con síndrome de piernas inquietas se trataron con sulfato ferroso durante dos meses, y los puntajes de severidad del síndrome mejoraron en un valor medio de 4 puntos en 6 pacientes con ferritina menor o igual de 18 µg/L, y en 3 puntos en 4 pacientes con ferritina mayor de 18 µg/L, menor o igual de 45 µg/L, y en un punto en 5 pacientes con niveles de ferritina mayor de 45 µg/L y menores de 100 µg/L. Se concluyó que la deficiencia de hierro con anemia y sin esta es un factor importante en el desarrollo del síndrome de piernas inquietas y el suplemento de hierro puede generar una reducción significativa de los síntomas (55).
Las concentraciones de ferritina menores de 45-50 µg/L se han asociado con una mayor severidad de los síntomas, y el suplemento de hierro se sugiere si los niveles de ferritina son menores de 75 µg/L. Esta recomendación se basa en ensayos clínicos controlados que han mostrado el beneficio de la terapia. Un ensayo clínico aleatorizado con control con placebo, doble ciego, asignó pacientes a terapia con hierro oral vs. placebo durante 12 semanas. Luego de este periodo los puntajes de las escalas de valoración disminuyeron más en el brazo de tratamiento (p = 0,01), y los niveles de ferritina incrementaron más en este grupo (p = 0,04).
Este fue el primer estudio en demostrar una mejoría estadísticamente significativa de los síntomas del síndrome de piernas inquietas usaron la terapia con hierro oral en pacientes con ferritina normal baja (61). En otro ensayo clínico controlado doble ciego aleatorizado con control con placebo, 11 pacientes fueron asignados al azar para la administración de hierro dextrano, y 14 pacientes a la administración de solución salina. Los puntajes de severidad del síndrome mejoraron significativamente junto con los síntomas en los participantes expuestos a la terapia con hierro dextrano, y sucedió a la semana luego de la infusión (p = 0,03) y fue máxima la mejoría a las 2 semanas (p = 0,01) (62).
Finalmente, dos estudios evaluaron el papel de la carboximaltosa férrica. Uno fue un ensayo clínico controlado aleatorizado, multicéntrico, con control con placebo, en el que encontraron que esta mejoró significativamente la escala de severidad del síndrome de piernas inquietas de 8,9 puntos (p = 0,040), la calidad de vida y demostraron que es un tratamiento efectivo y seguro, pues no hubo efectos adversos (63). El segundo estudio fue un ensayo clínico controlado doble ciego, aleatorizado, con control con placebo en el que se tomaron pacientes con síndrome idiopático no anémicos, y recibieron 1000 mg del tratamiento o placebo en infusión única (64).
Estos sujetos estuvieron libres de medicamentos adicionales por, al menos, dos semanas antes de la evaluación de base. A la sexta semana posinfusión los pacientes con la terapia con carboximaltosa férrica demostraron una mejoría significativa en la escala de severidad de síndrome de piernas inquietas (p = 0,03) y una escala visual análoga de severidad (p = 0,001). Doce de los 32 sujetos tratados con hierro permanecieron libres de posteriores manejos a las 30 semanas con mejoría de los síntomas. Es importante aclarar que un metanálisis incluyendo varios de estos estudios encontró heterogeneidad significativa en la formulación del hierro usado, las características de los pacientes y la medición de los resultados, y encontró evidencia insuficiente para concluir el beneficio del hierro para el tratamiento del síndrome de piernas inquietas. Se debe avanzar en nuevos estudios para continuar esclareciendo el papel terapéutico del suplemento de hierro (65).
Trastornos cognitivos
Desde el ensayo clínico controlado de Brunner et al. (66), en 1996, que estudió pacientes adolescentes femeninas de los Estados Unidos con deficiencia de hierro sin anemia y que mostró una mejoría del aprendizaje verbal y en memoria con suplemento oral de hierro, hay más evidencia de que no solo la deficiencia de hierro con anemia, sino también la deficiencia de hierro sin anemia, afecta la cognición. Un estudio observacional transversal que evaluó 428 pacientes en adolescencia temprana de China midió las concentraciones de hierro séricas y evaluó el desempeño neurocognitivo de los participantes, y encontró que los pacientes con deficiencia de hierro se asociaron con menor desempeño en tareas de flexibilidad mental y abstracción y su habilidad de procesamiento espacial (67). Adicionalmente, los pacientes que sufren de deficiencia de hierro perinatal y posnatal muestran problemas en el neurodesarrollo, que altera el aprendizaje y la memoria (68).
Falkingham et al. (69) encontraron en una revisión sistemática y metanálisis de 2010 que el suplemento de hierro mejoraba la atención y la concentración en adolescentes y mujeres con déficit de hierro con anemia y sin esta. Desde entonces varios estudios han investigado esta relación y mediante sus intervenciones han establecido el papel de la deficiencia de hierro sin anemia en el desarrollo de trastornos cognitivos. Un ensayo clínico controlado aleatorizado doble ciego con control con placebo realizó una intervención en niños en Sudáfrica con ferropenia y pobre estado de ácidos grados omega 3.
Luego de varios meses de suplemento con hierro oral encontraron una mejoría cognitiva en los niños con deficiencia de hierro. Cabe resaltar que el 20 % presentaba anemia. Otro ensayo clínico controlado, con control con placebo, aleatorizado, asignó mujeres de 18 a 35 años con diferentes estados de hierro a la suplementación con hierro o a placebo (70). Se realizaron pruebas cognitivas. Las mujeres con un estado de hierro normal presentaban mejor desempeño en las pruebas cognitivas de base. Las mujeres con deficiencia de hierro y anemia se presentaban con menor desempeño y las que presentaban deficiencia de hierro sin anemia tenían un desempeño intermedio con respecto a los grupos previos. Luego del tratamiento durante 16 semanas de hierro oral, la mejoría de la ferritina sérica se asoció a una mejoría de 5-7 veces en el desempeño cognitivo, particularmente en las mujeres con deficiencia de hierro sin anemia (71).
Además de los efectos en personas jóvenes, se ha postulado el papel de la deficiencia de hierro en enfermedades neurodegenerativas, pues como hemos revisado previamente el hierro participa en el desarrollo cerebral, la neurogénesis y las funciones cognitivas (72). La deficiencia de hierro durante la gestación y en la vida posnatal temprana ha demostrado alterar la expresión de genes en la totalidad del cerebro y en el hipocampo. Un estudio utilizando modelos murinos confirmó que la deficiencia temprana de hierro altera la expresión de genes cuya disregulación está implicada en la etiología de la enfermedad de Alzheimer, como lo son Fnl1, Cst3, Apbb1, Clu, App y Htatip (73). Estos datos que presentaron en el estudio sugería que la deficiencia de hierro y no la anemia, altera la expresión de estos genes durante periodos vulnerables del desarrollo hipocampal (73).
Finalmente, la deficiencia de hierro, cuyo papel es clave en el transporte de oxígeno y almacenamiento, puede llevar a hipoxia cerebral y a deterioro cognitivo. Un estudio observacional transversal que evaluó pacientes ancianos que ingresaban al servicio de geriatría examinó a 622 pacientes valorando su función cognitiva y su estado de hierro. Encontraron una influencia negativa de la deficiencia de hierro sobre la función cognitiva y esta influencia fue independiente de la presencia de anemia. Los pacientes con deficiencia de hierro tenían menor puntaje en el Mini Mental State Examination (p < 0,001) y esta relación estaba presente en los pacientes sin anemia (p = 0,004) (74).
Sistema genitourinario
Enfermedad renal crónica
El déficit de hierro en enfermedad renal crónica (ERC) es de alta prevalencia (57,8-72,8 %), un gran porcentaje de estos pacientes cursan con anemia asociada y toda la morbimortalidad que esto implica (75,76,77). Esto ha llevado que alrededor del 85-90 % requieran tratamiento con agentes estimulantes de la eritropoyesis. Sin embargo, el uso de estos agentes no compensa a todos los pacientes y alteraciones en el metabolismo del hierro serían los responsables de la presencia de resistencia (78). Hay múltiples estudios que evidencian que es tan primordial tratar la deficiencia de hierro con suplencia de este como el uso de inductores de la eritropoyesis, que producen mejoría en morbimortalidad calidad de vida y pronóstico del paciente.
La ERC produce disbalance en el metabolismo y absorción del hierro, la inflamación crónica lleva a la producción de citocinas y otros productos de la inflamación, en especial la IL-6 aumenta la producción de hepcidina a nivel hepático, disminuyendo así la absorción de hierro digestiva por inhibición de canales ferroportina 1; además, aumenta la captación de hierro por los macrófagos, pero disminuyen su liberación en estas células y en el sistema hepático produciendo así una deficiencia de hierro (79,80,81,82). Se postula, además, que la uremia, característica de estos pacientes, inhibe factores hematopoyéticos y altera el metabolismo del hierro. También vemos que los pacientes con ERC tienen pérdidas directas de hierro asociado con hemorragias crónicas por disfunción plaquetaria producida por la uremia (79), flebotomías frecuentes y el atrapamiento de sangre en los circuitos de diálisis. Todo esto nos lleva a un déficit de hierro real; por otro lado, existe un déficit de hierro funcional o bloqueo de hierro en células reticuloendoteliales, asociado al uso de agentes estimulantes de la eritropoyesis (78,79,83).
El diagnóstico de déficit de hierro en ERC sin diálisis está basado en niveles de ferritina < 100 ng/dL y < 200 ng/dL en pacientes sometidos a diálisis, además de un índice de saturación de transferrina < 20 % (84). Las guías diagnósticas recomiendan determinar un porcentaje de glóbulos rojos hipocrómicos (< 6 %) y hemoglobina en reticulocitos (< 29 pg), ya que estos son parámetros más sensibles para determinar déficit de hierro funcional y no se alteran ante el uso de estimulantes de la eritropoyesis, además de ser mejores predictores de una adecuada respuesta al tratamiento a la suplementación de hierro (5,83,85,86).
Cuando encontramos niveles de ferritina bajos asociados con transferrina baja, estamos ante un déficit de hierro real; por otro lado, si hallamos niveles de ferritina altos con una transferrina baja, asociados con un aumento en el porcentaje de glóbulos rojos hipocrómicos y niveles bajos de hemoglobina en reticulocitos, hay reservas de hierro adecuadas pero inefectivas, es decir, un déficit de hierro funcional. Es importante determinar la diferencia entre estos dos tipos de déficit de hierro, ya que son mecanismos fisiopatológicos diferentes, y en el caso del déficit de hierro funcional, aumenta el estrés oxidativo y el riesgo de infección. Además, si no se diagnostica, suele aumentarse la dosis de agentes estimulantes de la eritropoyesis, sin adecuados objetivos terapéuticos, que aumentan la incidencia de reacciones adversas como hipertensión arterial, coágulos en las vías de diálisis, entre otras. A este fenómeno se le denomina hiporreactividad o resistencia a los estimulantes de eritropoyesis, definida como dos niveles consecutivos de hemoglobina < 10 g/dL mientras recibía eritropoyetina > 7700 unidades por dosis, que puede ocurrir en un 10-20 % de los pacientes (79,83).
Es necesario dividir a los pacientes con ERC en quienes son sometidos o no a diálisis. Los pacientes sin diálisis candidatos a tratamiento con suplemento de hierro son aquellos con transferrina < 20 % o ferritina < 100 ng/dL (recuérdese la definición de déficit de hierro funcional) o mayores a esto si presenta hemoglobina < 13 en hombres o mujeres posmenopáusicas o < 12 en mujeres en edad fértil (83,87). Varios estudios han señalado que el citrato ferroso estabiliza los parámetros mencionados de manera más eficaz (87,88,89). Se podrán utilizar agentes intravenosos cuando hay un déficit de hierro severo (transferrina < 12 %), riesgo de sangrado elevado (pacientes con comorbilidades gastrointestinales) y antecedente de no mejoría con el uso de hierro vía oral.
En este grupo de pacientes, el más utilizado es el gluconato férrico, en dosis de 250 mg, semanal, de 3 a 4 dosis. Otras opciones son el ferumoxutol, hierro sacarosa y carboximaltosa de hierro que muestran igual eficacia, pero con diferencia en costos. No se recomienda hierro dextrano, por la mayor incidencia de reacciones anafilácticas. El tratamiento oral, en comparación con el tratamiento intravenoso, es un tema de debate en este grupo de pacientes; algunos estudios muestran las ventajas de la terapia intravenosa respecto a la mejoría en los índices de homeostasia del hierro, además de disminuir las dosis de estimulantes de la eritropoyesis. Por lo tanto, hay evidencia de que esta es la vía de administración óptima (87,88,89,90,91,92); las guías recomiendan en este grupo de pacientes el uso de hierro oral, por temas prácticos, en aquellos que no usan agentes estimulantes de la eritropoyesis, o la usan en bajas dosis y ofrecen terapia intravenosa en aquellos que no toleran la vía oral o que no muestren mejoría en los primeros tres meses de tratamiento con hierro oral.
Conclusiones
Durante muchos años se ha enfocado la atención en la hemoglobina como el parámetro más importante en el diagnóstico de la anemia; no obstante, como podemos observar en el presente artículo, este hallazgo es tardío y existe un gran número de cambios que preceden la disminución de esta proteína en la sangre. En el caso de la anemia por déficit de hierro, son múltiples las ayudas diagnósticas que muestran las alteraciones en el metabolismo del hierro y que representan los distintos estadios de la disminución de los depósitos de hierro, que en su gran mayoría se presentan antes de la reducción en los valores de hemoglobina. La ferropenia sin anemia es el término que se acuñó a la alteración de estos parámetros sin aún tener descenso de hemoglobina.
Inicialmente, no se buscaba ni se conocía la importancia de este diagnóstico; sin embargo, con el avance en los métodos diagnósticos podemos darnos cuenta de que la presencia de este hallazgo se relaciona con cambios funcionales cardiacos, deterioro de la calidad de vida por disnea, alteraciones cognitivas, entre otras. En falla cardiaca y en insuficiencia renal se conoce mucho sobre el impacto de la ferropenia; pero aún existen brechas importantes en la fisiopatología, diagnóstico temprano y las implicaciones de su reposición en las distintas enfermedades.














