Introducción
El síndrome de Stevens-Johnson (SSJ) y la necrólisis epidérmica tóxica (NET) son reacciones adversas mucocutáneas severas poco frecuentes, con una incidencia mundial de uno a dos casos por millón, y una incidencia un poco mayor en pacientes mayores de 64 años de edad, siendo de hasta de 9,4 casos por millón (1,2). Generan necrosis extensa, desprendimiento de la epidermis y, usualmente, son inducidas por medicamentos (3). El SSJ y la NET hacen parte de un espectro continuo de la misma patología y se sobreponen; se diferencian por la severidad estimada según el porcentaje de superficie corporal afectada: menos del 10 % y más del 30 %, respectivamente (1,4). Estas reacciones tienen como etiología el uso de algunos medicamentos, tóxicos, agentes infecciosos o varios, sobre una susceptibilidad genética de base. Sin embargo, los factores predisponentes no se han identificado totalmente (5).
Comúnmente, los medicamentos asociados con estas reacciones son las sulfonamidas: fenobarbital, carbamacepina, lamotrigina, alopurinol, entre otras (6,7). De estos, la carbamacepina se asocia como desencadenante del 18 % de los casos, según una revisión sistemática realizada en la India (8). Los síntomas pueden aparecer de una a tres semanas tras el inicio del medicamento causal (9). Sin embargo, en este caso, la reacción adversa se presentó después de que se le aumentara la dosis de carbamacepina a una paciente que venía recibiendo dicho medicamento, sin complicaciones. Si bien esta asociación ha sido poco descrita en la literatura —y este es el primer caso descrito en Colombia—, es importante que el personal de salud conozca dicha asociación, ya que el retiro oportuno del agente causal tiene implicaciones pronósticas para el paciente.
Presentación del caso
El caso corresponde a una mujer de 79 años de edad con antecedente de demencia frontotemporal variante comportamental, con dependencia total para sus actividades básicas de la vida diaria e insomnio persistente, quien como comorbilidades presentaba hipertensión arterial, insuficiencia cardiaca, hipotiroidismo y miastenia grave en remisión. Se encontraba en manejo con enalapril, carvedilol, ácido acetil salicílico, levotiroxina, quetiapina y carbamacepina (400 mg/día) desde hacía dos meses. Esta última, por indicación de psiquiatría. Como otros antecedentes positivos, la paciente había sido llevada a varicosafenectomía y timectomía, y su última hospitalización había sido siete meses atrás, por agudización de sus síntomas comportamentales, y no presentaba alergias ni antecedentes tóxicos.
Ocho días previos a la consulta al servicio de urgencias, se le había incrementado la dosis de carbamacepina, por respuesta parcial, sin cambios adicionales en los demás medicamentos. Al ingreso a urgencias se refirió la aparición súbita de un sarpullido maculopapular generalizado, con afectación inicial en la cara y posterior extensión a las extremidades y el tronco. Tras la valoración médica y la realización de exámenes paraclínicos, sin alteraciones, se le dio egreso a la mujer con diagnóstico de reacción alérgica inespecífica versus eruptiva viral no complicada, y se le formuló un antihistamínico. Tres días después, reingresó por aumento de las lesiones cutáneas, fiebre y alodinia.
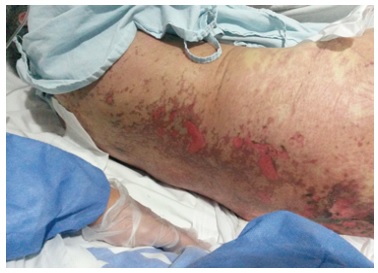
En el examen físico del reingreso se encontraba en regular estado general, deshidratada y álgica. En la inspección facial se evidenciaba secreción ocular amarillenta, inyección conjuntival, edema bipalpebral bilateral, labios fisurados, mucosa oral con varias ampollas y erosiones. El tronco y las extremidades tenían incontables placas eritematosas edematosas en diana, algunas con ampollas, varias con pérdida de la epidermis y signo de Nikolski positivo (figura 1), y en los genitales tenía algunas ampollas. En el examen neurológico estuvo alerta, desorientada, con inquietud motora. La escala SCORTEN se calculó en 2.
Por un aumento reciente de dosis, características clínicas y afectación del 10 % de la superficie corporal, se diagnosticó a la mujer con un SSJ secundario a carbamacepina. Como medidas terapéuticas se le retiró la carbamacepina y se hospitalizó, a cargo del servicio de geriatría. Se iniciaron medidas generales de soporte y aislamiento por contacto. Fue valorada por el servicio de dermatología, que indicó un corticoide sistémico de 1 mg/kg al día, fórmula magistral vía oral y betametasona tópica. El servicio de oftalmología diagnosticó blefaroconjuntivitis bacteriana bilateral, e indicó antibiótico y corticoide tópico. Durante la hospitalización, presentó un pico febril con leucopenia, y se le tomaron hemocultivos. También fue valorada por el servicio de infectología y se le indicó el inicio de cubrimiento antimicrobiano con oxacilina. Por aislamiento de Staphylococcus aureus y Staphylococcus hominis meticilino resistentes, se escalonó el antibiótico a vancomicina.
La mujer tuvo una evolución rápida de las lesiones cutáneas con pérdida epidérmica, que superaron el 30 % de la superficie corporal, por lo que se consideró la progresión a NET. Durante la hospitalización, recibió atención multidisciplinaria, manejo de lesiones en piel bajo protocolo de paciente quemado, aislamiento de contacto y vendajes vaselinados en áreas expuestas. Luego de esto, presentó una evolución clínica favorable, por lo que se le dio egreso en buenas condiciones, con seguimiento por consulta externa, sin evidencia de secuelas.
Discusión
Aproximadamente, del 5 % al 8 % de los pacientes hospitalizados experimentan una reacción adversa a los medicamentos, siendo el SSJ/NET, el extanema pustuloso agudo generalizado y el síndrome de erupción medicamentosa con eosinofilia y síntomas sistémicos reacciones cutáneas severas poco frecuentes asociadas con medicamentos de uso frecuente (9,10). Con regularidad, la carbamacepina se ha documentado como un medicamento asociado con el SSJ en adultos, al haberse encontrado una incidencia de 14 por cada 100.000 habitantes en Estados Unidos (11).
La mortalidad del SSJ/NET es aproximadamente de un 23 % a las 6 semanas y de un 34 % al año. Según datos de una cohorte europea, la severidad de la reacción es el factor de riesgo más importante de mortalidad en los primeros 90 días (12). La edad y las comorbilidades se han considerado un factor de riesgo independiente relacionado con la mortalidad. Las complicaciones, como falla multiorgánica y septicemia, con frecuencia conducen a la muerte (2). Mahar et al. (13), en un estudio retrospectivo con pacientes mayores de 70 años, encontraron una mortalidad del 57 %.
Generalmente, la presencia del SSJ/NET es secundaria al inicio del medicamento (9). En el caso presentado, la reacción se produce por un aumento en la dosis de carbamacepina. En un caso similar, tres semanas después del aumento de la dosis del medicamento, en un niño de 5 años de edad, con antecedente de síndrome convulsivo en terapia con carbamacepina, aparecieron síntomas característicos SSJ/NET (13). Por lo tanto, no se debe descartar como agente etiológico un medicamento previamente tolerado por el paciente.
En cuanto a la fisiopatología, si bien no se ha dilucidado el mecanismo fisiopatológico del SSJ, se plantea una reacción de hipersensibilidad mediada por la expansión clonal de los linfocitos T CD8, a través del complejo mayor de histocompatibilidad tipo I. Los linfocitos ejercen una toxicidad específica contra los linfocitos B autólogos y contra los queratinocitos, con posterior apoptosis de los últimos (3). Tras la apoptosis, se dan manifestaciones oculares del SSJ/NET, como inflamación y pérdida del epitelio de la superficie ocular. Hallazgos frecuentes son hiperemia conjuntival, inflamación de la superficie ocular, formación de seudomembranas, úlceras o perforaciones corneales. Las secuelas son fotosensibilidad crónica y ojo seco (14,15).
El diagnóstico de toxicodermias es eminentemente clínico, y ante la presencia de ampollas con afectación de las mucosas, los diagnósticos diferenciales son SSJ o NET, según el grado de extensión. En el caso de nuestra paciente, la afectación de más del 30 % de su superficie corporal configuró el diagnóstico de NET (10). Según la literatura, las manifestaciones clínicas del SSJ/NET están dadas por síntomas inespecíficos, fiebre, malestar general, aparición de lesiones dermatológicas, sarpullido maculopapular o lesiones eritematosas localizadas preferiblemente en el tronco (9).
Se describen lesiones típicas en diana, con centro eritematoso y lesiones atípicas, donde se presenta eritema sin edema y una ampolla central; las segundas confluyen generando lesiones secundarias (erosiones), con apariencia de quemadura de segundo grado. En las mucosas hay erosiones, especialmente en la boca, los labios, las conjuntivas y los genitales. Todo esto genera pérdida de líquidos y alto riesgo de infecciones bacterianas (8,16,17).
Deben tenerse en cuenta los principales cuadros cutáneos severos como diagnóstico diferencial del SSJ/NET. Entre estos, el eritema multiforme mayor, que al igual que el SSJ se caracteriza por lesiones eritematosas; sin embargo, en el primero las lesiones se localizan con mayor frecuencia en la cavidad oral, además de su etiología infecciosa ampliamente descrita. Otros diagnósticos diferenciales son: síndrome de hipersensibilidad y síndrome de reacción por drogas con eosinofilia y síntomas sistémicos (18,19).
La principal estrategia terapéutica consiste en la identificación y retiro temprano del medicamento causal, ya que un retraso excesivo puede condicionar un aumento importante en la mortalidad, hasta del 34 % al año (12). En el presente caso, gracias a un alto índice de sospecha, se consideró como desencadenante el incremento de la dosis de carbamacepina, previamente tolerada por la paciente, pero a una menor dosis.
En un estudio retrospectivo de Chantaphakul et al. (20), después del seguimiento a un grupo de pacientes con SSJ y NET hospitalizados, los autores encontraron que entre los grupos, sobrevivientes y no sobrevivientes, los factores edad, mayor de 70 años y afectación mayor al 20 % de la superficie corporal, tuvieron mayor impacto sobre la mortalidad. Además, observaron que aumentó la supervivencia el tratamiento, durante tres a diez días, con corticosteroide sistémico intravenoso.
Medidas adicionales al tratamiento son: suspensión del medicamento causante de SSJ/NET, manejo del paciente en una institución especializada, si es necesario en una unidad de quemados o cuidados intensivos. Por riesgo elevado de infecciones, se debe aislar el paciente para disminuir la posibilidad de contraer alguna infección (8,16,17). Otras medidas incluyen el uso de dispositivos que promuevan el cuidado de lesiones en piel como colchones neumáticos y sabanas antiadherentes. También, como en el caso reportado, control de líquidos, soporte nutricional y manejo del dolor (12, 20). Igualmente, es de resaltar la importancia del trabajo multidisciplinario, en el contexto de un paciente anciano, donde a partir de una situación basal se identifican factores que se deben intervenir y se plantean estrategias que disminuyan el tiempo de estancia y el menor deterioro funcional hospitalario (21).
Como se mencionó, Chantaphakul et al. (20) observaron un aumento en la supervivencia usando corticosteroides sistémicos. Por otro lado, un metanálisis reciente sugiere que el uso de inmunoglobulinas intravenosas no reduce de manera significativa la mortalidad, en comparación con pacientes en manejo de soporte (22). A estos dos tratamientos se les pueden sumar el uso de ciclosporina, ciclofosfamida e inhibidores de necrosis tumoral. Pero aún no hay evidencia contundente que respalde alguna de estas opciones (3, 20).
Conclusión
Un diagnóstico temprano y adecuado es vital. Identificar el agente etiológico, retirar el medicamento causal y prevenir complicaciones potenciales del SSJ/NET, disminuiría el deterioro del paciente y los costos de hospitalización. Es de resaltar la evolución favorable de la paciente del caso, pese a su edad, comorbilidades y extensión de la afectación cutánea, características que le adjudicaban un mal pronóstico, sin comprometer su funcionalidad basal meses después del alta. Adicionalmente, la detección temprana impacta de forma positiva en la calidad de vida y pronóstico general de pacientes con dicha patología. Por lo tanto, no se debe descartar como agente etiológico un medicamento tolerado antes por el paciente, ya que modificaciones en sus dosis pueden desencadenar reacciones adversas cutáneas severas, como la descrita aquí.