INTRODUÇÃO
Nos últimos anos a produção de melões no Brasil tem crescido expressivamente, apresentando um aumento de 250.000 Mg no período de 2004 a 2014, em uma área de aproximadamente 22.000 ha, com uma média de produtividade anual de 25,1 Mg ha-1. O Nordeste caracteriza-se como a principal região produtora e é responsável por cerca de 95% de toda a produção nacional (IBGE, 2016), mesmo a cultura tendo boa aptidão para ser produzida em praticamente todo o território nacional.
Popularmente conhecidos como melão japonês ou Cantaloupe, os melões nobres fazem parte do grupo de melões rendilhados (Cucumis melo var. reticulatus Naud.), do grupo cantalupensis. Esses melões têm despertado grande interesse por apresentar qualidade superior aos demais melões tradicionais quanto ao aroma, polpa com coloração mais atraente e maior teor de sólidos solúveis (Medeiros et al., 2007).
O alto valor de mercado dos frutos de meloeiro nobre permite que novas tecnologias sejam aplicadas a sua produção, visando à melhoria das qualidades fitotécnicas e tecnológicas de pós-colheita. Uma tecnologia a ser explorada é a utilização de bioestimulantes comerciais. Estes produtos vêm sendo utilizados para diferentes culturas, obtendo-se resultados variados dependendo da espécie em estudo (Izidório et al., 2015; Tavares et al., 2015; Vendruscolo et al., 2015).
O termo bioestimulante refere-se à mistura de dois ou mais reguladores vegetais ou de biorreguladores com outros produtos (Vieira e Castro, 2001). Estes compostos são aplicados de forma exógena nas plantas visando alterações nos processos vitais e estruturais, melhorias da produtividade e da qualidade do produto a ser comercializado e também dos manejos culturais (Chiavegato et al., 2007).
Apesar da quantidade considerável de estudos acerca da aplicação de bioestimulantes, informações sobre a utilização destes produtos diretamente sobre os frutos e, consequentemente, sobre o seu efeito no desenvolvimento destes, são escassos. Assim, a geração de novas informações de caráter técnico-científicas possui considerável significância.
Portanto, objetivou-se avaliar a ação de bioestimulante, aplicado diretamente sobre frutos de meloeiro rendilhado, sobre diferentes características físico-químicas dos mesmos.
MATERIAL E MÉTODOS
O estudo foi realizado em Goiânia, Goiás. O município situa-se na região central do Estado, tendo a área experimental a localização de 16°35’55,2” S e 49°16’39,1” W e altitude de 750 m. O cultivo foi feito em ambiente protegido previamente construído na Escola de Agronomia da Universidade Federal de Goiás. Foi utilizada uma estufa, modelo arco, possuindo dimensão de 21×7 m e altura de 4 m, coberta com lona transparente e possuindo em suas laterais tela antiafídica branca. Durante o período de condução do estudo a umidade relativa do ar média foi de 66,7% e a temperatura média de 24,9°C.
O solo presente na área experimental é classificado como Latossolo Vermelho distroférrico (Santos et al., 2013) e apresentou as seguintes características químicas na camada de 0-0,20 m: 0,7% de M.O.; pH 4,6 (CaCl2); 3,5 mg dm-3 P (Mehlich); 131,0 mg dm-3 K; 2,0 cmolc dm-3 Ca; 0,81 cmolc dm-3 Mg; 2,5 cmolc dm-3 H+Al; 0,0 cmolc dm-3 Al; 5,6 cmolc dm-3 CTC; m% igual a 0,0; V% igual a 55,7 (Donagemma et al., 2011).
Foi utilizado o delineamento em blocos ao acaso, com cinco tratamentos, formados pela variação da concentração de bioestimulante (0, 5, 10, 15 e 20 mL L-1), em cinco repetições. Cada parcela foi constituída por uma planta, com um fruto. O bioestimulante foi aplicado, com o auxílio de um pincel, diretamente sobre os frutos com tamanho igual ou inferior a um centímetro de diâmetro e reaplicado sete dias após.
Foi utilizado o bioestimulante comercial Stimulate® que possui em sua composição três reguladores vegetais nas seguintes proporções: 0,09 g L-1 de cinetina (citocinina), 0,05 g L-1 de ácido giberélico (giberelina), 0,05 g L-1 de ácido indolbutiríco (auxina) e 99,98% de ingredientes inertes (Agrofit, 2017).
O preparo da área de plantio constituiu da correção do pH para 6,0 com a aplicação de calcário (30% CaO, 18% MgO e PRNT de 100%), conforme recomendação de Sobrinho et al. (2008). Posteriormente à realização da calagem foi feito o revolvimento do solo com enxada rotativa acoplada a um micro trator de rabiça. O manejo de plantas espontâneas foi feito por meio de capinas manuais, conforme a necessidade.
As mudas de meloeiro nobre foram obtidas por meio da semeadura em bandejas preenchidas com substrato composto por três partes de substrato comercial turfoso para uma de esterco bovino curtido, onde permaneceram até atingirem altura aproximada de 0,15 m, sendo em seguida transplantadas para os canteiros, espaçadas 0,35 m entre si e tutoradas na forma de espaldeira. As linhas de plantio, na porção central do canteiro, foram espaçadas em 0,80 m entre si.
A irrigação foi realizada por meio de fitas gotejadoras, com gotejadores espaçados em 0,20 m entre si, que foram instaladas nas linhas de plantio e acionadas conforme a necessidade das plantas, observando-se as condições ambientais e o estágio de desenvolvimento (Sobrinho et al., 2008).
A adubação de plantio foi realizada no momento da confecção dos canteiros, utilizando-se três litros de esterco e 80 kg ha-1 de fósforo, tendo como fonte o fertilizante termofosfato “Yoorin Master” (Yoorin, Poços de Caldas-MG, Brasil). As adubações de cobertura foram feitas com base nas recomendações de Sobrinho et al. (2008), aplicando-se 10 kg ha-1 de nitrogênio (ureia) e 5 kg ha-1 de potássio (cloreto de potássio) semanalmente, via água de irrigação.
Na etapa final, no momento da colheita, foi avaliada, em laboratório, a massa dos frutos (g) por meio de pesagem em balança digital W15 (Welmy, Sta. Bárbara d’Oeste-SP, Brasil) com precisão de 5 g, as espessuras do epicarpo (mm), do mesocarpo (mm), do halo verde do mesocarpo (mm) e o diâmetro da cavidade interna do fruto, obtidos com paquímetro digital (Metrotools, São Paulo, SP, Brasil) e o teor de sólidos solúveis (°Brix) por meio da leitura em refratômetro manual RTA-50 (Instrutherm, São Paulo-SP, Brasil). Também foram mensuradas as circunferências longitudinal e transversal, para obtenção da razão entre as medidas.
Os dados experimentais foram submetidos à análise de variância e as médias do fator quantitativo (concentrações de bioestimulante) foram avaliadas pela análise de regressão a 5% de probabilidade.
RESULTADOS E DISCUSSÃO
Observou-se que a aplicação de doses crescentes de bioestimulante não afetou as variáveis de massa de frutos, razão entre circunferência longitudinal e transversal, as espessuras de epicarpo, mesocarpo e halo verde do mesocarpo e diâmetro da cavidade interna do fruto. No entanto, estimulou o aumento dos teores de sólidos solúveis (Tab. 1).
Tabela 1 Resumo da análise de variância e quadrados médios das variáveis de massa de frutos, razão entre circunferência longitudinal e transversal (CL/CT), espessuras de epicarpo, mesocarpo e halo verde do mesocarpo, diâmetro da cavidade interna do fruto e sólidos solúveis (SS) de frutos de melão Cantaloupe submetidos à aplicação de diferentes doses de bioestimulante.

FV: fator de variação; GL: graus de liberdade; CV: coeficiente de variação; ns e * = Não significativo e significativo a 5% de probabilidade pelo teste de regressão, respectivamente.
Para todos os tratamentos, os frutos obtidos apresentaram alta qualidade física. A média da massa por fruto obtida foi de 1.251,44 g, também se verificou que os frutos apresentavam formato esférico, adequado grau de maturidade e pequena cavidade interna, características favoráveis à comercialização, ao transporte e ao consumo in natura (Medeiros et al., 2015). Porém, apenas frutos tratados com concentrações de 15 e 20 mL L-1 de bioestimulante apresentaram teores de sólidos solúveis acima de 10°Brix, teor exigido para a comercialização deste tipo de melão (Sales Junior et al., 2004).
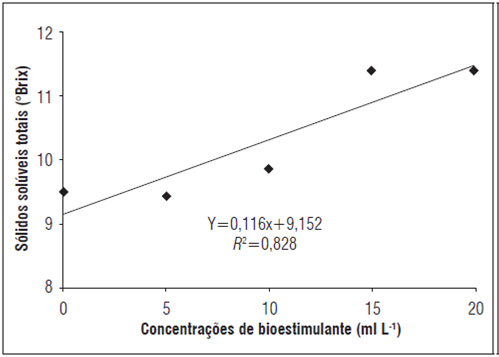
Obteve-se aumento dos teores de sólidos solúveis com a utilização de concentrações crescentes de bioestimulante, até 20 mL L-1, culminando em um teor máximo de aproximadamente 11,5°Brix (Fig. 1). Corroborando com os resultados obtidos, a aplicação combinada de ácido giberélico (1.000 mg L-1) e ácido naftaleno acético (450 mg L-1), direcionada aos frutos partenocárpicos de atemóia, propiciaram aumento do teor de sólidos solúveis (Pereira et al., 2014).
O resultado está relacionado com o aumento da atividade de divisão e alongamento celular, propiciada pela ação dos hormônios que compõem o bioestimulante (Taiz et al., 2017). Desta forma, eleva-se a capacidade dos frutos de atuarem como fortes drenos de compostos fotoassimilados, aumentando a fixação do fruto à planta (Talón et al., 1998; Prado et al., 2007) e, possivelmente, ocasionando um maior acúmulo de açúcares nos frutos fixados (Moreira et al., 2014).
Em estudo acerca da aplicação de doses crescentes do bioestimulante sobre cachos de uva ‘Niágara Rosada’ observou-se a diminuição linear do teor de sólidos solúveis dos frutos até a concentração máxima de 20 mg L-1 (Tecchio et al., 2006), resultado contrário ao obtido no presente estudo. Enquanto que, a aplicação do bioestimulante em tomates ‘Giuliana’ não surtiram efeitos sobre as características agronômicas dos frutos, em comparação ao tratamento controle (Ramos, 2013), demonstrando que a ação dos fitormônios pode depender da espécie em que estes são utilizados.
Destaca-se o ineditismo dos resultados obtidos no presente estudo. Diversos estudos têm abordado a utilização de bioestimulantes em culturas de interesse agronômico. No entanto, para cucurbitáceas esses trabalhos abordam a utilização destes produtos, a base de fitormônios, principalmente na fase vegetativa (Junglaus, 2007) ou mesmo sobre a forma de tratamento de sementes (Silva et al., 2014), não havendo estudos acerca da aplicação direta sobre frutos dessa família.
Assim, demonstra-se que a aplicação do bioestimulante diretamente sobre os frutos consta como uma técnica a ser explorada na produção de melões, podendo ser submetida a novos estudos visando sua utilização em outras espécies.