Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cirugía
Print version ISSN 2011-7582On-line version ISSN 2619-6107
rev. colomb. cir. vol.21 no.4 Bogotá Oct./Dec. 2006
Ante todo es necesario reconocer el valioso aporte de los autores de este artículo. Adelantar este tipo de estudios en esa unidad en particular permite a los cirujanos que participamos de las discusiones aprovechar el conocimiento y la experiencia generada en esta investigación. Asimismo, expreso mi agradecimiento a la Sociedad Colombiana de Cirugía y a la revista de la sociedad por la oportunidad de comentar tan interesante trabajo.
Para ordenar la discusión y profundizar en los temas específicos que influyen en el resultado final del curso clínico de los pacientes con pancreatitis aguda severa (PAS) abordamos la discusión comparando los resultados de este estudio a la luz de los hallazgos reportados en la literatura mundial.
Mortalidad
La mayoría de pacientes con pancreatitis aguda PA (80%) presenta un curso clínico autolimitado, requiriendo únicamente hospitalización corta y terapia médica exclusiva basada en reposo de la vía oral, hidratación endovenosa y analgésicos tipo opioides; estos pacientes tienen riesgo muy bajo de morir (<1%). El otro 20% corresponde a la categoría de severos con enfermedad rápidamente progresiva y en algunos casos fulminante; la pancreatitis necrotizante representa la forma más severa de la PA, llevando al paciente a falla orgánica múltiple (FOM) con signos de sepsis o sin ellos. Además, estos pacientes tienen estancias hospitalarias prolongadas de más de 30 días y mortalidad de hasta 50% (1).
En las últimas tres décadas se ha reportado disminución en la mortalidad de la pancreatitis necrotizante. Los factores relacionados con la mejoría de los resultados son: mayor comprensión de la historia natural de la enfermedad, refinamiento de las imágenes que ha permitido la identificación temprana y en tiempo real de las complicaciones pancreáticas, los avances en el cuidado crítico y la restricción de cirugía sólo para pacientes seleccionados. Una clave especial de este avance ha sido el entendimiento del papel primordial de la extensión de la necrosis del páncreas y la distinción entre necrosis estéril e infectada, su impacto en la terapia (antibiótico-profiláctico, necrosectomía, drenaje percutáneo) y por consiguiente en el resultado final (2).
La mortalidad en PAS se presenta en dos fases reconocidas: la primera corresponde a las dos primeras semanas desde el inicio de los síntomas; la enfermedad se caracteriza por un síndrome de respuesta inflamatoria sistémica (SRIS). Durante esta fase los pacientes muestran signos de hipovolemia, circulación hiperdinámica, pérdida del espacio intravascular e incremento en la permeabilidad capilar. Es importante entender que en esta fase se puede presentar SRIS en ausencia de necrosis significativa y de infección asociada con la necrosis. Durante esta fase la mortalidad se explica por insuficiencia respiratoria, cardiovascular o renal asociada con SRIS (3, 4).
La segunda fase de la enfermedad por lo general se presenta después de los primeros 15 días y la fisiopatología es dominada por complicaciones infecciosas; se ha reportado infección en 40 a 70% de los pacientes con pancreatitis necrotizante. Con esta fase la mortalidad obedece principalmente a falla de los órganos asociada con sepsis; durante este período se presenta la mayoría de las muertes (75%) (5, 6).
La mortalidad global encontrada en este estudio fue de 21,5% y la registrada en los pacientes con pancreatitis necrotizante infectados de 28,9%. Un promedio considerado aceptable dentro del universo reportado para este tipo de enfermedad, que oscila entre 20 y 50% (7, 8). No se menciona el momento de ocurrencia de las muertes con respecto al inicio de los síntomas, tampoco se practicaron autopsias para corroborar la sospecha clínica. Datos ambos necesarios para comprobar con certeza el diagnóstico final.
Las cifras de mortalidad en la PAS se deben evaluar en conjunto y a la luz de la severidad promedio de la población en estudio. Para esto, se emplean las diferentes escalas o criterios de severidad disponible como son los criterios de Ranson o la escala APACHE II, universalmente aceptados para valorar la severidad individual del paciente con PA. Sin embargo, al sacar el promedio del valor de la muestra de pacientes con PAS sirve como parámetro objetivo de comparación en las diferentes series publicadas.
Por lo tanto, no es posible analizar un valor aislado de mortalidad si no se tiene en cuenta la severidad de la muestra examinada. Para este estudio la población de pacientes con pancreatitis severa tuvo un APACHE promedio de 15,5 y la mortalidad global fue de 21,5%. Si la comparamos con otros estudios internacionales teniendo en cuenta únicamente la cifra de mortalidad, a pesar de ser un buen resultado, podría parecer muy alta. Por ejemplo, al equiparar esta serie con un estudio similar de Malangoni y cols., de 60 pacientes con pancreatitis severa definidos por una escala de Ranson >3 y/o APACHE > 8 o por la presencia de necrosis en la TAC dinámica, la mortalidad global fue de sólo 15%. Casi la mitad de la obtenida en este estudio con similar número de pacientes y edades (50 años); pero el APACHE promedio de la población de pacientes fue de 11, mientras que en el estudio nacional fue de 15,5 (9).
Esto obedece a que independientemente del manejo terapéutico que se adelante existen diferentes variables que influyen en el resultado del grupo de pacientes con PAS. Es decir, no todos los pacientes severos hacen necrosis y si la presentan no es lo mismo una necrosis menor al 30% que necrosis de >50%, necrosis sobreinfectada, infección por hongos, posibilidad de desarrollar falla de uno o de múltiples órganos, obesidad, las edades promedio de la muestra, la presencia de enfermedades comórbidas o la etiología de la pancreatitis, todas son variables poderosas que determinan la severidad del cuadro clínico y a la vez aumentan el riesgo de morir.
Factores pronósticos
El valor de identificar factores pronósticos reside en la posibilidad de estratificar rápidamente el riesgo al momento de la admisión y dirigir un monitoreo en un ambiente más amplio que permita identificar el desarrollo de complicaciones locales y sistémicas y FOM; simultáneamente, ofrecer una intervención dinámica hacia aquellos individuos que pueden beneficiarse. Es importante identificar apropiadamente los pacientes que sean candidatos de manejo en la UCI y evitar admisiones innecesarias para un uso racional de las camas disponibles y limitar el riesgo de infecciones nosocomiales y complicaciones iatrogénicas. Estas medidas especiales incluirían traslado a la UCI para monitorizar más estrechamente la reanimación que debe ser agresiva, soporte hemodinámico, cardiovascular, respiratorio, metabólico y nutricional. Detectar y tratar el desarrollo de complicaciones locales y sistémicas, soportar el o los órganos que muestren daño transitorio, detectar y tratar precozmente las infecciones con antibióticos apropiados, indicar una CPRE en pancreatitis biliar con obstrucción ampular, o una TAC dinámica para diagnosticar necrosis y cuantificar la extensión de la misma. Realizar aspirado-Gram/cultivo de tejido pancreático y decidir el desbridamiento pancreático cuando esté indicado en el momento más adecuado.
Debido al diseño retrospectivo del estudio en el que la recolección de los datos se obtiene a través de la revisión de historias clínicas, la secuencia cronológica de la medición de variables y la realización de procedimientos diagnósticos y terapéuticos, con respecto al inicio de los síntomas, no es anotada de forma precisa y esto es cada vez más importante para predecir el desenlace final de la enfermedad. En el estudio en mención se señala que la presencia de shock y la escala de APACHE II son factores asociados con mortalidad en PAS, pero no mencionan los tiempos o el momento en el que estos factores son predictores de mortalidad. Por ejemplo, ¿es el APACHE al ingreso o después de 48 horas de reanimación inicial o tal vez es el incremento significativo después del día 14 cuando es más probable la sobreinfección bacteriana? Si no se analiza en un contexto temporal el factor pierde fuerza. Todas las variables a estudiar como son en este caso factores pronósticos de mortalidad en pancreatitis aguda severa PAS, el momento de la realización de los exámenes diagnósticos y los procedimientos terapéuticos con respecto al inicio de los síntomas no son señalados con exactitud.
Así, al analizar la presencia y extensión de la necrosis y su impacto en la mortalidad hay que tener en cuenta primero el momento más apropiado para realizarla. Según varios reportes publicados la extensión máxima de la necrosis pancreática no se hace completamente evidente hasta cerca de 96 horas después del inicio de los síntomas. Este es el argumento más poderoso para realizar la TAC dinámica sólo en pacientes seleccionados al cuarto o quinto día de la admisión, para observar completamente el daño del páncreas (10).
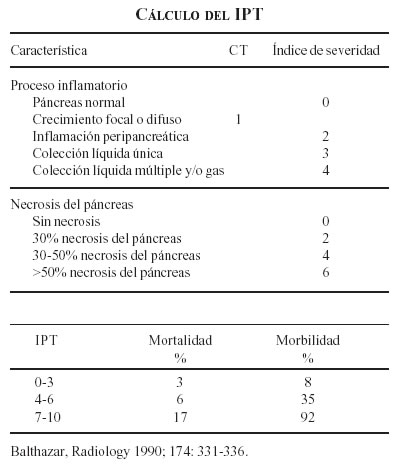
En otro estudio diseñado especialmente para evaluar el valor pronóstico de la TAC a las 48 horas de iniciados los síntomas y aplicando el índice pronóstico tomográfico (IPT) introducido por Balthazar y cols. (11), 79 pacientes fueron incluidos en este estudio prospectivo y divididos en tres grupos según el valor obtenido en el realizado a las 48 horas. IPT de 0-3 (n:52; 65%), 4-6 (n: 21; 27%) e IPT de 7 -10 (n:6; 8%). A todos los pacientes se les efectuó TAC dinámica a los siete días de la primera para evaluar la progresión de la necrosis y en ninguno hubo cambio de grupo o cambios en la interpretación al comparar con la TAC inicial. Los resultados demostraron que la TAC a las 48 horas fue predictor de complicaciones. En el grupo con IPT de 0-3, 42% presentaron al menos una complicación; el grupo con IPT de 4-6, 81% mostraron complicaciones y el grupo con IPT de 7-10 el 100% también revelaron alteraciones. Infección de la necrosis se presentó en 12, 33 y 50% respectivamente entre los grupos y la mortalidad fue de 2, 19 y 33% respectivamente entre los grupos. La muerte registrada en el primer grupo correspondió a un paciente de 86 años con antecedente de cardiopatía que murió en la UCI 24 horas después de la admisión por un IAM masivo (12).
Es razonable pensar que si la tomografía se hace antes de 48 horas del inicio de los síntomas o si no se hace de manera dinámica se subdiagnosticarían muchos pacientes con necrosis o no se podría valorar con certeza la extensión de la misma. En este estudio no se especifica claramente la técnica de la realización de la TAC, sólo se menciona en la metodología que se hace con protocolo para páncreas, pero no se indica claramente en qué consiste, lo cual es vital para corroborar los resultados, al menos los referentes a extensión de la necrosis y su relación con la posibilidad de infectarse. El rendimiento de la tomografía dinámica para evaluar la presencia y extensión de la lesión en el parénquima pancreático y el tejido peripancreático depende de varios factores, pero el más importante es la calidad del estudio (26). La administración endovenosa de medio de contraste es esencial, en particular en pacientes con pancreatitis severa para permitir una adecuada visualización de todo el páncreas y hacer la diferenciación de la glándula con respecto a las colecciones heterogéneas de fluido y tejido peripancreático inflamatorio. La TAC helicoidal permite la obtención rápida de imágenes secuenciales de menos de 5 mm. Las imágenes se deben obtener en la fase venosa portal temprana (60-70 seg. después de la inyección del medio: material de contraste yodado 150 ml a un flujo de 3 ml/seg.). El parénquima pancreático inflamado sin medio de contraste marca 40-50 HU y se espera después de la inyección del contraste que aumente a 100-150 HU en toda la glándula y durante toda la administración del medio de contraste. La falta de realce durante la infusión y cifras menores a 30 HU en una porción o en todo el páncreas indica disminución de la perfusión sanguínea (isquemia) y se relaciona con el desarrollo de necrosis (26).
Tampoco se anota el momento de la realización de la TAC con respecto al inicio de síntomas, que es un factor determinante para obtener el mejor rendimiento de la tomografía. Se ha determinado que la necrosis pancreática se desarrolla temprano, dentro de las primeras 24-48 horas, después del inicio de los síntomas. Si la tomografía se hace durante las doce horas iniciales puede mostrar sólo hallazgos equívocos, con disminución heterogénea en la atenuación pancreática (isquemia) pero con textura del parénquima normal. Al presentarse la necrosis las zonas de licuefacción tisular se definen mejor y son más fácilmente reconocidas dos a tres días después del inicio. De esa forma la TAC obtenida tres días después del inicio de los síntomas ofrece el mejor rendimiento diagnóstico de presencia y extensión de la necrosis y discriminación entre el tejido sólo isquémico del necrótico. Cuando se realiza una TAC temprana por duda diagnóstica o para ayudar a confirmar los hallazgos clínicos o descartar otras condiciones que simulan cuadros clínicos de pancreatitis es preferible repetirla con bolo endovenoso 48-72 horas después del inicio del ataque agudo para estadificar la extensión de la necrosis (26).
Antibióticos en pancreatitis aguda
La infección de la necrosis pancreática se desarrolla en 30-70%, según las series de los pacientes con necrosis pancreática documentada por TAC o cirugía. La frecuencia de infección se correlaciona con la extensión y la duración de la necrosis (13).
Aunque la infección se puede presentar durante la primera semana después del inicio de los síntomas, su pico de incidencia máximo es en la tercera semana (14). Como el desarrollo de necrosis infectada significa un incremento significativo en la mortalidad de pacientes con PA, se ha concentrado la atención en la prevención e identificación temprana de pacientes con riesgo de sepsis. En pacientes con necrosis estéril la mortalidad aumenta de 5-25 a 15-28% si ocurre sobreinfección de la necrosis (15). El mecanismo por el cual se contamina con bacterias la necrosis pancreática aún no es del todo claro, pero los datos clínicos y experimentales sugieren que el tracto gastrointestinal es la fuente principal, debido a que la colonización intestinal con bacterias patógenas precede a la infección pancreática (16, 17).
El espectro bacteriano primeramente consiste en bacterias gramnegativas del tubo digestivo. En series recientes, como la serie en evaluación, se ha demostrado un cambio hacia más bacterias grampositivas y en otras series se nota un incremento en la incidencia de infección por Candida (18). Entre los factores de riesgo para el desarrollo de infección por hongos se incluye el uso de un curso prolongado y de múltiples antibióticos. La infección por hongos resulta en un incremento significativo de la mortalidad, tanto en pacientes con infección primaria como secundaria (19).
Estos datos sumados al resultado adverso asociado con el desarrollo de necrosis infectada sustentan el uso racional de antibióticos profilácticos orales y endovenosos con el propósito teórico de disminuir la probabilidad de infección de la necrosis y las tasas de mortalidad. En las últimas dos décadas se ha discutido intensamente el uso de antibióticos sistémicos en pancreatitis, y los conceptos han cambiado con regularidad. Lo único claro es que en PA leve los antibióticos no tienen ninguna utilidad. Llegar a una conclusión definitiva del valor real del antibiótico profiláctico ha sido difícil por varias razones: falta de resultados contundentes, criterios de inclusión variables, metodología diferente entre las series, diferentes regímenes y duración de antibióticos e insuficiente número de pacientes para encontrar hallazgos significativos.
En la década del setenta se llevaron a cabo tres ensayos clínicos controlados con ampicilina en PA que revelaron su ineficacia para evitar la infección de la necrosis pancreática (20- 22). Posteriormente se demostró que la ampicilina no penetra el tejido pancreático ni tampoco actúa contra los gérmenes que infectan más frecuentemente la necrosis pancreática.
En 1993 se publicó un estudio italiano multicéntrico que utilizó imipenem profilácticamente en 41 pacientes. Se encontró una reducción significativa de la sepsis pancreática y no pancreática en comparación con 33 pacientes del grupo control sin antibióticos; sin embargo la incidencia de disfunción de múltiples órganos, el número de pacientes que requirieron necrosectomía y la mortalidad hospitalaria, disminuyeron pero no significativamente (23). En un estudio finlandés se utilizó cefotaxime en 30 pacientes obteniendo una reducción significativa en la mortalidad de 23,3 a 3,3%, mientras que la rata global de complicaciones infecciosas no se redujo significativamente. Estos estudios dejan la impresión de que la profilaxis antibiótica reduce la incidencia de infección de la necrosis pancreática y consecuentemente disminuye la disfunción de órganos y la mortalidad. En contraste, tres estudios clínicos más pequeños fallaron en demostrar el efecto benéfico de la profilaxis antibiótica (24, 25).
En otros dos estudios publicados en los que se comparan diferentes regímenes de antibióticos en pacientes con pancreatitis necrotizante, los resultados fueron limitados porque no eran ciegos y sólo se incluyó un pequeño número de pacientes. Estos estudios fallaron en demostrar que un régimen específico mejora el pronóstico de estos pacientes (26, 27).
Más recientemente un meta-análisis de la colaboración Cochrane evaluó el efecto de los antibióticos profilácticos endovenosos basados en los ensayos clínicos controlados disponibles hasta ese momento, este análisis recomendó el uso de antibióticos en pancreatitis necrotizante; sin embargo, debe anotarse que los datos de los dos estudios más recientes entre los que se incluye el primer estudio doble ciego controlado con placebo no fueron incluidos en este análisis. Estos resultados han hecho que guías internacionales incluyan dentro de los protocolos el uso del antibiótico profiláctico condicionado a la necesidad de más estudios que aborden este tema (28, 29).
Isenmann y cols. recientemente publicaron un estudio multicéntrico en el que incluyeron 114 pacientes randomizados para recibir ciprofloxacina combinada con metronidazol (grupo terapéutico) en comparación con placebo (grupo control). Se incluyeron sólo pacientes con ataques severos definidos por elevación sérica de la proteína C reactiva por encima de 150 mg/dl o por necrosis identificada en la TAC dinámica. Los pacientes fueron reclutados en los primeros tres días de aparición de los síntomas. Los antibióticos se administraban hasta que los pacientes respondieran al manejo médico o hasta que fueran cambiados por la detección de infección u alguna otra complicación infecciosa. Este estudio no mostró diferencia significativa en la incidencia de necrosis pancreática infectada en ninguno de los grupos. La estratificación de los pacientes basados en la presencia de necrosis en la TAC no mostró ventajas en el grupo terapéutico. La mortalidad fue de 11 frente a 7% y la incidencia de infección de la necrosis, de 14 frente a 17%. Sin embargo, teniendo en cuenta que el cambio a antibióticos de amplio espectro fue más frecuente y temprano en el grupo placebo (46 frente a 28%) (30). Esto indica que un subgrupo de estos pacientes aparentemente se beneficia de los antibióticos. Los resultados de este estudio han sido controvertidos. La baja tasa de infección de la necrosis en ambos grupos junto a la alta tasa de cambio a antibióticos de amplio espectro en el grupo placebo han sido puntos de crítica. En opinión de algunos autores, el monitoreo estrecho de los pacientes en búsqueda de signos de respuesta inflamatoria o pancreatitis severa persistente motivó a los autores a cambiar a antibióticos más potentes, lo cual finalmente se tradujo en una baja tasa de infección de la necrosis pancreática. Como el resultado de ambos grupos fue similar, los datos soportan la idea de que el uso de antibióticos a demanda o indicados según la sospecha clínica de sobreinfección, podría ser tan efectivo como el profiláctico en pacientes con PAS (31, 32) y sin los efectos adversos del uso de antibióticos por largos períodos.
Otro argumento que favorece el uso de antibiótico profiláctico o a demanda es el resultado obtenido en series recientes donde se reporta manejo exitoso de la necrosis pancreática infectada sin necrosectomía, tumbando el paradigma de que la infección de la necrosis es indicación absoluta de cirugía.
En un estudio de 88 pacientes con pancreatitis aguda severa, 28 desarrollaron infección de la necrosis demostrada por aspirado guiado en el día 19+/- 6 después de la admisión; ninguno fue intervenido de manera urgente. La terapia no quirúrgica se continuó hasta después de adaptar el régimen antibiótico a las bacterias encontradas. La escala de APACHE II promedio fue de 18,1, Ranson de 5,9 e IPT de 8,0 reflejando la severidad de la muestra. Once (68%) de estos pacientes tuvieron >50% de necrosis pancreática, cuatro (25%) de 30-50% y uno menos de 30% de NP. El régimen antibiótico utilizado fue mezlociclina (3x4 g, IV) en combinación con metronidazol (3x0,5 g, IV) para la mayoría de pacientes. Otros regímenes utilizados en pacientes alérgicos a la mezlociclina fueron ciprofloxacina+metronidazol. Los antibióticos se prolongaron hasta más de ocho semanas. La duración de la hospitalización fue de 54 +/- 10 días, diez pacientes (62%) mostraron falla de órganos. Dos pacientes (12,5%), ambos con APACHE II de 22 y Ranson de 6 con comorbilidades severas cardíacas desarrollaron un curso complicado y ambos fallecieron por taquiarritmias. Los catorce pacientes restantes (87,5%) se recuperaron completamente sin secuelas. Doce pacientes con APACHE inicial de 15,4 e IPT de 7,9 desarrollaron complicaciones locales severas con abscesos o infecciones locales que no respondieron a la terapia antibiótica (n: 10), un paciente con una fístula pancreática y otro con obstrucción intestinal fueron intervenidos quirúrgicamente 36+/-14 días después del diagnóstico de infección de la necrosis, de estos pacientes intervenidos dos (16,6%) fallecieron y los otros diez se recuperaron (33).
El estudio en revisión es confuso con respecto al uso dado a los antibióticos. Mientras que en el protocolo de manejo se afirma que no se utilizaron antibióticos profilácticos, al reportar los resultados se menciona que se empleó antibiótico profiláctico en el 81,3% de los pacientes y durante catorce días, predominantemente carbapenem. Después en la discusión nuevamente se menciona que sólo se utilizaron antibióticos terapéuticos y que a doce (18,5%) pacientes se les administró con intención profiláctica con resultados claramente negativos para una mortalidad en este pequeño subgrupo de 75%. Estos datos no se correlacionan con los resultados internacionales que reportan valores de sobreinfección y de mortalidad más bajos para los pacientes con necrosis infectada y antibiótico profiláctico. Habría que analizar los datos en este subgrupo de pacientes para encontrar una explicación razonable a estos resultados.
Con respecto a los resultados bacteriológicos, teniendo en cuenta que no se menciona la toma de muestra para cultivo y gram durante la necrosectomía pancreática y que hubo pacientes sometidos a cirugía por deterioro clínico persistente sin demostración bacteriológica previa, y que además de los 38 pacientes con necrosis infectada sólo se reporta crecimiento bacteriano en 60%, hace suponer que hubo un número de pacientes considerados infectados que no tenían demostración microbiológica y ser un sesgo que hace que se interpreten pacientes con necrosis estéril que fueron cuantificados como infectados, mejorando los resultados globales de mortalidad en el grupo de pacientes con necrosis infectada.
El uso rutinario de antibióticos profilácticos de amplio espectro en PAS altera el ambiente microbiológico de la infección secundaria de la necrosis pancreática haciendo que la flora bacteriana cambie de coliformes gramnegativos a organismos grampositivos predominantemente, sin cambiar la tasa de resistencia a antibióticos betalactámicos o sobreinfección por hongos. No está completamente demostrado que el uso de antibióticos profilácticos por largos períodos promueva infección por hongos. En un estudio se encontró infecciones por hongos en 37% de los pacientes con pancreatitis aguda severa y necrosis pancreática sobreinfectada (33).
Nutrición y pancreatitis
La supresión de las secreciones exocrinas pancreáticas con el reposo a la vía oral es una estrategia importante para estabilizar la PA, por lo que históricamente se ha preferido la nutrición parenteral (NPT) (Ranson JH. Acute pancreatitis: pathogenesis, outcome and treatment. Clin Gastroenterol. 1984; 13: 843-863). Después de que se demostró que la nutrición enteral (NE) es segura y disminuye las complicaciones infecciosas se empezó a utilizar en estos pacientes. Como se demostró en estudios en animales, el ayuno prolongado produce atrofia de la mucosa, lo cual es preservado por la NE. Desde que se considera que la fuente de la bacteria que infecta la necrosis pancreática es el tubo digestivo, la NE al prevenir la atrofia disminuye la probabilidad de translocación y bacteremia y a su vez reduce las complicaciones infecciosas. En contraste a lo que anteriormente se pensaba, la nutrición con sonda enteral avanzada no estimula las secreciones pancreáticas ni altera los valores séricos de las hormonas digestivas de forma significativa, como sí lo hace al entregar el alimento en el duodeno. Kalfarentzos y cols. son los autores del único ensayo clínico en el que sólo pacientes con PAS fueron elegidos (n=38), se aplicó igual cantidad de calorías (24,1 kcal/kg frente a 24,5 kcal/kg) y proteínas (1,43 frente a 1,45 g/kg) por NE y NPT respectivamente y se encontró una disminución significativa de todas las complicaciones, particularmente las de tipo infeccioso (Kalfarentzos F, Kehagias J. Mead N, et al. Enteral nutrition is superior to parenteral nutrition in severe acute pancreatitis: results of a randomized prospective trial. Br J Surg 1997; 84: 1665-1669). Tres ensayos clínicos encontraron disminución significativa en los costos con NE en comparación con NPT. En un meta-análisis recientemente publicado en el que se incluyen seis ensayos clínicos equiparando NE contra NPT en pancreatitis aguda se encontró disminución no significativa en la mortalidad de los pacientes (10,3 frente a 11,6%), pero las complicaciones infecciosas particularmente las producidas por catéter central o por sepsis pancreática fueron significativamente menores en el grupo de NE. Al analizar el subgrupo con pancreatitis severa aunque hay tendencia a la disminución con la NE, la diferencia no es significativa (15,8 frente a 20,9%) (37).
Finamente, teniendo en cuenta la disminución en la tasa de complicaciones infecciosas y la reducción de los costos, a pesar de que la mortalidad no varía significativamente se prefiere la administración NE con sonda avanzada a yeyuno, empezando antes de 48 horas desde el inicio.
En un ensayo clínico se suministró el alimento a través de sonda nasogástrica; parece ser seguro pero requiere mayor confirmación. En otro ensayo clínico se suministró la NE enriquecida con sustrato de avena y probióticos (Lactobacillum plantarum), demostrándose una disminución de las complicaciones infecciosas en el grupo estudio; la diferencia fue significativa, redujo la sepsis pancreática y el número de intervenciones quirúrgicas (Olah A, Belagyi T, Issekutz A, et al. Randomized clinical trial of specific lactobacillus and fibre supplement to early enteral nutrition in patients with acute pancreatitis. Br J Surg 2002; 89: 1103-1107).
En el estudio en mención se suministró nutrición mixta en la mayoría de los pacientes (n=34), NE (n=24) y NPT (n=22), no se discriminó por grupos para conocer el impacto del tipo de nutrición con la extensión de la necrosis y la posibilidad de infectarse y finalmente en la mortalidad, tampoco era un objetivo de la investigación.
Necrosis pancreática
Si bien es cierto como afirman los autores del artículo que "no siempre la severidad se correlaciona con la extensión de la necrosis", en la mayoría de las series se demuestra que el riesgo de infección se incrementa con la extensión de la necrosis intra y extra pancreática (34). La experiencia del grupo alemán de Ulm demostró que la extensión de la necrosis pancreática se relaciona directamente con la falla de órganos, mientras que en la necrosis infectada, la falla de órganos es relativamente alta, independiente de la extensión de la misma (35).
Por lo tanto, se puede concluir que en necrosis pancreática estéril el principal factor determinante del resultado final es la extensión de la misma, mientras que en necrosis infectada se desarrolla FOM y la muerte independientemente de la extensión de la misma.
Al no ser mencionado el grado, extensión o porcentaje de necrosis, no se define el impacto real de la misma en la mortalidad y su relación con la posibilidad de infectarse o de complicarse al seguir siendo estéril. Al analizar este factor hay que tener en cuenta además el momento y la técnica de realización de la tomografía que obligatoriamente debe ser dinámica.
Pancreatitis biliar
Como la mayoría de los pacientes que ingresaron consecutivamente a la UCI tenía pancreatitis severa de origen biliar (51,6%), llama la atención que no se menciona en el protocolo la realización de CPRE más papilotomía y extracción de cálculos, como una estrategia de manejo específica en este tipo de casos.
Existe evidencia suficiente de que los cálculos biliares inician el episodio de pancreatitis biliar por obstrucción temporal o persistente del colédoco distal en la papila de Vater (36). La intervención endoscópica ha remplazado ampliamente la exploración quirúrgica de la vía biliar durante los últimos años; sin embargo, la esfinterotomía y la inyección de medio de contraste en el conducto pancreático posee el riesgo inherente de empeorar el curso de la pancreatitis y otras complicaciones, por lo cual, hay que evaluar la indicación precisa de colangiopancreatografía endoscópica retrógrada (CPRE) en pancreatitis biliar.
En un meta-análisis que incluye tres ensayos clínicos randomizados (Fan y cols., Neoptolemos y cols., y Folsch y cols.), se encontró que la CPRE de emergencia con papilotomía y extracción de cálculos reduce significativamente el porcentaje de complicaciones (41,8 frente a 31,3%) sin efecto en la tasa de mortalidad (7,2 frente a 6,4%). Al analizar el subgrupo de pacientes con pancreatitis biliar leve no se demostró diferencia en la tasa de complicaciones (14,5 frente a 14,7%) o en la mortalidad (0,7 frente a 0,7%), a diferencia de los pacientes con pancreatitis biliar severa donde la realización de CPRE papilotomía redujo significativamente todas las complicaciones (57,1 frente a 18,2%) y la mortalidad (17,9 frente a 3,6%). Por lo tanto, la mayoría de los autores concluye que la CPRE papilotomía no influye en el curso de la pancreatitis leve; mientras que en la contraparte severa debe ser fuertemente considerada (37).
La balanza de la evidencia existente se inclina más a favor de realizar la CPRE/papilotomía preferiblemente dentro de las primeras 48 horas después del inicio de los síntomas. En un ensayo clínico recientemente publicado por Acosta y cols., se demostró que existe un período no mayor de 48 horas, desde el inicio de los síntomas, en el que tanto la desobstrucción espontánea de la papila como terapéuticamente (CPRE más papilotomía) evitaría la progresión de la pancreatitis y limitaría la severidad. Por lo tanto, los pacientes con signos clínicos, de laboratorio o radiológicos que demuestren obstrucción de la papila después de las primeras 24 horas deben ir a CPRE más papilotomía desobstructiva, lo cual disminuiría la posibilidad de complicaciones. La crítica que se le haría a este estudio es el bajo número de participantes con pancreatitis severa definidos por Ranson < de 3 de apenas un 10% (38).
Cirugía y momento de practicarla
La demostración imaginológica (gas o abscesos en el lecho pancreático), bacteriológica (aspirado guiado: gram y cultivo) o por sospecha clínica (FOM persistente) de infección de la necrosis pancreática es indicación de necrosectomía pancreática (39, 40).
Existen varias formas de abordar al paciente dentro de las cuales se mencionan:
1. Necrosectomía con abdomen abierto y marzupialización del lecho pancreático con o sin empaquetamiento.
2. Necrosectomía con abdomen cerrado sobre drenes múltiples.
3. Necrosectomía con abdomen cerrado e irrigación continua del lecho pancreático.
4. Necrosectomía con abdomen cerrado y técnica de empaquetamiento cerrado.
5. Necrosectomía endoscópica transgástrica.
6. Necrosectomía retroperitoneal guiada por laparoscopia.
7. Drenaje cerrado guiado por imágenes.
Se mencionan varias formas de abordar intraoperatoriamente la necrosis pancreática: a través del epiplón menor o mayor, a través del mesocolon transverso o haciendo una maniobra de koher movilizando medialmente el duodeno y la cabeza del páncreas. Otros prefieren guiar el abordaje intraoperatorio según la localización de la necrosis.
En el estudio nacional se abordaron los pacientes a través de la transcavidad de los epiplones, dejando la cavidad marzupializada y realizando relaparotomías programadas cada 24 horas. No hay muchos datos del procedimiento quirúrgico en lo referente a tiempo quirúrgico, sangrado calculado, requerimientos de transfusiones, procedimientos adicionales en el mismo acto quirúrgico, sensación subjetiva de la calidad del primer desbridamiento pancreático. Los pacientes fueron intervenidos cuatro veces en promedio y cerrados después del último lavado y desbridamiento quirúrgico abierto.
Hay acuerdo general de postergar el desbridamiento pancreático mientras el paciente responda positivamente al manejo médico. La razón de retrasar la intervención quirúrgica es para permitir una demarcación apropiada de la necrosis pancreática y peripancreática. En general, se acepta que entre la tercera y cuarta semanas después del inicio de los síntomas, sería el momento con condiciones óptimas para realizar la necrosectomía, logrando limitar la extensión de la cirugía, facilitando el desbridamiento, dismuyendo la posibilidad de hemorragia y de desbridamiento del tejido pancreático sano con el consecuente desarrollo de fístula y minimizar la pérdida de tejido sano pancreático y la eventual aparición de insuficiencia pancreática (41).
Las series que han realizado cirugías tempranas (dentro de las dos primeras semanas) han mostrado resultados negativos e incremento en las cifras de morbi-mortalidad en comparación con intervenciones después de la segunda semana. La Sociedad Internacional de Pancreatología en el consenso de noviembre de 2002 recomienda no realizar desbridamiento dentro de los primeros catorce días después de iniciados los síntomas y la clasifican como una recomendación grado B (42). Dicha recomendación fue confirmada en otro consenso de cuidado crítico en PAS publicado en abril de 2004 (43).
En el estudio en mención se practicó cirugía en 53 de los 64 pacientes, lo que corresponde al 81,3%. De los 53 operados, 38 tenían necrosis infectada (73%), lo cual está acorde con los reportes internacionales que mencionan la probabilidad de infección de la necrosis entre 40 y 70% cuando no se utiliza antibiótico profiláctico. Con el uso de antibiótico profiláctico tipo imipenem y cilastatina algunas series han mostrado una reducción significativa en el porcentaje de infección de la necrosis hasta de 34% (44). En el presente estudio no se menciona el momento de la intervención quirúrgica con respecto al inicio de los síntomas, lo cual como dijimos anteriormente puede ser determinante para el resultado final.
Por último, quisiera agregar las recomendaciones basadas en la evidencia de la Sociedad Internacional de Pancreatología IAP, en lo que se refiere a la cirugía en PA exclusivamente:
1. La PA leve no es indicación de cirugía pancreática.
2. La punción dirigida debe realizarse para diferenciar la necrosis pancreática estéril de la infectada en pacientes con signos de sepsis.
3. El uso de antibióticos profilácticos de amplio espectro reduce la infección de la necrosis probada por TAC, pero puede no influir en la sobrevida.
4. La necrosis pancreática infectada en pacientes con signos y síntomas clínicos de sepsis es una indicación para intervención, incluyendo drenaje percutáneo o necrosectomía.
5. Los pacientes con necrosis estéril deben ser manejados conservadoramente y sólo intervenir quirúrgicamente en casos muy seleccionados.
6. La cirugía temprana en los primeros catorce días desde el inicio de los síntomas no es recomendada en pacientes con pancreatitis necrotizante, salvo en casos seleccionados específicos.
7. La cirugía y otras formas de terapia intervencionista deberían practicarse enfocadas a la preservación del órgano.
8. La colecistectomía se debe realizar para evitar la recurrencia en pancreatitis biliar.
9. En pancreatitis biliar leve la colecistectomía se debe realizar tan pronto el paciente se recupere de la inflamación sistémica, idealmente durante la misma hospitalización.
10. En pancreatitis biliar severa la colecistectomía se puede postergar hasta la resolución de la respuesta inflamatoria y la recuperación clínica.
11. La esfinterotomía endoscópica es una alternativa a la colecistectomía en aquellos pacientes que no tolerarían un procedimiento quirúrgico; sin embargo, existe un riesgo teórico de contaminar la necrosis pancreática estéril.
Referencias
1. Fenton-Lee D, Imrie CW. Pancreatic necrosis: assessment of outcome related to quality of life and cost of management. Br J Surg 1993; 80:1579-1582.
2. Neoptolemos, Raraty, Finch, et al. The cost of acute pancreatitis. Gut 1998; 42: 886-891.
3. Tenner S, Sica G, Hughes M, et al. Relationship of necrosis to organ failure in severe acute pancreatitis. Gastroenterology 1997; 113: 899-903.
4. Lankisch PG, Pflichthofer D, Lehnick D. No strict correlation between necrosis and organ failure in acute pancreatitis. Pancreas 2000; 20: 319-322.
5. Beger HG, Bittner R, Block S, Büchler M. Bacterial contamination of pancreatic necrosis. A prospective clinical study. Gastroenterology 1986; 91: 433-438.
6. Bassi C, Falconi M, Girelli F, et al. Microbiological findings in severe pancreatitis. Surg Res Commun 1989; 5: 1-4.
7. Isenmann R, Rau B, Beger HG. Bacterial infection and extent of necrosis are determinants of organ failure in patients with acute necrotizing pancreatitis. Br J Surg 1999; 86: 1020-1024.
8. Le Mee J, Paye F, Sauvanet A, et al. Incidence and reversibility of organ failure in the course of sterile or infected necrotizing pancreatitis. Arch Surg 2001; 136:1386-1390.
9. Malangoni MA. Outcome of severe acute pancreatitis. Am J Surg 2005; 189: 273-277.
10. Lucarotti ME, Virjee J, Alderson D. Patient selection and timing of dynamic computed tomography in acute pancreatitis. Br J Surg 1993; 80: 1393-1395.
11. Balthazar EJ, Robinson DL, Megibow AJ, Ranson JHC. Acute pancreatitis: value of CT in establishing prognosis. Radiology 1990; 174: 331-336.
12. Vriens et al. CT Severity Index for Acute Pancreatitis. J Am Coll Surg 2000; 201: 4.
13. Isenmann R, Rau B, Zoellner U, Beger HG. Management of patients with extended pancreatic necrosis. Pancreatology 2001; 1: 63-68.
14. Beger HG, Bittner R, Block S, et al. Bacterial contamination of pancreatic necrosis. A prospective clinical study. Gastroenterology 1986; 91: 433-438.
15. Rau B, Pralle U, Uhl W, Schoenberg MH, Beger HG. Management of sterile necrosis in instances of severe acute pancreatitis. J Am Coll Surg 1995; 181: 279- 288.
16. Tarpila E, Nystrom PO, Franzen L, et al. Bacterial translocation during acute pancreatitis in rats. Eur J Surg 1993; 159: 109-113.
17. Luiten EJ, Hop WCJ, Endtz HP, et al. Prognostic importance of Gram-negative intestinal colonization preceding pancreatic infection in severe acute pancreatitis. Intensive Care Med 1998; 24: 438-444.
18. Hoerauf A, Hammer S, Müller-Myhsok B, Rupprecht H. Intra-abdominal Candida infection during acute necrotizing pancreatitis has a high prevalence and is associated with an increased mortality. Crit Care Med 1998; 26: 2010-2015.
19. Isenmann R, Schwarz M, Rau B, Trautmann M, Schober W, Beger HG. Characteristics of infection with Candida species in patients with necrotizing pancreatitis. World J Surg 2002; 25: 372-376.
20. Craig CP. Gram-negative septicemia and shock. Compr Ther 1982; 8: 13-18.
21. Howes R, Zuidema GD, Cameron JL. Evaluation of prophylactic antibiotics in acute pancreatitis. J Surg Res 1975; 18: 197-200.
22. Finch DRA, Lee E. Acute pancreatitis complicating pregnancy in the Oxford region. Br J Surg 1974; 61: 129-130.
23. Pederzoli P, Bassi C, Vesentini S, Campedelli A. A randomized multicenter clinical trial of antibiotic prophylaxis of septic complications in acute necrotizing pancreatitis with imipenem. Surg Gynecol Obstet 1993; 176: 480-483.
24. Delcenserie R, Yzet T, Ducroix JP. Prophylactic antibiotics in treatment of severe acute alcoholic pancreatitis. Pancreas 1996; 13: 198-201.
25. Schwarz M, Isenmann R, Meyer H, Beger HG. Antibiotika bei nekrotisierender Pankreatitis-Ergebnisse einer kontrollierten Studie. Dtsch Med Wochenschr 1997; 122: 356-361.
26. Bassi C, Falconi M, Talamini G, et al. Controlled clinical trial of pefloxacin versus imipenem in severe acute pancreatitis. Gastroenterology 1998; 115: 1513-1517.
27. Nordback I, Scand J, Saaristo R, Paajanen H. Early treatment with antibiotics reduces the need for surgery in acute necrotizing pancreatitis - A single-center randomized study. J Gastrointest Surg 2001; 5: 113-120.
28. UK Working Party on Acute Pancreatitis UK guidelines for the management of acute pancreatitis. Gut 2005; 54; 1-9.
29. IAP Guidelines for the Surgical Management of Acute Pancreatitis Pancreatology 2002; 2: 565-570.
30. Isenmann R, Rünzi M, Kron M, et al. Prophylactic antibiotic treatment in patients with severe acute pancreatitis - A placebo-controlled, double-blind trial. Gastroenterology 2004; 126: 997-1004.
31. HG Beger B, Raud R, Isenmannb M, Schwarzc F, Gansaugec B. Pochc. Antibiotic Prophylaxis in Severe Acute Pancreatitis. Pancreatology 2005; 5: 10-19.
32. Lankisch and Lerch (Clin Gastroenterol 2006; 40: 2.
33. Runzi, et al. Nonsurgical treatment of infected necrosis. Pancreas 2005; 30: 195-199.
34. Beger HG, Bittner R, Block S, Büchler M. Bacterial contamination of pancreatic necrosis. A prospective clinical study. Gastroenterology 1986; 91: 433-438.
35. Isenmann R, Rau B, Beger HG. Bacterial infection and extent of necrosis are determinants of organ failure in patients with acute necrotizing pancreatitis. Br J Surg 1999; 86: 1020-1024.
36. Forsmark CE. The clinical problem of biliary acute necrotizing pancreatitis: epidemiology, pathophysiology, and diagnosis of biliary necrotizing pancreatitis. J Gastrointest Surg. 2001; 5: 235-239.
37. Heinrich, et al. Evidence-based treatment of acute pancreatitis. Ann Surg 2006; 243 (2).
38. Acosta, et al. Ann Surg 2006; 243: 1.
39. British Society of Gastroenterology. United Kingdom guidelines for the management of acute pancreatitis. Gut 1998; 42 (suppl 2): S1-S13.
40. Büchler MW, Gloor B, Müller CA, Friess H, Seiler CA, Uhl W. Acute necrotizing pancreatitis: Treatment strategy according to the status of infection. Ann Surg 2000; 232: 619-626.
41. Fernández-del Castillo C, Rattner DW, Makary MA, et al. De'bridement and closed packing for the treatment of necrotizing pancreatitis. Ann Surg 1998; 228: 676-684.
42. Uhl, et al. Pancreatology 2002; 2: 565-573.
43. Nathens AB, J. Curtis R, et al. Management of the critically ill patient with severe acute pancreatitis. Crit Care Med 2004; 32: 2524-2536.
44. Buchler and Others. Acute necrotizing pancreatitis: treatment strategy according to the status of infection. Ann Surg 232; 5: 619-626.














