Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cirugía
Print version ISSN 2011-7582
rev. colomb. cir. vol.30 no.3 Bogotá July/Sept. 2015
Mario López1, Fabián Martínez1, Jaime Camacho2, Álvaro Sanabria3, Luis Carlos Domínguez4, Valentín Vega4
1 Médico, residente de Cirugía General, Departamento de Cirugía General, Universidad de La Sabana, Chía, Colombia.
2 Médico, cirujano vascular; jefe, Cirugía Vascular y Endovascular, Clínica de la Aorta, Fundación Cardioinfantil-Instituto de Cardiología, Bogotá, D.C., Colombia.
3 Médico, cirujano de cabeza y cuello, Hospital Pablo Tobón Uribe; profesor, Departamento de Cirugía, Universidad de Antioquia, Medellín, Colombia; profesor asociado, Universidad de La Sabana, Chía, Colombia.
4 Médico, cirujano general, Departamento de Cirugía General; profesor asociado, Universidad de La Sabana, Chía, Colombia.
Segundo puesto en el concurso del residente quirúrgico. 41° Congreso Nacional Avances en Cirugía, 2015.Fecha de recibido: 14 de mayo de 2015. Fecha de aprobación: 14 de agosto de 2015.
Correspondencia: Jaime Camacho, MD, Chía, Colombia. jcamachomackenzie1@gmail.com y mariofdolopez@hotmail.com
Fecha de recibido: 14 de mayo de 2015. Fecha de aprobación: 14 de agosto de 2015.
Resumen
Introducción. La insuficiencia renal aguda es una complicación común después del reparo de un aneurisma infrarrenal de aorta abdominal; sin embargo, su incidencia es variable según el estudio y todavía existe controversia respecto a si es más frecuente en pacientes sometidos a reparación endovascular o a cirugía abierta.
Objetivo. Determinar la incidencia de insuficiencia renal aguda posoperatoria en pacientes sometidos a corrección electiva por técnica abierta frente a la endovascular, de aneurisma de aorta abdominal infrarrenal no roto, en la Fundación Cardioinfantil-Instituto de Cardiología entre 2002 y 2014.
Materiales y métodos. Se hizo un estudio de cohorte retrospectiva, que incluyó 326 pacientes con aneurisma de aorta infrarrenal no roto a los que se les practicó cirugía abierta (n=273) o reparación endovascular (n=53).
Resultados. No existieron diferencias estadísticamente significativas entre la incidencia de insuficiencia renal aguda en el grupo con tratamiento abierto y aquella en el grupo con terapia endovascular (11 % Vs. 3,8 %) (p=0,1). El antecedente de infarto agudo de miocardio (odds ratio (OR)=4,21; IC95% 1,65-10,74; p=0,003) y de transfusión de glóbulos rojos (OR=2,65; IC95% 1,16-6,09; p=0,021), fueron los factores más importantes para desarrollar insuficiencia renal aguda.
Conclusiones. No se evidencian diferencias estadísticas en el resultado de insuficiencia renal aguda posoperatoria según el tipo de abordaje. Sin embargo, el antecedente de infarto agudo de miocardio y la necesidad de transfusión en el posoperatorio están relacionados con la insuficiencia renal aguda.Palabras clave: aneurisma de la aorta abdominal; procedimientos quirúrgicos vasculares; procedimientos endovasculares; prótesis vascular; injerto vascular; insuficiencia renal.
Palabras clave: aneurisma de la aorta abdominal; procedimientos quirúrgicos vasculares; procedimientos endovasculares; prótesis vascular; injerto vascular; insuficiencia renal.
Abstract
Introduction: Acute renal failure is a common complication after elective repair of an infrarrenal aortic aneurysm; however, the incidence varies according to different studies. There is still controversy on whether it is more frequent in patients undergoing endovascular repair as opposed to open surgery.Objective: To determine the incidence of postoperative acute renal failure in patients with infrarenal abdominal aortic aneurysm undergoing elective repair by open technique versus endovascular repair at Fundación Cardioinfantil - Instituto de Cardiología (Bogotá, Colombia) in the period between 2002 and 2014.Method: We conducted a retrospective cohort study that included 326 patients with nomruptured infrarenal aortic aneurysm who underwent open surgery (n = 273) and endovascular repair (n = 53).
Results: No statistically significant difference was found between the incidence of acute renal failure in the open treatment group and in the endovascular therapy group (11 % Vs 3.8%) (p 0.1), The history of acute myocardial infarction odds ratio (OR): 4.21; 95% CI 1.65- 10.74, p 0.003) and receiving red cells transfusion (OR: 2.65; 95% CI 1.16- 6.09, p 0.021) appeared as the most important risk factor for the development of acute renal failure.
Conclusions: In this study we found that there is no difference in the outcome of postoperative acute renal failure comparing both techniques. However, previous myocardial infarction and the requirement of postoperative transfusion are associated with acute renal failure.
Key words: Aortic aneurysm, abdominal; vascular surgical procedures; endovascular procedures; blood vessel prosthesis; vascular grafting; renal insufficiency.
Introducción
La American Association for Vascular Surgery define al aneurisma de aorta abdominal como una dilatación permanente y localizada del diámetro de la arteria de 50 % o más del valor esperado 1,2. Esta enfermedad es más frecuente en hombres mayores de 65 años de edad, fumadores y con antecedentes familiares de aneurismas 3-6.
La tomografía computadorizada (TC) de abdomen con contraste, es la técnica más fiable para el diagnóstico y la toma de decisiones en casos de aneurisma de aorta abdominal 7,8. Independientemente de la etiología, la cirugía está indicada cuando el diámetro máximo de la aorta abdominal es de 55 mm o mayor; cuando este es menor, se puede considerar si existen factores de riesgo adicionales, como hipertensión arterial, coartación de la aorta o aumento en el diámetro de la aorta de 10 o más mm al año 9.
La reparación quirúrgica se hace por dos abordajes: abierto, que incluye la vía transperitoneal a través de laparotomía mediana o la vía extraperitoneal a través de lumbotomía izquierda, o cerrado, con técnica endovascular 10,11.
En la técnica quirúrgica endovascular se practican dos pequeñas incisiones en la ingle, para exponer las arterias femorales. Con el uso de guías, catéteres, introductores y sistemas especialmente diseñados, bajo guía fluoroscópica y con medio de contraste para obtener el aortograma, se introduce una endoprótesis en el interior del aneurisma de la aorta abdominal, y así, se excluye el saco del aneurisma sin abrir el abdomen.
Se utilizan criterios como la presencia de un cuello aórtico infrarrenal adecuado, la ausencia de tortuosidad aorto-ilíaca seria y la ausencia de calcificación de la pared arterial, para la elección de esta técnica 12. Cuando se cumplen estos criterios anatómicos, la técnica endovascular se asocia con una reducción de 66 % de la mortalidad operatoria. Cuando las condiciones no son adecuadas para la técnica endovascular, la reparación abierta sigue siendo el método estándar de referencia 9-12.
La primera colocación de injerto fue reportada por Dubost en 1951. El reparo abierto fue la única opción para prevenir la ruptura de los aneurismas de aorta abdominal hasta 1991, cuando Parodi informó el primer reparo endovascular 12. La evolución de esta última técnica ha permitido ampliar las opciones terapéuticas; ofrece la posibilidad de un manejo endovascular, al parecer, menos mórbido, en pacientes con mayor riesgo de complicaciones antes y después de la cirugía 13, 14.
Las complicaciones descritas en el abordaje endovascular, son la endofuga (25 %), las lesiones vasculares (0 a 3 %) y la infección de la endoprótesis (1 %). En algunos estudios se sugiere que con la técnica endovascular son menores la tasa de complicaciones (pulmonares, hemorrágicas), el tiempo quirúrgico, la duración de la asistencia respiratoria mecánica posoperatoria, el tiempo de estancia en cuidados intensivos y hospitalaria total, y la necesidad de líquidos intravenosos, productos sanguíneos y medicamentos diuréticos intraoperatorios 15,16.
La insuficiencia renal aguda es una complicación frecuente después de la corrección de un aneurisma infrarrenal de aorta abdominal, mediante cirugía abierta o terapia endovascular. La fisiopatología de la insuficiencia renal aguda en la técnica endovascular es compleja. Se ha considerado que en ella influyen la nefropatía inducida por el medio de contraste, la 'microembolización' renal y la necrosis tubular aguda 17, por lo cual se han implementado estrategias para disminuir la toxicidad renal (extrapoladas de la protección contra la nefropatía por contraste), incluyendo el aumento del flujo tubular con solución salina, bicarbonato de sodio o diuréticos 18-21. El aumento de la presión hidrostática en los túbulos proximales disminuye el gradiente para la filtración del capilar glomerular. Estos efectos disminuyen en forma importante cuando se utiliza medio de contraste isoosmolar o hipoosmolar 22-25.
Se considera que, durante la técnica endovascular, la inserción y la manipulación de los catéteres pueden dar lugar a ruptura de la placa y "microembolización" 22. La ruptura de la placa puede incrementarse por la dilatación con balón en el cuello proximal o en la fijación suprarrenal, y generar 'microembolización' y posterior infarto segmentario que pueden, en teoría, llevar a insuficiencia renal aguda 18.
La incidencia de insuficiencia renal aguda posoperatoria varía según el estudio y en nuestro medio su frecuencia no ha sido medida, y tampoco los factores que pueden estar asociados; incluso, se ha planteado como hipótesis que la insuficiencia renal aguda podría ser más frecuente en pacientes intervenidos con terapia endovascular, opinión que a la fecha aún es controversial.
El objetivo del presente estudio fue determinar la incidencia de insuficiencia renal aguda en pacientes con aneurisma infrarrenal no roto de la aorta abdominal sometidos a reparación endovascular con endoprótesis, comparados con aquellos tratados con técnica abierta, y determinar qué factores de riesgo pueden estar asociados, en una institución con experiencia en esta entidad, como lo es la Clínica de la Aorta de la Fundación Cardioinfantil-Instituto de Cardiología de Bogotá.
Materiales y métodos
Previa aprobación del Comité de Ética de la Fundación Cardioinfantil y de la comisión de investigaciones de la Facultad de Medicina (posgrados) de la Universidad de La Sabana, se analizó retrospectivamente una cohorte de pacientes sometidos a corrección de aneurisma infrarrenal de aorta abdominal, mediante técnica abierta o técnica endovascular con endoprótesis.
Los criterios para decidir la intervención endovascular fueron los anatómicos, un diámetro adecuado (10-15 longitud del cuello) del cuello aórtico infrarrenal y la ausencia de tortuosidad aortoilíaca grave, y la capacidad socioeconómica para el seguimiento posoperatorio.
Los criterios de inclusión fueron pacientes mayores de 18 años, intervenidos de forma electiva bajo las técnicas mencionadas, en la Fundación Cardioinfantil, entre enero de 2002 y diciembre de 2014. Los criterios de exclusión fueron: signos agudos o crónicos de ruptura, diagnóstico o tratamiento de falla renal previa al procedimiento, antecedentes de síndrome de Marfan o enfermedad del colágeno, intervenciones primarias practicadas en otra institución o fallecimiento en las primeras 72 horas posoperatorias por causas diferentes a falla renal.
La insuficiencia renal aguda se definió como la disminución de 50 % de la tasa de filtración glomerular o el aumento de 1,5 veces de la creatinina sérica basal prequirúrgica comparada con la posquirúrgica 25. La tasa de depuración de la creatinina se calculó por medio de la fórmula de Cockroft-Gault 26.
Para el análisis estadístico, se utilizó el programa Stata 10. Los datos se presentaron mediante frecuencias absolutas y porcentajes para variables cualitativas; según las características de distribución de las variables cuantitativas, las medidas resumen se presentaron en medias o medianas y desviaciones estándar o rangos. Se compararon los diferentes factores entre los dos grupos (cirugía abierta y endovascular) mediante la prueba de ji al cuadrado para variables categóricas y la t de Student para variables continuas. Posteriormente, se estableció la prevalencia de la insuficiencia renal aguda en cada uno de los grupos.
Se hizo el análisis bivariado para la asociación de las variables de exposición con la insuficiencia renal aguda y, posteriormente, el de regresión logística con las variables que presentaron un valor de p<0,2 en el anterior, mediante un abordaje por etapas (un modelo para variables demográficas, otro para factores de riesgo y un tercer modelo global con las variables previamente identificadas como asociadas). La principal variable de ajuste fue el método de corrección del aneurisma. Los resultados se muestran como odds ratio (OR) e intervalos de confianza (IC) del 95 %. Se consideró estadísticamente significativo un valor p<0,05.
Resultados
De un total de 457 pacientes, 326 cumplieron con los criterios de inclusión, 53 con técnica endovascular y 273 con técnica abierta. En la tabla 1 se presentan las características demográficas de ambos grupos, evidenciando que los pacientes operados por técnica endovascular tenían mayor edad, peso y talla, en comparación con el grupo de técnica abierta; sin embargo, en este último el diámetro de los aneurismas fue mayor.
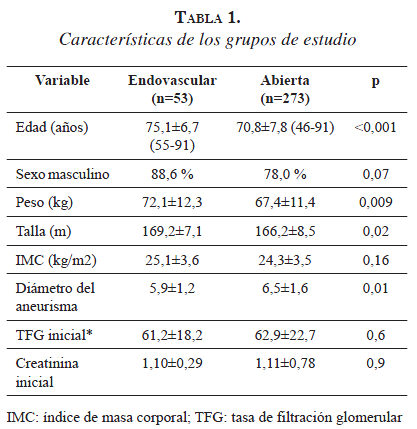
Entre los factores de riesgo, se encontró una mayor prevalencia de enfermedad pulmonar obstructiva crónica en el grupo con cirugía endovascular. Las transfusiones fueron más frecuentes y el número de unidades transfundidas de glóbulos rojos fue mayor en el grupo con cirugía abierta (tabla 2).
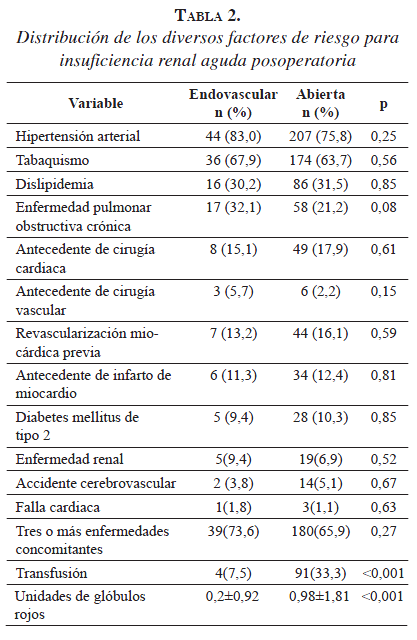
La insuficiencia renal aguda fue más frecuente en el grupo con cirugía abierta (11 % Vs. 3,8 %), pero la diferencia que no fue estadísticamente significativa (p=0,1). En el posoperatorio, la tasa de depuración de creatinina y la tasa de filtración glomerular fueron similares entre los grupos (p=0,1), como también lo fue la mortalidad (1,9 % Vs. 2,2 %) (p=0,88) (tabla 3).
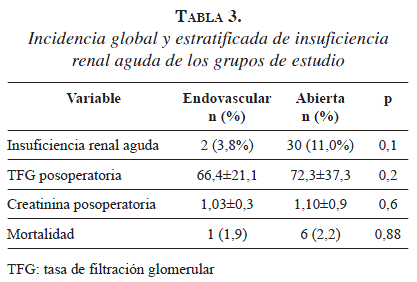
Los factores de riesgo conocidos (demográficos, enfermedades concomitantes, y las características quirúrgicas y de la transfusión), se evaluaron en la regresión logística (tablas 4 y 5). Las variables significativas, como son el sexo (p=0,136), el diámetro del aneurisma (p=0,037), la creatinina sérica preoperatoria (p=0,038), el antecedente de infarto agudo del miocardio (p=0,003), el abordaje (p=0,573) y la transfusión (p=0,021), se identificaron como asociadas con la presencia de insuficiencia renal aguda.
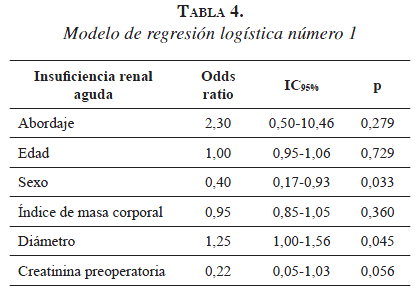
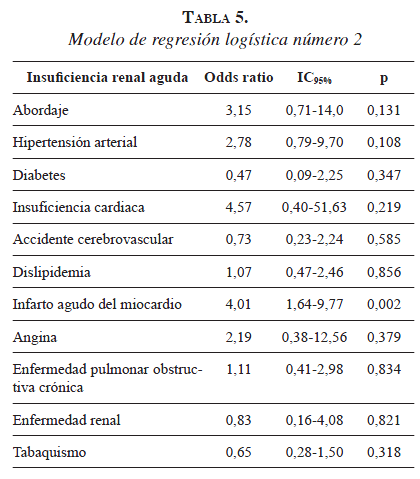
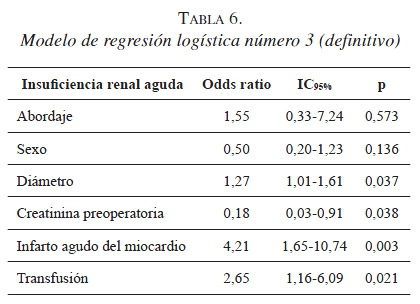
Según los resultados obtenidos en la regresión logística sobre el principal resultado de este estudio, la insuficiencia renal aguda, no se observan diferencias significativas entre los dos tipos de abordaje. Además, el diámetro del aneurisma de la aorta abdominal, el valor de la creatinina sérica preoperatoria, el tener un infarto agudo de miocardio previo y el recibir transfusión de glóbulos rojos empaquetados fueron los factores asociados más importantes para desarrollar insuficiencia renal aguda.
Discusión
Desde el primer reparo endovascular que fue reportado por Parodi en 1991 11, la evolución de esta técnica ha permitido ampliar las opciones terapéuticas; ofrece la opción de un manejo endovascular menos invasivo en los pacientes con mayor riesgo de complicaciones antes y después de la cirugía 11, 12.
La fisiopatología de la insuficiencia renal aguda se ha considerado multifactorial a lo largo del tiempo. Entre los factores más relevantes, se incluyen la nefropatía inducida por medio de contraste, la 'microembolización' renal y la necrosis tubular aguda. El manejo de estas diferentes condiciones no es fácil; sin embargo, deben identificarse con el fin de prevenir la insuficiencia renal aguda. Debe adoptarse una estrategia multifocal y lo más importante es que el paciente con mayor riesgo se identifique con prontitud 22.
A pesar de que la insuficiencia renal aguda se considera una complicación frecuente en los procedimientos endovasculares, su incidencia y factores de predicción no están bien estudiados. Esto puede ser así por diferentes razones, a saber: las comparaciones entre los estudios son difíciles debido a las diferencias entre las muestras de pacientes, la etiología es heterogénea, y la extensión de las lesiones aóticas es variable; no obstante, lo más importante es que los criterios para diagnosticar insuficiencia renal aguda posoperatoria son diferentes, lo cual produce confusión inevitablemente 27.
La lesión renal aguda con la técnica endovascular se ha documentado en varios estudios 28-31, con incidencias que van desde 1 % hasta 19 %. Según los estudios de Wald, et al., y Adriaensen, et al., la incidencia de insuficiencia renal aguda es menor con la técnica endovascular en comparación con la abierta 31, 32. Por el contrario, en el estudio holandés Randomized Endovascular Aneurysm Management (DREAM), se encontró que los cambios perioperatorios en la creatinina sérica son similares en ambos grupos 33, como lo fueron en el presente caso. En el estudio de Gawenda, et al., en el que se evaluaron 485 pacientes sometidos a reparo quirúrgico de aneurisma abdominal, se encontró un aumento significativo de la creatinina sérica (1,0 a 1,08 mg/dl) con disminución de su depuración con la técnica endovascular, pero no con la abierta 34. En otros dos estudios, se observó una mejoría transitoria en la depuración de creatinina en los primeros siete días después de la técnica endovascular, seguida por su deterioro al año 35,36. En contraste con lo anterior, la mayoría de los estudios han mostrado una mayor incidencia de falla renal con la técnica abierta 28-31.
Aunque en los resultados obtenidos no se demostraron diferencias en la incidencia de insuficiencia renal posoperatoria entre la técnica abierta y la endovascular (3,8 % Vs. 11 %) (p=0,1), entre sus limitaciones se debe mencionar que los pacientes operados mediante técnica endovascular tenían mayor edad y, posiblemente, un riesgo quirúrgico más alto; además, en el grupo con técnica endovascular el tamaño de la muestra fue limitado.
Los efectos de la transfusión, considerada un factor asociado (OR=2,65; IC95% 1,16-6,09) (p=0,021), podrían relacionarse con la reacción fisiológica a la transfusión, la cual provoca una respuesta directa de los mediadores inflamatorios y, por ende, una intensificación del proceso inflamatorio que lleva a lesión tubular renal 37.
La mortalidad reportada en este estudio (endovascular 1,9 % Vs. abierta 2,2 %), es similar a la reportada por centros especializados en la literatura científica (1,4 % Vs. 1,8 %). En una revisión de 64 estudios, se encontró una tasa promedio de mortalidad de 5,5 % con la técnica abierta 38 y, en un metaanálisis de 161 estudios, una tasa de mortalidad operatoria combinada de 3,3 % (IC95% 2,9-3,6) con la endovascular. Sin embargo, los resultados han mejorado rápidamente con el tiempo, obteniéndose tasas más bajas de mortalidad, que llegan a 1,4 %, en estudios recientes 39. Se cree que la presencia de enfermedades cardíacas y respiratorias, así como de insuficiencia renal, aumenta la mortalidad perioperatoria.
Es controversial el impacto de la edad del paciente y, en la mayoría de los centros especializados, se considera muy importante la experiencia del cirujano (40). Se espera que, con la creciente experiencia en estas dos técnicas y con la estandarización de las medidas de soporte, se optimicen los beneficios esperados y se amplíen las diferencias entre estos procedimientos. Además, consideramos que el presente puede ser una base para desarrollar estudios de casos y controles, con un tamaño de muestra calculado según la prevalencia de los factores de riesgo de insuficiencia renal aguda posoperatoria en nuestro medio que, de esta forma, se podrían evaluar mejorar.Conclusiones
No se evidencian diferencias estadísticas en el tipo de abordaje con el desenlace de insuficiencia renal aguda postoperatoria. Sin embargo, el antecedente de infarto agudo de miocardio y el requerimiento de transfusión en el postquirúrgico están relacionados con insuficiencia renal aguda. Lo que podría conducir a estudios futuros con el fin de identificar la asociación de la insuficiencia renal aguda postoperatoria con los agentes causales.
Declaración de conflicto de intereses, autoría y financiación. Declaramos no presentar conflictos de intereses con los datos descritos y analizados en este estudio, la autoría es de los autores y las instituciones vinculadas al mismo y manifestamos que las fuentes de financiación para el desarrollo del mismo provienen de recursos personales del grupo investigador.
Referencias
1. Johnston KW, Rutherford RB, Tilson MD. Suggested standards for reporting on arterial aneurysms. J Vasc Surg. 1991;13:452-8. [ Links ]
2. Park BD, Azefor N, Huang C-C, Ricotta JJ. Trends in treatment of ruptured abdominal aortic aneurysm: Impact of endovascular repair and implications for future care. J Am Coll Surg. 2013;216:745-54 [ Links ]
3. Camacho J, Arroyo F, Barrera G, Caicedo V, Espinel C, Al E. Guía de diagnóstico y tratamiento del aneurisma de aorta abdominal Infrarenal. Asociación Colombiana de angiología y cirugía vascular. Rev Col Cir Vasc. 2009;5:12-3. [ Links ]
4. Weiss N, Rodionov RN, Mahlmann A. Medical management of abdominal aortic aneurysms. Vasa. 2014;43:415-21. [ Links ]
5. Kuivaniemi H, Elmore JR. Opportunities in abdominal aortic aneurysm research: Epidemiology, genetics, and pathophysiology. Ann Vasc Surg. 2012;26:862-70. [ Links ]
6. Björck M, Wanhainen A. Pathophysiology of AAA: Heredity Vs.environment. Prog Cardiovasc Dis. 2013;56:2-6. [ Links ]
7. Takayama T, Yamanouchi D. Aneurysmal disease: The abdominal aorta. Surg Clin North Am. 2013;93:877-91. [ Links ]
8. van Walraven C, Wong J, Morant K. Incidence, follow-up, and outcomes of incidental abdominal aortic aneurysms. J Vasc Surg. 2010;52:282-9. [ Links ]
9. Raimund E, Victor A, Catherine B, Eduardo B, Roberto Di B, Holger E, et al. ESC Guidelines on the diagnosis and treatment of aortic diseases. The task force for the diagnosis and treatment of aortic diseases of the European Society of Cardiology (ESC). Eur Heart J. 2014;35:2884-88. [ Links ]
10. Hallin A, Bergqvist D, Holmberg L. Literature review of surgical management of abdominal aortic aneurysm. Eur J Vasc Endovasc Surg. 2001;22:197-204. [ Links ]
11. Edwards ST, Schermerhorn ML, O'Malley AJ, Bensley RP, Hurks R, Cotterill P, et al. Comparative effectiveness of endovascular versus open repair of ruptured abdominal aortic aneurysm in the Medicare population. J Vasc Surg. 2014;59:575-82. [ Links ]
12. Picel AC, Kansal N. Essentials of endovascular abdominal aortic aneurysm repair imaging: Postprocedure surveillance and complications. AJR Am J Roentgenol. 2014;203:W358-72. [ Links ]
13. Wahlgren C-M, Wahlberg E. Management of thoracoabdominal aneurysm type IV. Eur J Vasc Endovasc Surg. 2005;29:116-23. [ Links ]
14. McCullough PA, Wolyn R, Rocher LL, Levin RN, O'Neill WW. Acute renal failure after coronary intervention: Incidence, risk factors, and relationship to mortality. Am J Med. 1997;103:368-75. [ Links ]
15. Carpenter JP, Baum RA, Barker CF, Golden MA, Mitchell ME, Velazquez OC, et al. Impact of exclusion criteria on patient selection for endovascular abdominal aortic aneurysm repair. J Vasc Surg. 2001;34:1050-4. [ Links ]
16. Taiga I, Yoshitaka A, Yushi A, Matsuyuki D, Shigehito S. Acute kidney injury following open Vs. endovascular repair of infrarenal abdominal aortic aneurysm. Am Soc Anesthesiol. 2010;3:8-13. [ Links ]
17. Melas N, Saratzis A, Saratzis N, Lazaridis J, Psaroulis D, Trygonis K, et al. Aortic and iliac fixation of seven endografts for abdominal-aortic aneurysm repair in an experimental model using human cadaveric aortas. Eur J Vasc Endovasc Surg. 2010;40:429-35. [ Links ]
18. Saratzis AN, Goodyear S, Sur H, Saedon M, Imray C, Mahmood A. Acute kidney injury after endovascular repair of abdominal aortic aneurysm. J Endovasc Ther. 2013;20:315-30. [ Links ]
19. Reber PU, Vogt B, Steinke TM, Patel AG, Kniemeyer HW. Surgery for aortoiliac aneurysms in kidney transplant recipients. J Cardiovasc Surg (Torino). 2000;41:919-25. [ Links ]
20. D'Ayala M, Deitch JS, Wise L. Complications of endovascular surgery for abdominal aortic aneurysms. Curr Surg. 2004;61:163-5. [ Links ]
21. MD RWK, MD RL. Contrast-Induced nephropathy after intravenous administration: Fact or fiction? Radiol Clin North Am. 2009;47:789-800. [ Links ]
22. Antoniou GA, Karkos CD, Antoniou SA, Georgiadis GS. Can an accessory renal artery be safely covered during endovascular aortic aneurysm repair? Interact Cardiovasc Thorac Surg. 2013;17:1025-7. [ Links ]
23. Buijs RVC, Willems TP, Tio RA, Boersma HH, Tielliu IFJ, Slart RHJA, et al. Current state of experimental imaging modalities for risk assessment of abdominal aortic aneurysm. J Vasc Surg. 2013;57:851-9. [ Links ]
24. Ten Bosch JA, Teijink JAW, Willigendael EM, Prins MH. Endovascular aneurysm repair is superior to open surgery for ruptured abdominal aortic aneurysms in EVAR-suitable patients. J Vasc Surg. 2010;52:13-8. [ Links ]
25. Peter A, Alison M, Rashad S, Eknoyan G, Lameire N, Abboud O, et al. KDIGO clinical practice guideline for acute kidney injury. KDIGO. 2012;2:3. [ Links ]
26 Cockcroft DW, Gault MH. Prediction of creatinine clearance from serum creatinine. Nephron. 1976;16:31-41. [ Links ]
27. Gabriele P, Giovanni M, Stefano B, Sarcina A, Gelpi G, Bellosta R, et al. Predictors and outcomes of acute kidney injury after thoracic aortic endograft repair. J Vasc Surg. 2012;56:1531. [ Links ]
28. James MT, Ghali WA, Knudtson ML, Ravani P, Tonelli M, Faris P, et al. Associations between acute kidney injury and cardiovascular and renal outcomes after coronary angiography. Circulation. 2011;123:409-16. [ Links ]
29. Bellomo R, Ronco C, Kellum JA, Mehta RL, Palevsky P, Lameire N, et al. Acute renal failure - definition, outcome measures, animal models, fluid therapy and information technology needs: The Second International Consensus Conference of the Acute Dialysis Quality Initiative (ADQI) Group. Crit Care. 2004;8:R204-12. [ Links ]
30. Mehta RL, Kellum JA, Shah SV, Molitoris BA, Ronco C, Warnock DG, et al. Acute kidney injury network: Report of an initiative to improve outcomes in acute kidney injury. Crit Care. 2007;11:R31. [ Links ]
31. Wald R, Waikar SS, Liangos O, Pereira BJ, Chertow GM, Jaber BL, et al. Acute renal failure after endovascular Vs. open repair of abdominal aortic aneurysm. J Vasc Surg. 2006;43:460-6. [ Links ]
32. Adriaensen ME, Bosch JL, Halpern EF, Myriam Hunink MG, Gazelle GS, et al. Elective endovascular Vs. open surgical repair of abdominal aortic aneurysms: A systemic review of short-term results. Radiology. 2002;224:739-47. [ Links ]
33. Blankensteijn JD, de Jong SE, Prinssen M, Buth J, van Sterkenburg SM, Verhagen HJ, et al. Dutch Randomized Endovascular Aneurysm Management (DREAM) trial group. Two-year outcomes after conventional or endovascular repair of abdominal aortic aneurysms. N Engl J Med. 2005;352:2398-2405. [ Links ]
34. Gawenda M, Brunkwall J. Renal response to open and endovascular repair of abdominalaortic aneurysm: A prospective study. Ann Vasc Surg. 2008;22:1-4. [ Links ]
35. Parmer SS, Carpenter JP. Endovascular aneurysm repair with suprarenal Vs. infrarenalfixation: A study of renal effects. J Vasc Surg.2006;43:19-25. [ Links ]
36. Cayne NS, Rhee SJ, Veith FJ, Lipsitz EC, Ohki T, Gargiulo NJ 3rd, et al. Does transrenal fixation of aortic endografts impair renal function? J Vasc Surg. 2003;38:639-44. [ Links ]
37. Mariscalco G, Lorusso R, Dominici C, Renzulli A, Sala A. Acute kidney injury: A relevant complication after cardiac surgery. Ann Thorac Surg. 2011;92:1539-47. [ Links ]
38. Hallin A, Bergqvist D, Holmberg L. Literature review of surgical management of abdominal aortic aneurysm. Eur J Vasc Endovasc Surg. 2001;22:197-204. [ Links ]
38. Franks SC, Sutton AJ, Bown MJ, Sayers RD. Systematic review and meta-analysis of 12 years of endovascular abdominal aortic aneurysm repair. Eur J Vasc Endovasc Surg. 2007;33:154-71. [ Links ]
39. Steyerberg EW, Kievit J, de Mol van Otterloo JC, van Bockel JH, Eijkemans MJ, Habbema JD. Perioperative mortality of elective abdominal aortic aneurysm surgery. A clinical prediction rule based on literature and individual patient data. Arch Intern Med. 1995;155:1998-2004. [ Links ]
40. Camacho J, Arroyo F, Barrera G, Caicedo V, Espinel C, Al E. Guía de diagnóstico y tratamiento del aneurisma de aorta abdominal infrarenal. Asociación Colombiana de angiología y cirugía vascular. Rev Col Cir Vasc. 2009;5:22-5. [ Links ]













