Figura 1. Difractograma de rayos X de la muestra 2.
Figure 1. XRD spectra of the sample 2
STUDY OF SOME PARAMETERS THAT DETERMINE THE SYNTHESIS OF HYDROXYAPATITE BY THE PRECIPITATION ROUTE
CLAUDIA GARCIA
Universidad Nacional de Colombia sede Medellín, Facultad de Ciencias, Escuela de Física, AA3840 Medellín cpgarcia@unalmed.edu.co
CARLOS PAUCAR
Universidad Nacional de Colombia sede Medellín, Facultad de Ciencias, Escuela de Química, AA3840 Medellín cgpaucar@unalmed.edu.co
JAIR GAVIRIA
Universidad Nacional de Colombia sede Medellín, Facultad de Ciencias Escuela de Química, AA3840 Medellín jgarango@unalmed.edu.co
Recibido para revisar 1 de Abril de 2005, aceptado 7 de Julio de 2005, versión final 1 de Agosto de 2005
RESUMEN: La hidroxiapatita sintética es un biomaterial muy usado en diversas aplicaciones en medicina. Una de las rutas más económicas y de mayor aplicación industrial para la síntesis de este material es la precipitación. En el presente trabajo se sintetizó hidroxiapatita mediante la ruta de precipitación a partir de soluciones acuosas de nitrato de calcio (Ca(NO3).4H2O) y fosfato de amonio (H2(PO4)NH4). Se evalúa el efecto de variables fisicoquímicas tales como pH de la mezcla, temperatura, tiempo de agitación y reposo y tratamiento térmico. Mediante la caracterización de las muestras obtenidas a diferentes condiciones, se concluye acerca de las variables óptimas para sintetizar este material.
]]> PALABRAS CLAVE: Hidroxiapatita, variables fisicoquímicas, síntesis, caracterización.ABSTRACT: The synthetic hydroxyapatite is a very useful and with very many applications as a biomaterial. One of the most economical routes to obtain this material is the precipitation. In the present work, it was prepared synthetic hydroxyapatite using the precipitation route, beginning with aqueous solutions of calcium nitrate (Ca(NO3).4H2O ) and ammonium phosphate (H2(PO4)NH4). The effect of physical-chemical variables such as pH of the mixture, temperature, time of agitation and rest and heat treatment was evaluated. By means of the characterization of the samples obtained to different conditions, it was possible to conclude about the optimal variables to synthesize this material
KEY WORDS: Hydroxyapatite, physical-chemistry variables, synthesis, characterization.
1. INTRODUCCIÓN
La reparación de defectos en tejidos duros es un reto permanente en ortopedia y aplicaciones dentales [1]. La hidroxiapatita (Ca10(PO4)6(OH)2) ha sido ampliamente usada como un sustituto de hueso debido a su biocompatibilidad ya que sus componentes minerales son similares a los del hueso y dientes del cuerpo humano. La hidroxiapatita sintética es un biomaterial muy importante usado para varias aplicaciones en medicina bien sea como monolito, recubrimientos o como uno de los componentes de los composites [2-5]. Se han desarrollado muchas rutas para sintetizar hidroxiapatita usando métodos de hidrólisis, hidrotermales o de precipitación [4-7]. De estos métodos, la precipitación se caracteriza por su simplicidad, bajo costo y aplicación a nivel industrial [8].
En el presente trabajo se obtiene hidroxiapatita por la ruta de síntesis química, haciendo reaccionar soluciones acuosas de fosfato de amonio diácido y nitrato de calcio tetrahidratado, bajo control de parámetros tales como pH, orden de adición de los reactivos, temperatura de la mezcla, tiempo de reposo y tratamiento térmico. Para evaluar el efecto de dichos parámetros, se hicieron varias síntesis en las que se manipuló una variable por ensayo.
Los resultados intermedios y finales, se evaluaron por medio de difracción de rayos X y espectroscopía de infrarrojo con transformada de Fourier.
2. MATERIALES Y MÉTODOS
Las soluciones acuosas iniciales se prepararon utilizando Nitrato de Calcio tetrahidratado (Ca(NO3).4H2O) (Aldrich) y Fosfato amónico (H2(PO4)NH4) (Aldrich) en concentraciones 1M y 0.48M respectivamente.
Para evaluar la influencia del pH sobre el producto final, en los ensayos correspondientes a las muestras 1-9 (Ver Tabla 1), las soluciones se basificaron una vez preparadas antes de mezclarse, utilizando hidróxido de amonio p.a. (Aldrich) hasta alcanzar un pH de 1011, mientras que en los ensayos correspondientes a las muestras 10-13 (Tabla 1), las soluciones se utilizaron con su pH característico de 6 para el nitrato de calcio y de 8 para el fosfato de amonio de tal manera que al realizar la mezcla, el pH de la mezcla resultó ser 5.
]]> Tabla 1. Muestras y parámetros que se variaron durante la síntesis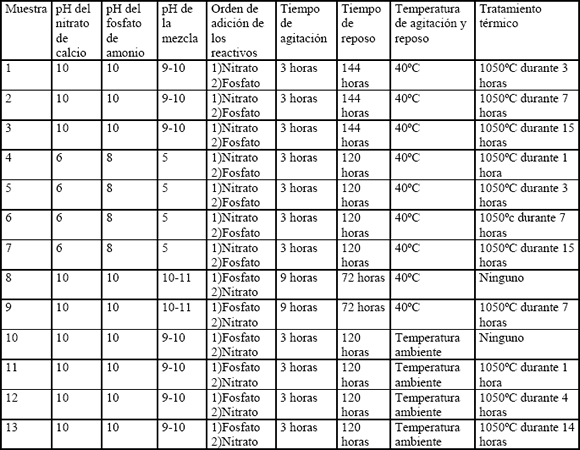
Una vez preparadas las soluciones acuosas y basificadas según la necesidad, se mezclan siguiendo un orden determinado, que varía según el ensayo, dejando caer lentamente un producto sobre el otro en un balón con permanente agitación a 240 rpm. La agitación continúa durante 3 a 9 horas una vez mezclados los dos productos. Posteriormente, la mezcla se deja reposar, bien a temperatura ambiente o a 40ºC durante tiempos variables, según el ensayo. Luego del reposo, se recupera el precipitado, se lava con agua destilada y se deja secar lentamente a 60ºC. Después de secado, el polvo se somete a 1050ºC durante tiempos variables de acuerdo con las condiciones del ensayo, luego de lo cual se evalúan las fases cristalinas presentes en el producto final por medio de difracción de rayos X en un equipo Siemens difrac 5000. Las diferentes variables experimentales que se utilizaron en los 13 ensayos efectuados para la obtención de hidroxiapatita, pueden observarse en la Tabla 1.
Con el fin de evaluar la cinética de las reacciones y el efecto que tienen las variables analizadas sobre ésta síntesis, se realizó un ensayo en el que se tomaron muestras líquidas de la mezcla inmediatamente se terminó de añadir el nitrato al fosfato (mezcla 0 horas) y 9 horas después de agitarla permanentemente (mezcla 9 horas), muestras del precipitado formado al dejar en reposo la mezcla a 40ºC durante tiempos de 24 horas, 48 horas, 72 horas y 115 horas, y muestra después de haber lavado el precipitado y haberlo sometido a un tratamiento térmico a 1050ºC durante 7 horas. A estas muestras se les realizaron análisis de espectroscopia de infrarrojo con transformada de Fourier en un equipo Perkin Elmer 1760 en el intervalo de 4000 a 400 cm-1. Para las muestras sólidas, se mezclaron 2 mg. de la muestra problema con 2 mg. de KBr usando un mortero de ágata, seguido de la aplicación de una presión de 100 MPa para formar las pastillas. Para las muestras líquidas, se utilizó una celdilla con ventanas de AgCl.
3. RESULTADOS Y DISCUSIÓN
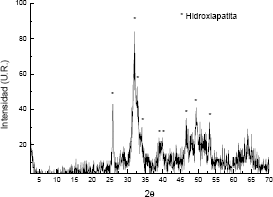
La Figura 1 muestra el difractograma de rayos X de la muestra 2. Se puede observar que para una mezcla hecha con las soluciones iniciales basificadas a pH 10, agregando el fosfato de amonio al nitrato de calcio, un tiempo de agitación de 3 horas a 40ºC, un tiempo de envejecimiento de 6 días, y un tratamiento térmico de 7 horas a 1050ºC, se obtiene una formación incipiente de hidroxiapatita con un alto porcentaje de fase amorfa.

Figura 1. Difractograma de rayos X de la muestra 2.
Figure 1. XRD spectra of the sample 2
El pH juega un papel fundamental en la formación de hidroxiapatita cristalina. En las pruebas correspondientes a las muestras 5-7, el pH de la mezcla no se varió con la adición de hidróxido de amonio y la síntesis se realizó a pH 5. Como resultado, se obtuvo una mezcla de fosfatos cálcicos amorfos. A pesar de que estas muestras se sometieron a 1050 ºC durante 15 horas, no hay presencia de hidroxiapatita en el producto final; por el contrario, continúa la formación de fase amorfa en gran cantidad. Esto se comprobó mediante difracción de rayos X. A pH básico, la solubilidad decrece y la presencia de OH- favorece la precipitación de fosfatos de calcio hidratados.
La Figura 2 muestra el difractograma de rayos X de la muestra 9. Aquí se puede observar, que para una síntesis hecha con el pH de las soluciones iniciales ajustado a 10, adición de nitrato de calcio al fosfato de amonio, un periodo de agitación de 9 horas, un periodo de envejecimiento de 3 días a 40ºC y un tratamiento térmico de 7 horas a 1050ºC, resulta en la presencia de una fase cristalina adicional (fosfato tricálcico [9]).
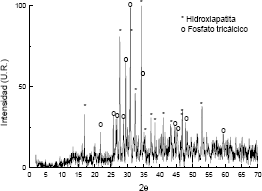
Figura 2. Difractograma de rayos X de la muestra 9.
Figure 2. XRD spectra of the sample 9.
La Figura 3 presenta el difractograma de rayos X de la muestra 11. En ella se puede observar que con soluciones iniciales con pH ajustado a 10, adición de nitrato de calcio al fosfato de amonio, periodo de agitación de 3 horas, periodo de reposo de 5 días, y tratamiento térmico de 1 hora a 1050 ºC, fueron suficientes para obtener hidroxiapatita bien cristalizada como la única fase presente en la muestra. Las muestras preparadas con un tratamiento térmico más prolongado (muestras 12 y 13) no muestran diferencias significativas respecto a la que fue tratada térmicamente solo una hora. Bajo esas condiciones, la mezcla antes del tratamiento térmico (muestra 10) ya presenta la formación incipiente de hidroxiapatita amorfa.
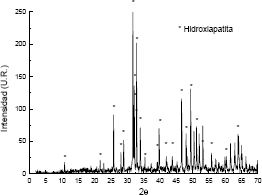
Figura 3. Difractograma de rayos X de la muestra 11.
Figure 3. XRD spectra of the sample 11.
La velocidad de nucleación y crecimiento de cristales determina la aparición de fases cristalinas en la síntesis de un material. Cada especie mineral tiene una cinética característica de nucleación y crecimiento que depende del tiempo que los reactivos necesiten para desempeñar su papel en la reacción. Si este tiempo no se respeta, es posible que se formen otras especies (que no están en equilibrio), porque las reacciones no se completan. En el caso particular de la hidroxiapatita, un periodo de envejecimiento de 5 días fue necesario para obtener reacciones completas que dan lugar a la formación y buen desarrollo de la fase cristalina.
En la reacción del nitrato de calcio con el fosfato de amonio para obtener hidroxiapatita, es necesario inicialmente obtener un equilibrio de los reactivos en medio acuoso. Por ello, es necesario estabilizarlos antes de la reacción. El ion fosfato tiene menor solubilidad que el ion nitrato. Cabe la posibilidad que, cuando el fosfato de amonio se adicione al nitrato de calcio, una buena cantidad de fosfato de amonio precipite y esto no permite la reacción con el calcio para la formación de hidroxiapatita. Cuando el orden de adición de los reactivos se invierte, la reacción se favorece por la alta solubilidad del nitrato de calcio.
La Figura 4 muestra los espectros de infrarrojo con transformada de Fourier para las muestra liquida correspondiente a la mezcla después de 9 horas de agitación y para muestras sólidas correspondientes al precipitado luego de un reposo de 24 y 115 horas, luego de haberlo sometido a un tratamiento térmico de 1050ºC durante 7 horas y para una hidroxiapatita comercial (CEROS 80, USA).
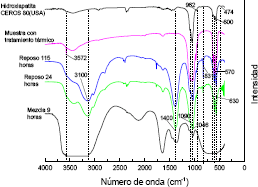
Figura 4. FTIR obtenidos durante distintas etapas del proceso de síntesis de la hidroxiapatita
Figure 4. FTIR spectra for samples obtained during different stages of the process
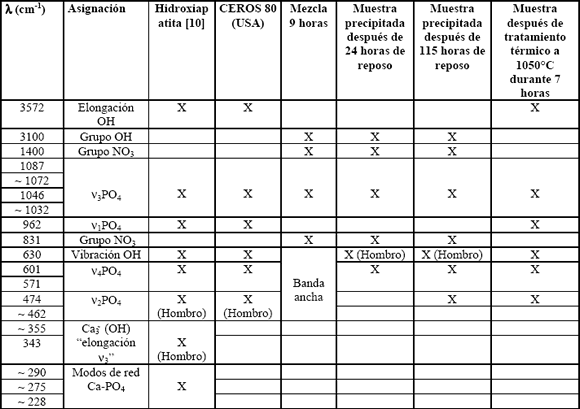
La Tabla 2 resume las frecuencias asignadas de los FTIR para la hidroxiapatita [10], la muestra de hidroxiapatita comercial (CEROS 80, USA) y para todas las etapas de preparación de la muestra en estudio.
Tabla 2. Frecuencias (cm-1) y asignaciones para hidroxiapatita [2], Hidroxiapatita comercial (ceros80, USA), y para las muestras recuperadas durante diferentes etapas de la síntesis de hidroxiapatita de la muestra 2.
Table 2. Frequencies (cm-1) and assignments for hydroxyapatite [11] , Commercial hydroxyapatite (ceros80, USA ), and for all the stages of preparation of the studied sample. ]]>
Para un tiempo de envejecimiento de 24 horas, se observan bandas bien definidas a 570 cm-1, 600 cm-1, 1046 cm-1 y 1090 cm-1 así como un hombro pequeño a 630 cm-1. De acuerdo a las asignaciones de la Tabla 2, estas bandas corresponden a los modos de absorción de los grupos PO4 [1] en la hidroxiapatita y el hombro a 630 cm-1 corresponde a una banda vibracional de OH- en el mismo material [1,4]. La presencia de estas bandas en las muestras sometidas a diferentes tiempos de envejecimiento, indican que la estructura de la hidroxiapatita se forma desde el principio del proceso. La pequeña banda a 474 cm-1 y la mejor definición de las correspondientes a los grupos PO4 para un tiempo de envejecimiento de 115 horas y para la muestra sólida tratada térmicamente, muestra la relevancia de ambos factores en la síntesis. Un periodo mas largo de envejecimiento y un tratamiento térmico apropiado, hace que las bandas correspondientes a los grupos PO4 se definan mejor en la estructura de la hidroxiapatita.
Las bandas que aparecen a 831 cm-1 y 1400 cm-1, que se definen con el reposo, permanecen invariables en el tiempo y casi desaparecen con el tratamiento térmico, corresponden a grupos NO3.
4. CONCLUSIONES
El pH de la mezcla es uno de los factores decisivos en la cristalización de hidroxiapatita. Los pH básicos (10-11) favorecen la formación de hidroxiapata bajo las condiciones de precipitación estudiadas.
El orden en que se añaden los reactivos para realizar la mezcla es muy importante. Se debe añadir lentamente el nitrato de calcio al fosfato de amonio pues de lo contrario, se dificulta la formación de hidroxiapatita pura y cristalina.
El tiempo de reposo, juega un papel importante en la síntesis de hidroxiapatita pura. Para tiempos de reposo menores que 5 días, se forma además de la hidroxiapatita, fosfato dicálcico y fases amorfas no definidas.
La temperatura de la síntesis no parece desempeñar un papel preponderante en la formación de hidroxiapatita. Tanto a temperatura ambiente como a 40ºC es posible formar hidroxiapatita pura, bien cristalizada.
El tratamiento térmico es crucial a la hora de definir las fases cristalinas presentes en la mezcla. Bajo las condiciones ideales basta con un tratamiento térmico de 1 hora para lograr sintetizar hidroxiapatita pura y bien cristalina. Bajo otras condiciones, se hace necesario prolongar el tratamiento térmico hasta por 15 horas para lograr este efecto.
De las condiciones estudiadas, las mejores para la obtención de hidroxiapatita cristalina pura, son:
REFERENCIAS [ Links ][2]
AGRADECIMIENTOS
Este trabajo ha sido financiado parcialmente por CYTED, Proyecto VIII-9 y Red VIII-E, DINAIN proyecto DI00C272 y DIME proyecto 30802494 de la Universidad Nacional de Colombia.
]]>