MINERALOGICAL EVOLUTION OF PORTLAND CEMENT DURING HYDRATION PROCESS
MANUEL ALEJANDRO GIRALDO M.
Ingeniero Geólogo magirald@unalmed.edu.co
JORGE IVÁN TOBÓN
Ingeniero Geólogo, MSc. Profesor Asociado, Universidad Nacional de Colombia, Medellín: jitobon@unalmed.edu.co
Recibido para revisar 25 de Abril de 2005, aceptado 29 de Agosto de 2005, versión final 29 de Septiembre de 2005
RESUMEN: Se presenta la evolución mineralógica del cemento Pórtland tipo I durante el proceso de hidratación, usando las técnicas de caracterización de materiales difracción de rayos X (DRX) y microscopia electrónica de barrido (SEM), con el fin de entender los cambios que se dan en los minerales anhidros del cemento (alita, belita, celita y felita entre otros) durante su transformación en las fase estables hidratadas (tobermorita, ortlandita, etringita, etc.).
Se encontró que, en general, el proceso de hidratación ocurre de manera diferente en cada mineral ya sea por la velocidad de reacción, o por los cambios cristalinos experimentados por éstos durante la transformación de fase anhidra a hidratada. Se pudo apreciar la formación de tobermorita gel (CSH), portlandita y etringita primaria. Además, como cambia la apariencia de la pasta a medida que avanza la hidratación.
PALABRAS CLAVE: Evolución mineralógica, minerales del cemento, SEM, DRX
]]> ABSTRACT: An investigation about mineralogical evolution during hydration process of the portland cement was carried out in this work using techniques of materials characterization, such as X ray diffraction (XRD) and scanning electron microscopy (SEM) in order to understand the behaviour shown by the different minerals of the cement (alite, belite, celite and felite) and their transformation in the stables hydrate phases (tobermorite, portlandite, ettringite)It was found that, in general, the hydration process happens in a different way in each mineral either because of the reaction speed, or the crystalline changes experienced by them in the transformation from the anhydrous to the hydrated phase. The tobermorite gel (CSH), portlandite and ettringitre formation and the changing in appearance of the paste during the hydration advances, could be appreciated.
KEY WORDS: Mineralogical evolution, Cement minerals, SEM, XRD.
1. INTRODUCCIÓN
En la industria del cemento Pórtland, conocer la composición química de la materia prima, de los productos intermedios y del producto final es de vital importancia, tanto para el desarrollo del proceso de fabricación
como para obtener un producto que cumpla con las especificaciones técnicas esperadas. Por esto, las reacciones que se dan en la pasta hecha de cemento mezclado con agua han sido ampliamente estudiadas con técnicas que analizan principalmente sus propiedades físicas y químicas.
Por medio de métodos de caracterización se puede lograr un entendimiento más acertado del comportamiento de las pasta de cemento Pórtland tipo I durante el proceso de hidratación, lo que deriva en un conocimiento más real de los mecanismos de generación de propiedades como la resistencia y la durabilidad, las cuales son unas de las más importantes cuando se trata de seleccionar un cemento para una aplicación específica.
Este trabajo se realizó con el ánimo de aportar más elementos para la comprensión del proceso de hidratación de los diferentes minerales que constituyen la pasta del cemento, haciendo un seguimiento del desarrollo mineralógico en la pasta del cemento a diferentes edades de fraguado (3, 7 y 28 días).
2. GENERALIDADES
La hidratación del cemento es función de las reacciones entre los minerales del cemento (C3S, C2S, C3A, y C4AF) y el agua, además, de la presencia de yeso y otros aditivos. Los productos de las reacciones son principalmente silicatos de calcio hidratados, hidróxido de calcio y sulfoaluminatos de calcio hidratados, así:
]]> El C3S (alita) es el silicato cálcico más inestable de los presentes en el cemento, al reaccionar con el agua se convierte en silicato de calcio hidratado, conocido como tobermorita gel, y en hidróxido de calcio, así: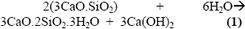
El silicato dicálcico (C2S - belita) al hidratarse también se convierte en tobermorita gel, y en hidróxido de calcio, pero a diferencia de (1) se produce menos hidróxido de calcio:
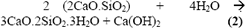
El aluminato de calcio (C3A - celita) al combinarse con yeso y agua produce la etringita:
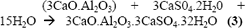
El aluminato de calcio con la etringita y con agua se convierte en monosulfato:
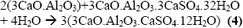
El aluminato de calcio (C3A) con el hidróxido de calcio y con agua se convierte en aluminato de calcio hidratado:
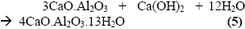
Tobermorita gel (CSH): Es el responsable de la armazón interna de la pasta de cemento, de la adherencia de ésta con los áridos en los morteros y hormigones y, en definitiva, de la resistencia mecánica de estos conglomerados (Calleja, 2001) por lo que resulta un constituyente de la pasta indispensable y siempre positivo.
Portlandita (hidróxido de calcio). Tiene efectos positivos en tanto que es el encargado de mantener el pH de la pasta en valores altos (12-13) pues actúa como una reserva alcalina, mantiene a los hormigones armados protegidos contra la corrosión electroquímica. También es positiva en el caso de hormigones y morteros con áridos calizos, ya que en ellos la adherencia árido-pasta es mayor que en el caso de los áridos silíceos (Calleja, 2001).
También tiene efectos negativos tales como: solubilidad en agua y fácilmente lixiviable por disolución; puede reaccionar con sulfatos y cristalizar en forma de dihidrato dando lugar a procesos de expansión y ruptura y posteriormente a la formación de etringita; es el primer material en descomponerse a altas temperaturas (600ºC) en caso de incendio generando el desplome de la estructura (Calleja, 2001). Varios de estos aspectos negativos pueden controlarse con la adición de puzolanas (cenizas volantes, humo de sílice, escoria de hornos, etc.)
En el microscopio electrónico la portlandita se presenta normalmente en forma de plaquetas hexagonales delgadas, a menudo de décimas de micrómetros de ancho, pero después se convierten en depósitos masivos (Diamond 1976, en Neville 1995)
Etringita (trisulfoaluminato de calcio): Los cristales de etringita son de formas alargadas, generalmente en hábitos fibrosos o en forma de varillas alargadas que se encuentran formando estructuras que asemejan un enrejillado que le da al cemento mayor cohesión, ya que se trata de la etringita positiva, pues la que genera expansión se encuentra generalmente dentro de las fisuras y grietas y se produce en edades tardías (mayores a 28 días) según lo afirman Marusin et al 2000: la etringita se encuentra generalmente en las fisuras del concreto dañado, alrededor de las partículas de agregado o en microfisuras de la pasta del cemento. Autores como Abo-el-Enein, Salah A.; Salem, Th. M.; Hekal, Eisa E. (1988) han sugerido que la formación de etringita conlleva a una expansión debido a su crecimiento orientado. Estos últimos autores plantean también que la expansión asociada a la formación de etringita depende de las condiciones de curado.
3. METODOLOGÍA
A 32 muestras de cemento, provenientes de una misma fábrica en diferentes fechas, se les hicieron análisis mineralógicos a 3, 7 y 28 días de fraguado mediante DRX (RIGAKU modelo MINIFLEX, con una lámpara de cobre de longitud de onda de 1.548 Å) y SEM (marca JEOL y referencia JSM 5910 LV), para un total de 192 especímenes analizados. Las muestras se prepararon de acuerdo con la norma NTC 112, usando las siguientes cantidades: Cemento 200 g, Arena estandarizada 550 g, Relación agua/cemento 0.47; una vez terminada la preparación la muestra se vertía en moldes de PVC de ½ pulgada de diámetro y 1 cm de altura. Se dejaba secar en un cuarto de curado a 23ºC ± 2ºC durante 24 horas y luego se desmoldaban y se sumergían en agua saturada en cal hasta alcanzar la edad de análisis (3, 7 y 28 días). Una vez cumplido el tiempo de curado las muestras eran extraídas del tanque de almacenamiento, sumergidas en acetona para parar la hidratación.
Las muestras para SEM se pulían con diferentes lijas (150, 400 y 600) y con varios abrasivos de alúmina (1, 0.3 y 0.05 micras) para darle el acabado espejo a la superficie. Se les hacía vacío, se metalizaban con oro por un tiempo de 150 segundos que era el que mejor resolución permitía, y se procedía a la observación.
Las muestras de DRX se trituraban hasta pasante malla 200 intentando que la mayoría de granos de arena quedaran retenidos, con el fin de que el cuarzo no enmascarara los picos de las fases que se quería estudiar, se empacaba y se llevaba al laboratorio respectivo para ser analizado.
]]> 4. RESULTADOS Y ANÁLISIS4.1 DIFRACCIÓN DE RAYOS X (DRX)
4.1.1 DRX a tres días: A esta edad de fraguado se detectaron los picos característicos de los principales productos de hidratación, los picos más resaltables de los difractogramas corresponden a tobermorita gel, está ubicado en el valor 2q = 29,12. El segundo pico más destacado corresponde a la portlandita ubicado a un valor de 2q entre 17.5 y 17.8. Los picos menores que se presentan en el difractograma corresponden en su mayoría a valores menores de la fase tobermorita (Figura 1). En el 80% de los difractogramas se observó un pico levemente insinuado que corresponde a la fase etringita, ubicado a un valor 2q de 8.6. lo cual se debe principalmente a que la este mineral es tan escaso que sus picos son opacados por las fases minerales más abundantes, como se confirmó por la observación al microscopio electrónico y como ya lo habían anotado otros investigadores (Hime et al, 2000) refiriéndose a los inconvenientes del DRX como herramienta para estudiar la presencia de etringita en la pasta: " La limitada habilidad para detectar definitivamente la etringita debido a las bajas concentraciones o a interferencias de los picos principales de otros componentes en el concreto."
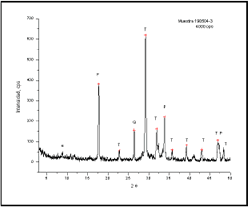
Figura 1. Mineralogía presente a tres días de hidratación (e: etringita, P: portlandita y T: tobermorita)
Figure 1. Mineralogy to three days of hydration (e: ettringite, P: portlandite y T: tobermorite)
Por los resultados obtenidos a partir de este método se puede afirmar que la fase más abundante a esta edad es la tobermorita, pues es la que mayor cantidad de picos presenta y la que alcanza una mayor intensidad.
4.1.2 DRX a siete días: A esta edad de fraguado se presenta un patrón similar al observado en los difractogramas de tres días (Figura 2). Como característica importante se puede resaltar el hecho de que a esta edad de fraguado es mucho más común encontrar el pequeño pico en el valor 2q = 8.6 ± 0.3, correspondiente a la fase etringita, quien a esta edad de hidratación se manifiesta de manera más evidente en el 85% de las muestras, debido a que está mejor cristalizada que a tres días de fraguado, lo cual se nota en la altura del pico, que aumenta levemente de intensidad respecto al valor alcanzado a tres días, a pesar de que sigue siendo una fase menor en comparación con el gel de tobermorita y la portlandita cuyos picos se presentan de manera más pronunciada y con mayor intensidad en los gráficos.
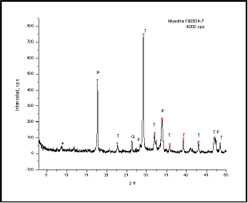
Figura 2. Mineralogía presente a siete días de hidratación (e: etringita, P: portlandita y T: tobermorita) ]]>
Figure 2. Mineralogy to seven days of hydration (e: ettringite, P: portlandite y T: tobermorite)
4.1.3 DRX a veintiocho días: El patrón mostrado a esta edad de hidratación es similar al obtenido a tres y siete días, se puede destacar a esta edad los valores en la intensidad alcanzados por el pico principal de tobermorita en los diferentes difractogramas, los cuales son muy altos, la mayoría de ellos superiores a 600 cps, lo cual tiende a disminuir los valores de intensidad alcanzados por las fases menores (Figura 3).
A esta edad de fraguado la etringita resultaba bastante difícil de reconocer, ya que debido a la baja intensidad de su pico característico (menor a 50 cps) es opacado en gran medida por los altos valores alcanzados por la fase tobermorita, podía fácilmente confundirse con el background propio de la muestra; por lo que el pico de etringita se pudo contar aproximadamente en el 53% de las muestras.
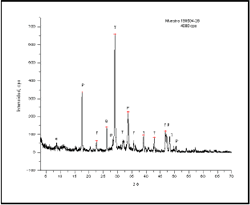
Figura 3. Mineralogía presente a 28 días de hidratación (e: etringita, P: portlandita y T: tobermorita)
Figure 3. Mineralogy to 28 days of hydration (e: ettringite, P: portlandite y T: tobermorite)
4.1.4 Evolución de la hidratación por DRX: De los difractogramas obtenidos para las diferentes muestras se puede abstraer una tendencia general (Figuras 1, 2 y 3):
Cuando se comparan las edades de tres y siete días se observa que a medida que avanza el tiempo de hidratación se presenta una disminución relativa en la diferencia de intensidades entre los picos principales de la fase tobermorita y la fase portlandita, es decir, la diferencia entre la intensidad del pico principal de tobermorita y portlandita presenta una disminución progresiva. Esta intensidad se estima midiendo la altura del pico respectivo en el eje Y y calculando la diferencia entre ambos. Lo mismo sucede cuando se comparan entre sí las edades de tres y veintiocho días. Sin embargo, la tendencia observada a partir de los difractogramas varía respecto a la mencionada anteriormente cuando se comparan las edades de 7 y 28 días, ya que entre estas dos edades de hidratación lo que se observa es un aumento de la diferencia entre ambas.
Una explicación posible para este hecho es que desde que el cemento comienza su hidratación se presenta una reacción de los minerales anhidros para formar tobermorita y portlandita, generándose de forma más rápida la tobermorita gel que se forma a partir de la alita, quien tiene una tasa de reacción mayor que la belita, mientras que la formación de portlandita ocurre de forma más lenta y por eso a los tres días la diferencia entre ambos picos es tan notoria. A medida que trascurre el tiempo de fraguado se alcanza a generar mayor cantidad de portlandita, por lo que en los difractogramas correspondientes a siete días la diferencia entre los picos de ambas fases minerales se reduce. Por último, a la edad de veintiocho días la diferencia entre ambos picos es muy pronunciada debido a que la abundancia de la fase tobermorita es mucho mayor relativa a la de la portlandita, además, vale la pena recordar que la intensidad de los picos en difracción de rayos X está referida tanto a la cantidad relativa de la fase mineral, como a su cristalinidad. Por tanto, se podría afirmar que a la edad de 28 días hay un contenido mayor de tobermorita gel que supera con gran ventaja la cristalinidad de la fase portlandita.
También se nota que a medida que avanza la hidratación el pico correspondiente a la etringita (2q = 8.6) se va definiendo cada vez mejor. Lo que implica que hay un aumento progresivo en la cristalinidad de esta fase mineralógica a medida que avanza la hidratación. Esta tendencia se observó en el 65% de las muestras, en las restantes no fue posible determinarla debido a que el background presente en el difractograma no permitía diferenciar los picos de etringita.
]]> 4.2 MICROSCOPÍA ELECTRÓNICA DE BARRIDO (SEM)4.2.1 SEM a tres días: Se encontró tobermorita gel como la fase hidratada más abundante, constituyendo la matriz. Se pudo apreciar que los cristales de C3S a medida que reaccionan van perdiendo su euhedralidad, convirtiéndose progresivamente en tobermorita de poca cristalinidad y de apariencia amorfa, esto se puede notar ya que los limites de los lados del cristal original no se observan bien definidos sino levemente insinuados a medida que se da la reacción (Figura 4).

Figura 4. Tobermorita a tres días.
Figure 4. Tobermorite to three days
También sucede que los granos de C3S, a medida que se hidratan y se van convirtiendo en tobermorita, se van uniendo los unos a los otros creando de esta forma una matriz continua y en forma de capas, a los que están unidos difícilmente se les diferencia el contorno de sus lados, mientras que este límite es más evidente en los cristales aislados (Figura 5). Además, En las diferentes muestras se observó la presencia de la fase portlandita, la cual se reconoce por su forma de cristalización en láminas o plaquetas hexagonales delgadas (Figura 5).

Figura 5. Formación de tobermorita gel.
Figure 5. Growth of tobermorite gels
A esta edad, es común encontrar cristales de minerales que aún no reaccionan completamente pues su proceso de hidratación es muy lento comparado con la tasa de reacción de la alita, especialmente la belita (C2S). Se observó etringita, en muy poca cantidad comparada con las otras fases como se expuso en difracción de rayos X, Las manifestaciones de etringita se encontraron de manera puntual y en pequeñas cantidades.
]]> Por otra parte, frecuentemente se encontraron fisuras debidas al calor de hidratación, producidas por las reacciones exotérmicas de hidratación. Estas fisuras se pueden reconocer porque se presentan rodeando los granos, en lugar de atravesarlos como ocurriría con otro tipo de fisuras (Figura 6).
Figura 6. Fisuras de hidratación
Figure 6. Hydration fissures
4.2.2 SEM a siete días: A esta edad fue posible reconocer los minerales en un estado mayor de hidratación, los minerales que no tienen una alta tasa de reacción se pueden distinguir fácilmente, como el caso del C2S, que se observa con un halo de reacción característico que empieza en la parte externa del mineral y se va extendiendo hacia adentro del mismo conforme avanza su estado de hidratación (Figura 7). A esta edad de hidratación el halo de reacción que envuelve las belitas presenta una mayor área cubierta que la observada a tres días, lo cual es indicativo del avance progresivo de la hidratación.
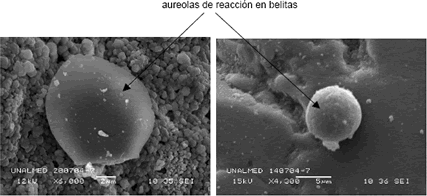
Figura 7. Belitas a siete días de hidratación.
Figure 7. Belites to seven days of hydration.
Se pudo observar claramente la diferencia en la velocidad de hidratación entre la alita y la belita, ya que es posible observar la aureola de reacción levemente insinuada en la belita, sin que se presente un cambio en la forma del mineral, mientras que los cristales de alita presentan un mayor grado de hidratación evidenciado en la pérdida de su euhedralidad característica (Figura 8).
 ]]>
Figura 8. Alita y belita en proceso de hidratación.
]]>
Figura 8. Alita y belita en proceso de hidratación.
Figure 8. Alite and belite in hydration process.
A esta edad se presenta una mayor formación de tobermorita lo cual está evidenciado en una mayor continuidad de la matriz, en ella es posible distinguir los minerales que se han transformado en gel pues todavía se insinúan los bordes del mineral anhidro.
Se pudo observar diferente tipos de tobermorita, la que predomina es la de agregado botroidal o en racimos donde puede notarse como las partículas que se hidratan se adhieren progresivamente una a la otra debido a fuerzas de Van Der Waals (Powers,1958 y Chatterji, 2003) para formar la ligazón propia del cemento, sin embargo, no se puede decir con exactitud, teniendo como criterio la morfología de la tobermorita, a partir de cual silicato cálcico se forma, pues a pesar de lo afirmado por Balázs et al, 1997 refiriéndose a la diferencia en la velocidad de hidratación entre el C3S y el C2S : lo más importante es la diferencia en la cinética debido a que la estructura de C3S es menos densa, entonces el proceso de hidratación tiene una tasa mayor que en el caso del denso empaquetamiento del b-C2S.
En el caso de los mecanismos existen diferencias y semejanzas. En ambos casos hay un mecanismo topoquímico, aunque la calidad, cantidad y morfología de los productos de reacción pueden diferir considerablemente no dan parámetros claros para distinguir morfológicamente el gel proveniente de uno u otro silicato cálcico.
Las portlanditas a esta edad se presentan con un aumento considerable en la cristalinidad, aparecen mejor cristalizadas, ya que es posible apreciar con claridad sus bordes bien definidos y la forma hexagonal que las caracteriza (Figura 9), también se encuentran los cristales menos dispersos. Se puede decir que las portlanditas bien cristalizadas se forman a partir del silicato tricálcico, ya que según lo afirmado por Balázs et al, 1997: Uno de los productos de hidratación tanto de C3S como de b-C2S es el Ca(OH)2, portlandita, aunque su grado cristalino es diferente: el Ca(OH)2 proveniente de C3S está bien cristalizado y se deshidrata a @ 50°C, mientras que el proveniente del C2S es mucho menor en cantidad y es casi amorfo.

Figura 9. Portlanditas formadas a siete días de hidratación
Figure 9. Portlandites formed to seven days of hydration
La etringita observada a esta edad se presenta bien cristalizada, en forma de agujas (Figura 10) y de un tamaño inferior a 1 micra, no se trata de una fase muy abundante, ya que las manifestaciones de este mineral son muy puntuales y no se observaron distribuidas a lo largo de toda la muestra.
]]>
4.2.3 SEM a veintiocho días: A esta edad se observa un gran desarrollo de la tobermorita, conformando una matriz mucho más densa, compacta y continua que en las muestras a edades menores. Para lograr identificar formas cristalinas dentro de la pasta a esta edad de curado se requieren grandes aumentos (mayores a 5000X), mientras que a edades inferiores se observaban con 2000 aumentos (Figura 11).

Figura 11. Tobermorita gel compacta a 28 días de hidratación
Figure 11. Tobermorite gel dense to 28 days of hydration
En contraste con la formación compacta del gel se observó la lenta tasa de reacción de la belita, a quien todavía a esta edad se le puede reconocer por su forma redondeada característica, pero la aureola de hidratación se extiende casi completamente a todo el mineral, quedando el contraste de color sólo en una pequeña parte de la esfera, lo que es indicativo de que la hidratación se encuentra en un estado bastante avanzado (Figura 12).

Figura 12. Belitas a 28 días de hidratación. ]]>
Figure 12. Belites to 28 days of hydration
En las portlanditas no se encontró un cambio notorio con respecto a lo observado a siete días. A esta edad presentaron un buen desarrollo cristalino, con sus lados bien delimitados y con la forma característica de plaquetas hexagonales (Figura 13).

Figura 13. Portlanditas a 28 días
Figure 13. Portlandites to 28 days of hydration
4.2.4 Evolución mineralógica a partir de SEM: A partir de las observaciones realizadas en las diferentes muestras se puede enunciar una hipótesis sobre la hidratación del cemento Pórtland y como ocurre la evolución mineralógica de los componentes del cemento:
Los aluminatos tricálcicos (C3A) y la belita (C2S) son las fases minerales en las cuales es mucho más evidente que la hidratación ocurre a través de una aureola de reacción que empieza en los bordes de los cristales y se va extendiendo de forma gradual hacia el centro del cristal a medida que avanza el proceso de hidratación, este grado de reacción alcanzado por los minerales está condicionado por la disponibilidad de agua al interior de la pasta, ya que la reacción ocurre primero en superficie y progresivamente el agua alcanza el interior de las partículas. Cabe aclarar que la hidratación sí se da de manera selectiva pues contrario a lo que concluye Browmiller (1952): ...no hay evidencia microscópica de que se formen canales y penetre el agua al interior de las partículas de cemento para hidratar selectivamente algún componente principal... , se puede apreciar que si bien no hay canales si hay minerales que tienen mayor avidez por el agua lo que los lleva a hidratarse primero.
El proceso de hidratación en las tres fases anhidras del cemento se identifican claramente, las celitas (primeras en hidratarse) lo hacen a través de una aureola de reacción que implica cambios de forma cristalina, aunque no de manera muy evidente, ya que de acuerdo a Neville (1995) Probablemente la forma estable del aluminato cálcico hidratado que exista en la pasta de cemento hidratada sea el cristal cúbico C3AH6, pero es posible que primero cristalice el C4AH12 hexagonal y después cambie a la forma cúbica. La alita -C3S- el mineral con la segunda tasa de hidratación más alta presenta un cambio cristalino drástico pasando a ser un gel prácticamente amorfo. Mientras que la belita, que presenta la más baja velocidad de hidratación, evidencia este proceso con halo de reacción muy evidente, estas tasas de hidratación ya las había planteado Browmiller (1952):...el C3A se hidrata más rápidamente que el C3S, que a su vez se hidrata más rápidamente que el C2S...
En el caso de la alita (C3S) desde la edad de tres días de fraguado puede verse una pérdida de cristalinidad progresiva que ocurre desde los bordes, donde los lados del cristal hexagonal característico de esta fase van perdiendo su definición para convertirse en hidrogel (tobermorita), puede además notarse que a medida que estos cristales individuales se van hidratando se atraen los unos a los otros para formar la capa continua que se precia en las imágenes, respecto a esto Powers (1958) y Chatterji (2003) han postulado que la atracción entre los cristales para formar el gel continuo ocurre debido a fuerzas de Van Der Waals. En la superficie compacta se necesita aumentar significativamente la resolución del microscopio electrónico para observar cristales al interior de esta matriz; lo anterior apoya una de las afirmaciones de Browmiller ... cuando progresa la hidratación se verifica una disminución uniforme en el tamaño de las partículas del cemento... es por esto que a mayor edad de fraguado es más complicado obtener imágenes de los cristales que conforman la matriz.
La portlandita (CH) se forma tanto a partir de C3S como de C2S, sin embargo, no hay un criterio microscópico definido para establecer, a partir del hábito mineral, de cual de los dos silicatos cálcicos proviene el cristal. Teniendo en cuenta el porcentaje de C3S y C2S empleado para la fabricación del cemento y las reacciones estequiométricas de hidratación postuladas en el capítulo dos se esperaría mucho más abundancia relativa de CH en las imágenes obtenidas a través del microscopio, pero de acuerdo con lo postulado por Diamond (1976): El Ca(OH)2 liberado por la hidrólisis de los silicatos cálcicos forma plaquetas hexagonales delgadas, a menudo de décimas de micrómetros de ancho, que después se convierten en depósitos masivos sería comprensible el hecho de que no se distinga gran cantidad de portlandita en las imágenes, pues una parte de ellas estaría en forma de depósitos masivos lo cual hace difícil reconocerla del gel de tobermorita en SEM pero no así por DRX.
]]> 5. CONCLUSIONESExiste una diferencia notable en el comportamiento de los minerales anhidros a medida que ocurre el proceso de hidratación.
Los difractogramas muestran un incremento progresivo de las fases hidratadas a medida que avanza este proceso reflejado en la intensidad y definición de los picos. Los picos más prominentes son los correspondientes a tobermorita y a portlandita, estando acompañados por una insinuación leve de picos de etringita en el cemento estudiado.
En la matriz a tres días se observan aún muchos granos de mineral sin reaccionar, a siete días la matriz ya muestra un mayor grado de reacción y no se notan tanto los minerales anhidros pues estos han ido formando una capa más o menos continua que le da la adherencia al cemento (tobermorita), a 28 días se necesita aumentos mayores a 5000 X para lograr distinguir la presencia de minerales o de formas cristalinas dentro de la pasta.
El silicato de calcio que presenta mayor tasa de reacción es la alita, debido a que desde la edad de tres días se aprecia su rápida conversión a gel de tobermorita, además es el constituyente principal del clínker, lo cual lo convierte en uno de los agentes principales para la ganancia de resistencias y otras propiedades mecánicas del cemento. La hidratación de esta fase anhidra involucra la pérdida total de estructura cristalina (hexagonal) para convertirse en la fase hidratada tobermorita gel la cual no tiene un sistema de cristalización definido.
La hidratación de las fases anhidras ocurre a través de una aureola de reacción que ataca primero los bordes del cristal y progresivamente se va extendiendo hacia el centro del mismo, este halo o aureola fue más fácilmente observado en el C2S, debido a la tendencia de este mineral a hidratarse lentamente
La belita mostró una tasa de reacción muy lenta, lo cual implica que su aporte, como generador, a la resistencia mecánica del cemento alcanza gran importancia a edades tardías (mayores a 28 días) y su rol en el desarrollo de resistencias es más bien servir de soporte para mantener los valores obtenidos por minerales como la alita y la celita.
El calor de hidratación liberado durante el proceso de hidratación produce microfisuras caracterizadas por formarse siguiendo el contorno del cristal que reacciona, estas fisuras generan un plano de discontinuidad que interfiere en el correcto desarrollo de la capa de gel encargada de la adherencia y por tanto, en el correcto desarrollo de las resistencias, además estas fisuras se convierten en lugares adecuados para la formación de etringita tardía, cuyos efectos son nocivos por generar expansión y ruptura.
AGRADECIMIENTOS
A la empresa Cementos El Cairo S. A patrocinadora logística y económica del proyecto. A los laboratorios de Petrografía y Microscopía avanzada de la Universidad Nacional y al de Catalizadores y Absorbentes de la Universidad de Antioquia
]]>REFERENCIAS [ Links ][2]