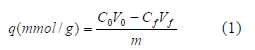
KINETC MODELING BIOSORPTION OF Cr(III) USING ORANGE SHELL
MARTHA LUCIA PINZÓN-BEDOYA
Ingeniera Química Ph.D, Universidad de Pamplona, mlpinzon@unipamplona.edu.co
LUZ ESTELLA VERA VILLAMIZAR
Grupo de Investigación en Recursos Naturales, Universidad de Pamplona, lusvister@gmail.com
Recibido para revisar noviembre 20 de 2008, aceptado marzo 3 de 2009, versión final marzo 30 de 2009
PALABRAS CLAVE: Bioadsorción, Cinética, Cromo, Cáscara de naranja, Modelo de Elovich.
ABSTRACT: In this work it used as bioasorbent material orange peel for removing crhomium ions presents in hypothetical solutions diluted used as model of wastewater with low concentrations of this metal. The used operation conditions were: relationship solid/liquid 4 g/l, particle size F£0,425 mm, initial metal concentration of chromium solution were 100 mg/l (1,923 mmol/l), contact time of 60 h and constant pH (4 and 5). The chosen kinetic models to identify the mechanism reaction of bioasorption process using orgne shell were: first reversible order, pseudo-second order, Elovich and diffusion intraparticular. The results indicate that the Elovich equation provides the greatest accuracy for the kinetic data fit for the equilibrium experimental data. To evaluate the goodness of the fit of data was carried by non-linear regression using as approach the minimization of the function object it adds of the squares of the error, SSE, using as mathematical tool MATLAB.
KEYWORDS: Biosorption, Kinetics, Chromiun; Orange waste, Elovich Model.
1. INTRODUCCION
La presencia de los metales pesados en efluentes líquidos industriales y en corrientes naturales se ha convertido en un tema actual tanto en el campo ambiental como en el de la salud pública.
El aumento de la contaminación ambiental como consecuencia de la creciente utilización de metales pesados es motivo de preocupación, debido a que no son química ni biológicamente degradables. Aún cuando se encuentren presentes en cantidades bajas e indetectables, su persistencia en el recurso hídrico implica que através de algunos procesos naturales pueden llegar a estar biodisponibles con los consecuentes efectos de biomagnificación en los seres vivos. Una vez en un curso de agua, estos pueden permanecer en el ambiente durante cientos de años debido a su alta movilidad en los ecosistemas acuáticos naturales.
La concentración en los seres vivos aumenta a medida que son ingeridos por otros, por lo que la ingesta de plantas o animales contaminados puede provocar intoxicación, dada su alta toxicidad para las formas de vida superiores, considerándose algunos de ellos carcinogénicos [1].
Colombia no es ajena a la problemática de la contaminación ambiental por metales pesados, teniendo especial relevancia la contaminación del recurso hídrico con cromo, ya que la industria de las curtiembres está catalogada como de alta significación ambiental por la presencia en sus efluentes de cromo en sus diferentes estados de oxidación Cr(III) y Cr(VI), lo cual le infiere al recurso hídrico una carga contaminante significativa que impacta negativamente tal recurso. Esta industria se caracteriza por el uso de tecnología de tipo artesanal, en especial las Pequeñas y Medianas Empresas, PYMES, las cuales por su escasa tecnología, poca inversión en infraestructura, baja capacitación de su personal operativo e inadecuada utilización de las materias primas e insumos [2], conllevan a la problemática afrontada en el presente trabajo de investigación. Dentro de este contexto la bioadsorción surge como una alternativa tecnológica para el tratamiento de este tipo de aguas contaminadas, cuando los iones metálicos se encuentran presentes a bajas concentraciones. En el desarrollo de esta investigación se aborda la bioadsorción como alternativa de solución utilizando como precursor un residuo típico regional de bajo costo y de fácil consecución como lo es la cáscara de naranja.
]]>2. BIOADSORCIÓN
La bioadsorción es un proceso de adsorción que consiste en la captación de diversas especies químicas por una biomasa (viva o muerta), a través de mecanismos fisicoquímicos como la adsorción o el intercambio iónico.
El proceso de bioadsorción implica una fase sólida -biomasa- (sorbente o adsorbente) y una fase líquida (solvente) que contiene las especies disueltas (adsorbatos) que van a ser retenidas por el sólido. Para que este proceso se lleve a cabo debe existir afinidad del adsorbente por los adsorbatos, para que estos últimos sean transportados hacia el sólido donde van a ser retenidos por diferentes mecanismos. Esta operación continúa hasta que se establece un equilibrio entre el adsorbato disuelto y el adsorbato enlazado al sólido [3].
El uso de biomasa muerta tiene ventajas sobre la utilización de biomasa viva, ya que en este último no es necesario adicionar nutrientes, el adsorbente resulta inmune a la toxicidad o a condiciones de operación adversas, los procesos no están gobernados por limitaciones biológicas, la recuperación de metales es más fácil y la biomasa se comporta como un intercambiador de iones. No obstante lo anterior, se deben tener en cuenta los inconvenientes que este proceso conlleva tales como: una rápida saturación del sólido, alta sensibilidad hacia los cambios de pH, y el hecho que el estado de valencia del metal no puede ser alterado biológicamente, entre otros [4].
Los primeros intentos en el campo de la bioadsorción se atribuyen a Adams y Holmes (1935) [5]. Estos investigadores describieron la eliminación de iones Ca2+ y Mg2+ por resinas de tanino.
Desde los primeros intentos en la aplicación de la bioadsorción, han transcurrido más de 65 años, pero sólo desde hace dos décadas y por razones fundamentalmente de tipo económico y ambiental, las investigaciones desarrolladas se han centrado principalmente en el empleo de esta técnica para la eliminación de especies metálicas presentes a bajas concentraciones en efluentes líquidos, utilizando materiales bioadsorbentes de bajo costo.
Existen numerosos materiales naturales tales como los microorganismos y las algas que pueden actuar como bioadsorbentes. Las algas constituyen una fuente abundante y económica de biomasa [6]. Las algas marrones, fundamentalmente las del género Sargassum, han mostrado su capacidad para adsorber selectivamente oro a bajos valores de pH [7], además de iones cadmio, cobre, plomo, níquel y zinc [8]. También poseen propiedades potenciales como materiales bioadsorbentes una serie de productos de desecho procedentes de fermentaciones industriales a gran escala tales como: hongos, bacterias y levaduras. Así por ejemplo, el hongo Absidia orchidis es capaz de eliminar eficazmente plomo [9]. Recientemente se reportan trabajos de investigación usando turba [10], desechos de cítricos [11-15], hojas de Neem, árbol medicinal de uso popular en la India [16], entre otros.
3. MATERIALES Y MÉTODOS
]]> 3.1 Ensayos Previos 3.2 Preparación de la Biomasa
Una vez seleccionadas las cáscaras de naranja en buen estado y en cantidad suficiente, se llevó a cabo el tratamiento preliminar de la muestra, el cual consistió en un lavado sucesivo con agua corriente para eliminar impurezas y compuestos solubles adheridos a éste que pudiesen acompañar al material e interferir con posterioridad en el desarrollo de los ensayos. Tras la limpieza, el material fue secado en estufa en un rango de 50 – 60 ºC hasta peso constante, para su posterior reducción y clasificación por tamaños. De esta manera se obtuvo el sólido adsorbente en diferentes fracciones de peso, listo para utilizar en los ensayos posteriores, en concordancia con los resultados obtenidos en los ensayos previos.
3.3 Reactivos
Para la preparación de las soluciones sintéticas de trabajo de 100 mg/l ( 1,923 mM ), se utilizó Cr (NO3)3 9H2O. Los ajustes de pH se realizaron mediante adición de disoluciones 0,01N, 0,1N y 1N de HCl y NaOH. Todos los reactivos empleados en la experimentación fueron de grado analítico, Merck.
3.4 Procedimiento Experimental de los Ensayos de Adsorción
El procedimiento experimental para llevar a cabo los ensayos de adsorción se realizó mediante procesos en discontinuo a temperatura ambiente y pH constante de 4 y 5. El sólido adsorbente se peso e introdujo en un recipiente de vidrio, el que con anterioridad contenía la disolución de 100 mg/l ( 1,923 mM ). Esta mezcla se puso en contacto mediante agitación magnética durante 60 horas, con toma de muestras a diferentes intervalos de tiempo. El pH de las disoluciones se controló mediante la adición de HCl y NaOH para garantizar un valor constante del pH. Finalizado el tiempo de contacto sólido-líquido, se filtro la mezcla con prefiltros de fibra de vidrio (Millipore AP40) y al filtrado se le analizó el contenido del ión metálico presente en la disolución, por espectrofotometría de absorción atómica, en un espectrofotometro Perkin Elmer modelo AA 3000. Todos los experimentos se llevaron a cabo por triplicado, con el objeto de realizar el tratamiento estadístico de la información obtenida, utilizando como criterio el valor medio de las concentraciones de cromo adsorbido por unidad de sólido adsorbente y como error experimental ± dos veces la desviación estándar de los mismos.
La cantidad de cromo adsorbida por la biomasa (mmol/g) se calculó haciendo uso de la siguiente expresión matemática:
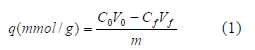
C0 = concentración inicial de cromo en la disolución (mmol/l).
Cf= concentración final de cromo en la disolución (mmol/l).
V0 = volumen inicial de disolución (l).
Vf= volumen final de disolución (l).
m= masa de bioadsorbente utilizada en los ensayos (g).
4. ASPECTOS TEÓRICOS
4.1 Cinética de la Bioadsorción ]]> La cinética de la adsorción describe la velocidad de atrapamiento del adsorbato, lo cual controla el tiempo de residencia de éste en la interfase sólido-disolución y además su conocimiento permite predecir la velocidad a la cual el contaminante se remueve del efluente tratado, por tal razón se requiere el conocimiento de las leyes de velocidad que describen el sistema de adsorción, las cuales se determinan por experimentación y no pueden ser inferidas en ningún caso [18-20].
En general, la remoción de iones metálicos de soluciones acuosas por bioadsorción depende de los mecanismos químicos que involucran las interacciones de los iones metálicos con los grupos activos específicos asociados con la pared celular del biosorbente [21]. Por lo tanto la cinética de la bioadsorción indica la evolución de cada una de las etapas a través de las cuales ésta se lleva a cabo y cuál de ellas es la que controla el proceso (reacción química, difusión y/o transferencia de masa). En este trabajo en particular se tomará como hipótesis que la adsorción de cromo por cáscaras de naranja está controlada por reacción química y no por difusión. Para corroborar lo anterior, se ha considerado usar los modelos que se describen a continuación, a fin de determinar el mejor ajuste de los datos experimentales a cada uno de ellos [18-20], [22], [23-26].
4.1.1 Modelo de Primer Orden Reversible
Este modelo se ha aplicado a varios sistemas de adsorción, tales como cáscaras de cacahuate para la adsorción de Cr(VI), residuos de té y café para la adsorción de Cr(VI), Cd(II) y Al(III), carbón activado para CN-, ceniza volátil para Cr(VI) y ortoxileno, tal y como lo reportan Ho y McKay [18].
La expresión matemática correspondiente a la cinética de primer orden reversible se basa en la suposición de que a cada ión metálico se le asigna un sitio de adsorción del material adsorbente, lo cual en términos de velocidad de reacción se expresa como:
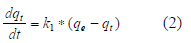
Donde qt (mmol/g) es la cantidad adsorbida en un tiempo t, qe (mmol/g) es la cantidad adsorbida en el equilibrio y k1 (min-1) es la constante cinética de primer orden. Integrando la ecuación (2) y aplicando como condiciones de contorno a t=0, qt=0 y a t=t qt=qt:
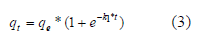
4.1.2 Modelo de Pseudo Segundo Orden
Este modelo fue desarrollado por Ho y McKay [18] y dado a conocer en 1999. En él se supone que el adsorbato se adsorbe en dos sitios activos de la biomasa. A partir de esta fecha, muchas más investigaciones han reportado un mejor ajuste de los datos experimentales obtenidos a este modelo, con coeficientes de correlación superiores a los de los otros modelos ensayados [27-37]. En este caso, la ecuación de velocidad de la cinética de adsorción se expresa como:
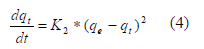
Integrando la ecuación anterior y manteniendo constantes las condiciones de contorno descritas para el modelo anterior, se tiene:
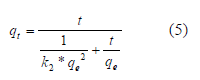
Donde k2 es la constante cinética de Pseudo-segundo orden (g/mmol.min) y h=k2*qe2 siendo h (mmol/g.min) la velocidad inicial de adsorción.
4.1.3 Modelo de Elovich
Este modelo, de aplicación general en procesos de quimiadsorción, supone que los sitios activos del bioadsorbente son heterogéneos [38] y por ello exhiben diferentes energías de activación, basándose en un mecanismo de reacción de segundo orden para un proceso de reacción heterogénea. Este modelo ha mostrado resultados satisfactorios en la identificación del mecanismo controlante en procesos de adsorción de un soluto en fase líquida a partir de un sólido adsorbente [15], [26], [38-40].
La expresión matemática que rige el comportamiento de este modelo es la siguiente:
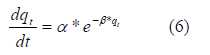
Donde 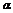 (mmol.g-1.min-1) es la velocidad inicial de adsorción y
(mmol.g-1.min-1) es la velocidad inicial de adsorción y 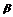 está relacionado con la superficie cubierta y la energía de activación por quimiadsorción (mmol.g-1). Integrando la ecuación y manteniendo constantes las condiciones de contorno descritas para el Modelo de Primer Orden Reversible, se tiene:
está relacionado con la superficie cubierta y la energía de activación por quimiadsorción (mmol.g-1). Integrando la ecuación y manteniendo constantes las condiciones de contorno descritas para el Modelo de Primer Orden Reversible, se tiene:
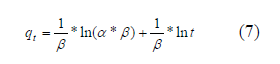
Weber y Morris (1963) concluyeron que en un proceso controlado por la adsorción en los poros, la velocidad inicial es directamente proporcional a la concentración del soluto. La difusión intraparticular se caracteriza por la dependencia entre la adsorción específica y la raíz cuadrada del tiempo, siendo la pendiente la velocidad de difusión intraparticular.
Con base en lo anterior, la ecuación que define la difusión intraparticular viene dada por:
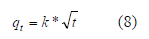
Donde k (mmol.g-1.min-1/2) es la constante de velocidad de difusión intraparticular. Esta ecuación ha sido utilizada por diferentes investigadores [39], [41-43], para determinar si la difusión intraparticular es la etapa controlante de la dinámica de bioadsorción de iones metálicos.
5. RESULTADOS Y ANALISIS
5.1 Datos Experimentales Obtenidos
Para la identificación de la dinámica de bioadsorción de Cr(III) sobre cascaras de naranja, se estudió la evolución de la concentración del cromo en la disolución con respecto al tiempo, a pH 4 y 5. Las condiciones de operación para esta experimentación fueron las siguientes: msólido = 1g; Vdisolución = 500 ml; C[Cr(III)]= 100 mg/l.
En esta gráfica se observa que la cantidad de cromo adsorbida por unidad de masa de sólido adsorbente en función del tiempo, sigue una tendencia exponencial y se encuentra favorecida con el aumento del pH.
Inicialmente la velocidad con que transcurre el proceso es muy elevada y disminuye posteriormente en forma paulatina hasta alcanzar el equilibrio (velocidad de adsorción = 0). El proceso de adsorción se puede dar por finalizado, transcurridos 2400 minutos, desde donde se observa que la concentración de cromo en la disolución, prácticamente permanece constante. Una vez alcanzadas estas condiciones, se obtiene un porcentaje de adsorción de de 44,23% y 61,52%, para pH 4 y 5, respectivamente.
Figura 1. Evolución del % de adsorción contra el tiempo.
Figure 1. Evolution of % adsorption versus time.
5.2 Identificación del Modelo Cinético
Obtenidos los resultados experimentales, se procedió al análisis matemático de los mismos a fin de identificar el modelo cinético que mejor describe el proceso de bioadsorción en consideración. Para ello se realizó el tratamiento matemático de los mismos, utilizando técnicas de ajuste no lineal, haciendo uso de la herramienta matemática MATLAB. Este ajuste se llevó a cabo para los modelos cinéticos de Primer Orden Reversible, de Pseudo Segundo Orden, de Elovich y de Difusión Intraparticular, con el fin de establecer qué modelo predice con mayor exactitud la cinética de bioadsorción.
5.2.1 Modelo Cinético Primer Orden Reversible
Teniendo en cuenta la tendencia exponencial de las curvas representadas en la Figura 1, se podría esperar que los datos cinéticos se ajustaran a un Modelo Cinético de Primer Orden Reversible, teniendo en cuenta lo indicado por Bhattachayra y Venkobachar (1984) [44], quienes establecieron que la cinética de adsorción de metales pesados desde una fase líquida a una fase sólida (biomateriales), se puede explicar como una reacción reversible en donde se establece un equilibrio entre ambas fases [45] y [46].
Con el objeto de comprobar si el proceso de adsorción de iones cromo sobre cascara de naranja, corresponde al modelo cinético de primer orden reversible, se realizó el ajuste no lineal de los datos experimentales a este modelo. Los resultados obtenidos a pH 4 y 5 se muestran en Figura 2.
]]> Los valores de los parámetros característicos obtenidos para los modelos estudiados, junto con los coeficientes de correlación obtenidos, se resumen en la Tabla 1.Como puede observarse en la Figura 2, los datos obtenidos no se ajustan de forma aceptable al modelo, lo que se corrobora con los bajos coeficientes de correlación encontrados, de 0,7740 (pH = 5) y de 0,8317 (pH = 4).
Figura 2. Ajuste de los resultados experimentales al Modelo Cinético Primer Orden Reversible
Figure 2. Fit from experimental results to the First-Order Reversible Kinetics Model
5.2.2 Modelo Cinético de Pseudo-Segundo Orden
Teniendo en cuenta la revisión bibliográfica hecha, donde se reporta un ajuste adecuado de los datos experimentales de procesos de adsorción de metales pesados desde una fase líquida a una fase sólida, a un Modelo Cinético de Pseudo Segundo Orden [47-51], podría esperarse que los datos cinéticos de esta experimentación, se ajustaran a un Modelo Cinético de Pseudo Segundo Orden.En la Figura 3 se observa que los datos experimentales obtenidos no se ajustan de forma aceptable a este modelo. Lo anterior se verifica con el valor del coeficiente de correlación, el cual corresponde a 0,930, por lo que puede asegurarse que los datos experimentales no se ajustan de forma adecuada a este modelo.
Figura 3. Ajuste de los resultados experimentales al Modelo Cinético de Pseudo-Segundo Orden
Figure 3. Fit from experimental results to the Second-Order Kinetics Model
5.2.3 Modelo Cinético de Elovich
A pesar de no encontrarse una amplia bibliografía que reporte un ajuste adecuado de los datos experimentales de procesos de adsorción de metales pesados sobre materiales bioadsorbentes al Modelo Cinético de Elovich, podría esperarse que los datos cinéticos se ajustaran a este Modelo Cinético. Para ello y teniendo en cuenta los criterios establecidos en este trabajo de investigación, se realizó el ajuste correspondiente de los datos a este modelo.
En este modelo el parámetro α está relacionado con la energía de quimiadsorción y el parámetro β con la superficie cubierta. Tal y como puede observarse en la Taba 1, los valores de α aumentan con el valor del pH, es decir el incremento en el pH viene acompañado de un aumento en la velocidad de quimiadsorción. Sin embargo, se observa a su vez una ligera disminución en el parámetro β con el aumento del pH, lo cual indica una disminución de la superficie de adsorción disponible para los adsorbatos con el incremento del pH [15].
Tabla 1. Valores de los parámetros característicos y coeficientes de correlación
Table 1. Value of the characteristic parameters and correlation coefficients
Figura 4. Ajuste de los resultados experimentales al Modelo Cinético de Elovich
Figure 4. Fit from experimental results to the Elovich Kinetics Model
5.2.4 Modelo Cinético de Difusión Intraparticular
A continuación se muestra la representación gráfica del ajuste de los resultados experimentales obtenidos a pH 4 y 5, Figura 5, y sus correspondientes parámetros característicos y coeficiente de correlación de igual forma, se resumen en la Tabla 1.
Figura 5. Ajuste de los resultados experimentales al Modelo Cinético de Difusión Intraparticular
Figure 5. Fit from experimental results to the Intraparticle Diffusion Kinetics Model
5.3 Análisis de la Función Error
Los parámetros característicos que representan la dinámica de la adsorción de iones cromo sobre cáscaras de naranja, fueron obtenidos mediante la técnica de optimización por regresión no-lineal, utilizando como criterio de minimización la función error SCE, suma de los cuadrados del error [45], [52-56], la cual se representa mediante la siguiente expresión:
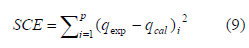
Donde n es el número de puntos experimentales, qexp y qcal corresponden a la cantidad de adsorbato en el equilibrio determinada experimentalmente y la calculada mediante el modelo, respectivamente.
Esta es una expresión ampliamente usada [45], [55], [57], para la optimización de los parámetros característicos en procesos experimentales de bioadsorción, cuando se usan técnicas de regresión lineal y no lineal. En estos casos, generalmente la función objeto utilizada para la minimización es la suma del cuadrado de los errores, SCE. En este trabajo de investigación, este valor corresponde al la ecuación del modelo de Elovich, que sin lugar a dudas es la que proporciona un mejor ajuste de los datos experimentales. Recientes trabajos de investigación confirman el uso de este tipo de tratamiento matemático de la información para la determinación del modelo cinético en procesos de bioadsorción [58]. No obstante lo anterior, también se reporta el valor del error cuadrático medio SECM que da una medida de las diferencias en promedio entre los valores pronosticados y los valores observados, por lo tanto a los valores característicos seleccionados, de acuerdo con el criterio anterior, deberá corresponderles además el menor valor de este parámetro. Los resultados obtenidos se resumen en la Tabla 2.
Tabla 2. Análisis de la función error SSE y r2para cada modelo cinético
Table 2. Analysis of error function SSE and r2 for each kinetics model
6. CONCLUSIONES
]]> Los resultados obtenidos en este estudio indican que las cáscaras de naranja pueden considerarse como un material bioadsorbente potencial para la eliminación de iones Cr(III) de disoluciones acuosas, por lo tanto este material se constituye en una alternativa para el tratamiento de aguas residuales industriales con contenido de este ión metálico.Bajo las condiciones de esta experimentación, la cinética de la bioadsorción de Cr(III) sobre cáscaras de naranja es rápida y el equilibrio se alcanza después de las 40 horas de iniciado el proceso.
El ajuste de los datos experimentales obtenidos a los diferentes modelos seleccionados en este trabajo de investigación, indica que el modelo de Elovich es el que mejor describe la cinética de la bioadsorción de Cr(III) sobre cáscaras de naranja.
Los resultados obtenidos permiten corroborar que el proceso de bioadsorción de Cr(III) sobre cáscaras de naranja está controlado por reacción química y no por difusión intraparticular, tal y como se había supuesto inicialmente.
Los valores de los parámetros característicos del modelo de Elovich, están de acuerdo con las suposiciones sobre las cuales se basa el modelo, ya que α aumenta con el incremento en el valor del pH, es decir el incremento en el pH viene acompañado de un aumento en la velocidad de quimiadsorción y una disminución de la superficie de adsorción disponible, β. Por lo tanto, una disminución en los valores de β indica un agotamiento de la superficie libre de la cáscara de naranja disponible para la adsorción de Cr(III).
REFERENCIAS
[1] CIMINO, G. AND CARISTI, C. Acute toxicity of heavy metals to aerobic digestion of waste cheese whey. Biological Wastes, 33 (3), 201-210, 1990. [ Links ]
[2] PINTO S., J.A. Planes de Acción para el mejoramiento Ambiental de las Curtiembres de San Benito. DAMA, 1996. [ Links ]
[3] CAÑIZARES-VILLABUENA, R. O. Biosorción de metales pesados mediante el uso de biomasa microbiana. Revista Latinoamericana de Microbiología, 42, 131-143, 2000. [ Links ]
[4] MACASKIE, L. E. An immobilized cell bioprocess for the removal of heavy metals from aqueous flows. J. Chem. Tech. Biotechnol, 49, 357-379, 1990. [ Links ]
[5] ADAMS, B.A. AND HOLMES, E.L. Adsorptive properties of synthetic resins. I. J. Soc. Chem. Ind., 54, 1-6, 1935. [ Links ]
[6] KUYUCACK, N. AND VOLESKY, B. Biosorption by algal biomass, in Biosorption of heavy metals. Volesky, B., Ed.; Boca Ratón, FL. 2, 4, 173-198, 1990. [ Links ]
[7] KUYUCAK, N. AND VOLESKY, B. Accumulation of gold by algal biosorbent. Biorecovery, 1, 189-204, 1989. [ Links ]
[8] LEUSCH A. AND VOLESKY B. The influence of film diffusion on cadmium biosorption by marine biomass. Journal of Biotechnology, 43, 1, 1-10, 1995. [ Links ]
[9] HOLAN, Z.R. AND VOLESKY, B. Accumulation of cadmium, lead and nickel by fungal and wood biosorbents. Appl. Biochem. Biotechnol, 53, 133-146, 1995. [ Links ]
[10] HO, Y.S. AND McKAY, G. The kinetics of sorption of divalent metal ions onto sphagnum moss peat. Water Research, 34 (3), 735-742, 2000. [ Links ]
[11] SIVARAJ R., NAMASIVAYAM C., AND KADIRVELU K. Waste Management Orange peel as an adsorbent in the removal of Acid violet (acid dye) from aqueous solutions. Waste Management, 21, 105-110, 2001. [ Links ]
[12] ANNADURAI, G., JUANG, R-S AND LEE,D-J. Use of cellulose-based wastes for adsorption of dyes from aqueous solutions. Journal of Hazardous Materials, 92(3), 263-274, 2002. [ Links ]
[13] GHIMIRE, K.N., INOUE, K., YAMAGUCHI, H., MAKINO, K. AND MIYAJIMA, T. Adsorptive separation of arsenate and arsenite anions from aqueous medium by using orange waste. Water Research, 37, 4945-4953, 2003. [ Links ]
[14] ZHEXIAN X., YANRU T., XIAOMIN L., YINGHUI L. AND FANG L. Study on the equilibrium, kinetics and isotherm of biosorption of lead ions onto pretreated chemically modified orange peel. Biochemical Engineering Journal, (31), 160-164, 2006. [ Links ]
[15] PÉREZ MARÍN A.B, MESEGUER Z.V., ORTUÑO J.F., AGUILAR M, SÁEZ J., LLÓRENS M. Removal of cadmium from aqueous solutions by adsorption onto orange waste. Journal of Hazardous Material, B139; 122-131, 2007. [ Links ]
[16] VENKATESWARLU, P., VENKATA R, M., RAO S.D. , AND VENKATESWARA R., M. Removal of chromium from an aqueous solution using Azadirachta indica (neem) leaf powder as an adsorbent. International Journal of Physical Sciences, 2 (8), 188-195, 2007. [ Links ]
[17] PINZÓN-BEDOYA, M.L Y TAMAYO CARDONA A.M. Caracterización de la cáscara de naranja para su uso como material bioadsorbente. Revista BISTUA, 6(1), 28-37, 2008. [ Links ]
[18] HO,Y.S. AND McKAY, G. Pseudo-second order model for sorption processes. Process Biochemistry, 34 (5), 451-465, 1999. [ Links ]
[19] HO,Y.S. AND McKAY, G. A kinetic study of dye sorption by biosorbent waste product pith. Resourcess Conservations and recycling, 25B, 171-193, 1999. [ Links ]
[20] HO,Y.S. AND McKAY, G. The sorption of lead (II) ions on peat. Water Research, 33 (2), 578-584, 1999. [ Links ]
[21] BAI, R. S. AND ABRAHAM, T. E. Studies on Enhancement of Cr(VI) Biosorption by Chemically Modified Biomasa of Rhizopus nigricans. Water Research, 36, 1224-1236, 2002. [ Links ]
[22] LAGERGREN, S. Zur theorie der sogenanten adsorption gelöster stoffe, Kungliga Svenska Vetenskapsakademiens. Handlingan, Band 24, No. 24 1-39, 1898. [ Links ]
[23] CHEUNG, C.W., PORTER, J.F. AND McKAY, G. Elovich equation and modified second-order equation for sorption of cadmium ions onto bone char. Journal of Chemical Technology & Biotechnology, 75 (11), 963-970, 2000. [ Links ]
[24] CHEUNG, C.W., PORTER, J.F. AND McKAY, G. Sorption kinetics for the removal of copper and zinc from effluents using bone char. Separation and Purification Technology, 19 (1-2), 55-64, 2000. [ Links ]
[25] LOUKIDOU, M.X., ZOUBOULIS, A.I., KARAPANTSIOS, T.D. AND MATIS, K.A. Equilibrium and kinetic modelling of chromium (VI) biosorption by Aeromonas caviae. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 242, (1-3), 93-104, 2004. [ Links ]
[26] ÖZACAR, M. AND SENGIL, I.A. A kinetic study of metal complex dye sorption onto pine sawdust. Process Biochemistry, 40 (2) 565-572, 2005. [ Links ]
[27] NAMASIVAYAM, C. AND KADIRVELU, K. Uptake of mercury (II) from wastewater by activated carbon from an unwanted agricultural solid by-product: coirpith. Carbon,37 (1), 79-84, 1999. [ Links ]
[28] HAMADI N. K., CHEN X. D, FARID M. M. AND LU G. Q. Adsorption kinetics for the removal of chromium (VI) from aqueous solution by adsorbents derived from used tyres and sawdust. Chemical Engineering Journal, 84, 95-105, 2001. [ Links ]
[29] ANOOP KRISHNAN, K. AND ANIRUDHAN, T.S. Removal of Cadmium(II) from aqueous solutions by steam-activated sulphurised carbon prepared from sugar-bagasse pith: kinetics and equilibrium studies. Water S.A. , 29 (2), 147-156, 2003. [ Links ]
[30] BENGUELLA, B. AND BENAISSA, H. Cadmium removal from aqueous solutions by chitin: kinetic and equilibrium studies. Water Research, 36 (10), 2463-2474, 2002. [ Links ]
[31] BANAT , F., AL-ASHEH, S. AND AL-MAKHADMEH, L. Evaluation of the use of raw and activated date pits as potential adsorbents for dye containing waters. Process Biochemistry, 39 (2), 193-202, 2003. [ Links ]
[32] CHEUNG,W.H., Ng,J.C. AND McKAY, G. Kinetic analysis of the sorption of copper(II) ions on chitosan. Jorunal Chemical Technology and Biotechnology, 78: 562-571, 2003. [ Links ]
[33] TATY-COSTODES,V.C., FAUDUET, H., PORTE,C. AND DELACROIX, A. Removal of Cd(II) and Pb(II) ions, from aqueous solutions, by adsorption onto sawdust of Pinus sylvestris. Journal of Hazardous Materials, 105 (1-3), 121-142, 2003. [ Links ]
[34] MACHADO, R., CARVALHO, J.R. AND NEIVA , C.M.J. Removal of trivalent chromium (III) from solution by biosorption in cork powder. Journal of Chemical Technology & Biotechnol, 77 (12), 1340-1348, 2002. [ Links ]
[35] KESKINKAN, O., GOKSU, M.Z.L., YUCEER, A., BASIBUYUK, M. AND FORSTER, C.F. Heavy metal adsorption characteristics of a submerged aquatic plant (Myriophyllum spicatum). Process Biochemistry, 39 (2), 179-183, 2003. [ Links ]
[36] HO, Y.S., CHIU, W.T., HSU, C.S. AND HUANG, C.T. Sorption of lead ions from aqueous solution using tree fern as a sorbent. Hydrometallurgy 73 (1-2), 55-61, 2004. [ Links ]
[37] KESKINKAN, O., GOKSU, M. Z. L., BASIBUYUK, M. AND FORSTER,C.F. Heavy metal adsorption properties of a submerged aquatic plant (Ceratophyllum demersum). Bioresource Technology, 92 (2), 197-200, 2004. [ Links ]
[38] CHEUNG, C.W., PORTER, J.F. AND McKAY,G. Sorption kinetic analysis for the removal of cadmium ions from effluents using bone char. Water Research, 35 (3), 605-612, 2001. [ Links ]
[39] CHEUNG, C.W., CHAN, C.K., PORTER, J.F. AND McKAY, G. Film pore diffusion control for the batch sorption of cadmium ions from effluents onto bone char. J.Colloid Interface Sci., 234 (2) 328-336, 2001. [ Links ]
[40] Ng,J.C.Y., CHEUNG,W.H. AND McKAY,G. Equilibrium studies for the sorption of lead from effluents using chitosan. Chemosphere, 52 (6), 1021-1030, 2003. [ Links ]
[41] ALLEN S.J., WHITTEN L.J., MURRAY M., DUGGAN O. AND BROWN P. The adsorption of pollutants by peat, lignite and actived chars. J. Chem. Tech. Biotechnol, 68, 442-452, 1997. [ Links ]
[42] CHOY, K.K.H., Ko, D.C.K., CHEUNG, C.W., PORTER, J.F. AND McKAY,G. Film and intraparticle mass transfer during the adsorption of metal ions onto bone char. J.Colloid Interface Sci., 271 (2), 284-295, 2004. [ Links ]
[43] CHOY, K.K.H., PORTER, J. F. AND McKAY, G. Film-pore diffusion models-analytical and numerical solutions. Chemical Engineering Science, 59 (3), 501-512, (2004). [ Links ]
[44] BHATTACHARYA, K. AND VENKOBACHAR, C. Removal of cadmium (II) by low cost adsorbents,Journal of Environmental Engineering, 110 (1), 18540, 1984. [ Links ]
[45] HO,Y.S., PORTER, J.F. AND McKAY, G. Equilibrium isotherm studies for the sorption of divalent metal ions onto peat : copper, nickel and lead single components systems. Water, Air and Soil pollution, 141: 1-32, 2002. [ Links ]
[46] RAO P.S., JAMMALA, A., NAGA K.V. Y ABBURI, K. Biosorption of hexavalent chromium using tamarind (Tamarindus indica) fruit shell-a comparative study. Electron. J. Biotechnol. [online], 10, (3), 358-367, 2007. [ Links ]
[47] CRUZ,C., DaCOSTA A., HENRIQUES, C. AND LUNA A. S. Kinetic modeling and equilibrium studies during cadmium biosorption by dead Sargassum sp. Biomass, Bioresource Technology, 91 (3), 249-257, 2004. [ Links ]
[48] WANG S. AND H. LI. Kinetic modelling and mechanism of dye adsorption on unburned carbon, Dye and Pigments, 72(3), 308-314, 2007. [ Links ]
[49] VENKATESWARLU P., VENKATA R.M., SUBBA R.D. AND VENKATESWARA RAO M. Removal of chromium from an aqueous solution using Azadirachta indica (Neem) leaf powder as an adsorbent. International Journal of Physical Sci. , 2 (8), 188-195, 2007. [ Links ]
[50] ARAMI M., LIMAE N.Y. , MAHMOODI N.M. AND TABRIZI N.S. Removal of dyes from colored textile wastewater by orange peel adsorbent: Equilibrium and kinetic studies, J.Colloid Interface Sci. , 288(2), 371-376, 2005. [ Links ]
[51] DOULATI F., BADII K., YOUSEFI L. AND MAHMOODI N.M. Numerical modelling and laboratory studies on the removal of Direct Red 23 and Direct Red 80 dyes from textile effluents using orange peel,a low-cost adsorbent, Dyes and Pigments, 73 (2) 178-185, 2007. [ Links ]
[52] HO,Y.S., HUANG, C.T. AND HUANG, H.W. Equilibrium sorption isotherm for metal ions on tree fern. Process Biochemistry 37 (12), 1421-1430, 2002. [ Links ]
[53] JUANG,R.S. Y SHAO,H.J. A simplified equilibrium model for sorption of heavy metal ions from aqueous solutions on chitosan. Water Research, 36 (12), 2999-3008, 2002. [ Links ]
[54] ALLEN,S.J., GAN,Q., MATTHEWS,R. AND JOHNSON,P.A. Comparison of optimised isotherm models for basic dye adsorption by kudzu. Bioresource Technology, 88 (2), 143-152, 2003. [ Links ]
[55] Ng,J.C.Y., CHEUNG, W.H. AND McKAY, G. Equilibrium Studies of the Sorption of Cu(II) Ions onto Chitosan. J.Colloid Interface Sci. , 255 (1), 64-74, 2002. [ Links ]
[56] WONG,Y.C.,SZETO,Y.S., CHEUNG, W.H. AND McKAY, G. (2004) Adsorption of acid dyes on chitosan-equilibrium isotherm analyses. Process Biochemistry 39 (6), 695-70. [ Links ]
[57] PORTER,J.F., McKAY,G. AND CHOY, K.H. The prediction of sorption from a binary mixture of acidic dyes using single- and mixed-isotherm variants of the ideal adsorbed solute theory. Chemical Engineering Sci., 54 (24), 5863-5885, 1999. [ Links ]
[58] JIANG H., XU Y.,ZHANG J.,ZHANG L., AND HAN R. Pseudo-second order kinetic model for the biosorption of lead onto waste yeast. Life Science Journal, 4(4), 42-45, 2007. [ Links ] ]]>