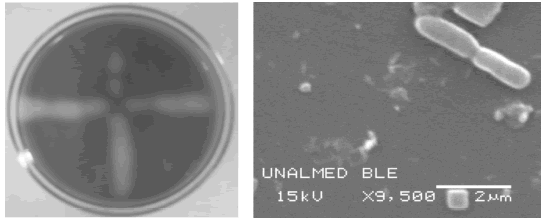
Figura 1. Detección de la a-amilasa y microscopía electrónica de barrido de Bacillus sp. BBM1 ]]> Figure 1. Detection of a-amylase and scanning electron micrograph of Bacillus sp. BBM1
PURIFICATION AND CHARACTERIZATION OF A a-AMYLASE PRODUCED BY Bacillus sp. BBM1
MÓNICA QUINTERO MORENO
Grupo de Biotecnología Microbiana. Estudiante de Ingeniería Biológica, Universidad Nacional de Colombia sede Medellín.
OLGA INÉS MONTOYA CAMPUZANO
Grupo de Biotecnología Microbiana. Profesora Asociada, Escuela de Biociencias, Facultad de Ciencias, Universidad Nacional de Colombia sede Medellín.
PABLO A. GUTIÉRREZ SÁNCHEZ
Grupo de Biotecnología Microbiana. Profesor Asistente, Escuela de Biociencias, Facultad de Ciencias, Universidad Nacional de Colombia sede Medellín. paguties@unalmed.edu.co
]]> Recibido para revisar Octubre 27 de 2008, Junio 2 de 2009, versión final Agosto 20 de 2009
RESUMEN: La cepa Bacillus sp. BBM1, productora de a-amilasas, fue aislada a partir de una muestra de suelo de la Universidad Nacional de Colombia sede Medellín. La caracterización morfológica, bioquímica y molecular indica que esta bacteria está filogenéticamente relacionada con las especies B. subtilis o B. amyloliquefaciens. La amilasa producida (BBM1) fue purificada por precipitación con sulfato de amonio y su peso molecular fue estimado en 77.6 kDa por electroforésis SDS-PAGE. Esta enzima es completamente estable a 60°C y presenta actividad significativa entre 30 y 80°C. La amilasa BBM1 tiene un pH óptimo entre 5.0-7.0 y no requiere calcio para su funcionamiento; estas propiedades hacen que esta enzima sea atractiva en aplicaciones industriales.
PALABRAS CLAVE: Bacillus, enzimas, a-amilasa
ABSTRACT:A novel a-amylase producing strain, Bacillus sp. BBM1, was isolated a soil sample from Universidad Nacional de Colombia sede Medellín. Morphological, Biochemical and molecular data suggests that this strain belongs to either B. subtillis or B. amyloliquefaciens species. a-amylase BBM1 was purified by ammonium sulphate precipitation and its molecular weight estimated as 77.7 kDa by SDS-PAGE electrophoresis. This enzyme was completely stable at 60°C as presents significant activity in the 30-80°C range. Amylase BBM1 has an optimal pH in the range 5.0-7.0 and does not require calcium. All this properties make this enzyme interesting for future industrial applications.
KEYWORDS: Bacillus, enzymes, a-amylase
1. INTRODUCCIÓN
Las a-amilasas (EC 3.2.1.1) son enzimas que catalizan la hidrólisis de enlaces glicosídicos a-1,4 presentes en el almidón, glicógeno y otros polisacáridos. El almidón está compuesto por dos polímeros de glucosa: la amilosa, que presenta únicamente enlaces a-1,4 y la amilopectina, que adicional a los enlaces a-1,4, posee sitios de ramificación a-1,6 [1]. La industria del almidón es una de las principales usuarias de amilasas para la hidrólisis y modificación de esta materia prima con el fin de obtener glucosa, maltosa y oligosacáridos, que pueden ser convertidos en jarabes de fructosa y dextrosa. La glucosa obtenida, también puede ser fermentada para producir etanol, aminoácidos y ácidos orgánicos [2]. Sin embargo, para la conversión enzimática de almidones es necesario utilizar amilasas termoestables, ya que estas son adicionadas luego de un paso de gelatinización que requiere temperaturas entre 70 °C y 110 °C [3]. El paso donde se adicionan las amilasas se conoce como liquefacción, y su objetivo es reducir la viscosidad de la solución mediante la hidrólisis parcial del almidón [4]. Se ha estimado que las enzimas hidrolíticas del almidón representan cerca del 30% del mercado mundial de enzimas, entre las que podemos mencionar Ultra-thin de la compañía Valley Research/Diversa, Multifect AA 21L® de Genencor y Termamyl® y Liquozyme® de Novozymes [5]. Las amilasas también pueden ser utilizadas como una alternativa a la adición de malta en la industria cervecera, en el mejoramiento de harinas en la industria panadera, la producción de almidones para la industria del papel, la remoción del almidón en la fabricación de textiles y como aditivos en detergentes [6].
Las a-amilasas bacterianas, y en especial aquellas provenientes de bacterias del género Bacillus como B. subtilis, B. stearothermophilus, B. licheniformis y B. amyloliquefaciens, han encontrado una amplia aplicación en procesos industriales gracias a sus rangos de temperatura óptima (25- 90 ºC), resistencia a pH extremos (1.0-11.5) y altos niveles de expresión [3]. En este trabajo se reporta la caracterización morfológica, bioquímica y molecular de la cepa nativa Bacillus sp. BBM1 productora de a-amilasas termoestables, y una metodología de producción y purificación de la enzima.
]]> Adicionalmente, se determinaron los rangos óptimos de temperatura y pH, termoestabilidad y dependencia de iones sobre la actividad de esta nueva amilasa.
2. MATERIALES Y MÉTODOS
2.1 Caracterización y cultivo del microorganismo
El microorganismo se aisló a partir de una muestra de suelo de la Universidad Nacional de Colombia sede Medellín y se caracterizó bioquímicamente con la prueba API 50 CH (API, Bio-Merieux) [7]. La caracterización molecular del Bacillus sp. BBM1 se realizó mediante secuenciación del gen ribosomal 16S (16S ADNr ). La amplificación de este gen se llevó a cabo mediante PCR, con los cebadores pA (5’-AGAGTTTGATCCTGGCTCAG- 3’) y pC5B (5’-TACCTTGTTACGACTT- 3’) [8].
La secuenciación del producto de PCR fue realizada por Macrogen Inc., Seul, Corea y depositada en GenBank con el código de acceso FJ411412.
La similitud con otras secuencias fue determinada por medio de una búsqueda con el programa BLAST [9].
El crecimiento del microorganismo se llevó a cabo en medio de cultivo LB, suplementado con 1% de almidón soluble e inoculado con esporas previamente activadas (1% del volumen final del medio de cultivo), Las condiciones de crecimiento fueron 40°C y 180 rpm durante aproximadamente 60 horas. El extracto enzimático se obtuvo centrifugación por 20 minutos a 7000g.
2.2 Purificación de la a-amilasa
La enzima se precipitó a partir del extractro enzimático mediante adición de sulfato de amonio hasta una saturación del 40%, incubación en hielo por 20 minutos y colectada por centrifugación (20 minutos a 7000g, 4 ºC). El pellet se resuspendió en un volumen mínimo de tampón citrato ( 50 mM, pH 6.0) y se pasó a través de una columna Biogel P100 preequilibrada con la solución de citrato. Se tomaron fracciones de 1 ml y se seleccionaron aquellas con actividad amilolítica. El grado de pureza fue evaluado mediante la relación actividad/[Proteína total] y electroforesis en poliacrilamida 10% (SDS-PAGE) [10]. La concentración de proteína fue estimada mediante el método de Bradford [11].
2.4 Caracterización de la enzima
La temperatura óptima de la a-amilasa fue estimada mediante la prueba del lugol en un rango de temperaturas entre 30 ºC y 90 ºC en tampón citrato almidón 1% a pH 6.0. La termoestabilidad de la enzima se estimó mediante incubación del extracto crudo en un rango de temperaturas entre 30ºC y 90ºC por quince minutos y medición de la actividad residual. El pH óptimo de la a-amilasa fue determinado mediante medición de la actividad en un rango de acidez entre 2.0 y 13.0 utilizando los siguientes tampones: Bis-Tris/HCl (pH 5.5-7.0), Tris/HCl (pH 7.5-8.5) y glicina/NaOH (pH 8.5-10.5). El efecto de diferentes concentraciones de calcio y EDTA fue evaluado en buffer citrato suplementado con NaCl ( 50 mM, 100mM, 200mM, 400mM y 800mM), CaCl2 ( 1 mM, 10 mM y 100 mM) y EDTA ( 1 mM, 10 mM y 100 mM).
3. RESULTADOS Y DISCUSIÓN
3.1 Caracterización de la cepa productora
La cepa BBM1 es un microorganismo Gram positivo que forma esporas subterminales elipsoidales. La bacteria tiene forma bacilar con dimensiones de ~1.8 mm x ~0.7 mm (Figura 1). Las colonias son color crema, de consistencia cremosa, con borde y superficie irregular. Al crecer la bacteria en un medio solido con almidon al 1% y tinción con yodo se aprecia la presencia de halos de degradación característicos de la producción de amilasas (Figura1). El análisis de la secuencia del gen ribosomal 16S confirma que esta bacteria pertenece al género Bacillus pero no da claridad sobre la identidad de la bacteria a nivel de especie. Luego de una búsqueda con el programa BLAST[9], se obtuvieron 51 cepas de Bacillus con el máximo puntaje (2488 bits), dividas así: Bacillus subtilis (27), Bacillus sp. (16), B. amyloliquefaciens (4), Bacillus velezensis (4). Recientemente se ha determinado que B. velezensis es un sinónimo heterotípico de B. amyloliquefaciens [12]. Lo que indica que nuestro aislamiento corresponde a B. subtilis o B. amyloliquefaciens, especies que no pueden ser diferenciadas fácilmente por métodos bioquímicos, siendo necesario el análisis de secuencias adicionales, como la región ITS 16S-23S, para la determinación a nivel de especie [13].

Figura 1. Detección de la a-amilasa y microscopía electrónica de barrido de Bacillus sp. BBM1 ]]>
Figure 1. Detection of a-amylase and scanning electron micrograph of Bacillus sp. BBM1
3.2 Purificación y caracterización de la enzima
La producción de a-amilasas por la cepa BBM1 alcanza un máximo aproximadamente a 60 horas después de la inoculación del medio de cultivo. La amilasa puede ser precipitada utilizando (NH4)2SO4 al 40 %. En este paso se obtiene una purificación significativa de la enzima,
lo cual puede evidenciarse por electroforesis SDS-PAGE (Figura 2A). A partir del gel, se estima que el peso de la enzima es de 77.6 kDa (Figura 2B). El análisis por electroforesis nativa del extracto indica que la proteína posee un punto isoeléctrico inferior a 6.8, ya que esta migra como un anión en las condiciones de corrido (Figura 2C).
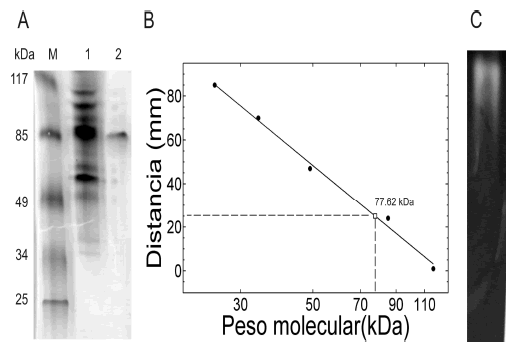
Figura 2. A) Electroforesis SDS-PAGE del proceso de purificación de la a-amilasa BBM1. 1, extracto libre de células; 2, precipitación con (NH4)2SO4; M, marcador de peso molecular. B) Estimación del peso molecular. C) zimograma de la a-amilasa
Figure 2. A) SDS-PAGE electrophoresis of a-amylase BBM1. 1, Cell-free extract; 2, (NH4)2SO4 precipitation; M, Molecular weight markers. B) Molecular estimation. C) a-amylase zimogram
3.3 Temperatura y termoestabilidad
La a-amilasa BBM1 presenta una actividad significativa entre 30°C y 80°C, con un máximo a 60°C, que también corresponde al máximo de estabilidad (Figura 3). La enzima trabaja con una eficiencia superior al 80% entre 45°C y 72 °C y su actividad decrece rápidamente por encima de 80ºC. Mediante una gráfica de Arrhenius (no mostrada), se estima que esta a-amilasa tiene una energía de activación catalítica de 5.98 kcal/mol y una energía de activación para la desnaturalización de 22 kcal/mol. La amilasa BBM1 es 100 % estable a una incubación por 15 minutos entre 30°C y 60°C. Sin embargo, a 70°C la actividad residual disminuye en un 85 % y se vuelve cero por encima de 80°C (Figura 3B).
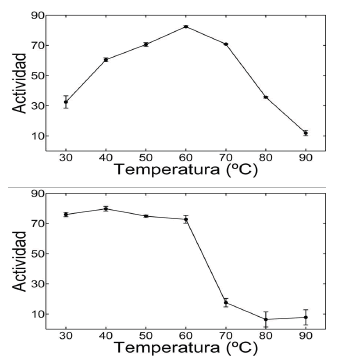 ]]>
Figura 3. Temperatura óptima (arriba) y termoestabilidad de la a-amilasa BBM1 (abajo)
]]>
Figura 3. Temperatura óptima (arriba) y termoestabilidad de la a-amilasa BBM1 (abajo)
Figure 3. Optimal temperature (above) and thermal stability of a-amylase BBM1 (below)
La mayoría de a-amilasas producidas por B. amyloliquefaciens y B. subtilis presentan una temperatura óptima cercana a los 70 ºC [14] y en el género Bacillus se han encontrado enzimas con temperaturas óptimas superiores aisladas a partir de B. licheniformis y B. stearothermophilus [15, 16]. Pese a que la termoestabilidad de esta amilasa es moderada si se compara con la producida por otros Bacillus, la temperatura óptima puede ser mejorada con técnicas como mutagénesis dirigida. En las décadas pasadas se ha adquirido una gran cantidad de información bioquímica, mutacional y estructural que han facilitado la comprensión de las propiedades térmicas de las a-amilasas [17]. Algunas variantes termoestables han sido construidas mediante sustitución en las posiciones H133 y A209 por los aminoácidos isoleucina y valina respectivamente [18]. Otro tipo de sustitución estabilizante consiste en reemplazar los aminoácidos glutamina y asparagina, ya que su deaminación a altas temperaturas contribuye de manera negativa a la termoestabilidad enzimática [19]. Esto ha sido demostrado con la mutación N190F para la amilasa de B. licheniformis [20].
El caso más sorprendente ha sido el descrito por Declerck et al, quienes lograron incrementar la termoestabilidad de una alfa-amilasa en 50 °C [21].
3.4 Rango de pH
La influencia del pH sobre la actividad enzimática se ilustra en la figura 4A. El perfil de actividad muestra que la a-amilasa BBM1 presenta actividad máxima en el rango 5.0-7.0. El efecto del pH sobre la catálisis enzimática refleja el estado de ionización de algunos aminoácidos importantes para que se lleve a cabo la reacción catalítica. El pKa de estos aminoácidos puede ser estimado usando una gráfica de Dixon-Webb [22]. Para el caso de la amilasa BBM1 la actividad está regida por aminoácidos con un pKa cercano a 3.8 y 8.2 que pueden corresponder a aspartato (3.9) y cisteína (8.37) respectivamente (Figura 4B).
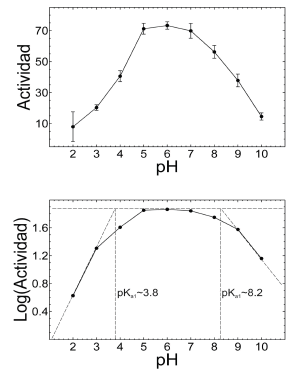
Figura 4. Efecto del pH sobre la a-amilasa BBM1 (arriba) y gráfica de Dixon-Webb (abajo)
Figure 4. Effect of pH on a-amylase BBM1 (above). Dixon-Webb plot (below)
El pH óptimo para las a-amilasas de B. subtilis o B. amyloliquefaciens es variable, pero se encuentra generalmente en el rango 6.0-7.0 [19]. Existen pocos reportes de a-amilasas con un pH óptimo por debajo de 5.0. Algunos casos excepcionales incluyen la alfa-amilasa producida por Alicyclobacillus acidocaldarius con un pH óptimo de 3.0 y la producida por Pyrococcus furiosus activa a un pH de 3.5 [23, 24].
]]> Debido a que la mayoría de las amilasas utilizadas en la sacarificación del almidón no son estables a pH ácido, este proceso debe ser ajustado a un pH cercano a 6.0 [14]. Se ha planteado que los costos de procesamiento del almidón pueden ser reducidos de manera significativa si se utilizan amilasas estables a la acidez en el paso de sacarificación ya que esto permitiría realizar la hidrólisis de almidón en un solo paso [14]. Lo anterior hace que la actividad de la amilasa BBM1 a pH ácido sea una propiedad muy interesante para su utilización en procesos industriales.3.5 Efecto del Calcio y EDTA
Una característica de la a-amilasas es el requerimiento de iones de calcio para mantener la integridad estructural y mejorar la estabilidad térmica [17]. La mayoría de las estructuras cristalográficas de a-amilasas demuestran que éstas contienen un sitio de unión al calcio localizado en la interface entre los dominios A y B. Sitios de unión al calcio adicionales, han sido reportados para otras amilasas de Bacillus licheniformis, B. amyloliquefaciens y B. stearothermophilus [25]. La remoción del calcio mediante la adición de agentes quelantes tiene un efecto negativo sobre la estabilidad y tasa catalítica de estas enzimas [26]. Esta dependencia al calcio es problemática en la industria del almidón, debido a la formación de oxalato de calcio, el cual puede bloquear tuberías e intercambiadores de calor [14]. Además, la presencia de calcio no es admisible en productos como la cerveza. La formación de oxalatos puede ser atenuada con la utilización de enzimas que requieran este elemento en bajas concentraciones y mediante disminución del pH durante el proceso de producción. Mediante ingeniería de proteínas ya se ha logrado la generación de enzimas que no requieren calcio y con una alta resistencia a pH ácido, como Termamyl LC® [27].
Una de las características más interesantes en la amilasa BBM1 es su baja dependencia del calcio para estimular su actividad (Figura 5). Solamente a concentraciones de 200 ppm se logra observar una leve mejora de la actividad respecto al control positivo. Eso se confirma con la incapacidad del EDTA de disminuir la actividad catalítica. Las amilasas que no requieren calcio son bastante raras, siendo una excepción la amilasa aislada a partir de Bacillus sp. KSM-K38 (Amyk38) la cual requiere iones de sodio como sustituto [28]. Sajedi et al. reportaron una enzima con características similares a BBM1 aislada a partir de Bacillus sp. KR-8104 (KRA), cuya actividad es independiente de la presencia de iones Ca2+, es activa a bajo pH y presenta una alta resistencia a la adición de EDTA [26].
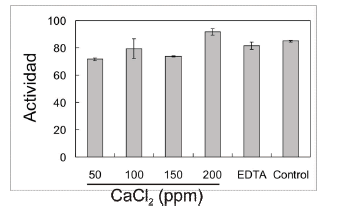
Figura 5. Efecto del calcio y EDTA sobre la a-amilasa BBM1
Figure 5. Effect of calcium and EDTA on a-amylase BBM1
4. CONCLUSIÓN
Bacillus sp. BBM1 produce una amilasa que es activa en un amplio rango de pH y con actividad significativa a pH ácido. Esta enzima no requiere calcio para su funcionamiento. Estas dos características hacen de la amilasa BBM1 una enzima con potencial aplicación en la industria del almidón. Por esta razón es importante llevar a cabo estudios enzimáticos complementarios, así como la secuenciación del gen codificante para esta enzima con el fin de entender el mecanismo de resistencia a bajo pH y su independencia al calcio. Finalmente de gran importancia será la identificación a nivel de especie de la cepa BBM1, con base en análisis de secuencias de otras regiones diagnósticas del genoma bacterial.
]]>5. AGRADECIMIENTOS
Agradecemos a los profesores Orlando Ruiz, Mauricio A. Marín y los estudiantes de Ingeniería Biológica Juan Esteban Ramírez, Juan Camilo Castrillón y Andrea Pareja por su colaboración en diferentes etapas de este proyecto. A Medardo Pérez del Laboratorio de Microscopía Avanzada por la imagen de microscopía. Este proyecto se realizó con financiación de la Dirección de Investigaciones de la Universidad Nacional de Colombia Sede Medellín (DIME, proyecto 802010013).
REFERENCIAS
[1] VAN DER MAAREL, M., VAN DER VEEN, B., UITDEHAAG, H., LEEMHUIS, H Y DIJKHUIZEN, L. Properties and applications of starch converting enzymes of the a-amylase family, J. Biotechnol., 94,137-55, 2002. [ Links ]
[2] KIRK, O., BORCHERT, T.B. Y FUGLSANG, C.C. Industrial Enzyme applications, Curr Opin Biotechnol, 13, 345-51, 2002. [ Links ]
[3] PANDEY, A., NIGAM, P., SOCCOL, C.R., SOCCOL, V.T., SINGH, D. Y MOHAN, R. Advances in microbial amylases, Biotechnol Appl Biochem, 31, 135-52, 2000. [ Links ]
[4] VAN DER VEEN, M.E., VEELAERT, S., VAN DER GOOT,A.J. Y BOOM, R.M. Starch hydrolysis under low water conditions: A conceptual process design, J Food Eng, 75, 178-86, 2006. [ Links ]
[5] TURNER, P., MAMO, G. Y KARLSSON, E.N. Potential and utilization of thermophiles and thermostable enzymes in biorefining, Microb Cell Fact, 6, 9. 2007. [ Links ]
[6] NIGAM, P. Y SINGH, D. Enzyme and microbial systems involved in starch processing, Enzyme Microb Technol, 17, 770-8. 1995. [ Links ]
[7] BEDOYA, G.P. Producción de un extracto con actividad amilolítica, a partir de una cepa nativa de Bacillus sp. Universidad Nacional de Colombia [Tesis de Maestría]. Medellín: Universidad Nacional de Colombia, 2007. [ Links ]
[8] DUNBAR, J., TAKALA, S., BARNS, S.M., DAVIS, J.A Y KUSKE, C.R. Levels of bacterial community diversity in four arid soils compared by cultivation and 16S rRNA gene cloning,. Appl. Environ. Microbiol, 65, 1662-69. 1999. [ Links ]
[9] ALTSCHUL, S.F., GISH, W., MILLER, W., MYERS, E.W. Y LIPMAN, D.J. Basic local alignment search tool, J Mol Biol, 215(3), 403-10. 1990. [ Links ]
[10] LAEMMLI, U.K. Cleavage of structural proteins during the assembly of the head of bacteriophage T4, Nature, 227, 680-5, 1970. [ Links ]
[11] BRADFORD, M.M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding, Anal. Biochem., 72, 248-54, 1976. [ Links ]
[12] WANG, L.T., LEE, F.L., TAI, C.J. Y KUO, H.P. Bacillus velezensis is a later heterotypic synonym of Bacillus amyloliquefacien,. Int J Syst Evol Microbiol, 58(Pt 3), 671-5. 2008, [ Links ]
[13] XU, D. Y CÔTÉ, J.C. Phylogenetic relationships between Bacillus species and related genera inferred from comparison of 3' end 16S rDNA and 5' end 16S-23S ITS nucleotide sequences, Int J Syst Evol Microbiol. 53(Pt 3), 695-704, 2003. [ Links ]
[14] HAKI, G.D. Y RAKSHIT, S.K. Developments in industrially important thermostable enzymes: a review, Bioresour Technol., 89(1), 17-34, 2003. [ Links ]
[15] VIARA, N., ELENA, P. Y ELKA, I. Purification and characterization of a thermostable alpha-amylase from Bacillus licheniformis, J. Biotechnol., 28, 277-89, 1993. [16] JEAYOUNG, K., TAKASHI, N. Y RYU, S. Thermostable, raw-starch-digesting amylase form Bacillus stearothermophilus, Appl. Environ. Microbiol, 55, 1638-39, 1989. [ Links ] [ Links ]
[17] NIELSEN, J.E. Y BORCHERT, T.V. Protein engineering of bacterial alpha-amylases, Biochim Biophys Acta, 1543(2), 253-274, 2000. [ Links ]
[18] DECLERCK, N., JOYET, P., TROSSET, J.Y., GARNIER, J. Y GAILLARDIN, C. Hyperthermostable mutants of Bacillus licheniformis alpha-amylase, multiple amino acid replacements and molecular modeling, Protein Eng., 8(10), 1029-37, 1995. [ Links ]
[19] TOMAZIC, S.J. Y KLIBANOV, A.M. Mechanisms of irreversible thermal inactivation of Bacillus alpha-amylases. J Biol Chem, 263(7), 3086-91, 1988. [ Links ]
[20] DECLERCK, N., MACHIUS, M., WIEGAND, G., HUBER, R. Y GAILLARDIN, C. Probing structural determinants specifying high thermostability in Bacillus licheniformis alpha-amylase, J Mol Biol, 301(4), 1041-57, 2000. [ Links ]
[21] DECLERCK, N., MACHIUS, M., JOYET, P., WIEGAND, G., HUBER, R. Y GAILLARD, C. Hyperthermostabilization of Bacillus licheniformis alpha-amylase and modulation of its stability over a 50 degrees °C temperature range, Protein Eng, 16(4), 287-93, 2003. [ Links ]
[22] ENGEL, P.C.. Enzymology LabFax. Academic Press, San Diego, 1996. [ Links ]
[23] MATZKE, J., SCHWERMANN, B. Y BAKKER, E.P. Acidostable and acidophilic proteins:, the example of the alpha-amylase from Alicyclobacillus acidocaldariu,. Comp Biochem Physiol, 118(3), 475-9, 1997. [24] JORGENSEN, S., VORGIAS, C.E. Y ANTRANIKIAN, G. Cloning, sequencing, characterization, and expression of an extracellular alpha-amylase from the hyperthermophilic archaeon Pyrococcus furiosus in Escherichia coli and Bacillus subtilis, J Biol Chem., 272(26), 16335-42, 1997. [ Links ] [ Links ]
[25] DAVIES, G. Y HENRISSAT, B. structures and mechanisms of glycosyl hydrolases, Structure, 3(9), 853-9, 1995. [ Links ]
[26] SAJEDI, R.H., NADERI-MANESH, H., KHAJEH, H., AHMADVAND, R., RANJBAR, B., SOODEH, A. Y MORADIAN, F. A Ca-independent a-amylase that is inactive and stable at low pH from the Bacillus sp. KR-8104, Enzyme Microb Technol,. 36, 666-71, 2005. [ Links ]
[27] HASHIDA, M. Y BISGAARD-FRANTZEN, H. Protein engineering of new industrial amylases, Trends Glycosci. Glycotechnol, 12, 139-147, 2000. [ Links ]
[28] TSUYOSHI, N., MASAHIRO, F., AKIKO, K., HIROSHI, H., KATSUYA, O., SUSUMU, I. Y KUNIO, M. Crystal structure of calcium-free alpha-amylase from Bacillus sp. strain KSM-K38 (AmyK38) and its sodium ion binding sites, J Biol Chem, 278(27), 24818-24., 2003. [ Links ] ]]>