Respuesta inmune humoral de una vacuna comercial contra la estomatitis vesicular en cerdos
John J Arboleda1, MV, MS; Ruth M Valbuena2, MV, MS; Nancy Naranjo2, MV; Jaime I Velásquez1, MV, Juan D Rodas1 ,
MV, Ph.D.; Andrés F Londoño, Est MV1 Gustavo A García1, Zoot MS.
1 Grupo Centauro, Escuela de Medicina Veterinaria, Facultad de Ciencias Agrarias, Universidad de Antioquia, AA 1226 Medellín, Colombia;
2 Instituto Colombiano Agropecuario, ICA, Bogotá, Colombia.
]]> (Recibido: 4 agosto, 2004; aceptado: 2 mayo, 2005)
Resumen
Con el objetivo de determinar la respuesta inmune humoral en porcinos inducida por una vacuna bovina comercial contra la estomatitis vesicular, se inmunizaron 30 cerdas comerciales y 20 más fueron dejadas como control. A todas se les realizó medición de los títulos de anticuerpos utilizando la prueba de seroneutralización para los serotipos Indiana (IN) y New Jersey (NJ), los días 0, 82, 182, 330, 404 y 599 post-vacunación; con revacunación a los 434 días. Tanto los animales vacunados como los no vacunados exhibieron bajos títulos de anticuerpos contra ambos serotipos antes de la vacunación. Sin embargo al día 82 post-vacunación se presentó un notable incremento en los títulos de anticuerpos en animales vacunados tanto para el serotipo IN como para el NJ, con promedios de 3.17 y 3.56 respectivamente. Para el día 404 se observó un descenso en el título de anticuerpos, los cuales incrementan para el día 599, por efecto de la revacunación. Los animales control mantuvieron bajos títulos de anticuerpos durante todo el experimento. Este estudio muestra que hay una respuesta inmune humoral con diferencias estadísticamente significativas entre las cerdas vacunadas y no vacunadas, sin reacciones adversas atribuibles al biológico, en los animales inoculados.
Palabras clave: cerdos, respuesta inmune humoral, vacuna comercial, VSV
Introducción
La Estomatitis Vesicular (EV) es una enfermedad viral que afecta a los bovinos, equinos, porcinos y a una gran variedad de animales vertebrados silvestres, caracterizándose por la producción de pápulas, vesículas y erosiones en la mucosa oral, sobre la piel de los pezones, el rodete coronario o en las áreas interdigitales de las patas (1). La enfermedad hace parte de la lista A de la OIE (Organización Internacional de Epizootias, recientemente renombrada como Organización Mundial de Sanidad Animal), por ser una enfermedad transmisible que presenta gran poder de difusión y especial gravedad, que puede extenderse más allá de las fronteras nacionales, con consecuencias socioeconómicas y sanitarias graves, lo cual ocasiona restricciones en el comercio internacional de animales y sus subproductos (2).
La EV es una enfermedad exclusiva del continente americano, presentándose desde la parte sur de los Estados Unidos hasta el norte de sur América. La frecuencia y consecuencias de la infección son variables y de acuerdo con esto existen áreas consideradas endémicas para la EV como Centroamérica y Colombia; y áreas de presentación cíclica como la parte sur de los Estados Unidos y algunas áreas de México (3).
En Colombia la EV fue reconocida por primera vez alrededor de los años 30´s, iniciándose con dos focos primarios: uno en el departamento del Huila en 1929, el cual afectó bovinos, porcinos y equinos, y se extendió luego a otros departamentos del país; y otro en el Banco (Magdalena) en 1933, el cual se propagó en todas las direcciones del territorio nacional. Más tarde, en 1940, se presentó una grave epizootia en la Costa Atlántica y desde entonces la enfermedad se difundió por todo el país (4).
El agente causal de la enfermedad, es un virus perteneciente a la familia Rhabdoviridae, género vesiculovirus, con un genoma constituido por ARN de cadena simple y de sentido negativo. La organización del genoma es altamente conservada entre todos los vesiculovirus y consiste de cinco genes con el siguiente orden: 3‘ N-P (C-C) -M-G-L 5‘. El gen N, codifica para la proteína de la nucleocápside del virión la cual esta íntimamente unida al ARN viral. Las proteínas P (fosfoproteína) y L (ARN polimerasa dependiente de ARN), se unen con la nucleocápside y forman el complejo de transcripción y replicación viral. Dos proteínas mas, C y C´, son codificadas en un segundo ORF (del inglés Open Reading Frame o marco de lectura abierto) dentro del gen P pero su función es aún desconocida. La proteína M se localiza entre la nucleocápside y la envoltura, y ayuda a moldear la típica forma de bala del virión. La proteína G glicoproteína, es el principal componente de la membrana celular, y facilita tanto la absorción y penetración del virus como su salida de la célula infectada. Los anticuerpos neutralizantes están dirigidos contra esta proteína G y con base en ella se realiza la tipificación serológica del virus (5, 6).
]]> Serológicamente, el Virus de la Estomatitis Vesicular (VEV) posee dos tipos diferentes: New Jersey (NJ) e Indiana (IN), de este último existen además tres subtipos, Indiana I, Indiana II (Cocal) e Indiana III (Alagoas). La nucleoproteína viral, y en menor grado, la proteína de la matriz, son las responsables de las reacciones cruzadas entre los grupos serológicos (7). Aunque los tipos de NJ e IN son serológica e inmunológicamente distintos, el cuadro patológico que producen en las especies susceptibles es indistinguible desde el punto de vista clínico (4).La mayoría de los estudios sobre VEV se han realizado en bovinos debido a las grandes pérdidas económicas que esta enfermedad produce en esta especie, sobre todo en la ganadería de leche. Se debe resaltar sin embargo, que el bovino no es la única especie doméstica susceptible a la estomatitis vesicular; los porcinos y los equinos también sufren la enfermedad (8).
La EV es una enfermedad de alta prevalencia e incidencia en nuestro país, y de acuerdo con estudios realizados por Laserna en 1967, afecta al 10% del hato nacional, y al 12% de acuerdo con Orrego y Arbeláez (9), aunque más recientemente Arbeláez et al (1) reportan que la tasa de ataque de la enfermedad fluctúa entre el 4 y el 8%. Se considera que existe un gran subregistro de casos, pues por alguna razón, aún no esclarecida, el pequeño y mediano productor no consideran a la EV una enfermedad importante.
Estudios realizados en cerdos, por Howerth et al (8), han demostrado la transmisión por contacto directo entre animales, aislándose el VEV sin que necesariamente se desarrolle la enfermedad clínica. En otros estudios se reporta que, aunque los animales afectados por la enfermedad sólo eliminan el virus durante seis días después de la infección primaria (11), las cantidades de virus eliminadas son suficientes para infectar, ya sea por contacto o por transmisión mecánica, a otros animales (12).
En la literatura científica existen pocas publicaciones acerca de la prevención de la enfermedad utilizando vacunas. Uno de los ejemplos más novedosos de vacunas genéticamente modificadas fue publicado recientemente por los grupos de investigación de Gail Wertz en la Universidad de Alabama y Luis Rodríguez en Plum Island Animal Disease Center (PIADC) del departamento de Agricultura de los Estados Unidos. En ensayos experimentales con cerdos, ellos determinaron el efecto que la reorganización genética tiene sobre la capacidad replicativa e inmunogénica del VEV en su hospedero natural. En este experimento se pudo determinar que el desplazamiento de los genes N o G hacia el extremo 5’ (es decir alejándose del promotor), disminuía la expresión de las proteínas respectivas, lo que hacía que el agente perdiera capacidad replicativa y antigenicidad pero sin alterar su inmunogenicidad. De esta forma, concluyeron, se podrían generar en forma artificial, variantes genéticas del VEV que se comportaran como vacunas vivas atenuadas, pero a la vez más estables y seguras (13).
En Colombia existe en el mercado una vacuna bivalente contra la EV indicada solo para bovinos, la cual demostró ser efectiva en un 80% de los animales vacunados en un estudio realizado en cuatro fincas ubicadas en los departamentos de Caldas y Quindío, y en un 96% en otro estudio llevado a cabo entre los años 1995 y 1996, en 4000 bovinos de 23 fincas ubicadas en los municipios de Frontino y Abriaquí, en el departamento de Antioquia. Se ha reportado también un ensayo en el cual se vacunó un grupo de porcinos y se les determinaron los niveles de anticuerpos en los días 15 y 30 posvacunación, observándose una respuesta mayor que en los bovinos, lo cual demostraba que los porcinos pueden ser inmunizados con la vacuna en forma eficiente (5,8,14). A pesar de los anteriores resultados, hasta el momento no se han realizado ensayos de vacunación en cerdos con el fin de ofrecer una medida sanitaria que ayude a la prevención y control de la enfermedad en explotaciones porcinas. El propósito de este estudio fue probar serológicamente la respuesta de una vacuna comercial para bovinos contra la EV en cerdas adultas de una explotación comercial.
Materiales y métodos
Animales
En el estudio se utilizaron 50 cerdas, línea Dekalb, sometidas al mismo manejo productivo en la granja San Clemente, propiedad de intergranjas S.A., ubicada en la vereda Las Animas del municipio de Don Matías, altiplano norte antioqueño. Esta zona está ubicada a
2.220 m.s.n.m. y la zona posee una temperatura anual promedio de 16°C. La granja está dedicada a la explotación comercial de cerdos para la venta en la feria de Medellín y su alimentación es exclusivamente a base de concentrado comercial.
]]> VacunaSe utilizó una vacuna comercial bivalente contra la Estomatitis Vesicular, NJ e IN, compuesta de virus cultivados en línea celular de riñón de hámster lactante (BHK-21) en suspensión y monoestrato, inactivada químicamente y emulsionada en adyuvante oleoso (VECOL).
Vacunación
De las 50 cerdas, 30 fueron vacunadas y 20 se utilizaron como grupo control. Cada uno de los animales fue vacunado con 2.5 ml del biológico vía intramuscular profunda en el cuello al día 0 y se realizó una revacunación el día 434, con la misma dosis. Todos los animales fueron sangrados para extracción de suero sanguíneo, los días 0, 82, 182, 330, 404 y 599 postvacunación. Las muestras fueron enviadas al centro de diagnóstico de enfermedades vesiculares del ICA en Bogotá, para medición de títulos de anticuerpos por seroneutralización contra ambos serotipos del virus en cada uno de los animales.
Análisis estadísticoPara el análisis se utilizó el modelo de comparación de medias, donde los títulos obtenidos fueron la variable dependiente y los tratamientos (vacunadas y no vacunadas) y los días de medición fueron las variables independientes. Para ello se utilizó el programa SPSS version 8.0.
Resultados
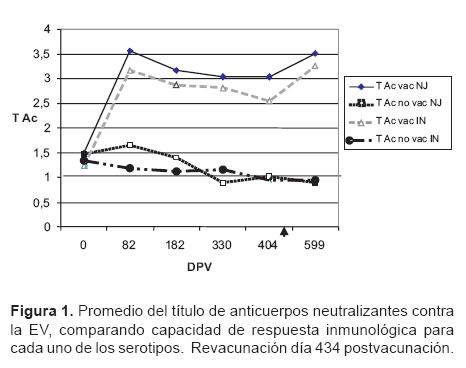
Los niveles de anticuerpos neutralizantes contra ambos serotipos de la EV fueron mayores en los cerdos vacunados que en los cerdos no vacunados (véase Figura 1). Las diferencias de los niveles de anticuerpos neutralizantes entre ambos grupos de cerdos fueron estadísticamente significativas y se mantuvieron constantes en las muestras tomadas a través de todo el experimento.
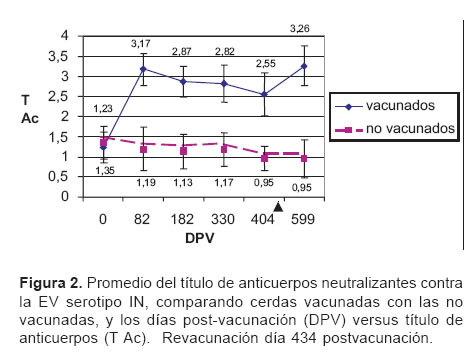
En la prueba de seroneutralización para el serotipo IN, no se encontró diferencia en el promedio de anticuerpos previo a la vacunación, día 0, para los cerdos vacunados comparados con los cerdos no vacunados. Sin embargo a partir de la primera muestra postvacunación, tomada al día 82, los cerdos vacunados presentaron un incremento de hasta dos logaritmos decimales en el título de anticuerpos (3.17). Los niveles de anticuerpos en el grupo vacunado se mantuvieron elevados hasta el día 404 y las diferencias entre los promedios de anticuerpos de los grupos vacunado y no vacunado fueron estadísticamente significativas en favor del grupo vacunado a través de todo el experimento.
En el día 434 se realizó una revacunación y los títulos de anticuerpos neutralizantes mostraron de nuevo un incremento de casi un logaritmo decimal para el día 599. Los animales no vacunados mantuvieron un promedio de anticuerpos neutralizantes durante todo el ensayo de 1.12, alcanzando valores máximos y mínimos de 1.35 y 0.95 (véanse Figuras 1 y 2).
]]>
Para el serotipo NJ el promedio de los títulos de anticuerpos neutralizantes en el día 0, fueron similares entre las cerdas vacunadas y las no vacunadas (1.49 y 1.47 respectivamente). Para el día 82 postvacunación sin embargo, las cerdas vacunadas presentaron un título de anticuerpos que fue aproximadamente 100 veces mayor que el detectado en las cerdas no vacunadas (3.56 comparado con 1,65). Los valores en ambos grupos descendieron paulatinamente en las muestras subsiguientes pero las diferencias de los promedios se mantuvieron a través de todo el experimento. De nuevo como en lo observado contra el serotipo IN, los niveles de anticuerpos neutralizantes contra el serotipo NJ aumentaron hasta medio logaritmo en la muestra tomada al día 599, después de la revacunación (434 días post-vacunación). En las cerdas no vacunadas se mantuvo un promedio de título de anticuerpos de 1.22, durante todo el estudio, alcanzando valores máximos y mínimos de; 1.65 y 0.89 respectivamente. (véanse Figuras 1 y 3)
Los títulos de anticuerpos neutralizantes contra el VEV serotipos IN y NJ fueron hasta 100 veces mayores en los animales vacunados comparados con los animales no vacunados. Las diferencias entre los títulos de anticuerpos neutralizantes fueron estadísticamente significativas desde la primera muestra tomada a los 82 días postinoculación y conservaron su nivel a través de todo el experimento. Los cerdos no vacunados, solo mostraron niveles basales de anticuerpos neutralizantes (véanse Figuras 1-3).
En este estudio todos los animales vacunados, presentaron un comportamiento similar en la dinámica del título de anticuerpos contra ambos serotipos, presentándose sin embargo, una mayor respuesta antigénica para el serotipo NJ (véase Figura 3).
En relación con la respuesta de anticuerpos contra el serotipo NJ, se encontraron diferencias estadísticamente significativas a usando la prueba de Fisher, cuando se compararon el grupo de los animales vacunados con el grupo de animales no vacunados y dicha diferencia se mantuvo a través de todo el tiempo que duró el experimento (p=0.0001) (véase Tabla 1).
El mismo análisis fue realizado para la medición de anticuerpos contra el serotipo IN en ambos grupos (vacunados y no vacunados) en los distintos días que se realizaron los muestreos y de nuevo los resultados fueron estadísticamente significativos (p=0.001) (véase Tabla 2).
DiscusiónLos resultados muestran una respuesta inmune humoral, con aumento en el título de anticuerpos para los dos serotipos, en cerdos inoculados con la vacuna oleosa indicada para bovinos. No se presentó ninguna reacción clínica adversa al biológico a través de todo el estudio (datos no mostrados).
]]> Durante este experimento no se presentaron brotes naturales del VEV, en la zona de estudio, ni se sometieron las cerdas a infección experimental para comprobar la eficacia de la vacuna, razón por lo cual se desconoce si los títulos de anticuerpos alcanzados en este estudio son protectores contra la presentación clínica de la enfermedad. Los títulos de anticuerpos neutralizantes sin embargo, se mantuvieron durante más de 404 días y en este punto se incrementaron después de la revacunación.Con este estudio se demostró que hay una respuesta inmune humoral, medida por la producción de títulos altos de anticuerpos específicos, en respuesta al biológico y quedan las puertas abiertas para determinar en futuros ensayos la dosis efectiva y la protección a la infección experimental o natural.
Adicionalmente dentro de este mismo estudio, se tomaron muestras de sangre a las crías de las cerdas vacunadas para medir los niveles de anticuerpos en lechones (datos no mostrados) y aunque los datos disponibles no son concluyentes y se requeriría un estudio específico para demostrarlo, los resultados preliminares obtenidos muestran una muy buena transferencia de inmunidad pasiva a través del calostro, con títulos similares a los detectados en el suero sanguíneo de las madres contra ambos serotipos. En experimentos futuros será necesario determinar la duración de la transferencia y el tiempo de protección, para poder así definir la edad de primo vacunación en lechones.
Los resultados de este estudio son similares a los reportados por Arbeláez et al (2, 5), en los cuales la respuesta humoral de los bovinos vacunados fue muy similar a la de las cerdas vacunadas aquí.
En nuestro medio se han realizado varios ensayos buscando producir un biológico efectivo que evite casos clínicos de EV. Todos los ensayos previos han buscado formular protocolos de inmunización en bovinos. De la mano de estos estudios se han realizado también algunas pruebas en cerdos y equinos (4), que muestran que el biológico en las dos especies mencionadas, induce la producción de títulos promedios de anticuerpos neutralizantes superiores a los promedios de los bovinos a los 30 días post-vacunación (6.97 y 6.60 comparados con 5.83). Se hace evidente entonces, la gran capacidad de respuesta en estas dos
especies a inmunógenos como el VEV y concluyen los autores que estos hallazgos posiblemente expliquen la escasa presentación de brotes, en los equinos y porcinos de las diferentes áreas endémicas del país (4).
Basados en estudios en bovinos, se ha concluido que animales con títulos de anticuerpos neutralizantes por encima de 104 están protegidos contra una descarga de 10.000 DICT50 por vía intra-dermo lingual con el virus homólogo. Estos resultados demostrarían no sólo calidad del inmunógeno sino también su uso promisorio en áreas endémicas de la enfermedad (11).
Con los resultados del presente trabajo, es posible concluir que la vacuna oleosa indicada para bovinos es segura y eficiente en generar altos niveles de anticuerpos en la especie porcina y que estos niveles de anticuerpos podrían ser indicadores de protección contra infecciones naturales o experimentales. Adicionalmente en resultados no mostrados se determinó que la inmunidad es transferida eficientemente a la descendencia, lo que podría convertirla en una poderosa herramienta para el control de la enfermedad en lechones.
Agradecimientos
Los autores expresan sus sinceros agradecimientos al personal encargado del manejo de los animales en la granja San Clemente, por su gran colaboración y disponibilidad para el trabajo de muestreo en los animales de estudio y por todas sus atenciones para con el grupo de investigación.
]]>Summary
Humoral immune response induced by a commercial vaccine against vesicular stomatitis virus (VSV) in pigs.
The goal of this study was to determine the humoral immune response induced by a previously tested bovine bivalent vaccine against the vesicular stomatitis virus in pigs. 30 female pigs were immunized with the biological product and 20 more remained as controls. We measured neutralizing antibody tittles against both serotypes of VSV, IN and NJ, in serum for all the pigs at day 0 (before inoculation) and then at 82, 182, 330, 404 days post-vaccination. Re-vaccination was performed at 434 days and again a new serum sample was tested at day 599. All the female pigs showed a similar average of background antibodies against both serotypes of VSV at day 0. At 82 days postvaccination there was a 100-fold difference between the vaccinated and unvaccinated groups in favor of the vaccinated pigs. The differences were statistically significant and remained the same through the whole experiment. Following the antigenic boost there was a new peak of NT antibodies, which was comparable to the one obtained 82 days after the first vaccination. The unvaccinated pigs only showed background levels of NT antibodies that did not change significantly along the experiment. The study shows that this is a safe and promising vaccine. This biological product induces an important immune humoral response, with potential for protection against natural VSV exposures. Future studies will show its capability to protect animals against viral challenge and prevent infection of piglets.
Key words: commercial vaccine, humoral immune response, pigs, VSV
Referencias
1. Arbeláez G, Aristizábal JA, Sánchez C, Morales LF, Piedrahita I, et al. Evaluación de una Vacuna Contra la Estomatitis Vesicular en Bovinos en los Municipios de Frontino y Abriaquí (Antioquia). Rev CORPOICA. Publicación en prensa. 1998. [ Links ]
2. Arbeláez G, Ariza F, Orjuela J. Inmunidad humoral en bovinos vacunados contra estomatitis vesicular New Jersey, utilizando vacuna oleosa inactivada. Rev ICA 1993; 28:1-3. [ Links ]
3. Arboleda JJ. Epidemiología molecular de la estomatitis vesicular. Monografía, Facultad de Ciencias Agrarias, Universidad de Antioquia, Medellín, 1998; pp: 52-58. [ Links ]
4. Arbeláez G, Mogollón J, Rincón M. La estomatitis vesicular: estrategias para su diagnóstico y control. Rev Porcicultura Col 2000; 68:4-8. [ Links ]
5. Arbeláez G, Rocha J, Bernal C. Ensayo de vacuna contra la estomatitis vesicular. Rev Acovez 1998; 12: 3. [ Links ]
6. Bedoya M. Estomatitis vesicular. Saninet, 2001. http://www.iicasaninet.net/pub/sanani/html/exoticas/ev.htm. [ Links ]
7. Brian EF, Joann MZ, Andrew B, Rodríguez LL, Wertz GW. Rearrangement of the genes of vesicular stomatitis virus eliminates clinical disease in the natural host: new strategy for vaccine development. J Virol 2001; 75:13. [ Links ]
8. Howerth E, Stallknecht D, Dorminy M, Pisell T, Clarke G. Experimental vesicular stomatitis in swine: effects of route of inoculation and steroid treatment. J Vet Diagn Invest 1997; 9:136-142. [ Links ]
9. Letchworth GJ, Rodríguez LL, Barrera JC. Vesicular Stomatitis. The Vet Journal 1999: 157. [ Links ]
10. OFFICE INTERNATIONAL DES EPIZOOTIES. (oie@oie.int) Clasificación OIE de las enfermedades. http://www.oie.int/esp/maladies/es_classification.htm Consulta Febrero 15 de 2002. [ Links ]
11. Redelman D, Nichol S, Klieforth R, Van Der MM, Whetstone C. Experimental vesicular stomatitis virus infection of swine: extent of infection and immunological response. Veterinary immunol and immunopathol 1989; 20:345-361. [ Links ]
12. Rodríguez LL. Epidemiología molecular de la estomatitis vesicular. Monografía, Facultad de Ciencias Agrarias, Universidad de Antioquia, Medellín, 1998; 52-58. [ Links ]
13. Stallknecht D, Howerth E, Reeves C, Seal B. Potential for contact and mechanical vector transmission of vesicular stomatitis virus New Jersey in pigs. Am J Vet Res 1999; 60: 1. [ Links ]
14. Zuluaga FN. Epidemiología molecular de la estomatitis vesicular. Monografía, Facultad de Ciencias Agrarias, Universidad de Antioquia, Medellín, 1998; 52-58 [ Links ]
]]>