Identificación de mutaciones puntuales del gen de la 21-hidroxilasa en pacientes afectados con hiperplasia suprarrenal congénita
Dora Fonseca 1-2, Andrés Gutiérrez 2, Claudia Silva 1, Mauricio Coll 3, Gustavo Malo 4, Camilo Orjuela 4, Clara Arteaga 5, Alejandro Giraldo 2-6
1 Facultad de Medicina, Instituto de Ciencias Básicas, Unidad de Genética, Universidad del Rosario, Bogotá, D. C., Colombia.
2
Fundación Arthur Stanley Gillow, Bogotá, D. C., Colombia.3
Departamento de Pediatría, Hospital de La Misericordia, Facultad de Medicina, Universidad Nacional de Colombia, Bogotá, D. C., Colombia.4
Departamento de Cirugía, Hospital de La Misericordia, Facultad de Medicina, Universidad Nacional de Colombia, Bogotá, D. C., Colombia.5
Departamento de Ginecología y Obstetricia, Instituto Materno Infantil, Facultad de Medicina, Universidad Nacional de Colombia, Bogotá, D. C., Colombia.6
Departamento de Medicina Interna, Facultad de Medicina e Instituto de Genética, Universidad Nacional de Colombia, Bogotá, D. C., Colombia.Introducción. La hiperplasia suprarrenal congénita es un trastorno autosómico recesivo debido a la inadecuada secreción de cortisol. Más del 95% de los casos de hiperplasia suprarrenal congénita son causados por defectos del gen de la 21 hidroxilasa, CYP21A2. Las manifestaciones clínicas incluyen la forma clásica y la forma no clásica.
]]> Objetivos. Determinar la frecuencia de las mutaciones puntuales P30L, IVS2-12A/C-G, Del 8pb, I172N, cluster Ex 6, V281L, Q318X, R356W y P453S en pacientes con hiperplasia suprarrenal congénita.Materiales y métodos. Se estudiaron 58 pacientes, de los cuales, 48 fueron clásicos y 10 no clásicos. Mediante PCR alelo-específica y ACRS (Amplified Creation Restriction Sites), se analizaron 9 mutaciones puntuales del gen CYP21A2 y se determinó la frecuencia en la población analizada.
Resultados. Los alelos afectados se identificaron en el 82,8% de los cromosomas. Las mutaciones más frecuentes fueron: IVS2-12A/C-G (26,7%), Q318X (21,5%), V281L (12,1%) e I172N (12,1%).
Conclusiones. Las mutaciones más frecuentes en Colombia son similares a las de otros países del mundo, excepto para Q318X que presentó una mayor frecuencia, pero similar a la de otros países latinoamericanos. Este hallazgo y la existencia de 17,2% de alelos no identificados puede indicar diferencia entre el acervo genético de las poblaciones. En la forma clásica perdedora de sal predominaron las mutaciones Q318X e IVS2-12A/C-G; en la virilizante simple, IVS2-12A/C-G e I172N y en la no clásica , V281L, lo cual está relacionado con el grado de actividad enzimática. En la forma no clásica, se encontraron alelos severos en el 66,7% de los casos, lo que determina el riesgo de tener hijos afectados con la forma grave virilizante simple o perdedora de sal. Los resultados reportados permiten ofrecer asesoramie nto genético y diagnóstico prenatal.
Palabras clave: hiperplasia suprarrenal congénita, PCR, esteroide 21-hidroxilasa.
Identification of point mutations in the 21-hydroxylase gene in patients affected with congenital adrenal hyperplasia
Introduction. Congenital adrenal hyperplasia (CAH) is an autosomal recessive disorder due to impaired cortisol secretion. Approximately 95% of CAH cases are caused by defects in the 21-hydrodylase2 (CYPA2) gene. The spectrum of clinical manifestations includes a severe and mild form of expression. The frequency of the following point mutations was determined: P30L, IVS2-12A/C-G splice, Del 8pb, I172N, cluster Ex6, V281L, Q318X, R356W and P453S.
Materials and methods. The 58 patients consisted of 48 with the severe form of CAH and 10 with the mild form. Point mutations in the hydroxylase gene were isolated by allele-specific PCR and PCR-ACRS (amplification created restriction site), and their frequency was determined.
Results. Alternate alleles were identified in 82.8% of the samples. The most frequent mutations were IVS2-12A/C-G splice (26.7%), Q318X (21.5%), V281L (12.1%) and I172N (12.1%).
Discussion. The most frequent mutations were similar to those observed in other countries, except for Q318X. Although its frequency was higher but similar to that observed in Latin American countries, it contrasted with those of other continents and indicated the possible influence of genetic background in its expression. Several of the mutations were associated with specific clinical forms related to the enzyme activity. In the milder forms of CAH, several alleles were detected. These were important because these patients can have children with the virilizing and salt wasting forms. Recognition of the allelic forms of CAH will permit more specific genetic counseling and prenatal diagnosis.
]]> Key words: congenital adrenal hyperplasia, PCR, salt wasting, virilizing, 21-hydroxylase.La hiperplasia suprarrenal congénita comprende un grupo de trastornos genéticos que se producen como consecuencia del bloqueo en la vía metabólica de la síntesis de cortisol y la aldosterona a partir de colesterol, lo cual genera un incremento en la secreción de la hormona adrenocorticotrópica (ACTH), con subsecuente hiperplasia de la corteza suprarrenal, acúmulo de precursores de cortisol y exceso en la producción de andrógenos (1,2).
La corteza de la glándula suprarrenal produce tres clases de hormonas. Los glucocorticoides, principalmente el cortisol, tienen como función elevar las concentraciones de glucosa en la sangre. Los mineralocorticoides, principalmente la aldosterona, regulan los electrolitos de los líquidos extracelulares, en particular, sodio y potasio. Los esteroides sexuales no tienen papel fisiológico esencial a partir de esta glándula, pero en las mujeres, producen -bajo condiciones de producción elevada- virilización de los genitales externos (3,4).
La hiperplasia suprarrenal congénita clásica se caracteriza en las mujeres por la virilización de los genitales externos, asociada a crisis de pérdida salina o sin ella y, en los hombres, aunque no se hay virilización, se puede presentar crisis de pérdida salina que los lleva, incluso, a la muerte a los pocos días de edad. La forma clásica de la enfermedad involucra dos fenotipos clínicos: perdedores de sal y virilizantes simples. Las formas no clásicas se caracterizan porque las pacientes son asintomáticas o presentan sus síntomas durante la adolescencia (5).
En los pacientes masculinos, los andrógenos testiculares conllevan una masculinización normal sin importar el exceso procedente de los andrógenos suprarrenales. Los niños con este problema escapan al diagnóstico hasta la edad de 4 a 7 años, momento en que la aparición de vello púbico, facial y axilar indica una pseudopubertad precoz (1).
En la forma no clásica de hiperplasia suprarrenal congénita se da un grado leve de deficiencia enzimática y se presenta con una alta frecuencia entre las diferentes poblaciones. La forma no clásica de hiperplasia suprarrenal congénita afecta a hombres y mujeres, quienes presentan genitales normales al nacimiento. El exceso de andrógenos en este tipo de presentación causa hirsutismo, acné, síndrome de ovario poliquístico y oligomenorrea (6-9).
Hay dos genes humanos para el esteroide 21-hidroxilasa, uno activo denominado CYP21A2 y un seudogén inactivo altamente homólogo llamado CYP21A1P. Esos genes están localizados en el extremo 3' de cada uno de los genes que codifican para el cuarto componente del complemento sérico, C4A y C4B, en la región del complejo mayor de histocompatibilidad dentro del HLA, clase III, sobre el cromosoma 6p21.3 (10,11).
Los genes CYP21A2 Y CYP21A1P tienen 3,4 kb en longitud y consisten de 10 exones; el análisis de su secuencia ha revelado una homología del 98% en los exones y de 96% en los intrones, y difieren solamente en 88 de sus bases (11).
Las lesiones genéticas que causan deficiencia de 21 hidroxilasa son: deleciones (15%), grandes conversiones (9%), duplicaciones (2%) y mutaciones puntuales ( 75%). Los mecanismos genéticos que causan los defectos moleculares del gen de la 21 hidroxilasa son, principalmente, la recombinación homóloga meiótica desigual y la "conversión génica" (12-15).
El diagnóstico prenatal de la deficiencia de 21 hidroxilasa es importante para conocer la condición fetal, principalmente, en búsqueda de los casos más seriamente afectados en quienes la alta virilización puede llevar a error en la asignación de sexo; así mismo, el diagnóstico temprano en varones afectados con la forma clásica perdedora de sal permite evitar las crisis que los conduzcan a una muerte temprana (16-18).
]]> En el presente estudio se analizaron 58 pacientes afectados de hiperplasia suprarrenal congénita y mediante las metodologías de PCR alelo específica y ACRS (Amplified Creation Restriction Sites) (reación de sitios de restricción mediante amplificación) se estudiaron 9 de las mutaciones más comúnmente asociadas con hiperplasia suprarrenal congénita. A pesar de que se han referenciado y descrito previamente (19), su frecuencia en Colombia no se ha determinado.Las titulaciones analizadas fueron:
1. Del 8 pb: corresponde a la deleción de 8 pares de bases en el exón 3, produce un desplazamiento en el marco de lectura y se relaciona con una actividad enzimática nula.
2. IVS2-12A/C-G: en esta mutación se cambia A (o C) por G en la posición 655, lo cual genera un nuevo sitio aceptor de empalme, y se crea un codón de parada prematuro en el exón 3; actividad enzimática nula.
3. ILE172ASN (I172 N): mutación de sentido equivocado (missense), con cambio de T por A en el codón 172 (exón 4). El aminoácido no polar isoleucina (ATC) es sustituido por el aminoácido polar aspargina (AAC). Se produce una desestabilización en la unión con la membrana del retículo endoplasmático liso; actividad enzimática del 2%.
4. VAL281LEU (V281L): mutación de sentido equivocado (missense), con cambio de G por T en el exón 7, codón 281, lo cual da como resultado el cambio del aminoácido valina (GTG) por leucina (TTG); este cambio no produce alteración de la afinidad de la enzima, pero sí provoca una disminución de ocho veces en su velocidad máxima; actividad enzimática del 50%.
5. GLN318TER (Q318X): mutación sin sentido (nonsense) con cambio de C por T en el exón 8, codón 318, que produce la sustitución del aminoácido glicina (CAG) por un codón de parada (TAG); actividad enzimática nula.
6. PRO453SER (P30L): mutación de sentido equivocado (missense), con cambio de C por T en el exón 10, codón 30, que produce el cambio del aminoácido prolina por leucina; actividad enzimática del 60%.
7. Agrupación del exón 6: IVS2-12A/C-G36N, V237E, M239K: es una agrupación de mutaciones en el exón 6 que corresponden al tipo de sentido equivocado (missense); Ile236 a Asn, Val237 a Glu y Met239 a Lys resultan de la transversiones T por A en las posiciones 1380, 1383 y 1389, respectivamente. Se producen sustituciones en esta región de la proteína con muchos residuos cargados; actividad enzimática nula.
8. ARG356TRP(R356W): mutación de sentido equivocado (missense), con cambio de C por T en el exón 8, codón 356, que produce un cambio de arginina por triptófano; actividad enzimática nula.
]]> 9. PRO453SER (P453S): se produce un cambio de C por T en el exón 10, codón 453, que produce cambio de prolina por serina, y se da una sustitución de un aminoácido conservado; actividad enzimática del 60%.Materiales y métodos
Se analizaron 58 pacientes no relacionados (116 cromosomas), afectados con hiperplasia suprarrenal congénita debida a déficit de 21 hidroxilasa. De ellos, 26 (44,8%) se clasificaron en la forma clásica perdedora de sal, 22 (37,9%) en la forma clásica virilizante simple, y 10 (17,2%) en la forma no clásica.
El diagnóstico de la forma clínica de hiperplasia suprarrenal congénita se hizo en el 69% de los pacientes por el grupo interdisciplinario que conforma la Clínica de Desarrollo Genital del Hospital de La Misericordia. El 31% restante fueron remitidos por medicina endocrinológica a la Fundación Arthur Stanley Gillow. Los criterios que tuvieron en cuenta los médicos remitentes para establecer el diagnóstico fueron la evaluación clínica y el análisis de los datos hormonales de 17-hidroxiprogesterona, testosterona, sulfato de dehidroepiandrosterona (DHEAS), Na y K, y en algunos casos, renina y cortisol.
El 46% de los pacientes afectados con hiperplasia suprarrenal congénita clásica, perdedora de sal, presentó genitales ambiguos al nacimiento, momento en el que se realizó el diagnóstico; el 19,2% de los casos fue diagnosticado en los primeros 6 meses de vida, mientras que en el resto de los pacientes el médico remitente no registró el dato de edad de diagnóstico. Para las formas virilizantes simples se reportó ambigüedad genital en el 45% de los casos; en el 4,5% de los pacientes, el diagnóstico se realizó antes del año de vida, y después del primer año de vida, en el 27,2%; no se registraron los datos del 22,7%. En las formas no clásicas, el 30% de los casos se diagnosticó entre los 20 y los 30 años; el 20%, entre los 30 y 40 años; el 10%, menos de 10 años, y no se reportó el dato de edad de diagnóstico en el 40% de los casos.
Luego de diligenciar el consentimiento informado, se tomaron muestras de sangre periférica de los pacientes analizados y, en algunos casos, de sus padres. Se realizó extracción del ADN mediante el método de salting out (20).
La metodología de PCR alelo-específica descrita por Wilson et al. (21) se utilizó para la identificación de las mutaciones puntuales P30L, IVS2-12A/C- G, del 8pb, I172N, cluster Ex6 (no se analizaron los cambios individuales), V281L, Q318X y R356W; cada muestra se analiza en reacciones separadas para la identificación de secuencias normales y mutadas. Si el individuo es homocigoto normal para una mutación dada, se genera un producto amplificado solamente en la mezcla de reacción que contiene los iniciadores que identifican la secuencia normal; si la muestra es heterocigota, se obtienen productos de las reacciones con iniciador normal y mutado y, si es homocigota, para la mutación la señal sólo se evidencia en la mezcla que contiene los iniciadores para la secuencia mutada (21).
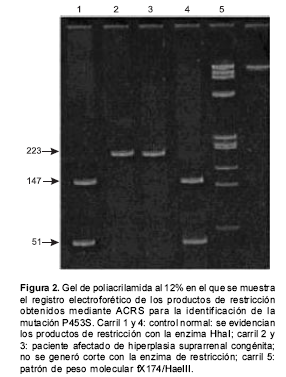
La mutación P453S se analizó por el método de creación de sitios de restricción mediante amplificación (ACRS), descrito por Oriola en 1997. Este método se basa en la amplificación de un segmento determinado con un par de iniciadores que presentan en su secuencia uno o varios nucleótidos modificados, de tal forma que el producto obtenido presenta ciertos cambios con respecto a la secuencia original sin involucrar la mutación específica, lo cual permite crear un sitio de reconocimiento para una determinada enzima de restricción. Para la identificación de P453S se utilizó la enzima de restricción HhaI que digiere los productos amplificados cuando la mutación no está presente (22).
Los productos de amplificación y restricción se analizaron en geles de agarosa (1,5%) y poli-acrilamida (12%), respectivamente (
figura 1 y figura 2). Se determinó el genotipo de cada paciente mediante la visualización de los productos sobre transiluminador y se analizó la frecuencia de las mutaciones estudiadas por conteo directo. Estos datos se compararon con los descritos en otros estudios a nivel mundial y, por medio de la prueba de una tabla de contingencia, se estableció la existencia de diferencias significativamente relevantes o su ausencia. Se consideró diferencia significativa para los valores de P menores de 0,05, con valor de significancia de 5% y un grado de libertad. ]]>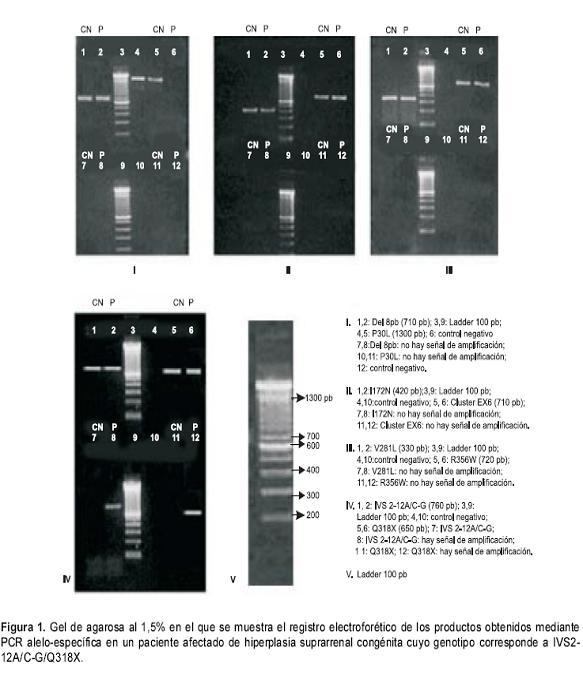

Resultados
En la población estudiada se encontró mutación en 96 de los 116 alelos analizados, lo que corresponde al 82,8%. De los 58 pacientes, en 40 fue posible identificar la mutación en los dos alelos (69%);la mayor proporción de alelos no genotipificados se presentó en la forma clásica perdedora de sal (11,9%), seguida de la virilizante simple (6,0%) y de la no clásica (0,9%). En 16 pacientes (8 con hiperplasia suprarrenal congénita clásica, perdedora de sal; 7 con hiperplasia suprarrenal congénita clásica, virilizante simple, y 1 con hiperplasia suprarrenal congénita no clásica) se identificó la mutación en uno de sus alelos, mientras que en dos pacientes con hiperplasia suprarrenal congénita clásica, perdedora de sal, no se identificó ninguna mutación. En total, se encontraron 19 genotipos diferentes en la población analizada (cuadro 1).
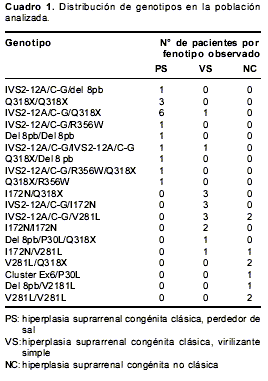
Del total de pacientes completamente genotipifi-cados, 75% fueron heterocigotos compuestos y 25% homocigotos. El genotipo predominante en la población general fue IVS2-12A/C-G/Q318X (12%).
La frecuencia de las 9 mutaciones en la población analizada se observa en la
figura 3; de allí se resalta que las mutaciones más frecuentes fueron IVS2-12A/C-G (26,7%) y Q318X (21,5%), mientras que ningún paciente analizado tenía la mutación P453S (0%). En el 17,2% de los alelos no se detectó ninguna de las 9 mutaciones analizadas. ]]>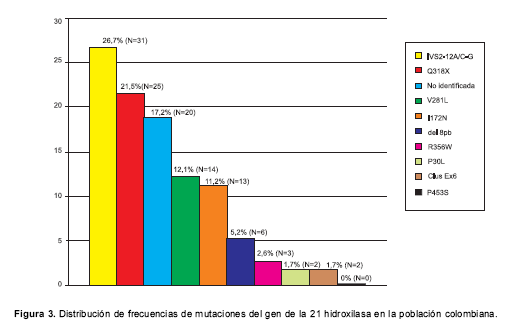
En cada forma clínica predominó alguna de las mutaciones, de tal forma que, en el fenotipo clásico perdedor de sal se encontraron con mayor frecuencia las mutaciones IVS2-12A/C-G y Q318X; en la virilizante simple, I172N, y en la no clásica, V281L (
figura 4).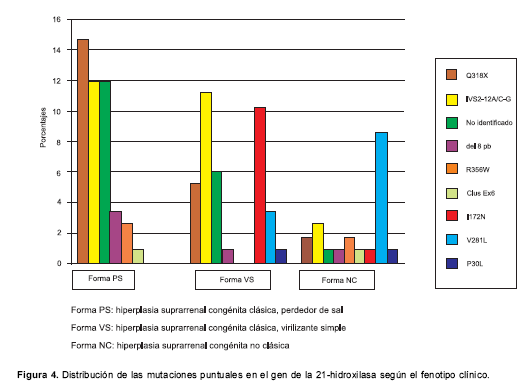
El análisis estadístico que permitió comparar los resultados obtenidos con los reportados en 19 estudios de diferentes partes del mundo indicó, en general, pocas diferencias estadísticamente significativas, excepto para países como Francia, Taiwán y Japón. La mutación Q318X mostró diferencia significativa con la mayoría de los países, excepto con Chile y Argentina.
Discusión
Con la metodología de PCR alelo-específica y la ACRS aplicada al análisis de las 9 mutaciones puntuales más frecuentemente asociadas con hiperplasia suprarrenal congénita, fue posible la identificación de mutaciones en el 82,8% de los alelos analizados. Este resultado está acorde con lo reportado en otros estudios que de manera similar han analizado únicamente mutaciones puntuales y han indicado valores de genotipificación que oscilan entre el 68% y el 80% (12,14,23). Teniendo en cuenta la naturaleza de las mutaciones que afectan el gen de la 21 hidroxilasa, este resultado está en el valor a priori que se podría esperar en estudios de mutaciones puntuales, ya que se ha determinado que las deleciones y las macroconversiones son el defecto molecular del 25% de los alelos afectados; los estudios que analizan conjuntamente mediante Southern blot o PMSG (multiplexed peptide mass signature genotyping) deleciones o macro-conversiones y mediante otros protocolos, mutaciones puntuales, han indicado que se puede lograr la identificación de hasta el 98% de los alelos afectados (24-26).
En el 17,2% de los alelos en los que no se detectó ninguna de las mutaciones en estudio, es posible que presenten deleciones, grandes conversiones y mutaciones puntuales indetectables con el presente diseño metodológico ya que, si bien es cierto que las 9 mutaciones analizadas son las más frecuentes, hasta la fecha se han descrito más de 50. La estrategia de la obtención de la secuencia del gen de la 21 hidroxilasa es la única metodología que permite reconocer el 100% de las mutaciones puntuales. La alta heterogeneidad de mutaciones que se presenta en el gen de la 21 hidroxilasa se debe a la alta homología de éste con el seudogen y al evento de conversión génica que lleva a la transferencia de mutaciones que determinan inactivación parcial o total del gen activo (14,27,28).
Los estudios latinoamericanos, como los desarrollados por Bachega, en Brasil, Dardi, en Argentina y Ordóñez-Sánchez en México, han reportado un porcentaje de alelos no identificados de hasta el 20%; esto ha llevado a suponer que existen diferencias en el acervo genético entre poblaciones caucásicas y latinoamericanas argumentado por la posibilidad que nuevas mutaciones estén presentes en nuestras poblaciones las cuales, muy probablemente, emergieron en poblaciones establecidas (23,29,30).
En la población analizada se observaron 19 genotipos diferentes, y se encontró en la forma clásica perdedora de sal una alta prevalencia de IVS2-12A/C-G/Q318X mientras que, en las formas clásicas virilizante simple y no clásica, no se presentó un genotipo relevante; aun así, el 60% de las personas con la forma virilizante simple tenía en uno de sus alelos, por lo menos, la mutación I172N y el 88,9% de las afectadas con la forma no clásica, la V281L. Esta observación y su relación con formas específicas de hiperplasia suprarrenal congénita ha sido también descrito en otras poblaciones y representa un conocimiento relevante en la aplicación de predicción de fenotipo en los estudios de diagnóstico prenatal (31). El 75% de los pacientes fueron heterocigotos compuestos y el 25%, homocigotos, resultado que es comparable con lo reportado en otros estudios (14). Esta característica tiene su implicación más importante en el hecho que, en la mayoría de los casos, la expresión clínica de la enfermedad se correlaciona con el alelo que está menos gravemente afectado; no obstante, se deben tener en cuenta otros factores como la presencia de múltiples mutaciones sobre un mismo alelo, las mutaciones en la región reguladora de la transcripción del gen, la alteración de proteínas reguladoras y la actividad 21hidroxilasa extra suprarrenal en las correlaciones genotipo-fenotipo (13,32).
]]> La asociación de ciertas mutaciones con formas específicas de la enfermedad está determinada por el grado de actividad enzimática que se ha atribuido mediante estudios in vitro a cada una de las mutaciones. Este y otros trabajos publicados en otras partes del mundo han indicado asociación de la mutación V281L con la hiperplasia suprarrenal congénita no clásica, I172N con hiperplasia suprarrenal congénita clásica virilizante simple, e IVS2-12A/C-G con hiperplasia suprarrenal congénita clásica perdedora de sal. Se han documentado algunas excepciones a estas categorizaciones en diferentes pacientes y es una de las posibles causas de discordancia entre el genotipo y el fenotipo (21,33).La frecuencia de la mutación Q318X evaluada en nuestra población fue la que mostró mayor diferencia significativa con el resto de las poblaciones analizadas; esta diferencia se encontró en 13 de los 19 reportes con los que se comparó. Es importante resaltar que no se observó ninguna diferencia significativa con un estudio previo realizado en la población colombiana ni con otras poblaciones latinoamericanas como Argentina y Chile, países en que se resalta la alta frecuencia de esta mutación (30,34). En la población española, que es influyente en nuestro acervo genético, la mutación Q318X es la cuarta en frecuencia con valores que alcanzan hasta el 9,2% (35). Esta es una observación muy importante ya que corresponde a una característica propia no sólo de la población colombiana sino de otros países latinoamericanos y es el reflejo de un posible efecto fundador.
En el 66,7% de las pacientes afectadas con la forma no clásica, uno de los alelos genotipificados correspondió a una de las mutaciones considerada como grave (IVS2-12A/C-G, Q318X y cluster Ex6); este hecho se ha reportado en otros estudios como el descrito por Deneux, en el cual se presenta el análisis molecular de la mayor cantidad de pacientes afectadas con esta forma clínica de la enfermedad, hecho que puede constituir una fuente de variación fenotípica en mujeres afectadas y significa, en términos prácticos, que un gran porcentaje de ellas pueden tener un hijo afectado con la forma clásica de la enfermedad, si el padre es heterocigoto portador de una mutación severo (8,36).
El conocimiento generado en este estudio es de gran importancia en la aplicación de metodologías moleculares que permitan realizar diagnóstico prenatal en gestantes con riesgo de tener fetos afectados. El tratamiento prenatal ha indicado tener una gran efectividad en evitar la virilización de fetos femeninos afectados con las formas más graves de la enfermedad, lo que evitaría el impacto psicológico, social y económico que trae consigo un caso de ambigüedad genital; así mismo, el diagnóstico temprano de fetos masculinos con la forma perdedora de sal permitirá la instauración de terapéutica precoz que evite la gran mortalidad asociada con las crisis de pérdida de sal que se presentan en los primeros días de vida. La implementación de estrategias moleculares que evalúen el gen de la 21-hidroxilasa es también de importancia en el apoyo diagnóstico de casos que no son concluyentes, hormonal o clínicamente.
El espectro analizado de las mutaciones en nuestro país, revela características propias de nuestra población, las cuales se han observado en otros países latinoamericanos, lo que determina la necesidad de realizar estudios futuros tendientes a caracterizar completamente los alelos de los pacientes afectados en búsqueda de nuevas mutaciones puntuales o rearreglos en el gen de la 21-hidroxilasa.
Conflicto de intereses
Los autores declaran que no tienen intereses de ningún tipo con las empresas comerciales que puedan beneficiarse de la presente investigación.
Agradecimientos
Los autores expresan sus agradecimientos a la Fundación Arthur Stanley Gillow, en cuyas instalaciones y equipos se realizó esta investigación; a Clemencia Sabogal y Heidi Mateus y a los miembros del grupo de la Clínica de Desarrollo Genital del Hospital de La Misericordia.
Financiación
]]> Esta investigación fue financiada con fondos de la Fundación Arthur Stanley Gillow, organismo privado sin ánimo de lucro, que posee y genera sus propios fondos, de acuerdo con las normas legales vigentes.Referencias
1. Donohoue P, Parker K, Migeon J. Congenital adrenal hyperplasia. En: The metabolic and molecular bases of inherited disease. New York: McGraw-Hill Inc.; 1995. p.2929-66. [ Links ]
2. Bornstein SR, Rutkowski H. The adrenal hormone metabolism in the immune/inflammatory reaction. Endocr Res 2002;28:719-28. [ Links ]
3. Guyton A. El riñón y los líquidos corporales. En: Fisiología médica. Octava edición. México, D.F.: Interamericana McGraw Hill; 1992. p.284-94. [ Links ]
4. Miller WL. Clinical review 54: genetics, diagnosis, and management of 21-hydroxylase deficiency. J Clin Endocrinol Metab 1994;78:241-6. [ Links ]
5. Dracopoulou-Vabouli M, Maniati-Christidi M, Dacou-Voutetakis C. The spectrum of molecular defects of the CYP21 gene in the Hellenic population: variable concordance between genotype and phenotype in the different forms of congenital adrenal hyperplasia. J Clin Endocrinol Metab 2001;86:2845-8. [ Links ]
6. Merke DP, Bornstein SR, Avila NA, Chrousos GP. Future directions in the study and management of congenital adrenal hyperplasia due to 21-hydroxylase deficiency. Ann Intern Med 2002;136:320-34. [ Links ]
7. Hughes IA. Congenital adrenal hyperplasia-a continuum of disorders. Lancet 1998;352:752-4. [ Links ]
8. Deneux C, Tardy V, Dib A, Mornet E, Billaud L, Charron D et al. Phenotype-genotype correlation in 56 women with nonclassical congenital adrenal hyperplasia due to 21-hydroxylase deficiency. J Clin Endocrinol Metab 2001;86:207-13. [ Links ]
9. Kovacs J, Votava F, Heinze G, Solyom J, Lebl J, Pribilincova Z et al. Lessons from 30 years of clinical diagnosis and treatment of congenital adrenal hyperplasia in five middle European countries. J Clin Endocrinol Metab 2001;86:2958-64. [ Links ]
10. Morel Y, Tardy V. Molecular genetics of 21-hydroxylase deficient adrenal hyperplasia. En: Azziz R, Nestler JE, Dewailly D, editors. Androgen excess disorders in women. Philadelphia: Lippincott-Raven; 1997. p.159-7. [ Links ]
11. Miller WL, Morel Y. The molecular genetics of 21- hydroxylase deficiency. Annu Rev Genet 1989;23: 371-93. [ Links ]
12. Baumgartner-Parzer SM, Schulze E, Waldhausl W, Pauschenwein S, Rondot S, Nowotny P et al. Mutational spectrum of the steroid 21- hydroxylase gene in Austria: Identification of a novel missense mutation. J Clin Endocrinol Metab 2001;86:4771-5. [ Links ]
13. Koyama S, Toyoura T, Saisho S, Shimozawa K, Yata J. Genetic analysis of Japanese patients with 21- hydroxylase deficiency: identification of a patient with a new mutation of a homozygous deletion of adenine at codon 246 and patients without demonstrable mutations within the structural gene for CYP21. J Clin Endocrinol Metab 2002;87:2668-73. [ Links ]
14. Krone N, Braun A, Roscher AA, Knorr D, Schwarz HP. Predicting phenotype in steroid 21-hydroxylase deficiency? Comprehensive genotyping in 155 unrelated, well defined patients from Southern Germany. J Clin Endocrinol Metab 2000;85:1059-65. [ Links ]
15. Sinnott P, Collier S, Costigan C, Dyer PA, Harris R, Strachan T. Genesis by meiotic unequal crossover of a de novo deletion that contributes to steroid 21- hydroxylase deficiency. Proc Natl Acad Sci USA 1990; 87:2107-11. [ Links ]
16. Mercado AB, Wilson RC, Cheng KC, Wei JQ, New MI. Prenatal treatment and diagnosis of congenital adrenal hyperplasia owing to steroid 21-hydroxylase deficiency. J Clin Endocrinol Metab 1995;80:2014-20. [ Links ]
17. Belgorosky A, Marino R, Rivarola M. Molecular analysis of the 21-hydroxylase gene. Clin Endocrinol 2003;58:247. [ Links ]
18. Bartha JL, Finning K, Soothill PW. Fetal sex determination from maternal blood at 6 weeks of gestation when at risk for 21 hydroxylase deficiency. Obstet Gynecol 2003;101:1135-6. [ Links ]
19. OMIM, Online Mendelian Inheritance in Man. http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?db=OMIM
20. Miller SA, Dykes DD, Polesky HF. A simple salting out procedure for extracting DNA from human nucleated cells. Nucleic Acids Res 1988;12:1215. [ Links ]
21. Wilson RC, Wei JQ, Cheng KC, Mercado AB, New MI. Rapid deoxyribonucleic acid analysis by allele-specific polymerase chain reaction for detection of mutations in the steroid 21-hydroxylase gene. J Clin Endocrinol Metab 1995;80:1635-40. [ Links ]
22. Oriola J, Plensa I, Machuca I, Pavia C, Rivera-Fillat F. Rapid screening method for detecting mutations in the 21-hydroxylase gene. Clin Chem1997;43:557-61. [ Links ]
23. Bachega TA, Billerbeck AE, Madureira G, Marcondes JA, Longui CA, Leite MV et al. Molecular genotyping in Brazilian patients with the classical and nonclassical forms of 21-hydroxylase deficiency. J Clin Endocrinol Metab 1998;83:4416-9. [ Links ]
24. Ferenczi A, Garami M, Kiss E, Pek M, Sasvari-Szekely M, Barta C et al. Screening for mutations of 21-hydroxylase gene in Hungarian patients with congenital adrenal hyperplasia. J Clin Endocrinol Metab 1999;84:2369-72. [ Links ]
25. Zeng X, Witchel SF, Dobrowolski SF, Moulder PV, Jarvik JW, Telmer CA. Detection and assignment of CYP21 mutations using peptide mass signature genotyping. Mol Genet Metab 2004;82:38-47. [ Links ]
26. Tukel T, Uyguner O, Wei JQ, Yuksel-Apak M, Saka N, Song DX et al. A novel semiquantitative polymerase chain reaction/enzyme digestion-based method for detection of large scale deletions/conversions of the CYP21 gene and mutation screening in Turkish families with 21-hidroxylase deficiency. J Clin Endocrinol Metab 2003;88:5893-7. [ Links ]
27. Lee HH, Chao HT, Lee YJ, Shu SG, Chao MC, Kuo JM et al. Identification of four novel mutations in the CYP21 gene inn congenital adrenal hyperplasia in the Chinese. Hum Genet 1998;103:304-10. [ Links ]
28. Lajic S, Wedell A, Bui TH, Ritzen EM, Holst M. Long term somatic follow-up of prenatally treated children with congenital adrenal hyperplasia. J Clin Endocrinol Metab 1998;83:3872-80. [ Links ]
29. Ordóñez-Sánchez ML, Ramírez-Jímenez S, López-Gutiérrez AU, Riba L, Gamboa-Cardiel S, Cerrillo-Hinojosa M et al. Molecular genetic analysis of patients carrying steroid 21-hydroxylase deficiency in the Mexican populations: identification of possible new mutations and high prevalence of apparent germ-line mutations. Hum Gen 1998;102:170-7. [ Links ]
30. Dardis A, Bergada I, Bergada C, Rivarola M, Belgorosky A. Mutations of the steroid 21-hydroxylase gene in an Argentinian population of 36 patients with classical congenital adrenal hyperplasia. J Pediatr Endocrinol Metab 1997;10:55-61. [ Links ]
31. New MI, Carlson A, Obeid J, Marshall I, Cabrera MS, Goseco A et al. Prenatal diagnosis for congenital adrenal hyperplasia in 532 pregnancies. J Clin Endocrinol Metab 2001;86:5651-7. [ Links ]
32. Speiser PW, Dupont J, Zhu D, Serrat J, Buegeleisen M, Tusie-Luna MT et al. Disease expression and molecular genotype in congenital adrenal hyperplasia due to 21- hydroxylase deficiency. J Clin Invest 1992;90: 584-95. [ Links ]
33. Torres N, Mello MP, Germano CM, Elias LL, Moreira AC, Castro M. Phenotype and genotype correlation of the microconversion from the CYP21A1p to the CYP21A2 gene in congenital adrenal hyperplasia. Braz J Med Biol Res 2003;36:1311-8. [ Links ]
34. Pineda P, Fardella C, Poggi H, Torrealba I, Cattani A, Soto J et al. Diagnóstico molecular de hiperplasia suprarrenal congénita por déficit de 21-hidroxilasa, variedad perdedora de sal, en población chilena. Rev Med Chile 1997;125:987-92. [ Links ]
35. Lobato MN, Ordóñez-Sánchez L, Tusié-Luna M, Meseguer A. Mutation analysis on patients with congenital adrenal hyperplasia in the Spanish population: identification of putative novel steroid 21-hydroxylase deficiency alleles associated with the classic form of the disease. Hum Hered 1999;49:169-75. [ Links ]
36. Berenbaum SA, Bailey JM. Effects on gender identity of prenatal androgens and genital appearance: evidence from girls with congenital adrenal hyperplasia. J Clin Endocrinol Metab 2003;88:1102-6. [ Links ] ]]>