Catalase, Peroxidase and Polyphenoloxidase from Pitaya Amarilla (Acanthocereus pitajaya) Fruits: Ripening and Senescense
LUCÍA ESTRELLA BAQUERO DUARTE, JHON ALEXANDER CASTRO RIVERA, CARLOS EDUARDO NARVÁEZ CUENCA
Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia, Bogotá, Colombia.
Presentado abril 1 de 2005, aceptado junio 13 de 2005, correcciones agosto 9 de 2005.
RESUMEN
Se evaluó la relación entre algunos síntomas de deterioro y la actividad de enzimas vinculadas tanto con el pardeamiento como con el sistema antioxidante en frutos de pitaya amarilla (Acanthocereus pitajaya) cosechados en su madurez fisiológica y almacenados durante 15 días a 24 °C y 85% de humedad relativa. En los frutos enteros se evaluaron la intensidad respiratoria y el color externo; en la corteza se determinaron la actividad de catalasa (CAT), peroxidasa (POD) y polifenoloxidasa (PFO). Los frutos exhibieron un comportamiento climatérico luego de seis días de la cosecha. El pardeamiento de la corteza tuvo una relación directa con la actividad de POD y PFO. La máxima actividad de CAT observada en el climaterio responde al balance adecuado con la alta producción de H2O2 esperada en ese momento.
Palabras clave: catalasa, peroxidasa, polifenoloxidasa, maduración, Acanthocereus pitajaya.
ABSTRACT
We evaluate the relation between some symptoms of deterioration and the activity of enzymes entailed with both the browning and the antioxiding system in fruits of yellow pitaya (Acanthocereus pitajaya), harvested in its physiological maturity and stored for 15 days at 24°C and 85% of relative humidity. In the whole fruits, the respiratory intensity and the external colors were evaluated; further, the activity of catalase (CAT), peroxidase (POD) and polyphenoloxidase (PPO) was studied in the peel of the fruit. The fruit exhibited a climacteric behavior six days after the date of the harvest. The browning of the peel had a direct relation with the activity of POD and PPO. The maximum observed activity of CAT in the climacterium, responds to the proper balance with the high production of H2O2 expected at that moment.
]]> Key words: Catalase, peroxidase, polyphenoloxidase, ripening, Acanthocereus pitajaya.INTRODUCCIÓN
La pitaya amarilla es una cactácea originaria de la región Caribe de Suramérica. En Colombia se cultiva en departamentos como Boyacá, Cundinamarca, Cauca, Caldas, Valle y Tolima. Este fruto está reportado con un diverso número de nombres científicos, dentro de los que se encuentra Acanthocereus pitajaya, Cereus triangularis, Acanthocereus colombianus, Hylocereus triangularis, Selenicereus megalanthus, Hylocereus sp. (Bibliowicz y Hernández, 1998). La pitaya amarilla es un fruto exótico que se ha abierto a un mayor número de adeptos tanto en Colombia como en el exterior. Teniendo en cuenta las exportaciones totales de los últimos cuatro años, el país ha recibido en promedio por año US$ 637.883 por 111.642 Kg de pitaya amarilla (DANE, 2004), índice que puede ir en aumento dada su mayor aceptación por parte de los mercados nacionales e internacionales gracias a su exótico sabor dulce y refrescante, además de sus propiedades biofuncionales y medicinales (Patiño y Rodríguez, 2003).
Durante el almacenamiento de la pitaya amarilla a diversas temperaturas se reporta que el pardeamiento y la necrosis parcial de la corteza aparecen como principales factores de deterioro, constituyendo una de las principales causas de las pérdidas poscosecha (Camargo y Moya, 1995; Patiño y Rodríguez, 2003). Mientras que el pardeamiento ha sido relacionado con la acción de la polifenoloxidasa (CE 1.10.3.2, PFO) y de la peroxidasa (CE 1.11.1.7, POD; Mayer, 1987; Halpin et al., 1989; Cano et al., 1990; Takahama y Egashira, 1991; Marín y Cano, 1992; Fúster et al., 1994; Sánchez Ferrer et al., 1995; Rubio, 1999; Martínez Parra y Muñoz, 2001; Stewart et al., 2001; Narváez y Restrepo, 2003; Zhou et al., 2003; Rivera et al., 2004), la necrosis y los eventos que conducen a la senescencia de los frutos se han vinculado con el incremento de las especies reactivas de oxígeno (EROS), entre las que se encuentran los radicales superóxido (O2-.), oxígeno singlete (O21), radicales hidroxilo (OH) y peróxido de hidrógeno (H2O2; Rogiers et al., 1998; Hansberg, 2002; Jiménez et al., 2002). Es así como los niveles de H2O2 deben ser controlados por cuanto pueden originar radicales hidroxilo (OH), que son los principales agentes oxidantes de las proteínas, ácidos nucleicos y lípidos (Hansberg, 2002). En el control de las EROS actúan enzimas como: la superóxido dismutasa (SOD, EC 1.15.1.1) que dismuta los superóxidos a H2O2 y O2, y la catalasa (CAT, EC 1.11.1.6) que convierte el H2O2 en H2O y O2. El H2O2 también puede ser degradado por la guaiacol peroxidasa (POD, EC 1.11.1.7) en tetrahidroguaiacol y por la ascorbato peroxidasa (APX, EC 1.11.1.11) en agua más alcohol, empleando como donador de protones el guaiacol y el ascorbato, respectivamente. La APX reutiliza el ascorbato reducido por la glutation reductasa (GR, EC 1.6.4.2; Cano et al., 1990; Stryer, 1995; Sala y Lafuente, 1999; Gong et al., 2000; Sala y Lafuente, 2000).
Entorno al pardeamiento se sabe que PFO y POD catalizan la oxidación de fenoles propios de las células a quinonas, las cuales son altamente reactivas con proteínas, ácidos nucleicos, flavonoides y otras quinonas; estas reacciones, además de generar colores pardos, reducen las propiedades sensoriales de textura, color y savor, disminuyen la calidad nutricional del alimento y desembocan finalmente en la muerte del fruto (Mayer y Harel, 1979; Mayer, 1987; Halpin et al., 1989; Cano et al., 1990;Takahama y Egashira, 1991; Marín y Cano, 1992; Fúster et al., 1994; Sánchez Ferrer et al., 1995; Rubio, 1999; Martínez Parra y Muñoz, 2001; Stewart et al., 2001; Narváez y Restrepo, 2003; Zhou et al., 2003; Rivera et al., 2004). La POD tiene la capacidad de degradar el H2O2 a expensas del consumo de sustancias de tipo fenólico, aunque con la generación de sustancias pardas, razón por la cual ha sido ubicada dentro del sistema enzimático antioxidante (Hansberg, 2002).
El interés de este trabajo es evaluar el papel que desempeñan CAT, POD y PFO durante la maduración y senescencia de la pitaya amarilla, con el objeto de proporcionar herramientas que contribuyan con el desarrollo de métodos efectivos que disminuyan el pardeamiento de la corteza de la pitaya amarilla durante su comercialización, y por lo tanto, se logre prolongar su vida útil en anaquel; además de evidenciar el funcionamiento complementario que presentan estas enzimas en el sistema antioxidante del fruto.
MATERIALES Y MÉTODOS
Material vegetal. Los frutos de pitaya amarilla fueron clasificados con el cód. COL314508 como Acanthocereus pitajaya por el Herbario Nacional Colombiano del Instituto de Ciencias Naturales de la Universidad Nacional de Colombia. Los frutos, de pulpa blanca, se adquirieron en los principales mercados de Bogotá, Colombia, en estado verde-pintón (verde 90%-amarillo 10%), visiblemente sanos. Una vez los frutos fueron desinfectados con hipoclorito de sodio al 10%, se almacenaron a 24 °C durante 15 días a una humedad relativa del 85% y con fotoperíodos naturales de iluminación, dado que se buscó simular las condiciones normales de maduración. Cada tres días fueron retirados de la cámara de almacenamiento, completamente al azar, tres frutos y sobre cada uno de ellos se efectuó la medida de la intensidad respiratoria y el análisis sensorial del color de la corteza. Posteriormente, se retiró la corteza y sobre cada una de las tres muestras se efectuó la extracción de proteínas solubles, se cuantificaron la proteína y la actividad de CAT, POD y PFO.
Intensidad respiratoria. Se evaluó el CO2 producido por los frutos a través de la técnica cromatográfica. La pitaya fue pesada y encerrada por más de una hora (tiempo en que el fruto respira y modifica la atmósfera) en una cámara hermética de vidrio con una capacidad de 2 L, luego se hizo un muestreo 1,00 mL de aire interno y se inyectó en el cromatógrafo de gases. Se empleó un cromatógrafo de gases Hewlett Packard 5890, con columna Carbosieve S II empacada a base de carbón activado y tamiz molecular a una temperatura inicial de 35 °C y rampa de calentamiento hasta 200 °C, con He como gas de arrastre a 32 mL/min, con sistema split 30:1 y detector de conductividad térmica a 250 °C. La cuantificación se hizo por el método de estándar externo empleando CO2 adquirido en AGA-FANO®. La intensidad respiratoria se reportó como mg de CO2 kg-1 de fruta h-1 (Rubio, 1999).
Color sensorial. Se evaluó el color de la corteza de los frutos enteros mediante la aplicación del método de puntajes por parte de un panel entrenado de catadores. Los descriptores de los atributos a evaluar fueron definidos en un trabajo previo (Camargo y Moya, 1995) y se muestran en la tabla 1.
| Puntuación | Descripción |
| (6) | Amarillo intenso característico; puede presentar leve coloración café en la punta de las mamilas o coloración verde en un 20 a 30%. |
| (3-5) | Color rojizo hasta un 60%, y lo restante de color amarillo. |
| (0-1) | Color rojizo en más de un 60% de la corteza o color verde, en una proporción mayor al 70% de la misma. |
ACTIVIDAD ENZIMÁTICA
Extracción de las enzimas. La técnica de extracción simultánea para las tres enzimas empleada en este trabajo se basó en reportes previos, en los que se obtenía una buena eficiencia en la extracción de proteína y en la actividad enzimática (Sala y Lafuente, 1999; Narváez, 2002; Rivera et al., 2004). Los polvos de acetona permitieron que el extracto presentara una alta actividad con una mayor estabilidad, además de evitar la inactivación enzimática durante la extracción, porque con la acetona se retiran los fenoles, b-carotenos y ácidos orgánicos del extracto disminuyendo así la reacción de las enzimas. Se empleó la relación (1:5) corteza:extractante en la que se obtuvo mayor eficiencia en la extracción de proteína y que a su vez fue cuantificable (datos no mostrados). Se emplearon 5 g de muestra representativa del total de la corteza del fruto, se homogenizaron con 25 mL de acetona a -8 °C, se filtró al vacío, y el retenido (polvos de acetona) fue lavado dos veces con 25 mL de acetona a -8 °C hasta que estuviera blanco. Los polvos de acetona fueron resuspendidos en 25 mL buffer de fosfatos 200 mM, pH 6,8 bajo agitación continua por 24 h a 2 °C. Posteriormente, la suspensión fue centrifugada a 12.000 x g durante 20 min a 2 ºC; el sólido se desechó, el sobrenadante fue mantenido a 2 ºC durante máximo 2 h, tiempo en el que se efectuó la cuantificación de proteína y de actividad enzimática. Las medidas de actividad enzimática fueron desarrolladas a las condiciones de temperatura, pH y concentración de sustrato en las que se obtuvieron las máximas respuestas, evaluadas en un trabajo previo en nuestro laboratorio (Castro, 2005).
Cuantificación de proteína. Para cuantificar la proteína en los extractos enzimáticos se empleó el método de Bradford modificado por Zor y Sellinger (1996), en el que se mide la absorbancia a 450 y 590 nm y se interpola la relación entre las dos absorbancias en la curva de calibración. Para la curva de calibración se usó como patrón de proteína la albúmina sérica bovina (BSA) y se graficó la relación entre las absorbancias para las dos longitudes de onda A590nm / A450nm contra diferentes concentraciones de proteína.
Medida de actividad de CAT. Para la medida de actividad CAT se empleó el método permanganométrico (Ulrich, 1974). La mezcla de reacción con volumen final de 1 mL, contenía 100 μL de extracto enzimático (24 – 40 μg de proteína), H2O2 500 mM preparado en buffer fosfatos 200 mM pH 7,0; esta mezcla se mantuvo a 40 °C. Luego de 5 min de reacción se adicionaron 250 μL de H2SO4 (1:3) para desnaturalizar la enzima y detener la descomposición del H2O2. Al final, se tituló el H2O2 no descompuesto con KMnO4 estandarizado (10 mM). Puesto que dentro del extracto enzimático pueden existir otros componentes diferentes a la CAT que descompongan el H2O2 se efectuó un blanco; éste se preparó de la misma manera que las mezclas de reacción aunque con la incorporación del H2SO4 (1:3) previa a la adición del extracto enzimático, asegurando el no consumo de peróxido por parte de la enzima. Una unidad de actividad (UCAT) fue definida como los μmol H2O2 descompuesto/min. La actividad específica fue expresada en unidades de actividad por mg de proteína (UCAT/mg proteína).
Medida de actividad de POD. La actividad POD fue estimada por la medida del incremento de la absorbancia a 470 nm (Halpin et al., 1989) en un espectrofotómetro Genesys 5 UV-VIS cada 5 s durante 120 s. La celda de medida, para un volumen final de 2 mL, contenía 200 μL de extracto enzimático (48–80 μg de proteína) y una mezcla de guaiacol/H2O2 40mM/20mM en buffer de fosfatos pH 5,5; esta mezcla se mantuvo a 25 °C. El blanco difería en que el extracto enzimático fue hervido previamente en un baño maría a 92 °C durante 10 min asegurando la desnaturalización de la enzima, y en consecuencia, la no reacción con el sustrato. Una unidad de actividad (UPOD) fue definida como el cambio en una unidad de absorbancia por min. La actividad específica fue expresada en unidades de actividad por mg de proteína (UPOD/mg proteína).
Medida de actividad de PFO. Para medir la actividad de PFO se efectuó lectura de absorbancia a 475 nm (Sánchez Ferrer et al., 1995) en un espectrofotómetro Genesys 5 UV-VIS cada 5 s durante 120 s. La mezcla de reacción de 2 mL consistió en 1000 μL de extracto enzimático (240-400 μg de proteína) más L-DOPA 14 mM en buffer de fosfatos 200 mM pH 7,0; esta mezcla se mantuvo a 37 °C. El blanco fue preparado en forma igual que en POD. Tanto la unidad de actividad (UPFO) como la actividad específica (UPFO/mg proteína) fueron definidas de igual manera que en POD.
Análisis de datos. Debido a que los resultados de la evaluación sensorial no siguen una distribución normal y son discontinuos, fueron analizados por la prueba de Friedman. Se evaluaron las diferencias entre muestras por la prueba de la diferencia mínima significativa (dms) y se hallaron las modas (n = 15). Sobre las demás variables de respuesta se calcularon los valores promedio (n = 3), se efectuaron los ANOVA y se evaluaron las diferencias entre tratamientos por la prueba de Tukey.
RESULTADOS Y DISCUSIÓN
Intensidad respiratoria. En la figura 1 A se puede observar la tendencia respiratoria del fruto durante el tiempo de almacenamiento a 24 ºC que corresponde al comportamiento típico de un fruto climatérico, en el que se perciben dos fases: primera fase de los días 0 al 6, etapa en donde se observa un aumento de CO2 hasta el máximo respiratorio (máximo climatérico) en el día 6, que coincide con la mayor calificación en el color de la corteza; en la segunda fase, de los días 9 al 15, comienza la etapa desenescencia en donde disminuye la producción de CO2. De acuerdo con la prueba de Tukey la respiración de los frutos en el sexto día fue superior, de forma significativa, respecto de los otros días.
]]>
Figura 1A. Comportamiento respiratorio del fruto entero y B color sensorial de la corteza de los frutos de pitaya amarilla (Acanthocereus pitajaya) almacenados a 24 °C al 85% de humedad relativa durante 15 días. En A las letras diferentes indican diferencias significativas de acuerdo con la prueba de Tukey (n = 3), mientras que en B las letras diferentes indican diferencias significativas según la prueba de Friedman-dms (n = 15).
En la primera fase, los ácidos orgánicos, lípidos, carbohidratos y proteínas son metabolizados por el fruto produciendo en gran cantidad CO2, H2O y energía, por lo que se observa un aumento abrupto en la intensidad respiratoria del fruto. Todas las reacciones que ocurren durante la etapa comprendida entre los días 0 (madurez fisiológica) y 6 (madurez sensorial) conducen al desarrollo de las características sensoriales óptimas de color, textura, sabor y aroma. En la segunda fase se producen un conjunto de reacciones enzimáticas que conducen a la pérdida de la integridad celular, dentro de las que se pueden destacar las reacciones de pardeamiento, en las que actúan enzimas como polifenoloxidasas y peroxidasas sobre los fenoles, ocasionando condensaciones y polimerizaciones que generan los colores pardos en el fruto. El hecho de que los frutos de pitaya amarilla sean climatéricos indica que éstos siguen madurando aún después de haber sido cosechados, por lo que presentan un metabolismo activo (Narváez, 2002). Sin embargo, en otros trabajos se reporta que el etileno no puede ser cuantificado durante el curso de la maduración de estos frutos, por lo que algunos autores lo han clasificado como un fruto no climatérico (Patiño y Rodríguez, 2003). El máximo respiratorio observado en este trabajo se presentó de manera más temprana al reportado en trabajos previos en los que los frutos fueron almacenados a temperaturas entre 18 y 19 °C, temperaturas en las que la madurez sensorial se alcanzó entre los 13 y 15 días luego de la cosecha (Camargo y Moya, 1995; Patiño y Rodríguez, 2003). Lo anterior está en concordancia con lo planteado en estudios de almacenamiento a diferentes temperaturas (Wang, 2000), en los que se indica que la disminución en la temperatura de almacenamiento retarda la maduración, siempre y cuando ésta no se ubique por debajo de la temperatura crítica.
Color sensorial. En cuanto al color de la corteza se observó su máximo desarrollo después de seis días de almacenamiento (Fig. 1B), de acuerdo con la prueba de Friedman y el criterio de la diferencia mínima significativa se encontró que este atributo fue significativamente mayor en este día. Durante los primeros seis días el color de la corteza de la pitaya evolucionó desde verde pintón hasta el amarillo brillante característico; después del climaterio el pardeamiento se evidenció con la aparición de manchas entre rosadas y marrón, que con el tiempo se incrementaron en área, número e intensidad.
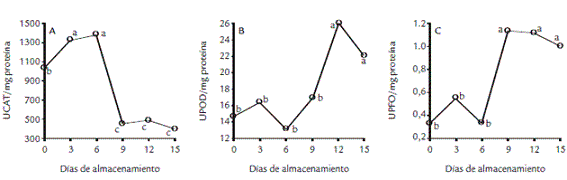
Actividad enzimática. En la figura 2A se observa que la actividad de CAT desde el día 0 al 6 es estadísticamente mayor que la actividad en los frutos senescentes, de acuerdo con la prueba de Tukey. Es importante anotar que aunque la actividad de la primera fase es alta, en el día 6 la actividad es máxima, coincidente con el máximo climatérico y la mayor calificación de color.
Figura 2. Actividad de A catalasa, B peroxidasa y C polifenoloxidasa en la corteza de los frutos de pitaya amarilla (Acanthocereus pitajaya) almacenados a 24 °C al 85% de humedad relativa durante 15 días. Letras diferentes indican diferencias significativas de acuerdo a la prueba de Tukey (n = 3).
Para POD (Fig. 2B), de acuerdo con la prueba de Tukey, se encontró que la actividad permaneció significativamente igual durante los nueve primeros días de almacenamiento y se incrementó de manera significativa en los frutos senescentes. La actividad de PFO (Fig. 2C), según la prueba de Tukey, permaneció estadísticamente igual desde el inicio del almacenamiento hasta el máximo climatérico. Posterior a este evento, la actividad se incrementó de manera significativa.
Las tendencias en las actividades enzimáticas observadas en este trabajo son similares a las encontradas en otros ensayos de almacenamiento en fresco: CAT en uva caimarona (Pourouma cecropiifolia; Narváez y Restrepo, 2003), POD tanto en kiwi (Actinida deliciosa); (Fúster et al., 1994), en mango (Mangifera indica; Marín y Cano, 1992) como en uva caimarona (Narváez y Restrepo, 2002) y PFO en lulo (Solanum quitoense; Rubio, 1999).
Es conocido que entre la madurez fisiológica y la madurez sensorial debe haber un alto metabolismo oxidativo con un alto consumo de O2. Esto favorece la aparición del O2 -. que es dismutado por SOD a H2O2, cuando la catalasa cumple un papel importante degradándolo. La actividad de CAT observada en el presente trabajo da una clave del por qué en el climaterio el fruto no se deteriora. Aunque durante el desarrollo de las características sensoriales la producción de H2O2 debe ser alta, la actividad de CAT también lo es, con su máximo valor en el pico climatérico, probablemente garantizando un equilibrio adecuado entre oxidantes y antioxidantes. Después del climaterio la oxidación continúa pero la actividad de CAT decae, por esto el equilibrio entre la producción y degradación de EROS se ve inclinado hacia lo primero. Si POD también consume H2O2 y su actividad es máxima en la senescencia, surge entonces la pregunta de por qué las frutas se deterioran. Esto sugiere que la CAT es más efectiva en la degradación del H2O2 que la POD, y además que la POD en el proceso de degradación del peróxido genera el pardeamiento. En general, se sabe que las CAT tienen bajas afinidades por el H2O2 si se comparan con las afinidades que suelen tener las POD por este mismo compuesto. Esto significa que las CAT toleran altas concentraciones de peróxido, exhibiendo bajas actividades a bajas concentraciones de peróxido; pero presentan altas actividades cuando la concentración de su sustrato es alta (Switala y Loewen, 2002).
]]> El aumento de actividad de POD y PFO en la etapa de senescencia, observado en este trabajo, puede darse por la activación de formas latentes, solubilización de las que estaban unidas a la pared celular (POD) y a membranas de organelos (PFO) o por síntesis de novo (Grierson y Pilet, 1984; Mayer, 1987; Fúster et al., 1994; Stewart et al., 2001). Considerando que en la senescencia los niveles de H2O2 se incrementan y que se produce lisis de las vacuolas que contienen los fenoles (Rogiers et al., 1998), se darían las condiciones adecuadas para que la actividad enzimática aumente significativamente, permitiendo así que esa actividad enzimática medida in vitro sea manifestada in vivo como el pardeamiento enzimático.Puesto que se encontró que la CAT muestra una alta actividad durante el desarrollo sensorial de los frutos de pitaya, y que la PFO y POD exhiben una alta actividad en frutos senescentes, en donde el pardeamiento y la necrosis fueron evidentes, se sugiere que la efectividad de los tratamientos de poscosecha que se apliquen a esta fruta deben estar enfocados en estimular la actividad de CAT e inhibir la de POD y PFO para asegurar un alargamiento en la vida útil de la pitaya amarilla (Camargo y Moya, 1995; Patiño y Rodríguez, 2003). Es así como en el intento de usar la refrigeración, como técnica para prolongar la vida útil de diversos vegetales, se ha encontrado que las lesiones generadas a causa del frío están relacionadas con una mayor actividad de PFO y menor actividad de CAT respecto de las frutas no refrigeradas. Igualmente, la tolerancia al frío inducida por ejemplo con tratamientos térmicos previos a la refrigeración, incrementan la actividad de CAT y disminuyen la de PFO; sin embargo, en este mismo tipo de trabajos no se ha encontrado una relación clara entre la actividad de POD y la sensibilidad-tolerancia al frío (Rubio, 1999; Sala y Lafuente, 1999 y 2000; Kang et al., 2002; Kang y Saltveit, 2002; Narváez y Restrepo, 2002; Zhou et al., 2003; Narváez y Restrepo, 2003; Rivera et al., 2004). Sería interesante efectuar un estudio de la actividad de estas enzimas tras la aplicación del choque térmico en pitaya amarilla a 25 ºC durante 24 h previo a la refrigeración a 2 ºC, puesto que se ha evidenciado que este tratamiento disminuye las lesiones por frío (Camargo y Moya, 1995).
AGRADECIMIENTOS
Los autores desean expresar sus agradecimientos a la Universidad Nacional de Colombia por el apoyo económico e infraestructura brindados para la ejecución de este trabajo.
BIBLIOGRAFÍA
BIBLIOWICKS A, HERNÁNDEZ LM. Organismos fungosos presentes en las estructuras reproductivas de la pitaya amarilla. [Trabajo de pregrado]. Bogotá, Colombia: Facultad de Agronomía, Universidad Nacional de Colombia. 1998. [ Links ]
CAMARGO A, MOYA OL. Influencia del choque térmico en la inhibición de los daños por frío en la pitaya amarilla (Acanthocereus pitajaya). [Trabajo de pregrado]. Bogotá, Colombia: Facultad de Ciencias, Departamento de Farmacia, Universidad Nacional de Colombia. 1995. [ Links ]
CANO P, MARÍN MA, FÚSTER C. Effects of Some Thermal Treatments on Polyphenoloxidase and Peroxidase Activities of Banana (Musa cavendishii, var enana). J Sci Agric. 1990;51:223-131.
CASTRO RJA. Extracción y caracterización parcial de polifenoloxidasa y peroxidasa de frutos de pitaya amarilla (Acanthocereus pitajaya). [Trabajo de pregrado]. Bogotá, Colombia: Facultad de Ciencias, Departamento de Química, Universidad Nacional de Colombia. 2005. [ Links ]
DANE (Departamento Administrativo Nacional de Estadística). Cálculos Proexport - Colombia. 2004. Disponible en: URL: http://www.Proexport.com.co/estudiosBID. [ Links ]
FÚSTER C, PRÉSTAMO G, CANO MP. Drip Loss, Peroxidase and Sensory Changes in Kiwi Fruit During Frozen Storage. J Sci Food Agric. 1994;64:23-19.
GONG Y, TOIVONEN PMA, WIERSMA PA, LU C. Effect of Freezing on the Activity of Catalase in Apple Flesh Tissue. J Agric Food Chem. 2000;48:5537-5542. [ Links ]
GRIERSON R, PILET PE. Cytoplasmatic and Wall Isoperoxidases in Growing Maize Roots. J Plant Physiol. 1984;118:189-199. [ Links ]
HALPIN B, PRESSEY R, JEN J, MONDY N. Purification and Characterization of Peroxidase Isoenzymes from Green Peas (Pisum sativum). J. Food Sci. 1989; 54: 644-649. [ Links ]
HANSBERG TW. Biología de las especies de oxígeno reactivas. Mensaje bioquímico. 2002;26:19-54. [ Links ]
JIMÉNEZ A, GÓMEZ JM, NAVARRO E, SEVILLA F. Changes in the Antioxidative Systems in Mitochondria During Ripening of Pepper Fruits. Plant Physiol Biochem. 2002;40:515-520. [ Links ]
KANG HM, PARK KW, SALTVEIT ME. Elevated Growing Temperatures During the Day Improve the Postharvest Chilling Tolerance of Greenhouse-Grown Cucumber (Cucumis sativus) Fruit. Postharvest Biol Technol. 2002;24:49-57. [ Links ]
KANG HM, SALTVEIT ME. Antioxidant Enzymes and DPPH-Radical Scavenging Activity in Chilled and Heat-Shocked Rice (Oryza sativa L.) Seedlings Radicles. J Agric Food Chem. 2002;50:513-518. [ Links ]
MARÍN MA, CANO MP. Patterns of Peroxidase in Ripening Mango (Mangifera indica, L.) Fruits. J Food Sci. 1992;57:690-92. [ Links ]
MARTÍNEZ PARRA J, MUÑOZ R. Characterization of Betacyanin Oxidation Catalized by a Peroxidase from Beta vulgaris L. Roots. J Agric Food Chem. 2001;49:4064-4068. [ Links ]
MAYER AM. Polyphenol Oxidase and Peroxidase in Plants-Recent Progress. Phytochemistry. 1987;26:11-10.
_______________, HAREL E. Review of Polyphenol Oxidases in Plants. Phytochemistry. 1979;18:193-115.
NARVÁEZ CCE. Evaluación del comportamiento fisiológico del fruto de uva caimarona (Pourouma cecropiifolia) a temperatura ambiente y a temperaturas de refrigeración. [Tesis de magíster]. Bogotá, Colombia: Química. Facultad de Ciencias, Departamento de Química, Universidad Nacional de Colombia. 2002. [ Links ]
_______________, RESTREPO P. Efecto del almacenamiento de la uva caimarona (Pourouma cecropiifolia) a diferentes temperaturas sobre la actividad de polifenoloxidasa y peroxidasa. Rev Col Quim. 2002;31:131-44. [ Links ]
_______________, RESTREPO P. Efecto del almacenamiento de uva caimarona (Pourouma cecropiifolia) a diferentes temperaturas sobre los sólidos solubles y la actividad de catalasa. Rev Col Quim. 2003;32:81-92. [ Links ]
PATIÑO GM, RODRÍGUEZ RDA. Efecto de dos índices de madurez y dos temperaturas de almacenamiento sobre el comportamiento poscosecha de la pitaya amarilla. [Trabajo de pregrado]. Bogotá, Colombia: Facultad de Agronomía, Universidad Nacional de Colombia. 2003. [ Links ]
RIVERA CAP, RESTREPO P, NARVÁEZ CCE. Polifenoloxidasa y peroxidasa de pulpa de uva caimarona (Pourouma cecropiifolia). Rev Col Quim. 2004;33:57-66. [ Links ]
ROGIERS SY, KUMAR GNM, KNOWLES NR. Maturation and Ripening of Fruit of Amelanchier alnifolia Nutt. are Accompanied by Increasing Oxidative Stress. Ann Bot. 1998;81:203-111.
RUBIO ME. Estudio del cambio de actividad de polifenoloxidasa, PFO, durante el proceso de maduración del lulo (Solanum quitoense L.). [Tesis de magíster]. Bogotá, Colombia: Química. Facultad de Ciencias, Departamento de Química, Universidad Nacional de Colombia. 1999. [ Links ]
SALA JM, LAFUENTE MT. Catalase in the Heat-Induced Chilling Tolerance of Cold-Stored Hybrid Fortune Mandarin Fruits. J Agric Food Chem. 1999;47:2410-1414.
]]>_______________, Catalase Enzyme Activity is Related to Tolerance of Mandarin Fruits to Chilling. Postharvest Biol Technol. 2000;20:81-89. [ Links ]
SÁNCHEZ FERRER A, RODRÍGUEZ LÓPEZ JN, GARCÍA CÁNOVAS F, GARCÍA CARMONA F. Tyrosinase: A Comprehensive Review of its Mechanism. Biochem Biophys Acta. 1995;1247:1-11. [ Links ]
STEWART RJ, SAWYER BJB, BUCHELI CS, ROBINSON SP. Polyphenol Oxidase is Induced by Chilling and Wounding in Pineapple. Aust J Plant Physiol. 2001;28:181-191. [ Links ]
STRYER L. Biochemistry. Freeman WH and Company Editors. New York; 1995. 1:195,554. [ Links ]
SWITALA J, LOEWEN PC. Diversity of Properties Among Catalases. Arch Biochem Biophys. 2002;401:145-154. [ Links ]
TAKAHAMA U, EGASHIRA T. Peroxidases in Vacuoles of Vicia faba leaves. Phytochemistry .1991; 30:73-77. [ Links ]
ULRICH BH. Catalase. Methods of Enzymatic Analysis. New York: Academic Press, Inc.; 1974. p. 673-684. [ Links ]
WANG CY. Chilling Injury of Crops of Tropical and Subtropical Origin. En: CRC Press Editors. Chilling Injury of Horticultural crops. Florida; 2000. p. 17-36. [ Links ]
ZHOU Y, DAHLER JM, UNDERHILL SJR, WILLS RBH. Enzymes Associated with Blackheart Development in Pineapple Fruit. Food Chem. 2003;80:565-572. [ Links ]
ZOR T, SELLINGER Z. Linearization of the Bradford Protein Assay Increases its Sensivity: Theorical and Experimental Studies. Anal Biochem. 1996;236:302-308. [ Links ] ]]>