AEGY28 Cell Line of Aedes aegypti (Diptera Culicidae) is Infection Refractory to Dengue 2 and Yellow Fever Virus
NADIA Y. CASTAÑEDA1, B.Sc., M.Sc.; JAIME E. CASTELLANOS1, O.D., M.Sc., Ph. D.; ANGELA C. ZAPATA2, B.Sc., M.Sc.; FELIO BELLO3, B.Sc., M.Sc., Ph. D. 1Instituto de Virología, Universidad El Bosque. Bogotá, Colombia. Transversal 9A Bis No. 13255, Edificio de Rectoría Laboratorio 205, Bogotá, Colombia. Teléfono: 633 13 68, ext. 272. 2Laboratorio de Entomología, Biología Celular y Genética, Departamento de Ciencias Básicas, Universidad de La Salle. Bogotá, Colombia. Carrera 2 No. 1070. Teléfono: 353 53 60, ext. 2504. 3Departamento de Ciencias Básicas, Facultad de Medicina, Universidad del Rosario. Calle 63D No. 2431. Teléfono: 347 45 70, ext. 257 Autor para correspondencia: Jaime Eduardo Castellanos Parra, Fax: 648 90 66. castellanosjaime@unbosque.edu.co
Presentado 11 de diciembre de 2006, aceptado 27 de febrero 2007, correcciones 28 de mayo de 2007.
RESUMEN
Los cultivos celulares de mosquitos son frecuentemente utilizados para el aislamiento, identificación y caracterización de arbovirus. Para el estudio de los virus dengue (VDEN) y virus de fiebre amarilla (VFA) se emplean, principalmente, la línea celular C6/36 de Aedes albopictus y la línea celular AP61, obtenida de Aedes pseudoscutellaris. La línea celular de A. aegypti AEGY28, previamente obtenida a partir de tejidos embrionarios del vector, se utilizó en el presente trabajo para evaluar la susceptibilidad a la infección por VDEN y VFA. Para ello, los cultivos celulares se ensayaron a diferente multiplicidad de infección con los aislados clínicos de virus dengue tipo 2 (COL789, MOI: 1 y 5) y VFA (V341, MOI 0,02). Posteriormente se realizó la detección de antígenos virales por la técnica de inmunocitoquímica y su cuantificación por la técnica de CellELISA fluorométrica. Se usaron como controles positivos de infección, tanto células C6/36 como células VERO. Inesperadamente, no se observó inmunoreactividad en las células de A. aegypti infectadas con ambos tipos de virus en ninguno de los MOI o tiempos estudiados. Tampoco se evidenció antígeno por la técnica fluorométrica ni fue posible detectar RNA viral por RTPCR a partir de células infectadas. Por lo tanto, se puede concluir que la línea celular de A. aegypti no es susceptible a la infección por VDEN ni por VFA. Ello podría estar relacionado con características propias de la membrana celular o de la maquinaria enzimática necesaria para la replicación viral.
Palabras clave: flavivirus, línea celular, virus dengue, fiebre amarilla, arbovirus, infección.
ABSTRACT
Mosquito cell derived cultures are useful tools for arbovirus isolation, identification or characterization. For studying dengue (DENV) and yellow fever viruses (YFV) Aedes albopictus C6/36 or Aedes pseudoscutellaris AP61 cell lines, are normally used. The Aedes aegypti AEGY28 cell line was obtained from embryonic tissues and characterized previously by one of us. In order to evaluate its susceptibility to two Flavivirus, AEGY28 cells were inoculated with different multiplicity of infection (MOI) with type 2 DENV (COL789, MOI: 1 and 5) and YFV clinical isolates (V341, MOI 0,02) then processed at different times post infection (p.i.). Immunostaining and fluorometric cellELISA were carried out to identify and quantify viral antigens. C6/36 and Vero cells were used as positive controls. Unexpectedly, immunoreactivity was not found in inoculated AEGY28 cells, even in higher MOI or late times p.i., therefore antigen quantification using fluorometric cellELISA were not plausible. Reverse transcriptase PCR with specific primers did not detect viral RNA in AEGY28 inoculated cells. We can conclude that Aedes aegypti AEGY28 cell line is not susceptible to dengue and yellow fever Flavivirus, a finding possibly related with the lacking of specific molecules at the plasma membrane or absence of cell machinery necessary for viral replication.
Key words: Flavivirus, cell line, dengue virus, yellow fever, arboviruses, infection.
]]> INTRODUCCIÓNLos cultivos celulares derivados de mosquitos han jugado un papel importante en el estudio de los arbovirus, precisamente porque desde hace muchos años se han venido utilizando como sustrato para el aislamiento e identificación de estos agentes patógenos (Yunker, 1987). Tesh (1979) diseñó un método efectivo para aislar e identificar los virus del dengue utilizando las líneas celulares AP61 (Varma et al., 1974) y AA C6/36 (Igarashi, 1978), ambas derivadas de mosquitos del género Aedes. Los virus fueron inicialmente aislados de pacientes humanos en estos cultivos celulares y luego de lograr una amplia replicación en los sustratos seleccionados, se identificaron mediante inmunofluorescencia y se tipificaron con pruebas de fijación de complemento. Al comparar esta técnica con la inoculación de los virus directamente en mosquitos, se pudo evidenciar una mayor eficiencia y celeridad en la identificación y tipificación de los virus del dengue en los cultivos celulares, de tal forma que los menores títulos virales que se produjeron en estos sustratos celulares se vieron compensados por la utilización de un mayor título viral en las infecciones.
Los cultivos celulares de A. aegypti caracterizados previamente y que se usaron también en este trabajo se obtuvieron a partir de explantes de tejidos embrionarios. El crecimiento celular de estos cultivos se logró en el medio L15/Grace, tres semanas después de haber sido sembrados los tejidos embrionarios; sin embargo, se necesitaron seis meses y 28 subcultivos para la formación de una monocapa confluente. Desde agosto de 2003 hasta octubre de 2006, a través de subcultivos seriados, se realizaron 90 pases. Las células han sido caracterizadas morfológicamente, siendo predominantes, en pases altos, las formas epitelioides. También fueron reconocidas las particularidades morfométricas del cariotipo y se determinaron, adicionalmente, los perfiles isoenzimáticos y moleculares de los cultivos celulares, los cuales se compararon con muestras de adultos de la especie, tomadas de la misma colonia y con líneas celulares derivadas de otros insectos (Ardila et al., 2005). Esta nueva línea celular de A. aegypti fue llamada AEGY28.
La familia Flaviviridae, a la cual pertenecen los virus dengue 2 y fiebre amarilla, consiste de al menos 68 virus que poseen una estrategia similar de replicación y se consideran morfogenética y bioquímicamente relacionados y con características parecidas. Los Flavivirus son partículas esféricas de 35 a 50 nm de diámetro, consisten de una ribonucleoproteína rodeada de una membrana de bicapa lipídica de origen hospederocélula. El virión contiene tres proteínas estructurales separadas: la proteína C de la nucleocápside de 13 a 14 kDa, la proteína M de membrana de 7 a 8 kDa y la proteína E de envoltura de 50 a 60 kDa. El RNA viral codifica para siete proteínas adicionales no estructurales, las cuales participan en la replicación viral. La proteína E es el componente mayor de la superficie de envoltura de los Flavivirus. Se cree que los Flavivirus se unen a la superficie de las células hospederas a través de una interacción de la proteína E con uno o más receptores (Knipe et al., 2001). La entrada del virus se inicia con la adsorción y la penetración en la célula hospedera, uniéndose a receptores específicos de la célula diana. Estos receptores celulares específicos todavía no han sido identificados, pero estructuras como sulfatos de heparan y glicosaminoglicanos de la matriz extracelular podrían estar involucrados (BielefeldtOhmann, 1997; Pandey et al., 1998).
A pesar de que los cultivos celulares de mosquitos son utilizados corrientemente como sustrato para el aislamiento, identificación y caracterización de arbovirus, no todos estos patógenos infectan a una determinada línea celular de mosquito, algunos lo pueden hacer y otros no replican, es decir, que en este último caso, las células son refractarias a virus específicos (Yunker, 1987). Para el estudio de los virus del dengue y de la fiebre amarilla se utilizan, principalmente, los cultivos celulares C6/36 (clon derivado de A. albopictus) y las células Vero, estas últimas originarias de vertebrados, concretamente de riñón de mono verde africano. La línea celular AP61, obtenida de A. pseudoscutellaris,ha sido también usada para el aislamiento e identificación de los virus del dengue y de la fiebre amarilla. Sin embargo, previo a la realización del presente trabajo, no existía información sobre la susceptibilidad de la línea celular de A. aegypti, a la infección con los virus dengue 2 y virus de fiebre amarilla ni habían sido reportadas líneas celulares de A. aegypti y su interacción con Flavivirus. También es importante resaltar que previamente las características de crecimiento, morfológicas, citogenéticas, de perfiles isoenzimáticos y moleculares de la línea celular de A. aegypti AEGY28 fueron descritas, por lo cual ésta línea celular constituye un sistema in vitro disponible y bien descrito para realizar experimentos de susceptibilidad a la infección por diferentes patógenos. Por tanto, el objetivo del presente trabajo, fue analizar la susceptibilidad de los cultivos celulares derivados del mosquito A. aegypti a la infección con los virus dengue 2 y fiebre amarilla.
MATERIALES Y MÉTODOS
CULTIVOS CELULARES
La línea celular AEGY28 fue suministrada por el Laboratorio de Entomología; Biología Celular y Genética de la Universidad de La Salle y mantenida en el Instituto de Virología de la Universidad El Bosque. Las células se mantuvieron en medio de cultivo Grace/L15, suplementado con suero fetal bovino al 10%, sin atmósfera de CO2 e incubados a 28 °C de temperatura por 24 horas, antes de la infección con virus dengue 2 o virus de fiebre amarilla. Para los ensayos de inmunocitoquímica se sembraron 8.000 células por pozo en cajas de 24 pozos y para los de fluorometría se sembraron 5.000 células por pozo en cajas de 96 pozos. Para los experimentos de RTPCR, las células AEGY28 se sembraron en dos frascos de 12,5 cm2 (500.000 células por frasco) y fueron infectadas 24 horas después de la siembra. En uno de los frascos las células fueron infectadas con virus dengue 2 en un MOI: 1 por tres días, al cabo de los cuales se hizo extracción de RNA total; el otro frasco se usó como control sin virus. Las líneas celulares Vero (derivada de fibroblastos de riñón de mono verde africano) y LLCMK2 (derivada de células epiteliales de mono Rhesus) fueron cultivadas y usadas como controles positivos de infección, en razón a que la susceptibilidad a la infección por virus dengue 2 y virus de fiebre amarilla en estas células ya ha sido confirmada. Las células se cultivaron en medio DMEM, suplementado con suero fetal bovino (SFB) 10%, antibiótico (penicilina, 100 U/ml, estreptomicina, 100 µg/ml) y anfotericina (0,25 µg/ml). Se sembraron aproximadamente 6.000 células por pozo en cajas de 24 pozos. Las células de mamífero se mantuvieron a 37 °C con 5% de CO2 por 24 horas de cultivo antes de la infección con virus dengue o virus de fiebre amarilla.
VIRUS E INFECCIÓN DE LOS CULTIVOS
Todos los procedimientos que implicaron el manejo del virus fueron llevados a cabo en cabina de flujo de bioseguridad tipo II. El virus dengue serotipo 2, utilizado en los ensayos, fue aislado de un paciente, empleando células C6/36 y a partir de éste se hicieron cosechas virales usando el sobrenadante de células infectadas (virus COL789), que luego fueron tituladas por ensayo de plaqueo sobre células LLCMK2. El virus de fiebre amarilla aislado también de un paciente (V341) y donado por el Instituto Nacional de Salud, fue replicado en células Vero y los sobrenadantes congelados a 80 °C hasta su uso, previa titulación en células Vero. Las células fueron infectadas a un MOI de 1 (LLCMK2) o en MOI de 1 y 5 (AEGY28) con el virus dengue tipo 2 descrito, el cual tenía un título de 2,8x106 UFP/ml. Para los experimentos con el virus de fiebre amarilla, las células Vero y las células AEGY28 se infectaron a un MOI de 0,02 con un virus que tenía un título de 1,8x105 UFP/ml. Un MOI de 1 indica que la infección ocurre teóricamente con una relación de una partícula viral por célula. Las células infectadas con virus de fiebre amarilla fueron fijadas con paraformaldehído al 4%, 15 horas p.i. y las células infectadas con virus dengue 2 fueron fijadas de la misma manera pero tres días después de la infección.
]]> ENSAYO DE INMUNOCITOQUÍMICALas células fueron sembradas en cajas de 24 pozos con cuatro experimentos independientes con dos réplicas para cada condición experimental, infectadas y luego fijadas con paraformaldehído al 4% a las 15 horas p.i. para los ensayos con virus de fiebre amarilla y tres días p.i. para los ensayos con virus dengue 2. La monocapa fue protegida con gelatina al 1% por 10 min a 0 °C para evitar su desprendimiento. Luego las células fueron permeabilizadas con Tritón X100 al 0,1%, se hizo inactivación de peroxidasa endógena durante 45 min con H2O2 al 0,3% en metanol al 50% diluido en PBS. Después se hizo bloqueo de los sitios inespecíficos con suero de bovino recién nacido al 10%. Los antígenos virales fueron detectados con el anticuerpo monoclonal antiFlavivirus (CHEMICON, MAB8744), el cual reconoce antígenos virales de varios Flavivirus, incluyendo virus de fiebre amarilla y los cuatro serotipos de virus dengue. El anticuerpo primario fue preparado en una dilución de 1/500 en buffer de bloqueo (PBS 1X, albúmina sérica bovina 1%, suero de bovino recién nacido 10%, Tween20 0,05%) e incubado durante 1 hora a 37 °C. Luego se adicionó un anticuerpo antiIgG de ratón biotinilado (Vector Labs) en una dilución 1/200 por 30 min a temperatura ambiente, seguido por incubación con estreptavidina acoplada a peroxidasa (1 µg/ml, Vector Labs) por 30 min a temperatura ambiente. El revelado fue llevado a cabo con una mezcla 1:1 de H2O2 0,02% en agua y DAB 1% (diaminobenzimida) en buffer TrisHCl pH 7,2.
CELLELISA FLUOROMÉTRICAEl 4metilumbeliferilfosfato (4methylumbelliferyl phosphate (MUP), en inglés) es el sustrato fluorogénico más usado para la detección de la actividad de las fosfatasas alcalinas. La desfosforilación de MUP produce una alta fluorescencia y un producto estable (la 4metilumbeliferilferona, MU). Los productos de reacción de MUP son óptimamente fluorescentes a pH alcalino, haciendo ideal al MUP para la detección de la actividad de fosfatasas alcalinas. La excitación y emisión máxima es a 360 nm y 450 nm respectivamente. El MUP se ha usado para una variedad de protocolos de ELISA, en los cuales el pH óptimo es relativamente alto, permitiendo la detección continua de la tasa de formación de MU. En este estudio se empleó una cell ELISA fluorométrica estandarizada en nuestro laboratorio (Rincón et al., 2005). Las células AEGY28 fueron sembradas en cajas de 96 pozos (Corning 25870), infectadas de la forma descrita anteriormente y luego fijadas con paraformaldehído al 4% por 30 min después de 15 horas
p.i para los experimentos con virus de fiebre amarilla y tres días p.i. para los ensayos con virus dengue 2. La monocapa fue protegida con gelatina al 0,5% por 10 min a 0 °C para evitar su desprendimiento. Luego la monocapa se permeabilizó con Tritón X100 al 0,1%, se realizó un bloqueo para fosfatasas alcalinas endógenas con levamisol (20 mM) en ácido acético al 5% durante 1 hora. Después se bloquearon los sitios inespecíficos con buffer de bloqueo (suero bovino de recién nacido en Tris Buffer salino, Tris 10 mM y NaCl 0,14M, pH 7,4). Como anticuerpo primario se usó, al igual que para los ensayos de inmunocitoquímica, el anticuerpo monoclonal antiFlavivirus (CHEMICON MAB8744), el cual fue preparado en buffer de bloqueo (TBS 1X, albúmina sérica bovina 1%, suero de bovino recién nacido 10%, Tween20 0,05%) e incubado a 37 °C durante 30 min. Después de lavar con TBS, se incubó por 30 min a temperatura ambiente con el anticuerpo secundario, antiIgG de ratón biotinilado (Vector Labs. BA9200), en una dilución de 1/200. Luego se agregó estreptavidina conjugada a fosfatasa alcalina (1/250, SA5100 Vector Labs) por 30 min a temperatura ambiente. Por último se adicionó un substrato fluorogénico, el 4metilumbeliferilfosfato (Molecular Probes, M6491) preparado en buffer de revelado (NaCl 0,1 M, Tris 100 mM y MgCl2 50 mM, pH 9,5) y se realizó la medición de fluorescencia a diferentes tiempos en un fluorómetro de PR521 (TecnoSuma, Habana, Cuba) con filtros de excitación de 360 nm y emisión de 450 nm. Para normalizar los datos se utilizó el método del ácido bicinconínico (BCA) de Pierce para cuantificar la cantidad de proteína total en cada uno de los pozos (Smith et al., 1985; Wiechelman et al., 1988). La concentración de proteína se determinó interpolando los datos de absorbancia en una curva de calibración con concentraciones conocidas de albúmina sérica bovina. Los datos se reportaron como una relación de unidades de fluorescencia sobre la concentración de proteína total. Los datos normalizados se expresaron como media y error estándar de la media para dos experimentos independientes cada uno con cuatro réplicas de cada condición.
TRANSCRIPCIÓN REVERSA Y PCR
El RNA total de células AEGY28 fue obtenido usando el método de tiocianato de guanidinio/cloroformo (Trizol, Invitrogen). A partir de 2 µg de RNA total se realizó una transcripción reversa usando random primers y la enzima transcriptasa reversa MMLV (Promega). El cDNA sintetizado fue usado como plantilla para amplificar el gen E de virus dengue con los primers EDV2F (5’CATGCACACAGCACTCACAG3’) y EDV2R (5’ATTGCTCCGAAAACTTGGTG3’), los cuales fueron diseñados en el Laboratorio de Virología, Universidad El Bosque. Las condiciones de PCR para la amplificación del gen E fueron las siguientes: denaturación inicial por 2 min a 94 °C y 30 ciclos de denaturación por 45 seg a 94 °C, hibridación por 1:30 min a 65 °C y síntesis por 1 min a 72 °C. La extensión final fue realizada por 3 min a 72 °C.
RESULTADOS
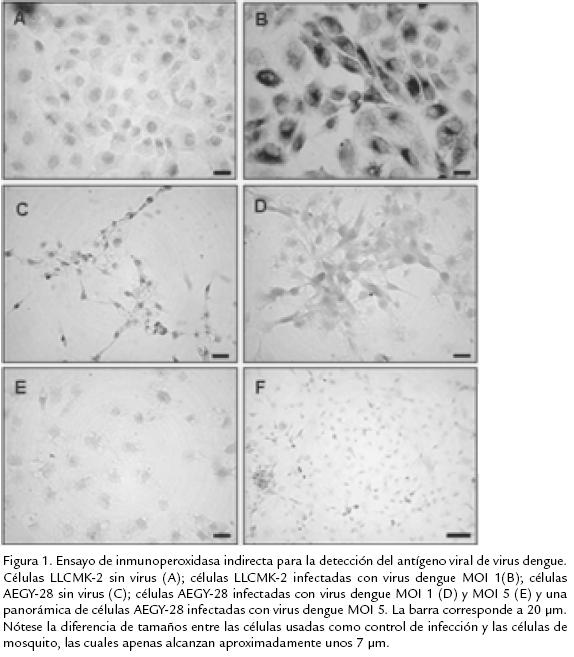
La dilución usada del anticuerpo monoclonal antiFlavivirus (1/500) permitió detectar antígenos de los virus dengue 2 y fiebre amarilla en las células Vero y LLCMK2 infectadas. En estas células se observó un marcaje citoplasmático polarizado hacia organelos celulares específicos, posiblemente retículo endoplásmico y aparato de Golgi donde puede estar llevándose a cabo un proceso activo de ensamblaje viral (Fig. 1 y 2, panel B). Adicionalmente en las células infectadas con virus de fiebre amarilla fue observado claramente el efecto citopático causado a las 15 horas de infección (Fig. 1 , panel B, cabeza de flecha). La inmunoreactividad en las células Vero y LLCMK2 infectadas fue muy evidente y observada en la mayor parte de la población celular. En contraste, en las células AEGY28 infectadas con virus fiebre amarilla o con virus dengue 2 no se observó inmunoreactividad lo cual reflejaría poca o ninguna susceptibilidad a la infección a los dos Flavivirus (Fig. 1 . 1C, 1D, 2D). Es importante detallar que aún usando un MOI de 5 para la infección con virus dengue 2 en las células de A. aegypti, no fue observada ninguna inmunoreactividad (Fig. 1E). En los controles de células no infectadas tampoco fue observada inmunoreactividad.
]]> Los resultados obtenidos usando la técnica fluorométrica confirmaron que las células AEGY28 no se infectaron con el virus de dengue 2 (en ninguno de los MOI usados, 1 y 5) ni con el virus de la fiebre amarilla en un MOI de 0,02 (Fig. 3 . 3A y 3B). Los valores correspondientes a la cuantificación de antígeno viral no tienen diferencias al comparar los controles sin virus y las células infectadas. El mismo comportamiento fue observado en los experimentos realizados independientemente con los dos flavivirus, lo cual confirma la no susceptibilidad de las células AEGY28 a la infección por los virus dengue 2 y fiebre amarilla.Para confirmar por una técnica molecular que las células AEGY28 no fueron susceptibles a la infección, se usaron los primers diseñados en el laboratorio de virología de la Universidad El Bosque, con el propósito de amplificar el gen que codifica para la proteína E del virus dengue tipo 2 usando como plantilla cDNA obtenido de células infectadas. No hubo amplificación específica del tamaño esperado en las muestras provenientes de las células de AEGY28, mientras que cuando se usó plásmido recombinante con el gen E como plantilla en el control positivo, fue obtenido el amplicón correspondiente. Lo anterior evidencia la resistencia de la línea celular a la infección con Flavivirus (Fig. 4 . ).
DISCUSIÓN
Los ensayos de inmunoquímica, fluorometría y PCR empleados para evaluar la susceptibilidad de las células de A. aegypti a la infección por virus dengue 2 y fiebre amarilla revelaron que no hubo infección o aunque hubiera infección no se produjo replicación viral en estos sustratos y por lo tanto se puede sugerir que éstas células resultaron refractarias a la infección con los dos Flavivirus estudiados. Este hallazgo inesperado, podría explicarse haciendo referencia a diferentes eventos del ciclo viral, en tal sentido y específicamente para el evento de entrada viral es probable que las células no presenten las moléculas de superficie que favorecen la adsorción viral. Adicionalmente, se puede pensar que a pesar de producirse la entrada de los virus, la maquinaria enzimática expresada en esta línea celular no es la óptima para permitir el proceso replicativo viral o quizás la respuesta celular antiviral sea lo suficientemente efectiva para impedir la infección. En esta última línea de pensamiento, específicamente en mosquitos ha sido reportado el desarrollo de especimenes de A. aegypti, genéticamente modificados, usando la ingeniería basada en RNA de interferencia, que son resistentes a la infección por virus dengue 2 por un mecanismo que dispara la respuesta antiviral basada en RNA de interferencia en el epitelio intestinal del mosquito (Franz et al., 2006).
Se ha demostrado, experimentalmente in vivo en mosquitos, que el proceso de infección de algunos Flavivirus en las células epiteliales del intestino se ve favorecido por un clivaje proteolítico en la superficie del virión, producido por la tripsina del tracto digestivo (MolinaCruz et al. 2005). Se podría inferir que este paso es necesario para que ocurra infección en algunos cultivos celulares, particularmente como en el presente caso donde la línea celular es derivada de tejidos embrionarios de A. aegypti, insecto vector en su ambiente natural de los virus del dengue y de la fiebre amarilla, que se ha adaptado genéticamente a este mecanismo de infección viral. Por lo tanto, al interactuar las células del vector con los virus en condiciones in vitro probablemente la replicación no progresó por la ausencia de tripsina, como condición necesaria que facilitara el desencadenamiento de la infección. Contrariamente, en otros cultivos celulares esta mediación bioquímica posiblemente no sea necesaria en razón a que otros mecanismos de interacción, como por ejemplo la fusión de membranas y/o la endocitosis mediada por receptores, podrían facilitar la penetración de los virus y desencadenar el proceso replicativo, tal como se ha demostrado en las células C6/36 (Hase et al., 1989, Barth y Schatzmayr, 1992). Otra posible explicación de la ausencia de susceptibilidad de los cultivos celulares de A. aegypti a la infección con los virus del dengue y la fiebre amarilla podría estar relacionada con las características de las cepas virales utilizadas en el presente trabajo, las cuales se han cosechado y mantenido en cultivos celulares (C6/36), donde probablemente este tipo de adaptación hubiese modificado el fenotipo impidiendo a su vez que ocurriera la infección en otras células de mosquitos, tal como las AEGY28. El razonamiento anterior cobra relevancia si tenemos en cuenta los resultados de los experimentos de susceptibilidad in vivo en mosquitos, infectados por vía oral con virus producido en estos mismos insectos (por inoculación torácica), donde se ha registrado mayor proporción de infección y una más alta diseminación que los mosquitos infectados con virus cosechado en células C6/36 (Bosio et al., 2000).
También, otra hipótesis probable a considerar por la ausencia de infección de los virus en cuestión, en las células AEGY28, podría ser la condición innata de estas células a ser resistentes a la infección de determinadas cepas de virus de dengue y fiebre amarilla. Un fenómeno similar ha sido reportado en poblaciones de A. aegypti que son resistentes a la infección por virus de fiebre amarilla y dengue. Al parecer esta característica en algunos mosquitos, estaría asociado con una tasa normal de replicación en las células del intestino pero con un pobre transporte hacia el hemocele y posterior infección de las glándulas salivares (Miller y Mitchell, 1991). Si bien, los cultivos celulares AEGY28 al infectarse con los virus dengue 2 y fiebre amarilla resultaron refractarias a estos patógenos, bajo las condiciones del presente trabajo, pudo haber incidido una o una combinación de variables que ocasionaron esta situación, tal como se ha discutido. Sin embargo, se necesita confirmar o rechazar los resultados de la susceptibilidad de la línea celular derivada del mosquito vector con la utilización de otras cepas de los virus dengue 2 y fiebre amarilla.
AGRADECIMIENTOS
Este trabajo fue financiado por la Universidad de La Salle, Universidad del Rosario y Universidad El Bosque. Los autores declaran que no tienen intereses particulares que pudieran influenciar los resultados presentados.
]]> BIBLIOGRAFÍAARDILA A, ESCOVAR J, BELLO F. Características de nuevos cultivos celulares derivados de tejidos embrionarios de Aedes aegypti (Diptera: Culicidae). Biomedica. 2005;25:65-75
[ Links ]BARTH OM, SCHATZMAYR HG. Brazilian Dengue Virus Type I Replication in Mosquito Cell Culture. Mem Inst Oswaldo Cruz. 1992;87:1-7.
[ Links ]BIELEFELDTOHMANN H. Pathogenesis of Dengue Virus Diseases: Missing Pieces in the Jigsaw. Trends Microbiol. 1997;5:409-413.
[ Links ]BOSIO CF, FULTON RE, SALASEK ML, BEATY BJ, BLACK WC. Quantitative Trait Loci that Control Vector Competence for Dengue2 Virus in the Mosquito Aedes aegypti. Genetics. 2000;156:687-698.
[ Links ]FRANZ AW, SANCHEZVARGAS I, ADELMAN ZN, BLAIR CD, BEATY BJ, JAMES AA, et al. Engineering RNA InterferenceBased Resistance to Dengue Virus Type 2 in Genetically Modified Aedes aegypti. Proc Natl Acad Sci U S A. 2006;103:4198-4203.
[ Links ]HASE T, SUMMERS PL, ECKELS KH. Flavivirus Entry Into Cultured Mosquito Cells and Human Peripheral Blood Monocytes. Arch Virol. 1989;104:129-143.
[ Links ]IGARASHI A. Isolation of a Singh's Aedes albopictus Cell Clone Sensitive to Dengue and Chikungunya Viruses. J Gen Virol. 1978;40:531-544.
[ Links ]KNIPE D, HOWLEY P. Fields Virology. 4ed. Philadelphia. Lippincott Williams and Wilkins; 2001.
[ Links ]MILLER BR, MITCHELL CJ. Genetic Selection of a FlavivirusRefractory Strain of the Yellow Fever Mosquito Aedes aegypti. Am J Trop Med Hyg. 1991;45:399-407.
[ Links ]MOLINACRUZ A, GUPTA L, RICHARDSON J, BENNETT K, BLACK W 4TH, BARILLASMURY C. Effect of Mosquito Midgut Trypsin Activity on Dengue2 Virus Infection and Dissemination in Aedes aegypti. Am J Trop Med Hyg. 2005;72:631-7.
[ Links ]PANDEY B, ICHINOSE A, IGARASHI A. Electron Microscopic Examination of Aedes albopictus Clone C6/36 Cells Infected with Dengue Virus 2 at Elevated Incubation Temperature. Acta Virol. 1998;42:35-39.
[ Links ]RINCÓN V, CORREDOR A, MARTÍNEZGUTIÉRREZ M, CASTELLANOS J. Fluorometric cellELISA for Quantifying Rabies Infection and Heparin Inhibition. J Virol Methods. 2005;126:158-165.
[ Links ]SMITH PK, KROHN RI, HERMANSON G, MALLIA A, GARTNER FH, PROVENZANO M. et al. Measurement of Protein Using Bicinchoninic Acid. Anal Biochem. 1985;150:76-85.
[ Links ]TESH R. A Method for the Isolation and Identification of Dengue Viruses, Using Mosquito Cell Cultures. Am J Trop Med Hyg. 1979;28:1053-1059.
[ Links ]VARMA MG, PUDNEY M, LEAKE CJ. Cell Lines from Larvae of Aedes (Stegomia) malayensis Colless and Aedes (S) pseudoscutellaris (Theobald) and their Infection with Some Arboviruses. Trans R Soc Trop Med Hyg. 1974;68:374-82.
[ Links ]WIECHELMAN K, BRAUN R, FITZPATRICK J. Investigation of the Bicinchoninic Acid Protein Assay Identification of the Groups Responsable for Color Formation. Anal Biochem. 1988;175:231-237.
[ Links ]YUNKER CE. Preparation and Maintenance of Arthropod Cell Cultures: Acari, with Emphasis on Ticks, En: C. E. Yunker (ed.), Arboviruses in Arthropod Cells in vitro, vol. 1. CRC Press, Boca Raton; 1987. p. 35-51.
[ Links ] ]]>