INDUCCIÓN DE POLIFENOLOXIDASA EN FRUTOS DE LULO (Solanum quitoense) COMO RESPUESTA A LA INFECCIÓN CON Colletotrichum acutatum
Polyphenol Oxidase Induction in Lulo Fruits (Solanum quitoense) Infected by Colletotrichum acutatum
OBRADITH CAICEDO O1, Ms. Sc. CienciasBioquímica; BLANCA L. HIGUERA1, Dr. Sc. CienciasQuímica.
1Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia, Sede Bogotá, Carrera 30 No. 4508. AA 14490, dirección blhiguerad@unal.edu.co
Presentado el 12 de junio de 2007, aceptad el 25 de julio de 2007, correcciones el 4 de septiembre de 2007.
RESUMEN
Se evaluó la actividad polifenoloxidasa (PFO) en corteza de frutos de lulo con el fin de determinar su participación en respuestas hacia el patógeno Colletotrichum acutatum, causante de la antracnosis. Se estudiaron condiciones para la adecuada extracción de esta enzima, encontrándose que con buffer fosfatos 100 mM pH 7, 1% SDS y 1% PVPP se logran las mayores actividades. Se determinaron como mejores parámetros para medir la actividad de la enzima extraída, sustrato catecol 40 mM, pH 7,0, 23 °C y 30 µL de extracto. Para determinar su posible inducción en la interacción con el patógeno, se realizó un ensayo in vivo usando frutos verdes, pintones y maduros, inoculados con el hongo o con agua estéril. A nueve tiempos postinoculación se determinó la actividad PFO encontrándose que hay una respuesta diferencial con el tiempo y la madurez de los frutos y por efecto del patógeno. Se obtuvo aumento de actividad en lulos verdes a 48, 96 y 144 horas postinoculación (hpi) y en maduros a la mayoría de los tiempos evaluados, siendo éste estado en el que se presentó la respuesta más notable de inducción. En pintones aumentó solo a 72 y 144 hpi. Los mayores valores se registraron en general para frutos en estado verde. Los frutos respondieron al estrés ocasionado por la herida activando también esta enzima. La inducción de actividad se presentó a tiempos más rápidos en los frutos menos afectados por la enfermedad (verdes y maduros), por lo que se puede postular una relación positiva entre inducción de PFO y respuesta de tolerancia a la antracnosis.
Palabras clave: Lulo, Colletotrichum acutatum, polifenoloxidasa, antracnosis, Solanum quitoense.
ABSTRACT
]]> Polyphenol oxidase (PFO) activity induction was evaluated in lulo fruits to determine the role of this enzyme in resistance responses towards the pathogen Colletotrichum acutatum which causes anthracnose disease. We studied the experimental conditions to obtain the enzyme, using lulo peel, and found that extraction with phosphates buffer 100 mM pH 7, 1% SDS y 1% PVPP showed higher activities. The adequate parameters for activity measurement was also evaluated and established as cathecol 40 mM, pH 7,0, 23 °C and 30 µL of extract. Then, we performed an in vivo assay using lulo fruits in three maturity stages, green, semimature and mature, which were inoculated with the fungus or with sterile water. Enzymatic induction of this protein was studied at nine postinoculation times, and it was found that the induction was differential according to the time, the maturity stage, and as consequence of pathogen presence. The PFO activity increased in green fruits at 48, 96 y 144 (hours postinoculation (hpi), and in mature lulos for the majority of times studied, with the most significant induction response at this stage. In semimature lulo, the induction was observed only at 72 and 144 hpi. The highest nominal value of activity was found in green fruits. Fruits responded to incision with enzyme activation. The increase in the activity of the enzyme was faster in the fruits with the minor anthracnose symptoms than the ones that were more affected. Therefore, it is possible to postulate a positive relation between PFO induction and tolerance to anthracnose symptoms.Key words: lulo, Colletotrichum acutatum, polyphenoloxidase, anthracnose, Solanum quitoense.
INTRODUCCIÓN
En Colombia los cultivos de frutales han adquirido importante auge, el cual se evidencia con el aumento de las áreas destinadas a su siembra1. Esta actividad agrícola se perfila como una alternativa económica dada la creciente demanda de frutas frescas y procesadas en los mercados nacionales e internacionales, para los que las preferencias se dirigen actualmente hacia el consumo de alimentos frescos, sanos e inocuos, que tengan un alto contenido de vitaminas y fibra. Aunque los frutos exóticos colombianos se encuentran dentro de las nuevas preferencias por sus particulares características sensoriales y nutricionales, ha sido muy difícil posicionarlos en el mercado internacional por la poca continuidad y los bajos volúmenes, ocasionados por la invasión de los cultivos por patógenos, entre otras causas. A su vez, el desconocimiento de los mecanismos bioquímicos básicos implicados en las enfermedades causadas por microorganismos no ha permitido avanzar en alternativas sostenibles de control, a través de la generación de variedades resistentes a éstas. Uno de los frutos considerados promisorios para el mercado internacional es el lulo (o naranjilla), de origen tropical y altamente apetecido por su sabor agridulce y su aroma particular y apreciado por sus características nutricionales. En Colombia, su cultivo está distribuido en varias regiones (cerca de 22 departamentos) y representa el 1,7% de la producción nacional de frutas, siendo Huila el mayor productor2. Sin embargo, este fruto es susceptible a plagas y enfermedades, en especial a las ocasionadas por hongos y virus, siendo la antracnosis una de las de mayor impacto en su productividad. En el país se han realizado estudios sobre el fruto de lulo, tendientes básicamente a caracterizar procesos fisiológicos de poscosecha. Es así como se han evaluado indicadores de actividad antioxidante durante la maduración (Cortés, 2006) y se ha estudiado el comportamiento de enzimas como polifenoloxidasa durante la maduración y conservación (Rubio, 1999). Sin embargo, no se tienen reportes conocidos hasta el momento, ni al nivel nacional o internacional, de estudios referentes a la caracterización de los eventos bioquímicos que median la interacción del fruto de lulo con el patógeno que causa la antracnosis y que aporten al conocimiento científico básico de la enfermedad, el cual es fundamental para poder buscar estrategias tendientes a disminuir la susceptibilidad del fruto frente al patógeno, por ejemplo, a través de la búsqueda de variedades resistentes que permitan la generación de alternativas productivas más rentables y sostenidas. La presente investigación buscó aportar al conocimiento de esta interacción hospederopatógeno a través de la evaluación de algunas respuestas bioquímicas que se pueden desencadenar cuando el fruto de lulo se ve enfrentado al patógeno que ocasiona la antracnosis. Es así como se estudió la tposible inducción de enzimas del tipo oxidasas, como es el caso de polifenoloxidasa, la cual con mucha frecuencia se ha encontrado asociada a respuestas defensivas vegetales en otros modelos de interacción.
MATERIALES Y MÉTODOS
MATERIAL BIOLÓGICO
Se utilizó un aislamiento del hongo Colletotrichum acutatum, proporcionado por el Departamento de Biología de la Universidad Nacional de Colombia, Sede Bogotá, el cual fue cultivado en medio PDA (papadextrosaagar). El inóculo se preparó transfiriendo parte del micelio a medio líquido papadextrosa y manteniéndolo por 7 días a 17 °C con agitación (80 rpm) en la oscuridad. A partir de este cultivo se preparó una suspensión (1x106 conidias/mL) para la inoculación de los frutos. El material vegetal usado consistió en frutos de lulo (Solanum quitoense) variedad quitoense, cosechados en tres estados de madurez (verde, pintón y maduro), provenientes del municipio de Junín (Cundinamarca) situado a 2.300 msnm y temperatura promedio de 17 °C. Una muestra del material vegetal usado fue remitida al Instituto de Ciencias Naturales para su clasificación botánica y reposa bajo el número COL. 513823.
DETERMINACIÓN DE LAS CONDICIONES EXPERIMENTALES PARA LA EXTRACCIÓN DE POLIFENOLOXIDASA (PFO E.C. 1.10.3.1) A PARTIR DE LA CORTEZA DE LOS FRUTOS
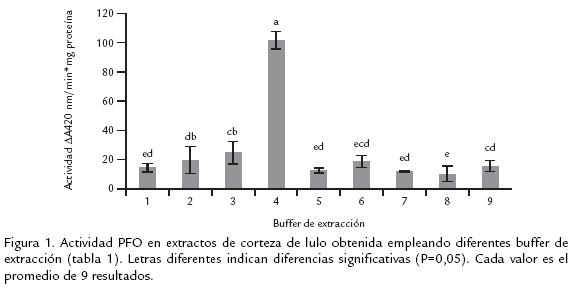
Con el fin de lograr una adecuada extracción de la enzima de interés, a partir de la corteza de frutos de lulo, se estudiaron nueve sistemas de buffer fosfatos con algunos aditivos, evaluados usando un diseño experimental tipo cuadrado latino (Zimmermann, 2004), los cuales presentaron la composición que se muestra en la Tabla 1.
]]>
El proceso de extracción se llevó a cabo tomando como base reportes previos (Cortés, 2006) y consistió en macerar 500 mg de corteza de lulo en presencia de nitrógeno líquido, seguido de tres lavados consecutivos con acetona fría (4 ºC), cada uno con 3 mL. Las muestras fueron luego centrifugadas por 10 min a 10.000 g. Sobre el péllet obtenido se evaluó la extracción usando cada uno de los nueve sistemas (Tabla 1). Una vez obtenidos los extractos enzimáticos, se determinó la actividad PFO con el fin de establecer el buffer con el cual se logra la mayor actividad de esta enzima. Se evaluó así mismo la relación buffer: material vegetal, para lo cual se probaron relaciones 1:2, 1:4 y 1:6.
SELECCIÓN DE LOS PARÁMETROS ADECUADOS PARA LA MEDIDA DE ACTIVIDAD ENZIMÁTICA PFO
Se estudiaron diversas condiciones experimentales para la medida de actividad PFO como pH, para el cual se ensayaron los siguientes valores: 6,0; 6,5; 7,0; 7,5 y 8,0; temperatura: 23, 27, 32, 37 y 40 °C; concentración de sustrato: catecol 20, 30, 40, 50, 75 y 100 mM y, volumen de extracto enzimático crudo: 10, 20, 30 y 40 µL, tomando como base para la escogencia de estos intervalos reportes previos (Ardila e Higuera, 2005). La actividad enzimática se determinó haciendo un seguimiento espectrofotométrico (Genesys UV 10™) durante 30 s a 420 nm y se expresó como ΑA420nm/min*mg de proteína. La mezcla de reacción contenía el extracto enzimático, 460 µL de sustrato (catecol, según concentración a evaluar con ácido pirúvico al 1,64% adicionado para eliminar posibles interferencias con peroxidasas) y buffer fosfatos 100 mM, con pH según valor a evaluar. Los parámetros se estudiaron siguiendo un diseño experimental escalonado, es decir, que al ensayar una de las variables las demás permanecieron constantes. Una vez establecida cada variable, esta condición se utilizó para evaluar la siguiente. Para cada condición experimental se contó nueve con determinaciones.
CUANTIFICACIÓN DE PROTEÍNA
El contenido de proteína se determinó en los diferentes extractos por el método de Lowry (Deutscher, 1990) usando BSA (albúmina de suero bovino) como estándar. Cada determinación se realizó por triplicado.
EVALUACIÓN DE LA INDUCCIÓN DE PFO POR EFECTO DE LA INFECCIÓN DE LOS FRUTOS DE LULO CON C. acutatum
Los frutos para el ensayo in vivo fueron clasificados en verde, pintón y maduro haciendo uso del índice de madurez (°Brix/acidez titulable). Luego fueron lavados y desinfectados con hipoclorito de sodio al 1% y enjuagados con agua estéril. Se separaron al azar en tres grupos para conformar los tres tratamientos: grupo control, almacenado sin ningún tratamiento adicional; grupo testigo, frutos a los que se les realizó una pequeña incisión con bisturí en dos lados opuestos y se aplicaron en cada una 15 µL de agua estéril, y grupo inoculados, a los cuales se les realizaron incisiones similares y se aplicaron 15 µL de la suspensión de hongo en cada una. Este procedimiento se realizó con frutos en los tres estados de madurez. Se almacenaron luego en frascos de vidrio provistos de una servilleta humedecida con agua (todo el sistema previamente esterilizado) con el fin de mantener una humedad relativa elevada. Se taparon con vinilpel y se mantuvieron todos los frutos bajo las mismas condiciones de temperatura y luz. Se realizaron muestreos a las cero, 6, 12, 24, 30, 36, 48, 72, 96 y 144 horas postinoculación (hpi), tomando al azar tres frutos por tratamiento y por estado de madurez a los que se les retiró la corteza cercana al área de inoculación (en todos los casos se tomó un área de 1 cm). Sobre estas muestras se realizó la extracción y se evaluó la actividad PFO, teniendo en cuenta los parámetros establecidos según se indicó antes. Se determinó a cada muestra el contenido de proteína, usando el procedimiento antes indicado.
ANÁLISIS ESTADÍSTICO
Los resultados obtenidos en todas las muestras (N=9) se procesaron usando análisis de varianza (ANDEVA) y pruebas de rango múltiple (P=0,05), usando el programa Statgraphics Plus 5.1®
]]> PROPIEDADES FISICOQUÍMICASCon el fin de establecer el índice de madurez de los frutos usados en el estudio, y para evaluar si se presenta alguna relación entre propiedades fisicoquímicas y desarrollo de los síntomas de antracnosis, se realizó la determinación de los parámetros: pH, dureza, acidez titulable y grados Brix. La acidez se evaluó realizando una titulación ácido base con NaOH 0,1 N (Norma Técnica Colombiana, NTC 4623) y se expresó como % de ácido cítrico. Los grados Brix (sólidos solubles) se evaluaron según NTC 4624, colocando la pulpa sobre un refractómetro (ATAGO 8682) a temperatura ambiente. Todas estas determinaciones se realizaron por triplicado.
EVALUACIÓN PRELIMINAR DE LOS PERFILES PROTEICOS POR ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDSPAGE) Y TINCIÓN ESPECÍFICA
Los extractos enzimáticos obtenidos durante el ensayo in vivo fueron dializados contra tres cambios de agua desionizada, usando membranas de celulosa con tamaño de poro de 12 kDa. Posteriormente se les determinó el contenido de proteína por el método de Lowry (1990). Se seleccionaron muestras de los tiempos en los que, según el ensayo in vivo, se había observado inducción de la actividad PFO como consecuencia de la inoculación con el hongo C. acutatum.
A las muestras seleccionadas (controles, testigos e inoculadas) se les realizó electroforesis SDSPAGE en un equipo Mini Vertical Gel System EC120®. Para ello se usaron geles de acrilamida y bisacrilamida (50%). Las muestras se desnaturalizaron por calentamiento y adición de SDS al 10%. Se aplicaron 20 µg de proteína en cada carril y se usaron 150 V para el gel de concentración (5%). Una vez se sobrepasó éste, se aplicaron 100 V durante el gel de separación. Los geles fueron teñidos con solución de azul de Coomassie R. Se realizó también electroforesis en condiciones nativas a las muestras seleccionadas, usando las mismas condiciones de voltaje y concentración de acrilamidabisacrilamida utilizadas en SDSPAGE, con la diferencia de que ni a los geles ni al buffer de corrido se les adicionó SDS. Una vez se corrieron las muestras, los geles fueron sometidos a tinción específica para PFO. Para ello se sumergieron en una solución de LDOPA 10 mM preparada en buffer fosfatos 100 mM pH 7,0 durante el tiempo necesario para que las bandas tomaran coloración. Posteriormente se lavaron con una solución de ácido acético al 10%.
RESULTADOS Y DISCUSIÓN
SELECCIÓN DE CONDICIONES ADECUADAS PARA LA EXTRACCIÓN DE LA ENZIMA PFO
Los resultados obtenidos al evaluar los nueve sistemas de buffer de extracción se muestran en la figura 1.

SELECCIÓN DE LOS PARÁMETROS ADECUADOS PARA LA MEDIDA DE ACTIVIDAD ENZIMÁTICA PFO
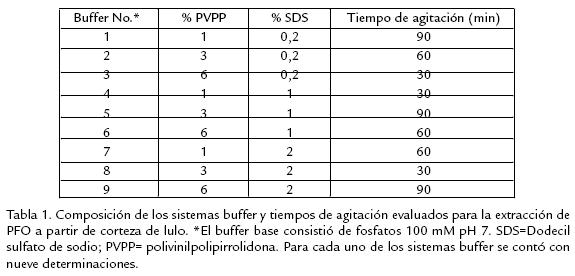
Para las diferentes medidas de actividad PFO, bajo cada condición experimental evaluada, se realizó una gráfica de tiempo contra la absorbancia leída y se tomó la parte lineal de la curva obtenida. Con el dato del contenido de proteína de cada extracto enzimático evaluado, se calculó la actividad específica como el cambio de absorbancia (ΑA) a 420 nm/min*mg de proteína. Se presentan en la figura 2 los valores obtenidos para cada parámetro experimental estudiado. Teniendo en cuenta estos resultados, se pudo establecer que los parámetros adecuados para la medida de actividad PFO, extraída a partir de corteza de lulo, son: pH 7,0; sustrato catecol 40 mM, 27 °C y 40 µL de extracto enzimático, dados los mayores valores de actividad obtenidos, con diferencias significativas (ANDEVA) respecto a las otras condiciones evaluadas. Al comparar con diversos reportes de literatura se encontró que estos parámetros son, en conjunto, similares a los obtenidos para PFO de alcachofa (Aydemir, 2004). Sin embargo, la mayor diferencia encontrada con respecto a datos cinéticos de otras PFOs estudiadas en diferentes fuentes vegetales, se presentan básicamente en la temperatura óptima. Es de anotar que para lulo, y en general para frutos tropicales, no se encuentran estudios de caracterización de enzimas involucradas en respuestas a enfermedades y patógenos, y tampoco se dispone de mayor información cinética sobre esta enzima en particular. Por tanto, se considera de interés evaluar los parámetros cinéticos luego de realizar el aislamiento y la purificación de la enzima PFO aislada de frutos de lulo, con el fin de aportar a la caracterización de la misma.
EVALUACIÓN DE LA INDUCCIÓN DE LA ENZIMA PFO EN FRUTOS DE LULO COMO RESPUESTA AL ATAQUE DEL PATÓGENO C. acutatum
Evaluación de síntomas de antracnosis
A todos los frutos de lulo usados en el ensayo in vivo se les realizó un seguimiento diario con el fin de evaluar su estado general, así como la aparición de síntomas visibles de antracnosis. Las observaciones permitieron establecer que los síntomas característicos, tales como mancha necrótica y ablandamiento, además de la aparición de micelio algodonoso sobre la zona de inoculación, se presentaron en promedio a las 72 hpi en los frutos inoculados con el hongo. Se pudo determinar también que los lulos en estado pintón fueron los más afectados, seguidos por los verdes, mientras que los maduros fueron los menos afectados. Los resultados en cuanto a síntomas coinciden con lo reportado por Cerón (2005), quien encontró que en lulos pintones la incidencia de los síntomas causados por el hongo C. acutatum es mayor. Ninguno de los frutos control o testigo presentó evidencias de antracnosis durante el tiempo que duró el experimento.
Evaluación de la inducción de actividad de la enzima PFO en los tres estados de madurez por efecto de la inoculación.
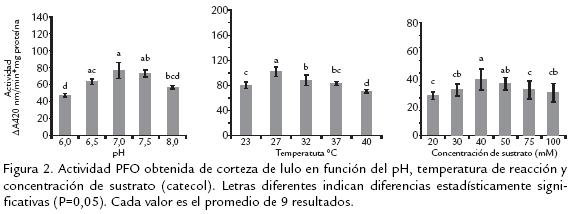
Los resultados de actividad PFO obtenidos a cada tiempo de muestreo se analizaron estadísticamente entre tratamientos, a un determinado tiempo, para establecer posible inducción por efecto del patógeno. a) Estado de madurez verde. En la figura 3 se comparan los resultados de actividad PFO obtenidos a los diferentes tiempos postinoculación para lulos en estado verde, durante el ensayo in vivo. Se observa que a 6 horas se presentó un incremento estadísticamente significativo en la actividad PFO en frutos testigo e inoculados, frente a los controles. Esta activación temprana de la enzima se presenta probablemente como respuesta al estrés producido por la herida realizada con el bisturí al efectuar la inoculación, ya sea con el patógeno o con agua. El hecho de que la actividad haya aumentado en los frutos testigo, no permite atribuir la inducción observada en este tiempo en los frutos inoculados, a una respuesta del hospedero específica a la presencia del patógeno.
]]>
Se pudo establecer también que hubo aumento significativo de la actividad PFO a las 48, 96 y 144 hpi en los frutos inoculados con el patógeno, con respecto a los inoculados solo con agua. Este resultado indica que a estos tiempos se presenta evidentemente una respuesta del fruto frente a la presencia del hongo, en términos de activar la enzima PFO. Es de resaltar que la primera inducción se presentó a las 48 hpi, es decir, 24 h antes del tiempo en que se sucedió, en promedio, la aparición de los síntomas visibles de la enfermedad en frutos en otro estado de madurez (pintón), hecho éste que podría estar relacionado con la baja severidad de los síntomas encontrada a las 72 hpi en lulos verdes. Ello indicaría que al activarse algún proceso metabólico en el que está involucrada la enzima PFO se puede retardar el desarrollo de la enfermedad, ya sea por inhibición del patógeno o por reforzamiento de estructuras de defensa de la planta, tal como ha sido planteado para diversos modelos de interacción hospederopatógeno. En durazno, por ejemplo (Wang et al., 2004), se reportó inducción de la enzima PFO 24 horas después de haber sido inoculado con Penicillium expansum y, a su vez, aumento de la incidencia de la enfermedad en el fruto cuando la actividad de la enzima disminuyó. En pera se encontró aumento en la actividad PFO en frutos inoculados con Alternaria alternata (Tian et al., 2005). En fuentes vegetales diferentes a frutos, como es el caso de trigo, se reportó que variedades resistentes a Sitobion avenae presentaron mayor actividad PFO (Chrzanowski et al.; 2003). En clavel (Ardila e Higuera, 2005) también se ha encontrado que en variedades tolerantes infectadas con el hongo Fusarium oxysporum f. sp. dianthi raza 2, la actividad PFO es significativamente mayor.
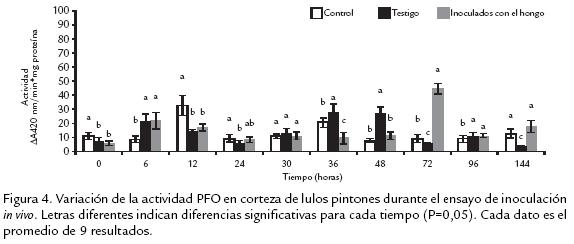
b) Estado de madurez pintón. En la figura 4 se muestran los resultados obtenidos para lulos en estado pintón. Se observó un incremento importante a las 72 y 144 hpi en los frutos inoculados con el hongo, respecto a los inoculados con agua. El mayor valor de actividad PFO en este estado de madurez se obtuvo a las 72 h y esta inducción se puede asociar evidentemente con una respuesta a la presencia del patógeno, dado que para el fruto inoculado solo con agua el valor fue significativamente menor (ocho veces menos), al igual que el del control. Aunque con magnitudes de actividad menores, este comportamiento de inducción de la enzima como respuesta a la inoculación con el hongo también fue observado a 144 hpi. Cabe anotar que, en general, las magnitudes de las actividades PFO en estado pintón fueron menores a las que se determinaron para frutos en estado verde, y que las respuestas de inducción enzimática en frutos inoculados se presentaron en tiempos posteriores a las presentadas en lulos verdes. Estas respuestas al parecer algo “tardías” podrían estar relacionadas con el grado de severidad de la enfermedad, pues en estado pintón los síntomas a las 72 hpi fueron más evidentes, si se comparan con los otros dos estados de madurez.
c) Estado maduro. En la figura 5 se muestran los resultados obtenidos para frutos en estado maduro. Como se observa, se tuvo un aumento significativo al tiempo 6 hpi en los frutos testigos e inoculados con el hongo, respecto a los controles. Este resultado permite postular de nuevo que hay una respuesta, en términos de inducción de PFO, del fruto frente al estrés ocasionado por la herida realizada con el bisturí. Este tipo de respuesta ha sido frecuentemente reportada para otros sistemas vegetales sometidos a estreses bióticos y abióticos y permite evidenciar la importancia de contar con controles adecuados en el momento de evaluar inducción de respuestas vegetales a patógenos. La respuesta más notable de inducción de PFO se obtuvo en este estado de madurez, dado que al comparar los valores obtenidos en varios de los tiempos para los frutos inoculados con el hongo, con sus respectivos controles, se notan aumentos estadísticamente significativos, por efecto de la presencia del patógeno. Desde que se realiza la inoculación hay una inducción, la cual se mantiene hasta el tiempo final de muestreo de este estudio.
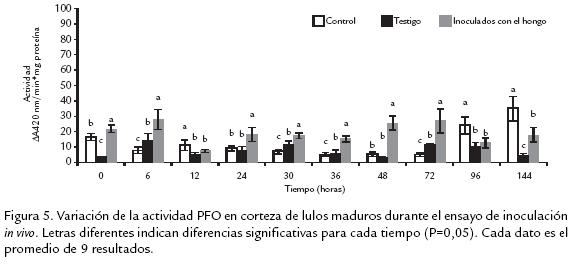
La inducción temprana de actividad PFO podría estar asociada con el menor grado de severidad de los síntomas ocasionados por el patógeno, ya que como se mencionó antes, los frutos en estado maduro fueron los que presentaron menores síntomas de la antracnosis en esta investigación. Las comparaciones de actividad se efectuaron para cada tiempo entre los tres tratamientos, con el fin de detectar posibles inducciones ocasionadas por el patógeno. Entre tiempos se observan variaciones que, como sucede en sistemas vivos, no obedecen a un patrón regular de aumento o disminución. Los resultados obtenidos indicaron que hay inducción de la enzima PFO en los lulos inoculados con el patógeno en todos los estados de madurez pero a diferentes tiempos y que el perfil de inducción depende de dicho estado. Se puede postular también de manera preliminar que la diferencia en el perfil de inducción enzimática puede estar relacionado con la enfermedad en el fruto, ya que como se anotó, la severidad de los síntomas varió en cada estado de madurez, observándose que en los frutos donde se presenta una inducción temprana de la actividad PFO (verde y maduro), coincidió con que éstos fueron menores. Aunque no existen reportes donde se correlacione la incidencia de la enfermedad con el estado de madurez en frutos como el lulo, es claro que durante los procesos de maduración se promueven cambios bioquímicos y/o histológicos que pueden tener incidencia durante la interacción hospedero patógeno.
]]> PROPIEDADES FISICOQUÍMICAS DE LOS FRUTOS DE LULOEn la Tabla 2 se reportan los resultados obtenidos en la determinación de parámetros fisicoquímicos de los frutos usados para el estudio. Con base en la relación entre los grados Brix y la acidez, se clasificaron los frutos para conformar los grupos correspondientes a los estados verde, pintón y maduro. Cabe mencionar que estos resultados, y la caracterización, están acordes con lo reportado por estudios previos (Casierra et al., 2004), realizados en lulos de esta misma variedad.
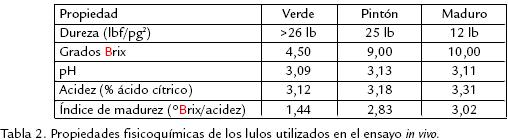
Como se discutió al analizar la inducción de la enzima PFO, fue evidente que el estado pintón fue el que presentó menor inducción, además, en este estado no hubo acumulación de fenoles (resultados por publicar) y la severidad de la enfermedad fue mayor. Sin embargo, estos resultados no parecen tener relación con las propiedades físicoquímicas evaluadas, pues como se muestra en la Tabla 2, no se obtuvieron diferencias marcadas en la mayoría de las propiedades medidas, por tanto, no es posible afirmar que alguna de éstas favorezca o no la invasión por parte del patógeno. En la propiedad que se observó mayor diferencia con el estado de madurez fue en la dureza, pero no se pudo establecer que existiera relación, por ejemplo, entre una menor dureza (frutos maduros) y la facilidad de invasión del patógeno, hecho éste que no debe estar necesariamente correlacionado. La poca diferencia en propiedades como pH y acidez entre los tres estados de madurez ya ha sido previamente documentada para el lulo y es por ello que estos parámetros no se utilizan por lo general para caracterizar el grado de madurez del fruto. No se puede descartar que existan otro tipo de moléculas propias del metabolismo y que estén correlacionadas con el estado de madurez, que sí tengan relación con la facilidad de la invasión o no. Un ejemplo claro son aquellas que confieren color o que forman parte de la composición misma de la capa cerosa de los frutos que puedan afectar o favorecer la invasión el hongo. Es así como en algunos reportes (Salisbury, 1992) se ha encontrado que compuestos de carácter fenólico (los cuales tienen origen en rutas metabólicas como la del ácido shiquímico y fenil propanoide) presentes por ejemplo en cebollas rojas consideradas resistentes al ataque de Colletotrichum circinans, no están presentes en cebollas blancas, consideradas susceptibles. Así mismo, ocurre en frutos de ají, en los que el ají verde es más susceptible al ataque del patógeno Colletotrichum gloesporioides que el ají rojo (Kim et al.; 1999).
EVALUACIÓN PRELIMINAR DE LOS PERFILES PROTEICOS POR ELECTROFORESIS SDSPAGE Y TINCIÓN ESPECÍFICA
Con base en perfiles electroforéticos preliminares obtenidos en diversos geles teñidos con azul de Coomassie (fotos no mostradas), se pudo visualizar que, en general, para un mismo estado de madurez hay aumento en el número de bandas a lo largo de las horas postinoculación. Se pudo establecer además que para un mismo tiempo de muestreo hay variación en el perfil según sea el estado de madurez del fruto, encontrándose que en el estado maduro se presenta mayor número de bandas, algunas de las cuales no se detectan en los extractos correspondientes al estado verde ni pintón, particularmente para horas tempranas postinoculación. Ello indicaría la actividad metabólica normal que se sucede durante el proceso de maduración, en el que sin duda se generan nuevas proteínas y otras cambian su nivel de actividad. Adicionalmente a estas observaciones, ciertas bandas se presentaron con mayor intensidad en las muestras de lulo inoculadas con el patógeno, que fue evidente a simple vista, a pesar que no se contó con cuantificación de las bandas. Este comportamiento ha sido reportado en diversos estudios, como en el modelo clavelFusarium oxysporum dianthi (Ardila e Higuera, 2005) en el que se observó que un conjunto de bandas de proteínas incrementaron su intensidad únicamente en extractos obtenidos a partir de una variedad tolerante inoculada con el hongo. En la fig 6 se muestra un gel con tinción específica para PFO en el que se observa, en primer lugar, que hay presencia de más de una banda dando la reacción específica para dicha enzima, es decir hay la posibilidad de la presencia de varias isoenzimas PFO. En el perfil que se muestra (lulos en estado maduro) se observaron mayor cantidad de bandas respecto a lulos verdes y maduros (resultados no mostrados), seguramente como consecuencia del proceso de maduración. Así mismo, se observó la aparición de una nueva banda de baja movilidad electroforética (fig 6, flecha de mayor longitud) la cual se presentó en la muestra de lulos inoculados con agua y con el patógeno, observándose más intensa en la muestra inoculada con el patógeno. Con estos resultados preliminares puede postularse que esta isoenzima haría parte de una respuesta del fruto frente al estrés al que fue sometido el fruto por efecto del corte con bisturí y que es también posiblemente una proteína de respuesta a la inoculación con el hongo, resultados que es importante confirmar a través de estudios de mayor profundidad. Es de resaltar que la aparición de nuevas isoenzimas o el aumento de la intensidad de las ya existentes en muestras inoculadas con el patógeno se presentó en algunos casos, como el que se ilustra, en extractos en los que se encontró inducción de la actividad enzimática PFO. Por tanto, es posible postular una inducción de nuevas isoenzimas con actividad PFO que podrían estar involucradas en el mecanismo de respuesta del fruto de lulo frente al ataque de C. acutatum. Estos resultados coinciden con algunos reportes en los que se han encontrado diferente números de isoformas de PFO, cuatro en kiwi, siete en trigo, tres en alcachofa y dos en álamo, y algunas de ellas como respuesta a ciertos patógenos (Wang et al.; 2004). Los resultados generales de este estudio se constituyen en un aporte al conocimiento, por lo demás escaso, de las respuestas bioquímicas en interacciones frutospatógenos, y son los primeros conocidos acerca de la interacción lulo C. acutatum, mostrando para este modelo evidencias que permiten postular la participación de la enzima polifenoloxidasa en respuestas del fruto a la presencia del patógeno que causa la enfermedad antracnosis. Es necesario indagar más a fondo si tales respuestas pueden catalogarse como de defensa vegetal en este modelo, lo cual se sugiere acá, dada la relación encontrada entre su inducción y el menor desarrollo de los síntomas típicos de la enfermedad.

NOTAS AL PIÉ DE PÁGINA
]]> 1 http://www.agrocadenas.gov.co2 Asohofrucol Dane. 2004. Primer Censo Nacional de 10 Frutas Agroindustriales y Promisorias.
AGRADECIMIENTOS
Los autores expresan su agradecimiento a la Vicerrectoría de Investigación, División de Investigación de la Sede Bogotá y al Departamento de Química de la Universidad Nacional de Colombia por el apoyo financiero y de infraestructura otorgados para este estudio.
BIBLIOGRAFÍA
ARDILA H, HIGUERA B. Inducción diferencial de polifenoloxidasa y ‚1,3glucanasa en clavel (Dianthus caryophyllus) durante la infección por Fusarium oxysporum f. sp. dianthi raza 2. Acta biol. Colomb. 2005;10(2):61-74. [ Links ]
AYDEMIR T. Partial Purification and Characterization of Polyphenol Oxidase from Artichoke (Cynara scolymus L.) heads. Food Chem. 2004;87:59-67. [ Links ]
CASIERRA F, GARCÍA E, LUDDERS P. Determinación del punto óptimo de cosecha en el lulo (Solanum quitoense Lam. var. quitoense y septentrionale). Agronomía Colombiana. 2004; 22(1):32-39. [ Links ]
CERÓN G S. Detección de Colletotrichum (Penz) Sacc en estructuras vegetativas y reproductivas de lulo Solanum quitoense Lam [tesis de maestría en Fitopatología]. Bogotá DC: Facultad de Agronomía, Universidad Nacional de Colombia; 2005. [ Links ]
CHRZANOWSKI G, CIEPIELA A, SPRAWKA I, SEMPRUCH C, SYTYKIEWICZ H, CZERNIEWICZ P. Activity of Polyphenol Oxidase in the Ears of Spring Wheat and Triticale Infested by Grain Aphid (Sitobion avenae/F/). Electronic Journal of Polish Agricultural Universities. 2003;6(2):1-5. [ Links ]
CORTÉS RA. Efecto de la refrigeración y el choque térmico sobre algunos indicadores de actividad antioxidante en lulo (Solanum quitoense Lam) [tesis de maestría]. Bogotá DC: Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia; 2006. [ Links ]
CRUZ I, FATIBELLO O. Flor Injection Spectrophotometric Determination of Hydrogen Peroxide Using a Crude Extract of Zucchini (Cucúrbita pepo) As a Source of Peroxidase. The Analyst. 1998;8:321-325. [ Links ]
DEUTSCHER M. Methods in Enzymology, Guide to Protein Purification. Vol 182. Academic Press. Inc. New York; 1990. [ Links ]
JIMÉNEZ M, GARCÍA F. The Effect of Sodium Dodecyl Sulphate on Polyphenol Oxidase. Phytochemistry. 1996;42(6):1503-1509. [ Links ]
KIM K, OH B, YANG J. Differential Interactions of a Colletotrichum gloesporioides Isolate with Green and Red Pepper Fruits. Phytoparasitica. 1999;27(2):1-10. [ Links ]
MAYER A. Polyphenol Oxidase in Plants and Fungi: Going Places? A Review. Phytochemistry. 2006;67:2318-2331. [ Links ]
PANDEY R, ARORA D, DUBEY R. Effect of Environmental Conditions and Inoculum Density on Infection of Guava Fruits by Colletotrichum gloesporioides. Mycopathologia. 1997;137:165-172. [ Links ]
RUBIO E. Estudio del cambio de actividad de polifenoloxidasa, PFO, durante el proceso de maduración del lulo (Solanum quitoense L.) [Tesis de Maestría en Ciencias Química]. Bogotá D C: Dpto. de Química, Facultad de Ciencias, Universidad Nacional de Colombia; 1999. [ Links ]
SALISBURY F, ROSS C. Fisiología vegetal. Grupo Editorial Iberoamericano. México 1992. p.351-359. [ Links ]
TIAN S, WAN Y, QIN G, XU Y. Induction of Defence Responses Against Alternaria Rot by Different Elicitors in Harvested Pear Fruit. Appl Microbial and Cell Physiol. 2005;18:115-119. [ Links ]
WANG Y, TIAN S, XU Y, QIN G, YAO H. Changes in the Activities of ProAntiOxidant Enzymes in Peach Fruit Inoculated with Cryptococcus laurentii or Penicillium expansum at 0 or 20°C. Postharvest Biol Technol. 2004;34:21-28. [ Links ]
ZIMMERMANN F. Estadística para investigadores. 1ed. Escuela Colombiana de Ingeniería. Bogotá; 2004. [ Links ] ]]>