DIVERSIDAD GENÉTICA DE Peronospora sparsa (PERONOSPORACEAE) EN CULTIVOS DE ROSA DE COLOMBIA
Genetic Diversity of Peronospora sparsa (Peronosporaceae) on Rose Crops From Colombia
MARILUZ AYALA-VÁSQUEZ1, I.A.; LUZ EDITH ARGEL-ROLDAN2, M.Sc.; SONIA JARAMILLO-VILLEGAS3, M.Sc.; MAURICIO MARÍN-MONTOYA2, Ph. D.
1Laboratorio de Estudios Moleculares, Departamento de Ciencias Agronómicas, Facultad de Ciencias Agropecuarias.
2Laboratorio de Biología Celular y Molecular, Facultad de Ciencias, Universidad Nacional de Colombia, Sede Medellín, Colombia. mayala@unalmed.edu.co; leargel@unalmed.edu.co sjaramal@unalmed.edu.co.
Correspondencia: Mauricio Marín Montoya, Departamento de Biociencias, Facultad de Ciencias, Universidad Nacional de Colombia, Sede Medellín. A.A. 3840. Fax: (4) 430 93 32. mamarinm@unal.edu.co.
Presentado: 4 de septiembre de 2007, aceptado 18 de octubre de 2007, correcciones 24 de enero de 2008.
RESUMEN
El mildeo velloso de la rosa es la enfermedad más limitante de este cultivo en Colombia. Aunque algunos trabajos de investigación se han adelantado recientemente sobre la epidemiología de esta enfermedad, uno de los campos menos estudiados es el nivel de variabilidad de su agente causal. El conocimiento de este aspecto es fundamental para definir las estrategias de manejo, especialmente aquellas relacionadas con la resistencia genética y el control químico. Los objetivos de esta investigación fueron confirmar la identidad taxonómica del agente causal del mildeo velloso de la rosa y profundizar en el conocimiento de su estructura poblacional en Colombia. Para esto se colectaron 34 aislamientos del pseudohongo en cultivos de rosas ubicados en Antioquia y la sabana de Bogotá y se extrajo su ADN, para proceder a la amplificación mediante PCR de la región ITS del ADNr utilizando los primers especieespecíficos PS3 y PS1. Dichos productos se emplearon tanto para su secuenciación directa como para la evaluación de variabilidad genética mediante la técnica PCRRFLP, resultados que se complementaron con la utilización de los marcadores RAPD y RAMS. La presencia de un amplicón de aproximadamente 700 pb que compartió un porcentaje de identidad del 100% con secuencias depositadas en el GenBank, permitió confirmar a los aislamientos como pertenecientes a Peronospora sparsa, mientras que el análisis de RFLP, RAPD y RAMS indicó un muy bajo nivel de variabilidad entre todos los aislamientos, concluyéndose que la población de P. sparsa en Colombia es predominantemente clonal.
]]> Palabras clave: ADNr, flores, ITS, marcadores moleculares, mildeo velloso, variabilidad genética.ABSTRACT
Downy mildew of roses is the most restrictive disease of this crop in Colombia. Although some studies have been carried out on the epidemiology of this disease, one of the fields less studied is the level of variability of its causal agent. The knowledge of this aspect is fundamental to define management strategies, especially those related with the genetic resistance and the chemical control. The objectives of this research were to confirm the taxonomic identity of the causal agent of downy mildew of rose and to deepen in the knowledge of their population structure in Colombia. Thirtyfour isolates of the pseudofungi were collected in rose crops located in Antioquia and the Savanna of Bogota and their DNA was extracted to amplify by PCR the ITS region of the DNAr using the species-specific primers PS3 and PS1. The products were used for their direct sequencing and to evaluate genetic variability by PCR-RFLP. Additionally the study was complemented throught RAPD and RAMS markers. Presence of a band of approximately 700 pb that shared a percentage of identity of 100% with sequences deposited in the GenBank, allowed to confirm the identity of the isolates as belonging to Peronospora sparsa, while the analysis of RFLP, RAPD and RAMS indicated a very low level of variability among all the isolates, concluding that the population of P. sparsa in Colombia is predominantly clonal.
Key words: rDNA, Downy mildew, Flowers, Genetic variability, ITS, Molecular markers.
INTRODUCCIÓN
Peronospora sparsa Berkeley, es uno de los patógenos más limitantes en los cultivos de rosa bajo invernadero en el mundo. El primer reporte del mildeo velloso de la rosa fue realizado en Inglaterra en el año 1862, y al poco tiempo se registró en Europa continental, específicamente en los países escandinavos y la antigua Unión Soviética. En 1880 la ocurrencia de esta enfermedad se reportó en el medio oeste de los Estados Unidos, y desde allí se dispersó por todo el país. Aunque la literatura científica registra a P. sparsa como un patógeno endémico del área norte del trópico de Cáncer, en la actualidad el mildeo velloso de la rosa causa daños significativos en países tropicales y subtropicales como Brasil, Colombia, Israel, Egipto y Nueva Zelanda (Horst, 1983; Arbeláez, 1999; Walter et al., 2004). Existen registros de la ocurrencia del mildeo velloso en los cultivos colombianos de rosa desde la década de los 70 (Martínez, 2002). En los últimos años, esta enfermedad se ha convertido en el principal problema fitosanitario de este cultivo en la sabana de Bogotá, reduciendo la producción de rosas considerablemente y aumentando los costos operativos debido a las medidas que se deben tomar para su control. Para el año de 1999, se estimó en cinco millones de dólares las pérdidas por la afección del mildeo velloso de la rosa (Zúñiga, 2003) y actualmente se considera que la enfermedad ocasiona una disminución del 10% en la producción total de rosas del país (Gómez, 2004). Los síntomas de la enfermedad se manifiestan sobre las hojas, tallos, pedúnculos, cáliz y pétalos de las plantas de rosa, aunque generalmente la infección es restringida a los tejidos jóvenes de las plantas. Sobre el haz de las hojas se desarrollan manchas irregulares de color rojizopúrpura a pardo-oscuro, las cuales se rodean de un halo clorótico, mientras que sobre el envés se producen los signos del patógeno, que corresponden a un micelio de color marrón claro con abundante producción de esporangióforos y esporangios, lo cual genera la apariencia vellosa característica de la enfermedad. Estas estructuras solo se producen bajo condiciones de alta humedad, llegando a ser escasas y difíciles de detectar en situaciones desfavorables para el desarrollo del patógeno (Horst, 1983; Arbeláez, 1999; Hollier et al., 2001). La enfermedad puede inducir a una defoliación severa sobre las variedades de rosa más susceptibles y es común que los síntomas foliares se confundan con quemaduras o toxicidad inducida por pesticidas. Sobre los tallos, cáliz y pedúnculos, la enfermedad se manifiesta como manchas púrpuras a negras que varían en tamaño e incluso pueden coalescer induciendo a la muerte de las ramas y a la momificación de los botones florales (Horst, 1983; Hollier et al., 2001; Infoagro, 2004) o propiciando la invasión secundaria de los tejidos afectados por parte de otros patógenos, tales como Botrytis spp. (Aegerter et al., 2002).
P.sparsa es un patógeno obligado que hace parte del grupo de los Oomycetes,los cuales son organismos miceliares semejantes a los hongos, que se conocen comúnmente como mohos acuáticos e incluyen saprófitos y patógenos de plantas, insectos, crustáceos, peces, animales vertebrados y de otros microorganismos (Kamoun, 2003). Taxonómicamente se consideran miembros del subreino Heterokonta, reino Chromista (Hawksworth et al., 1995), aunque algunos autores los ubican en el reino Straminopila (Kamoun, 2003). Pertenece al orden Peronosporales, familia Peronosporaceae; sin embargo la clasificación taxonómica de este grupo de pseudohongos se encuentra en una profunda revisión con base en análisis filogenéticos de las secuencias de regiones ITS del ADN ribosomal (ADNr; Cooke et al., 2000) y de la subunidad 28S del ADNr (Riethmüller et al., 2002, Göker et al., 2003). Morfológicamente, P. sparsa se caracteriza por poseer esporangios subelípticos (17-22 µm x 14-18 µm) producidos a partir de esterigmas presentes en esporangióforos erectos y dicotómicamente ramificados en ángulos agudos (Horst, 1983). El pseudohongo se reproduce sexualmente por medio de oosporas caracterizadas por poseer paredes gruesas que cumplen funciones como estructuras de resistencia. En las zonas templadas, la producción de oosporas es profusa en el mesófilo de las hojas así como también en la corteza de los tallos y pedúnculos de las plantas sintomáticas (Aegerter et al., 2002); sin embargo su presencia en los cultivos de rosa de Colombia aún no se ha determinado (Arbeláez, 1999). El pseudohongo penetra al hospedante en forma directa a través de la cutícula y la epidermis, y se alimenta de las células del parénquima por medio de haustorios y una profusa red de micelio intercelular (Michelmore et al., 1988). Estudios epidemiológicos han determinado que las condiciones más favorables para el desarrollo del mildeo velloso de la rosa bajo invernadero corresponden a temperaturas que oscilan entre 15 y 20 °C durante el proceso de infección y de 20 a 25 °C para la colonización del patógeno. La infección esta además fuertemente influenciada por la presencia de una lámina de agua libre sobre la superficie del tejido por un período mínimo de dos horas; sin embargo, el proceso infectivo se incrementa significativamente cuando dichas condiciones de humedad superan las 10 horas. El período de latencia del patógeno se ha estimado entre cuatro y siete días, determinándose además que P. sparsa es capaz de iniciar su ciclo de infección a temperaturas tan bajas como 5 °C, siempre y cuando exista una lámina de agua sobre el tejido durante al menos ocho horas (Aegerter et al., 2003). Además de los enormes daños que P. sparsa ha ocasionado en cultivos de rosa (Rosa spp.), este patógeno también ha sido reportado afectando plantas de diferentes especies del género Rubus que producen frutos comestibles tales como Rubus fructicosus, Rubus arcticus y Rubus chamaemorus (Lindqvist-Kreuze et al., 2002; Walter et al., 2004) y recientemente se ha indicado que esta especie es el agente causal del mildeo velloso de la mora (Rubus glaucus) en Venezuela (Montilla et al., 2003) y Colombia (Tamayo, 2001), lo cual incrementa la importancia económica de este patógeno en nuestro medio. Pocos estudios se han realizado en Colombia sobre P. sparsa, aunque en los últimos años, se ha avanzado en el conocimiento de la biología del patógeno y en la determinación de las condiciones óptimas para el desarrollo de la enfermedad (Gómez y Arbeláez, 2003a; Gómez y Arbeláez, 2003b; Gómez, 2004; Urrea y Arbeláez, 2004). Se ha encontrado que bajo las condiciones de la sabana de Bogotá, el óptimo térmico para la germinación de los esporangios de P. sparsa corresponde a 14 °C, mientras que se requiere un periodo mínimo de cuatro horas de agua libre sobre los tejidos para que ocurra el proceso infectivo del patógeno. La esporulación de P. sparsa en nuestro medio, ocurre principalmente cuando se presenta una humedad relativa superior al 85% y temperaturas que oscilan entre 18 y 22 °C (Gómez, 2004; Gómez y Arbeláez, 2004). De otra parte, Gómez y Arbeláez (2003a) estimaron que el periodo de latencia de un aislamiento de P. sparsa procedente de la sabana de Bogotá sobre tres variedades de rosa (Classy, Charlotte y First Red) comprende entre seis y siete días a 10 °C, mientras que a una temperatura de 18 a 22 °C, dicho periodo se reduce a tan solo 3-5 días. Con respecto al período de incubación, los mismos autores determinaron que este osciló entre siete y ocho días bajo condiciones de invernadero. En dicho estudio, la aparición de síntomas en los botones florales se presentó entre 14 y 16 días después de la inoculación, mientras que los síntomas en los tallos tardaron en aparecer de 17 a 21 días en promedio (Gómez y Arbeláez, 2003b). Filgueira (2004) realizó un estudio microscópico tendiente a evaluar las características morfológicas de los diferentes estados del ciclo de desarrollo de P. sparsa en rosas de corte, encontrando que la infección de este patógeno se produce tanto por el haz como por el envés de las hojas. El control del mildeo velloso de la rosa es difícil debido a la alta susceptibilidad de la mayoría de las variedades comerciales de rosa cultivadas en el mundo. En Colombia, el patógeno es altamente agresivo sobre las variedades Charlotte, Classy, Dolores, Frisco, Konfetti, Livia, Mystique, Osiana, Pavarotti y Ravel (Flórez, 1996; Restrepo, 1996). Con respecto al grado de susceptibilidad de los patrones, Martínez (2002), en una investigación tendiente a evaluar la respuesta de tres materiales injertados (Charlotte, Livia y Aalsmeer Gold) sobre los patrones Manetti y Natal Brier, determinó que las plantas injertadas sobre el primer patrón presentaban una mayor afección por la enfermedad en comparación con las del patrón Natal Brier. Sin embargo, dichos resultados fueron preliminares y requieren ser confirmados por futuros trabajos. El control del mildeo velloso tambi&eac ute;n requiere de un adecuado manejo cultural; prácticas como la remoción y destrucción de tallos, hojas y flores sintomáticas, son necesarias para reducir el nivel de inóculo en los cultivos. Adicionalmente se ha planteado que el manejo de las condiciones ambientales de los invernaderos mediante la apertura-cierre de ductos y cortinas y la ejecución de prácticas adecuadas de riego, son fundamentales para disminuir la severidad de la enfermedad, así como lo es el ajuste de los programas de fertilización, en los cuales se debe evitar el exceso en la aplicación de productos nitrogenados y garantizar un adecuado nivel de potasio en las plantas (Quitian, 1995; Restrepo, 1996). Debido al carácter epidémico de la enfermedad, los cultivadores de rosa han recurrido al control químico como su principal herramienta para el manejo del mildeo velloso. Varios son los fungicidas reportados contra este patógeno, entre otros se destacan: Dimetomorf (ácido cianimico), Metalaxil, Oxadixil (Fenilamida), Mancozeb, Propineb (Ditiocarbamato), Fosetil-Al (Fosfonato), Dithianon (Antraquinona), Ácido fosfórico, Azoxistrobin (Strobilurina), Dichlofluanid (Sulfamida), Cimoxanil (Cianoacetamida), Iprovalicarb (Carbamato; Quiroga, 2004; Walter et al., 2004). Sin embargo, la efectividad de algunos de ellos no esta aún bien establecida, tal como se concluye de investigaciones realizadas en cultivos de rosa ubicados en la sabana de Bogotá (Urrea y Arbeláez, 2004; Quiroga, 2004). En los últimos años uno de los aspectos más estudiandos en los Oomycetes han sido sus relaciones filogenéticas intra e intergenéricas. Para el caso particular de P. sparsa, los análisis de secuencias basados en la región ITS del ADNr, han ubicado a esta especie en un grupo filogenético que incluye además a Phytophthora megakarya, Phytophthora palmivora y Phytophthora arecae, especies tropicales que presentan carácteres evolutivos avanzados tales como esporangios caducopapilados y adaptación a habitats aéreos. La formación de este cluster entre especies de Phytophthora y Peronospora, confirma la hipótesis de que los mildeos vellosos posiblemente evolucionaron a partir de ancestros hemibiótrofos (Cooke et al., 2000). De otra parte, Riethmuller et al. (2002), luego de realizar un análisis filogenético de la familia Peronosporaceae con base en las secuencias de la región 28S del ADNr, determinaron que P. sparsa se encontraba relacionado con la especie Peronospora sanguisorbae en un cluster aislado del grupo que incluyó a la mayor parte de las especies del género Peronospora. Esto conduce a pensar que en el futuro próximo se requieren nuevos estudios tendientes a aclarar la posición taxonómica del agente causal del mildeo vellosos de la rosa. Además del empleo de las herramientas moleculares en estudios taxonómicos, dichas técnicas también se han utilizado para el desarrollo de aplicaciones prácticas como por ejemplo en la detección prematura de P. sparsa a partir de materiales de propagación de rosa. En este sentido, Aegerter et al. (2002) diseñaron un par de primers específicos con base en la región ITS del ADNr, los cuales resultaron altamente efectivos para la detección de cantidades tan bajas como 2 pg de ADN del patógeno, además de ser útiles para la amplificación de ADN obtenido a partir de plantas de rosa asintomáticas pero infectadas por el pseudohongo. Cuando los investigadores probaron la utilidad de la técnica, encontraron que el patógeno puede estar presente en tejidos de plantas de rosa tan diversos como tallos, raíces y ramas altamente lignificadas de plantas asintomáticas y sintomáticas, lo cual confirma la naturaleza sistémica de la infección por parte del mildeo velloso de la rosa. El conocimiento del nivel de variabilidad de un patógeno y de su estructura poblacional en una región determinada, es fundamental para el diseño de estrategias de control de la enfermedad que causa, por cuanto ofrece información valiosa sobre los linajes genéticos del patógeno que deben incluir los programas de resistencia varietal y de control químico y biológico. La presente investigación tuvo como objetivos: confirmar la identidad taxonómica del agente causal del mildeo velloso de la rosa en Colombia mediante PCR y secuenciación con primers específicos y evaluar la variabilidad genética de 34 aislamientos de este patógeno procedentes del oriente antioqueño y la sabana de Bogotá, utilizando la técnica molecular PCR-RFLP. Este estudio fue además complementado con el análisis de un grupo de 20 aislamientos mediante los marcadores RAPD y RAMS.
MATERIALES Y MÉTODOS
AISLAMIENTOS
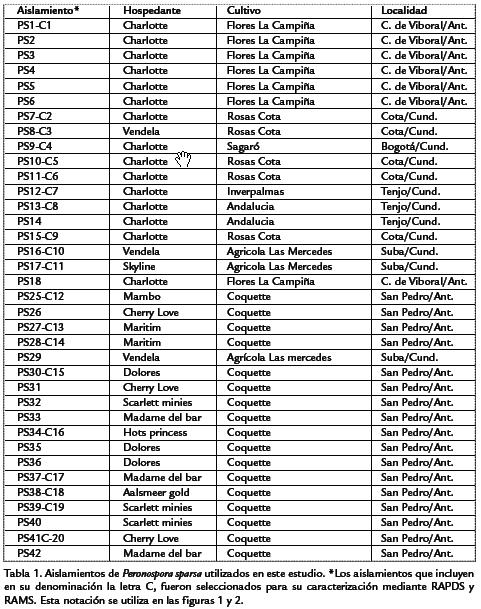
]]> Esta investigación se desarrolló en los Laboratorios de Estudios Moleculares y de Biología Celular y Molecular de la Universidad Nacional de Colombia, Sede Medellín. Las plantas de rosa empleadas para el mantenimiento de los aislamientos de P. sparsa fueron sembradas en el vivero de la Universidad. Treinta y cuatro aislamientos de P. sparsa fueron obtenidos a partir de folíolos de rosa de diferentes variedades con síntomas de mildeo velloso en cultivos ubicados en los municipios de Carmen de Viboral y San Pedro (Antioquia), Tenjo, Cota, Suba y Bogotá (Cundinamarca; Tabla 1). Los folíolos sintomáticos recolectados en campo se ubicaron en cámaras húmedas y una vez detectada su esporulación se procedía al incremento de inóculo mediante la transferencia de estructuras del pseudohongo utilizando un pincel fino humedecido a folíolos jóvenes de plantas de rosa variedad Charlotte, previamente desinfestados con solución de hipoclorito de sodio al 1%. Los folíolos así inoculados, fueron mantenidos en cajas de petri plásticas con medio de sobrevivencia (15 g de agar-agar suplementado con 2 mg/L de kinetina) y acondicionadas como cámaras húmedas, con el haz dirigido hacia la base e incubadas en un fitotrón (Indulab CAB-30, Medellín, Colombia) a 18 °C, una humedad relativa entre 90 y 100% y 12 horas de luz/oscuridad por 5-7 días.

EXTRACCIÓN DE ADN
Para la extracción del ADN de cada aislamiento de P. sparsa se agregaron 150 µL de buffer de extracción (CTAB 2%, NaCl 1,4 M, EDTA 20 mM, Tris-HCl 100 mM pH 8,0) sobre regiones del envés de los folíolos con signos del patógeno, los que mediante pipeteo continuo fueron recolectados y depositados en un tubo eppendorf de 1,5 mL, que se llevaba a -80 °C por 15 min para ser congelado y proceder a su maceración física utilizando un pistilo metálico previamente esterilizado. Posteriormente los tubos se incubaron al baño María a una temperatura de 65 °C por 10 min, tiempo después del cual se procedía a adicionar 1 volumen de Fenol:Cloroformo y un ciclo de centrifugación a 13.000 rpm por 15 min, tomándose el sobrenadante y realizando un segundo lavado mediante 1 volumen de cloroformo. Para la precipitación del ADN se emplearon 2 volúmenes de etanol absoluto y 0,1 volúmenes de acetato de sodio 3 M, incubación a -20 °C por 30 min y centrifugación a 13.000 rpm por 20 min. Luego, se adicionaron 100 µL de etanol al 70 % para proceder al lavado del pellet de ácidos nucleícos y finalmente se procedía a su secado utilizando un equipo Speed vac (Eppendorf 5301, Hamburgo, Alemania). El ADN obtenido, se resuspendía en 20 µL de agua destilada estéril y se almacenaba a 4 °C para su uso posterior.
CONFIRMACIÓN TAXONÓMICA POR PCR
Para confirmar la identidad taxonómica de los aislamientos que causan mildeo velloso de la rosa en Colombia, se realizó una prueba de PCR utilizando los primers específicos PS3 (5' ATT TTG TGC TGG CTG GC 3') y PSI (5' TGC CAC ACG ACC GAA GC 3'), diseñados por Aegerter et al. (2002) para amplificar diferencialmente la región ITS1, 5.8S e ITS2 del ADNr de P. sparsa. Las reacciones de PCR consistieron de 0,1 µM de cadaprimer, 1 U de Taq ADN polimerasa recombinante (Fermentas, Vilnius, Lithuania), 0,2 mM de cada dNTP, 1X de buffer de enzima (100 mM Tris-HCl (pH 8,8), 500 mM KCl, 0,8% Nonidet P40), 2 mM MgCl2, 5 µL de una dilución 1/10 de ADN y un volumen total de 50 µL. Las amplificaciones se realizaron en un termociclador T3 (Biometra, Ale-mania) y consistieron de una desnaturalización inicial a 94 °C por 3 min, seguida por 35 ciclos de 94 °C por 2 min, 60 °C por 1,3 min, 72 °C por 2,5 min y un peiodo final de extensión a 72 °C por 7 min. Luego de la amplificación, se tomaron 5 µL de los productos de reacción y se separaron por electroforesis en gel de agarosa al 1,5% suplementado con 3 µL de bromuro de etidio (10 mg/mL). La visualización de las bandas se realizó bajo luz ultravioleta utilizando el sistema digital de análisis Bio Doc Analyze (Biometra). Adicionalmente a la confirmación taxonómica utilizando el criterio de amplificación con primers específicos, se procedió a la secuenciación de cinco productos de PCR obtenidos en igual número de aislamientos. Para esto, se purificaron los amplicones utilizando el kit Wizard PCR Preps DNA Purification System (Promega, Madison, EEUU) para proceder a su secuenciación directa en ambas direcciones mediante el kit Big Dye Terminator Cycle Sequencing Ready Reaction Kit (PE Applied Biosystems, Foster City, EEUU) y su análisis en un secuenciador ABI Prism 3730xl (PE Applied Biosystems) de la compañía Macrogen (Corea del Sur). Las secuencias obtenidas fueron editadas mediante el software BioEdit (http://www.mbio.ncsu.edu/BioEdit/bioedit.html), alineadas manualmente y comparadas con la base de datos del GenBank (http://www.ncbi.nlm.nih.gov/blast/) utilizando el programa BLAST.
EVALUACIÓN DE VARIABILIDAD GENÉTICA
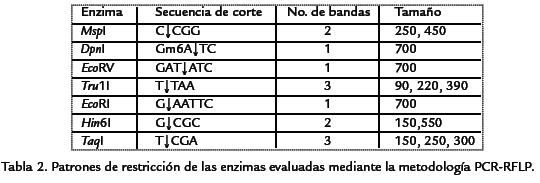
RFLP de regiones ITS. Los productos amplificados de las regiones ITS, fueron digeridos con las enzimas de restricción EcoRV, EcoRI, DpnI, Hin6I, MspI, Tru1I y TaqI. Cada reacción consistió de 2 µL de buffer 10X de enzima, 0,1 µL de cada enzima, 5 µL de producto de PCR y 12,9 µL de agua destilada estéril; incubándose a 37 °C por 24 h. La separación de los fragmentos de restricción se realizó por medio de electroforesis en gel de agarosa al 2%, 70 V y 2 h, visualizándose tal como se indicó anteriormente. Para cada patrón de restricción se determinó el número de bandas generadas y su tamaño aproximado por comparación con el marcador de peso molecular Generuler 100 pb DNA ladder (Fermentas). Con las secuencias depositadas en el GenBank de las regiones ITS2 del ADNr de P. sparsa se realizó un análisis de restricción virtual mediante el software Webcutter 2.0 (http://rna.lundberg.gu.se/cutter2/) utilizando las mismas enzimas empleadas en este estudio; de tal manera que fuera posible inferir el grado de variabilidad de la región ribosomal en este pseudohongo y tener así un patrón de comparación con los resultados de este trabajo. RAPD. Veinte primers RAPD de las series BA, E, M, N y 26 de Operon (Operon Technologies, Alameda, EEUU) fueron seleccionados al azar para su evaluación inicial en cinco aislamientos de P. sparsa provenientes de diferentes regiones de recolección, seleccionándose los cinco que generaron mayor cantidad de bandas legibles y repetibles para su utilización con 20 de los aislamientos bajo estudio. Las reacciones de PCR consistieron de 3 mM de MgCl2, 0,2 mM de dNTPs, 0,8 µM de primer RAPD, 1 U de Taq DNA polimerasa recombinante (Fermentas), 1X de buffer de enzima (100 mM Tris-HCl (pH 8,8), 500 mM KCl, 0,8% Nonidet P40), 10 a 50 ng de ADN y agua destilada ésteril tipo PCR, hasta completar un volumen de 25 µL. La amplificación de PCR se realizó en un termociclador T3 (Biometra) con el siguiente programa: desnaturalización inicial a 94 °C por 3 min, seguida por 40 ciclos de 94 °C por 1 min, 36 °C por 1 min y 72 °C por 2 min, y un periodo final de extensión a 72 °C por 7 min. Los productos amplificados fueron separados en geles de agarosa al 1,5% con 3 µL de bromuro de etidio (10 mg/mL). RAMS. La variabilidad genética de los 20 aislamientos estudiados con RAPDs fue adicionalmente evaluada mediante el empleo de los primers RAMS: NDV (CT)8, DBD (CCA)5, HV (GT)5 G, DBD (CAC)5, HBDB (GACA)4, HVH (GTG)5 y NDB (CAC)7. Las reacciones de amplificación, el programa de PCR y el análisis de agrupamiento se realizaron en forma similar al descrito para RAPD, con la única diferencia que la temperatura de annealing empleada fue de 45 °C.
ANÁLISIS DE DATOS
]]> El análisis de variabiliadad genética para RAPD y RAMS se realizó a partir de la construcción de una matriz binaria basada en ausencia/presencia de amplicones, que se utilizó para la elaboración de la matriz de similitud mediante el índice de Dice y el programa SimQual del software NTSYS-pc Version 1.8 (Exeter Software, Setauket, NY, USA). Posteriormente se generó un dendrograma UPGMA con la ayuda del programa SAHN de dicho software. La diversidad genética de Nei, el número de loci polimórficos y el índice de Shannon para cada grupo de datos, fueron calculados mediante la utilización del software POPGEN32 (University of Alberta, Canada).RESULTADOS
CONFIRMACIÓN TAXONÓMICA POR PCR
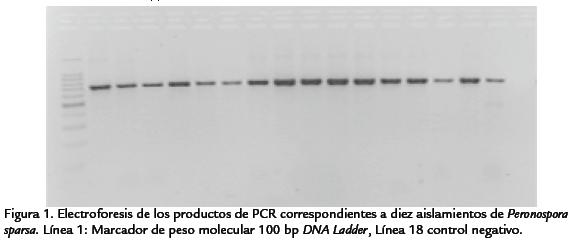
La metodología de extracción de ADN fue objeto de diferentes modificaciones, de tal forma que el protocolo presentado representa un proceso complejo de estandarización. Fue posible obtener ADN a partir de la totalidad de los 34 aislamientos colectados, encontrándose que la preparación de diluciones 1:10 fue la más apropiada para lograr productos óptimos de PCR en la gran mayoría de aislamientos. Así mismo, la realización de las pruebas de PCR fue precedida por un alto número de ensayos, que condujeron a determinar como condiciones óptimas de amplificación de los fragmentos específicos de la región estudiada, una temperatura de annealing de 60 °C, concentraciones de MgCl2 de 2 mM y programas de PCR de 35 ciclos. En todos los aislamientos incluídos en este estudio, fue posible amplificar un producto de aproximadamente 700 pb (Figura 1) que concuerda con el fragmento específico reportado por Aegerter et al. (2002) para los primers PS3 y PS1, de tal forma que esta prueba permite confirmar la identidad de los aislamientos que causan el mildeo velloso de la rosa en Colombia como pertenecientes a la especie P. sparsa. De otra parte, el análisis BLAST de las secuencias de los cinco productos de PCR seleccionados (número de accesión: DQ887773), arrojó un porcentaje de identidad nucleotídica del 100% entre dichas secuencias y la accesión AF266783 que corresponde a la región ITS1, 5.8S e ITS2 del ADNr de un aislamiento de P. sparsa procedente de Rosa sp. en Inglaterra y de un 99% con la accessión AY608610 procedente de un aislamiento del pseudohongo obtenido en Rosa multiflora en Corea del Sur.
EVALUACIÓN DE VARIABILIDAD GENÉTICA
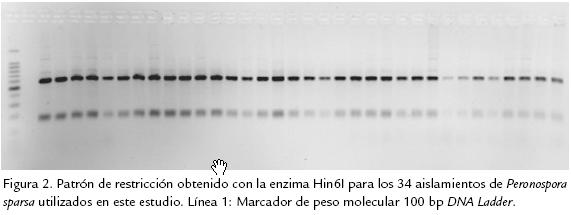
RFLP de regiones ITS. De las siete enzimas de restricción empleadas en esta investigación, tres de ellas (EcoRI, EcoRV y DpnI) no presentaron sitios de restricción en ninguno de los fragmento de ADN amplificados (Tabla 2), mientras que las enzimas MspI, Hin6I, Tru1I y TaqI presentaron de uno a varios sitios de corte dentro de estas secuencias (Figura 2). Los patrones de restricción obtenidos con la totalidad de enzimas empleadas fueron similares en todos los aislamientos de P. sparsa recolectados en esta investigación, de tal forma que se puede inferir que la región ITS1, 5.8S e ITS2 tiene un alto grado de similitud en la población de P. sparsa en Colombia, observación que por lo demás, fue confirmada por el análisis de secuencias de los cinco aislamientos estudiados.
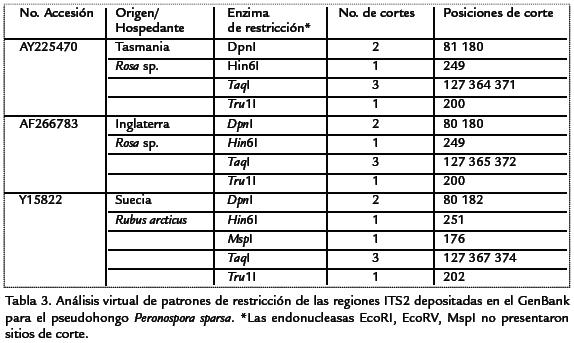
En la búsqueda de regiones del ADN empleadas en el estudio de taxonomía molecular depositadas en el GenBank para P. sparsa se obtuvieron 15 secuencias, todas ellas de origen ribosomal, siendo la región ITS2 la que presentó un mayor número de accesiones, aunque todas ellas procedentes de la planta Rubus arcticus en Suecia. De otra parte, para la subunidad 28S del ADNr solo se ha depositado una secuencia obtenida a partir de un aislamiento de P. sparsa en Prunus laurocerasus en Alemania, mientras que dos secuencias se registran para la región ITS1. Desafortunadamente, de esta búsqueda se desprende que no se ha realizado ningún estudio taxonómico en este patógeno utilizando otras regiones diferentes al ADNr tales como los genes que codifican para el factor de elongación o proteínas histonas, frecuentemente utilizadas en estudios micológicos.
Mediante el análisis virtual de restricción se encontró una gran homogeneidad en las regiones ITS2 del ADNr entre las diez secuencias analizadas, ya que presentaron los mismos patrones de corte con las siete enzimas evaluadas, independiente de que los aislamientos procedían de diferentes hospedantes y países. Las enzimas EcoRI, EcoRV y MspI no tienen regiones de reconocimiento en esta porción del ADNr, mientras que las demás enzimas tienen de 1 a 3 sitios de corte (Tabla 3). RAPD. Con los cinco marcadores RAPD utilizados se amplificaron un total de 48 loci, 18 de los cuales resultaron polimórficos (37,5%). Los tamaños de los fragmentos variaron de 220 a 2220 pb y en promedio correspondieron a 9,6 bandas por marcador. El dendrograma UPGMA generado permite identificar la formación de un grupo mayoritario con 17 de los aislamientos que presentan un grado de similitud superior a 0,89 y tres aislamientos que se ubican por fuera de dicho cluster, pero que aún así presentan una alta relación con el grupo principal (Coeficiente de similitud >0,84). Este bajo nivel de variación encontrado en la población de P. sparsa evaluada se confirmó por el bajo índice de Nei obtenido (h=0,076, desviación estandar (ds): 0,1175) así como de diversidad genotipíca de Shannon (I=0,13, desviación estandar (ds): 0,1878; Fig. 3A). RAMS. De los cinco primers evaluados con esta técnica, solo fue posible obtener información para todos los aislamientos con los primers DBD (CAC)5 y NDB (CAC)7; los demás primers no permitieron originar amplicones con algunos de los aislamientos, aún después de cambiar diferentes variables de la extracción de ADN y las reacciones de PCR, de manera que no fueron incluídos en el análisis. Con estos dos marcadores evaluados se amplificaron 20 loci, tres de los cuales resultaron polimórficos (15%), los fragmentos obtenidos presentaron un rango de 250 a 1000 pb. El dendrograma generado dividió los aislamientos en dos grupos relacionados con un coeficiente de similitud de 0,89 y un muy bajo grado de variación en su interior. Los valores de los índices de Nei y Shannon calculados mediante esta metodología fueron de h=0,0377 (ds: 0,1132) e I=0,0598 (ds: 0,1665), respectivamente (Fig. 3B).
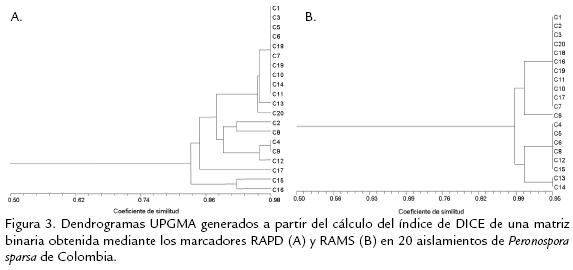
DISCUSIÓN
En esta investigación fue posible obtener una colección representativa de 34 aislamientos del pseudohongo causante del mildeo velloso de la rosa en la sabana de Bogotá y el oriente antioqueño, principales zonas cultivadoras de rosas para exportación en el país. Las visitas de colección permitieron corroborar la gravedad de este problema biótico y el uso excesivo de fungicidas químicos al que recurren los floricultures para su control. De igual manera fue evidente la relación entre el grado de severidad de la enfermedad, las condiciones medioambientales y las variedades cultivadas, confirmándose los resultados de las investigaciones realizadas por Arbeláez (1999) y Gómez y Arbeláez (2004) sobre los principales factores que influyen en los periodos de incubación y latencia del mildeo velloso de la rosa en Colombia, así como la alta susceptibilidad al patógeno de variedades como Charlotte, Vendela, Maritim, Dolores, Hots princess, Aalsmeer Gold, Scarlet minies, Skyline y Cherry Love. La condición holobiótrofa del patógeno y los estrictos requerimientos de humedad, luminosidad y temperatura para el desarrollo de la enfermedad, fueron el principal obstáculo para el establecimiento y mantenimiento bajo condiciones de laboratorio de los aislamientos recolectados. Afortunadamente los trabajos desarrollados Zuñiga (2003) y Gómez (2004), aportaron la metodología inicial a partir de la cual fue posible estandarizar bajo las condiciones propias un sistema eficiente de multiplicación y mantenimiento del inóculo de P. sparsa, utilizando la técnica del pincel y cámaras húmedas individuales constituídas a partir de capas delgadas de agar-agua + kinetina y papel absorbente. De esta forma fue posible obtener suficiente cantidad de material para proceder a la extracción de ADN. La realización de la extracción de ADN a partir de las estructuras del pseudohongo incluyó diferentes estados de variación de los protocolos originales reportados por Riethmuller et al. (1999) y Tian et al. (2004). En todos los casos el factor limitante para desarrollar el procedimiento correspondió a la escasa cantidad de signos del patógeno, característica de la cual se deriva el nombre de P. sparsa. Sin embargo, a pesar de estos incovenientes, fue posible estandarizar una metodología que produjo ADN de calidad adecuada para su utilización en las reacciones de amplificación mediante PCR.
]]> En este estudio fue posible confirmar la identidad taxonómica en la especie P. sparsa del patógeno causante del mildeo velloso de la rosa en Colombia mediante una prueba molecular basada en el empleo de los primers específicos PS1 y PS3 previamente diseñados por Aegerter et al. (2002) y por el análisis de las secuencias de la región ITS1, 5.8S e ITS2 del ADNr de cinco aislamientos seleccionados al azar. Este resultado refuerza lo encontrado en los estudios morfológicos realizados por Arbeláez (1999), en los cuales se describieron en forma detallada los caracteres taxonómicos de los aislamientos colombianos del patógeno (dicotomía de esporangióforos, angulación de esterigmas, dimensiones de esporangios y mecanismo de germinación) y se comparó con las características descritas por Horst (1983) para la especie P. sparsa. En general la prueba molecular demostró ser muy específica a una temperatura de annealing de 60 °C, obteniéndose un amplicón de alrededor de 700 pb, que además de ser utilizado en este estudio para la realización de pruebas de variabilidad intraespecífica mediante RFLP, fue secuenciado para contribuir a la confirmación de la identidad taxonómica de este pseudohongo en Colombia.El estudio de variabilidad intraespecífica utilizando la técnica de RFLP de las regiones ITS1, 5.8S e ITS2 del ADNr indicó que la población de P. sparsa en Colombia es muy homogénea, ya que las siete endonucleasas evaluadas presentaron los mismos per-files de restricción para la totalidad de los aislamientos analizados. Sin embargo este resultado refleja las diferencias en secuencia de una porción muy pequeña del genoma, que aunque ha sido ampliamente utilizada para estudios intra e interespecíficos en hongos y pseudohongos, no necesariamente permite inferir con absoluta certeza la estructura poblacional de los organismos fitopatógenos, tal como se desprende de las investigaciones realizadas en hongos como Botryosphaeria (Slippers et al., 2003), Calonectria y Phytophthora (Cooke et al., 2000). Por este motivo se recurrió a la utilización de otros marcadores moleculares (RAPD y RAMS) que exploran una mayor porción del genoma y que permitan realizar análisis cuantitativos de genética de poblaciones para definir los niveles de variación de un patógeno, encontrándose que efectivamente la población de P. spsarsa en las regiones estudiadas presentan un muy bajo nivel de variabilidad genética, reflejada por la presencia de pocos genotipos y por ende de un componente característicamente clonal. Estos resultados se ajustan a la realidad biológica del patógeno en nuestro medio, en donde bajo condiciones de campo no se presenta la producción de estructuras sexuales del hongo (Arbelaéz, 1999), mientras que la generación de esporangios (estructuras asexuales) es frecuente y puede alcanzar niveles copiosos bajo condiciones de alta humedad y en presencia de variedades vegetales altamente susceptibles a la enfermedad. Esta situación contrasta drásticamente con el único trabajo poblacional que a la fecha se había realizado sobre este patógeno, que corresponde a una investigación desarrollada por Linqvist-Kreuze et al. (2002) sobre la variabilidad de la población de P. sparsa afectando R. arcticus en Finlandia. En ese estudio se emplearon 226 marcadores AFLPs y se determinó que este patógeno presenta una alta variabilidad genética representada en distancias de Jaccard que oscilaron entre 0.53 y 0.88. Sin embargo la biología de P. sparsa en esta región escandinava se caracteriza por la producción masiva de oosporas, que resultan de la recombinación genética de los gametangios del patógeno y sirven además de estructuras de resistencia al patógeno durante los largos periodos invernales que soporta esta zona del mundo.
De otra parte, al realizar la búsqueda de las secuencias depositadas en el GenBank para P. sparsa, se encontró un bajo número de accesiones, todas correspondientes a porciones de las regiones ribosomales. La uniformidad de la región ITS del ADNr en P. sparsa encontrada en esta investigación, se vió confirmada al realizar el análisis virtual de restricción de la región ITS2 de las secuencias disponibles en el GenBank, ya que las diez secuencias analizadas presentaron los mismos patrones de restricción, indepedendientemente de los diferentes hospedantes (Rubus arcticus y Rosa sp.) y sitios de origen (Inglaterra, Tasmania y Suecia) de los aislamientos, lo cual refuerza la necesidad de explorar otras regiones del genoma para determinar las características de la estructura poblacional de P. sparsa. La realización de esta investigación permitió estandarizar el proceso de colección, mantenimiento, extracción de ADN y PCR en P. sparsa bajo las condiciones de los laboratorios de Estudios Moleculares y Biología Molecular y Celular, Universidad Nacional de Colombia, Sede Medellín. Estos procedimientos condujeron a la confirmación de P. sparsa como el agente causal del mildeo velloso de la rosa en Colombia y arrojaron resultados preliminares sobre un alto grado de homogeneidad de las regiones ITS del ADNr en el patógeno, uniformidad que se confirmó mediante los marcadores moleculares RAPD y RAMS. Se espera que esta información sea incorporada en los programas de evaluación de resistencia a fungicidas y de mejoramiento varietal de cultivares de rosa con tolerancia al ataque del patógeno, en el sentido que al presentarse una población principalmente clonal, el número de aislamientos que se requieren evaluar es relativamente bajo y las estrategias generadas tienen un mayor rango geográfico de aplicación, en comparación con aquellos sistemas en los que se presentan poblaciones de microorganismos con altos niveles de recombinanción genética.
AGRADECIMIENTOS
La realización de la presente investigación fue posible gracias a la colaboración de los floricultores del país que permitieron la colección de P. sparsa en sus cultivos. Así mismo, la compañía Bayer CropScience facilitó las plantas de rosa y el apoyo económico para la colección y mantenimiento de los aislamientos. La evaluación molecular se realizó con financiación de la Dirección de Investigaciones de la Universidad Nacional de Colombia, Sede Medellín, proyecto DIME # 30802871.
BIBLIOGRAFÍA
AEGERTER BJ, NUÑEZ JJ, DAVIS R M. Detection and Management of Downy Mildew in Rose Rootstock. Plant Dis. 2002;86(12):1363-1368. [ Links ]
AEGERTER BJ, NUÑEZ JJ, DAVIS RM. Environmental Factors Affecting Rose Downy Mildew and Development of a Forecasting Model for a Nursery Production System. Plant Dis. 2003;87(6):732-738. [ Links ]
ARBELÁEZ G. El mildeo velloso del rosal ocasionado por Peronospora sparsa Berkeley. Acopaflor. 1999;6(4):37-39. [ Links ]
COOKE DE, DRENTH A, DUNCAN JM, WAGELS G, BRASIER CM. A Molecular Phylogeny of Phytophthora and Related Oomycetes. Fungal Genet Biol. 2000;30:17-32. [ Links ]
FILGUEIRA JJ. Estudio microscópico del desarrollo biológico de Peronospora sparsa en rosa bajo condiciones controladas. XXV Congreso ASCOLFI. Palmira, Colombia 11-13 de agosto de 2004. [ Links ]
FLÓREZ RV. El papel de las fenilamidas en el manejo del mildeo velloso en ornamentales. Acopaflor. 1996;3(5):30-31. [ Links ]
GÖKER M, VOGLMAYR H, RIETHMÜLLER A, WEIB M, OBERWINKLER F. Taxonomic Aspects of Peronosporaceae Inferred from Bayesian Molecular Phylogenetics. Can J Bot. 2003;81:672-683. [ Links ]
GÓMEZ S. Determinación de componentes de la biología de Peronospora sparsa Berkeley, y caracterización de la respuesta de tres variedades de rosa a la infección del patógeno bajo condiciones de laboratorio e invernadero [tesis de Maestría]. Bogotá: Facultad de Agronomía, Universidad Nacional de Colombia; 2004. [ Links ]
GÓMEZ S, ARBELAEZ G. 2004. Biología de Peronospora sparsa agente causal de mildeo velloso en rosa y su relación con el desarrollo de la enfermedad bajo condiciones de invernadero en la Sabana de Bogotá. XXV Congreso ASCOLFI. Palmira, Colombia 11-13 de agosto de 2004. [ Links ]
GÓMEZ S, ARBELAEZ G. Evaluación del período de latencia y capacidad de producción de inóculo de Peronospora sparsa, agente causal del mildeo velloso en tres variedades de Rosa. XXIV Congreso ASCOLFI. Armenia, Colombia 25-27 de junio del 2003a. [ Links ]
GÓMEZ S, ARBELAEZ G. Evaluación del período de incubación de Peronospora sparsa, agente causal del mildeo velloso en tres variedades de Rosa. XXIV Congreso ASCOLFI. Armenia, Colombia 25-27 de junio del 2003b. [ Links ]
HAWKSWORTH DL, KIRK PM, SUTTON BC, PEGLER DN. Ainswork & Bisby's Dictionary of the Fungi. 8 ed. Egham ( UK ): CAB Internacional; 1995. [ Links ]
HOLLIER CA, OVERSTREET C, HOLCOMB GE. Rose Diseases. Publication 2613. Louisina, EEUU: Louisiana State University Agricultural Center; 2001. [ Links ]
HORST K. Compendium of Rose Diseases. St. Paul, EEUU: American Phytopathological Society Press; 1983. [ Links ]
INFOAGRO. El cultivo de rosas para corte [citado Junio de 2004]. Disponible en: www.infoagro.com/flores/flores/rosas.htm . [ Links ]
KAMOUN S. Molecular Genetics of Pathogenic Oomycetes. Eukaryotic Cell. 2003; 2(2):191-199. [ Links ]
LINDQVIST-KREUZE H, KOPONEN H, VALKONEN,J. Variability of Peronospora sparsa (syn. P. rubi) in Finland as Measured by Amplified Fragment Length Polymorphism. Eur J Plant Pathol. 2002;108:327-335. [ Links ]
MARTÍNEZ JC. Respuesta de tres variedades de rosa injertadas en dos patrones, al mildeo velloso, Peronospora sparsa, Berk [trabajo de pregrado]. Bogotá: Facultad de Agronomía, Universidad Nacional de Colombia; 2002. [ Links ]
MICHELMORE RW, ILOTT T, HULBERT SH, FARRARA B. The Downy Mildews. Advances in Plant Pathology. 1988;6:55-76. [ Links ]
MONTILLA JO, DELGADO B, JIMENEZ N. Agentes causales e intensidad de enfermedades fungosas en mora de castilla en el estado Lara. Fitopatología Venezolana. 2003;16(2):31-34. [ Links ]
QUIROGA B. Evaluación de la eficacia de cuatro fungicidas aplicados al suelo y al follaje para el control de mildeo velloso, ocasionado por Peronospora sparsa, en un cultivo comercial de rosa, variedad charlotte [trabajo de grado]. Bogotá: Facultad de Agronomía, Universidad Nacional de Colombia; 2004. [ Links ]
QUITIAN A. Algunos aspectos sobre mildeo velloso y su manejo. Acopaflor. 1995;2(5):25-26. [ Links ]
RESTREPO L F. Susceptibilidad de las rosas a los mildeos. Acopaflor. 1996; 3(5):3-6 [ Links ]
RIETHMÜLLER A, VOGLMAYR H, GÖKER M, WEIß, M, OBERWINKLER F. Phylogenetic Relationships of the Downy Mildews (Peronosporales) and Related Groups Based on Nuclear Large Subunit Ribosomal DNA Sequences. Mycologia. 2002;94(5):834-849. [ Links ]
SLIPPER B. Taxonomy, Phylogeny and Ecology of Botryosphaeriaceous fungi Occurring on Various Woody Hosts, Pretoria [Ph. D. Dissertation]. Pretoria: University of Pretoria; 2003. [ Links ]
TAMAYO, JP. Principales enfermedades del tomate de árbol, la mora y el lulo en Colombia. Rionegro: CORPOICA; 2001. [ Links ]
TIAN CM, SHANG YZ, ZHUANG JY, WANG Q, KAKISHIMA M. Morphological and Molecular Phylogenetic Analysis of Melampsora Species on Poplars in China. Mycoscience. 2004;45:56-66. [ Links ]
URREA K, ARBELAEZ G. Evaluación de la eficacia de fungicidas para el control del mildeo velloso (Peronospora sparsa) en un cultivo comercial de rosa bajo invernadero. XXV Congreso ASCOLFI. Palmira, Colombia 11-13 de agosto de 2004. [ Links ]
WALTER M, HARRIS-VIRGIN P, THOMAS W, TATE G, WAIPARA NW, LANGFORD G. Agrochemicals Suitable for Downy Mildew Control in New Zealand Boysenberry Production. Crop Prot. 2004;23:327-333. [ Links ]
ZUÑIGA REYES SA. Evaluación y ajuste de un módulo de condiciones ambientales controladas como unidad de producción constante de mildeo velloso en plantas de rosa [trabajo de grado]. Bogotá: Facultad de Ingienería, Departamento de Ingeniería Agrícola, Universidad Nacional de Colombia; 2003. [ Links ] ]]>