Recibido: 07/09/05. Aceptado: 12/10/05
La ecocardiografía es la técnica más utilizada para el diagnóstico y seguimiento de las enfermedades cardiovasculares; por lo tanto, su precisión diagnóstica ha adquirido una importancia vital en el manejo de los pacientes con patologías cardiovasculares. Sin embargo, con relativa frecuencia, la capacidad diagnóstica del examen ecocardiográfico está disminuida por limitaciones de la ventana acústica, sobre todo en pacientes con obesidad, enfermedades pulmonares y alteraciones de la pared torácica (1). Esto puede obviarse con el uso de la ecocardiografía transesofágica, si bien este es un procedimiento semi-invasivo y poco práctico de realizar en todos los pacientes con problemas de ventana acústica.
El desarrollo de los agentes de contraste ultrasónicos (Tabla 1) que atraviesan la circulación pulmonar y opacifican las cavidades izquierdas, ha revolucionado el campo diagnóstico de la ecocardiografía al permitir visualizar con mayor nitidez los bordes endocárdicos y las alteraciones morfológicas del ventrículo izquierdo, determinar mejor los registros de los flujos transvalvulares izquierdos con Doppler y evaluar las alteraciones de la perfusión miocárdica (1, 2). ]]>
En este artículo se revisarán las aplicaciones clínicas más comunes de la ecocardiografía de contraste.Evaluación de la función ventricular izquierda global y regional
Utilidad durante la ecocardiografía de estrés para el diagnóstico de enfermedad coronaria
Durante la ecocardiografía de estrés, la disminución de la calidad de la imagen, en especial en el estrés pico, permanece como el talón de Aquiles de la técnica. La falta o inadecuada visualización de algunos segmentos endocárdicos, es causa frecuente de resultados falsos positivos o negativos, con implicaciones potencialmente serias para el paciente. Un resultado falso positivo llevaría al paciente a la realización de una angiografía coronaria innecesaria, y un resultado falso negativo, daría una falsa tranquilidad al médico y al paciente, al no diagnosticar una enfermedad coronaria potencialmente severa (3). Varios estudios han demostrado el papel importante que pueden jugar los agentes de contraste durante los estudios de ecocardiografía de estrés, especialmente en los pacientes con ventanas sub-óptimas (4, 5).
Con relativa frecuencia, durante la ecocardiografía de estrés no es posible evaluar dos o más segmentos cardiacos, lo cual disminuye la exactitud diagnóstica del examen. La Sociedad Americana de Ecocardiografía recomienda la utilización de los agentes de contraste en los pacientes con estudios bi-dimensionales subóptimos donde dos de seis segmentos, en una ventana apical estándar, no se visualicen en el estudio basal (1).
El costo de los agentes de contraste es un factor que inhibe su uso en muchos servicios de ecocardiografía. En Norte América, tres estudios demuestran que la utilización de contraste puede ser costo-efectiva en términos de reducir el número de exámenes adicionales redundantes que pueden ordenarse (3, 6, 7). Además, la ecocardiografía de estrés se usa con frecuencia como parte del proceso de selección para la realización de procedimientos más costosos e invasivos, tales como la angiografía coronaria, la angioplastia coronaria percutánea o la cirugía de revascularización miocárdica.
Actualmente, en los laboratorios de ecocardiografía de Estados Unidos y Europa, los agentes de contraste de ultrasonido se emplean en más del 50% de los pacientes sometidos a ecocardiografía de estrés (4, 8-10).
Utilidad para la determinación de la función sistólica ventricular izquierda
La fracción de expulsión es un índice comúnmente utilizado en la evaluación de la función global ventricular izquierda. Es un método práctico y de extensa aplicación en los laboratorios de ecocardiografía para el diagnóstico de disfunción sistólica.
El cálculo de la fracción de expulsión (volumen fin diástole-volumen fin sístole/volumen fin diástole x 100), es uno de los índices más importantes para la toma de decisiones clínicas. Una fracción de expulsión menor de 40% es indicación para la suministración de inhibidores de la enzima convertidora de angiotensina y beta-bloqueadores en pacientes con falla cardiaca (11). Una fracción de expulsión menor de 30% a 35%, puede influenciar la decisión para la implantación de un cardiodesfibrilador (12, 13). Cuando no hay una adecuada visualización de los bordes endocárdicos, es muy difícil evaluar de manera correcta la función ventricular izquierda. En estos casos, la determinación de los volúmenes de fin de diástole y sístole necesarios para el cálculo de la fracción de expulsión, puede dar resultados erróneos y originar decisiones terapéuticas desacertadas (14, 15). La administración de los agentes de contraste ultrasónicos, ha mejorado notoriamente la capacidad para analizar a cabalidad la función ventricular izquierda global y regional, y ha permitido tomar decisiones terapéuticas más acertadas, al disminuir las fuentes potenciales de error secundarias a los problemas de interpretación por ventanas acústicas inadecuadas (14, 15).
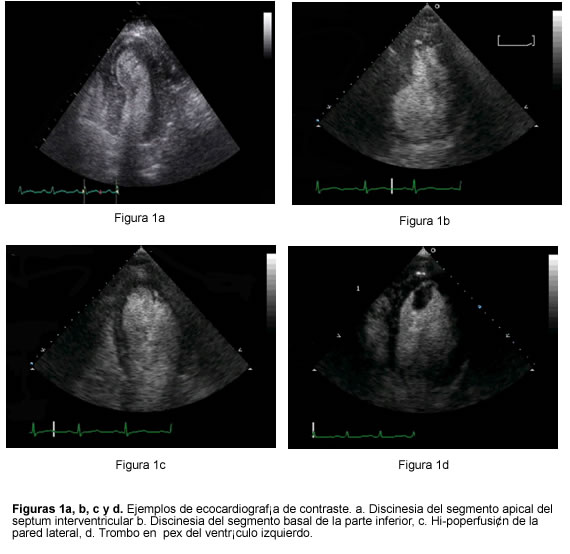
]]> Análisis de la geometría ventricular izquierda y patología intracardiacaCuando hay limitaciones en la calidad técnica de las imágenes, el diagnóstico de las alteraciones en la geometría del ventrículo izquierdo puede ser muy demandante. La ecocardiografía de contraste ha demostrado utilidad en el diagnóstico de la rotura de la pared libre del ventrículo izquierdo (16, 17) y de seudoaneurisma ventricular izquierdo después de infarto agudo del miocardio (18). En pacientes con ventanas acústicas subóptimas, es igual de difícil determinar la presencia de masas o de trombos intracardiacos. Cuando el ápex no se visualiza en forma adecuada, es fácil pasar por alto la presencia de un trombo intracardiaco (1)(Figura 1).

Análisis de registros Doppler
La utilización de Doppler pulsado, continuo, color y de tejidos ha sido de enorme utilidad para la evaluación de la función ventricular y de los flujos intra y yuxtacardiacos (19). Sin embargo, en los pacientes con problemas de ventana acústica, las señales Doppler pueden ser de escasa intensidad y no dar una interpretación adecuada de los gradientes y flujos transvalvulares. En estos casos, la ecocardiografía con agentes de contraste intravenoso, aumenta la intensidad de la señal Doppler. En pacientes con estenosis aórtica, el contraste es particularmente útil para delinear las velocidades que se obtienen con Doppler y aumentar la reproducibilidad de las determinaciones del área valvular aórtica (20).
En pacientes con insuficiencia tricúspide, usualmente se administra solución salina agitada para obtener un registro adecuado del perfil de velocidad de la insuficiencia tricúspide, lo que permite el cálculo de la presión sistólica de la arteria pulmonar. Sin embargo, en algunos casos, el perfil de velocidad no se obtiene adecuadamente con la solución salina y en ese caso es más acertada la administración de agentes de contraste. Otra aplicación práctica de los agentes de contraste, es en la evaluación del flujo venoso pulmonar, de utilidad para la evaluación de las presiones de llenado ventricular izquierdo. El contraste aumenta las señales de flujo en campo lejano, como es el caso del registro de las velocidades de las venas pulmonares en la proyección apical cuatro cámaras (10).
Análisis de perfusión miocárdica
La ecocardiografía miocárdica de contraste permite el análisis de la perfusión miocárdica, tanto en el paciente con síndrome coronario agudo, como en el paciente con enfermedad coronaria crónica. Es de gran utilidad para evaluar la presencia de viabilidad miocárdica en el paciente post-infarto agudo y en aquellos con miocardiopatías isquémicas. Así mismo, permite evaluar el miocardio hibernante con posibilidad de recuperación funcional después de un proceso de revascularización (21-23).
Síndromes coronarios agudos
]]> En los síndromes coronarios agudos, la ecocardiografía miocárdica de contraste permite analizar la función microvascular ya que define el área en riesgo durante la oclusión coronaria aguda; así mismo permite evaluar la presencia de daño microvascular después de la terapia de reperfusión.El área en riesgo puede definirse no sólo por medio de la administración intracoronaria del contraste sino también a través de su administración vía intravenosa periférica. Un estudio multicéntrico europeo (24) demostró alta sensibilidad de la ecocardiografía miocárdica de contraste intravenosa para la detección de los defectos de perfusión en los pacientes con oclusión total del vaso relacionado con el infarto, especialmente para infarto de pared anterior agudo. A los pacientes se les realizaron estudios seriados de perfusión antes y después de la realización de angioplastia primaria. En los pacientes con infarto anterior agudo, la evaluación correcta de los defectos de perfusión al momento de la admisión fue posible en el 100%; en los pacientes restantes, quienes tenían infarto de pared inferior agudo, el diagnóstico fue correcto en el 84%. Todos los pacientes con infarto agudo de la pared anterior demostraron un defecto de perfusión, excepto tres pacientes que tuvieron abierta la arteria relacionada con el infarto en la angiografía con flujo TIMI grado III. Los resultados de la ecocardiografía miocárdica de contraste en los infartos agudos de la pared inferior, no fueron tan exactos y 13 de 23 pacientes no evidenciaron un defecto de perfusión a pesar de un flujo TIMI grado 0 en la angiografía.
En resumen, la ecocardiografía miocárdica de contraste permite clasificar a los pacientes con infarto cardiaco agudo con relación al área en riesgo; ésta depende no sólo de la arteria relacionada con el infarto sino también de la presencia o ausencia de flujo colateral. La ecocardiografía miocárdica de contraste es muy útil para identificar la perfusión colateral en presencia de una arteria ocluida relacionada con el infarto (25).
El análisis del flujo sanguíneo miocárdico proveniente de colaterales es adecuado para determinar el pronóstico de los pacientes con infarto cardiaco agudo y también para definir la terapia de revascularización. El tejido miocárdico con flujo sanguíneo residual puede no sufrir necrosis, incluso con oclusión coronaria persistente de varios días de duración. En estos pacientes, la revascularización de la arteria culpable puede conducir a mejoría de la función regional, situación que Sabia y colaboradores (26) demostraron en un grupo de 43 pacientes con infarto agudo del miocardio referidos a cateterismo cardiaco para la realización de angioplastia coronaria, 2 a 5 semanas después de ocurrido el evento. Se hizo ecocardiografía miocárdica de contraste para analizar el porcentaje del lecho del infarto perfundido por circulación colateral. En los pacientes con angioplastia exitosa, aquellos con más del 50% del lecho del infarto irrigado por flujo colateral, tuvieron mayor movimiento de la pared y mejoría considerable en el movimiento de la pared durante el seguimiento, que aquellos con menos del 50% del lecho del infarto irrigado por flujo colateral. El grado de recuperación funcional no estuvo influenciado por el período de tiempo entre el infarto y la realización de la angioplastia.
En síntesis, la ecocardiografía miocárdica de contraste puede jugar un papel en la evaluación pronóstica de los pacientes con infarto agudo del miocardio no reperfundido, al determinar segmentos potencialmente viables y al seleccionar pacientes que se podrían beneficiar de un procedimiento de revascularización coronaria tardía de la arteria relacionada con el infarto.
Utilidad después de la reperfusión de los vasos epicárdicos
La ecocardiografía miocárdica de contraste ha demostrado ventaja en la evaluación del fenómeno de no-reflujo (27). Después de trombólisis o angioplastia primaria para el tratamiento de un infarto agudo del miocardio, el flujo epicárdico puede mejorar pero no está siempre acompañado por restauración del flujo sanguíneo miocárdico. Hasta 25% de los pacientes con infarto agudo del miocardio, puede demostrar flujo TIMI grado 3 y no signos de perfusión miocárdica, hallazgo que evidencia daño irreversible de la microcirculación coronaria y ausencia de viabilidad (28). Los pacientes que demuestran disfunción microvascular por ecocardiografía miocárdica de contraste después de infarto agudo del miocardio, evidencian mayor número de complicaciones tempranas y durante el primer mes de seguimiento; éstas son falla cardiaca congestiva precoz, derrame pericárdico y dilatación progresiva del ventrículo izquierdo. Adicionalmente, el riesgo relativo de presentar eventos cardiacos mayores durante el seguimiento a un año (muerte cardiaca, reinfarto del miocardio no fatal y rehospitalización por falla cardiaca), fue 8,5 veces más frecuente en los pacientes con disfunción microvascular (29, 30). Estos datos fueron confirmados por Porter y colaboradores (31) con ecocardiografía miocárdica de contraste intravenosa. Un defecto de contraste persistente en la zona del infarto después de la restauración del flujo TIMI grado III en la arteria relacionada con el infarto, identificó a los pacientes con aumento en el volumen de fin de sístole ventricular izquierdo y disminución de la fracción de expulsión durante el seguimiento.
Síndromes coronarios crónicos
Las arterias coronarias con estenosis de 50% a 85% del diámetro luminal coronario, demuestran una respuesta hiperémica disminuida cuando se incrementa la demanda miocárdica de oxígeno. Durante la ecocardiografía de estrés con adenosina, el flujo sanguíneo miocárdico aumenta de manera progresiva y la reserva de la velocidad del flujo miocárdico es proporcional a la reserva de la velocidad de las microburbujas (32). Los pacientes con estenosis coronaria mayor del 70%, tienen una reserva de flujo sanguíneo miocárdico menor de 1,5. La reducción en el flujo sanguíneo miocárdico se asocia con una reducción en el volumen sanguíneo miocárdico; por ejemplo, en el lecho vascular irrigado por una arteria estenótica, el volumen sanguíneo miocárdico está disminuido cuando se presenta hiperemia.
Es posible cuantificar la cantidad de miocardio que está en riesgo debido a estenosis coronaria moderada a severa. Kaul y colaboradores (33) demostraron que la localización de los defectos de perfusión reversibles e irreversibles con ecocardiografía miocárdica de contraste, es similar a la que se observa con la tomografía de emisión de fotón único. La sensibilidad y especificidad para detectar segmentos con perfusión anormal es de 92% y 84% respectivamente. Además, la combinación del análisis del movimiento de la pared con los hallazgos obtenidos de la ecocardiografía miocárdica de contraste, presenta el mejor balance entre sensibilidad (86%), especificidad (88%) y exactitud (86%) para la detección de áreas isquémicas (34).
]]> Viabilidad miocárdicaLa identificación de miocardio viable permite una mejor selección de los pacientes que requieren revascularización. La presencia de perfusión con ecocardiografía miocárdica de contraste, indica integridad microvascular y viabilidad tisular. De otra parte la ausencia de perfusión indica necrosis de las células miocárdicas y daño irreversible de la microvasculatura (35, 36).
Durante el infarto agudo del miocardio, la detección de integridad microvascular identifica la presencia de viabilidad. Ito y colaboradores (37), estudiaron un grupo de pacientes con infarto agudo del miocardio, y aquellos con evidencia de ausencia de flujo intramiocárdico demostraron peor función ventricular que aquellos con reperfusión exitosa. Sabia y colaboradores (25), demostraron que la recuperación de la función sistólica después de la reapertura del vaso epicárdico, fue significativamente mayor en los pacientes con colaterales intramiocárdicos dentro del área en riesgo, analizado por inyección de contraste intracoronario en la arteria no relacionada con el infarto.
Miocardio hibernante
En la situación de disfunción ventricular izquierda crónica a causa de enfermedad arterial coronaria crónica, la ecocardiografía miocárdica de contraste ayuda a diferenciar el miocardio hibernante del miocardio con disfunción irreversible (38). La sensibilidad y especificidad para identificar segmentos viables en pacientes post-infarto y que demuestran recuperación funcional en el seguimiento, fueron respectivamente 100% y 46% para la ecocardiografía miocárdica de contraste, y 71% y 88% para la ecocardiografía de estrés con dobutamina (39). Si la integridad microvascular dentro del área en riesgo post-infarto está preservada, la reserva contráctil y la recuperación funcional estarán en el seguimiento. En el daño anatómico de la microcirculación, la reserva contráctil y la recuperación funcional no estarán presentes. Senior y colaboradores (40), estudiaron un grupo de pacientes después de infarto agudo del miocardio; la ecocardiografía miocárdica de contraste mejoró la sensibilidad de la ecocardiografía de estrés con dobutamina para la detección de viabilidad miocárdica de 59% a 79%, y el valor predictivo negativo aumentó de 88% a 95%.
Ablación septal con alcohol en miocardiopatía hipertrófica
La inyección de alcohol a través de un catéter adentro de las arterias coronarias septales con el objetivo de crear un infarto localizado a nivel del septum basal, ha evolucionado como una alternativa menos invasiva que la miectomía quirúrgica en los pacientes con miocardiopatía hipertrófica (41, 42). Estas terapias alivian la obstrucción del tracto de salida ventricular izquierdo por reducir o remover el tejido miocárdico en el septum ventricular. La administración de contraste intracoronario permite la identificación del sitio más apropiado del septum intraventricular para la ablación septal con etanol. Durante el procedimiento, el agente de contraste se administra a través de un catéter localizado en la arteria perforante septal. La región irrigada por este vaso demuestra aumento de la ecogenicidad por el contraste. Si esta no es la porción que se desea necrosar, se procede a escoger otra arteria perforante septal (43).
Medición de la reserva de la velocidad del flujo coronario
La reserva del flujo coronario se define como el incremento pico en el flujo sanguíneo coronario, con relación al flujo basal, cuando la circulación coronaria está dilatada al máximo. La disminución de la reserva del flujo coronario es un marcador sensible de isquemia, estenosis coronaria funcionalmente significativa y disfunción endotelial. Con la introducción de transductores de alta frecuencia, imagen armónica y agentes de contraste, la ecocardiografía transtorácica permite la visualización de las arterias coronarias, especialmente la arteria descendente anterior, en más del 90% de los pacientes. La visualización de la arteria coronaria derecha es factible también en más del 75% de los pacientes (44). Cuando la reserva de la velocidad del flujo coronario es menor de 2, la sensibilidad, especificidad y exactitud para el diagnóstico de estenosis significativa (>50%) de la arteria que da origen a la descendente posterior, es de 84%, 83% y 83%, respectivamente; mientras que para la arteria descendente anterior es de 91%, 75% y 80% respectivamente (45).
Ecocardiografía de los pacientes en las unidades de cuidados intensivos
]]> Los estudios ecocardiográficos realizados en las unidades de cuidados intensivos, con frecuencia son subóptimos o de mala calidad desde el punto de vista diagnóstico, debido a la incapacidad para colocar al paciente en una posición adecuada y a problemas ambientales en la realización de estos estudios, tales como la luz del sol o de las lámparas, los vendajes y los tubos de tórax. Muchos de estos pacientes están intubados y habitualmente son incapaces de cooperar con el examen. De igual forma, las condiciones locativas a menudo son inapropiadas para una posición adecuada del equipo de ultrasonido.Hay gran interés en la utilización rutinaria de la ecocardiografía en las unidades de cuidados intensivos. La evaluación de la función ventricular y de las presiones de llenado por ecocardiografía, ofrece una alternativa no invasiva al cateterismo de arteria pulmonar (46). La ecocardiografía con contraste mejora el campo diagnóstico de los estudios transtorácicos realizados a los pacientes hospitalizados en las unidades de cuidados intensivos (47). Diversos estudios han demostrado que la ecocardiografía con agentes de contraste en las unidades de cuidados intensivos, clarifica la definición de los bordes endocárdicos, el movimiento de la pared y la fracción de expulsión del ventrículo izquierdo (48-54). Sin embargo, a pesar de su disponibilidad, los agentes de contraste ecocardiográfico aún se subutilizan y los principales factores parecen ser la falta de conocimiento en su utilización y el costo. Yong y colaboradores (50), han utilizado la ecocardiografía de contraste en los Estados Unidos con un costo promedio de 380 dólares por paciente. Esto deberá compararse con los costos del cateterismo y las mediciones y cuidados especiales asociados con los catéteres de Swan-Ganz en las unidades de cuidados intensivos, los cuales se estiman en 2.000 dólares por paciente (55).
Conclusiones
En la actualidad, la ecocardiografía de contraste tiene un papel importante y definido en la evaluación clínica de los pacientes con enfermedades cardiovasculares. No sólo es útil en la evaluación de los pacientes con alteraciones de la ventana acústica sino que abre nuevas perspectivas diagnósticas en la evaluación de los pacientes con disfunción ventricular izquierda, síndromes coronarios agudos y crónicos, determinación de la reperfusión y viabilidad miocárdica, evaluación del miocardio hibernante y de la reserva de flujo coronario, guía del tratamiento de la ablación septal con alcohol en los pacientes con miocardiopatía hipertrófica y mejora de la cobertura diagnóstica de los enfermos hospitalizados en las unidades de cuidados intensivos.
Bibliografía
1. Mulvagh S, DeMaria AN, Feinstein SB, et al. Contrast echocardiography: current and future applications. J Am Soc Echocardiogr 2000; 13: 331-42.
2. Kuecherer H. The added clinical value of second generation ultrasound contrast agents. Echocardiography 2003; 20 (Suppl 1): S3-S9.
3. Thanigaraj S, Perez JE. Image enhancement with second generation contrast agents improve diagnostic accuracy and reduces additional testing. J Am Soc Echocardiogr 1999;12: 366...
4. Rainbird AJ, Mulvagh SL, Oh JK, et al. Contrast dobutamine stress echocardiography: clinical practice assessment in 300 consecutive patients. J Am Soc Echocardiogr 2001; 15: 378-385.
5. Porter TR, Xie F, Kricsfeld A, et al. Improved endocardial border resolution during dobutamine stress echocardiography with intravenous sonicated dextrose albumin. J Am Coll Cardiol 1994; 23: 1440-1443.
]]> 6. Shaw LJ, Monaghan MJ, Nihoyannopolous P. Clinical and economic outcomes assessment with myocardial contrast echocardiography. Heart 1999; 82 (Suppl 3): 16-21.7. Shaw LJ, Dittrich HC. Use of intravenous Optison contrast echocardiography reduces downstream resource use and enhances savings. Acad Radiol 1998; 5 (Suppl): S250-S251.
8. Timperley J, Mitchell ARJ, Thibault H, et al. Safety of contrast dobutamine stress echocardiography: a single center experience. J Am Soc Echocardiogr 2005; 18: 163-67.
9. Monaghan MJ. Echo contrast enhancement of the left ventricle-imaging technology and micro-spheres, is the marriage critical? Eur J Echocardiogr 2001; 2: 143-144.
10. Pandian NG. Clinical applications of contrast echocardiography. Eur J Echocardiography 2004 (Suppl 2): S3-S10.
11. Swedberg K,Cleland J, Dragie H, et al. Guidelines for the diagnosis and treatment of chronic heart failure: executive summary (update 2005). The task force for the diagnosis and treatment of chronic heart failure of the European Society of Cardiology. Eur Heart J 2005; 26: 1115-1140.
12. Moss AJ, Zareba W, Hall WJ, et al. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction. N Engl J Med 2002; 346: 877-883.
13. Kaddesh A, Dyer A, Daubert Jp, et al. Prophylactic defibrillator in patients with nonischemic dilated cardiomyopathy. N Engl J Med 2004; 350: 2151-2158.
14. Thomson HL, Basmadjian AJ, Rainbird AJ, et al. Contrast echocardiography improves the accuracy and reproducibility of left ventricular remodeling measurements. J Am Coll Cardiol 2001; 38: 867-72.
15. Malm S, Frigstad S, Sagberg E, et al. Accurate and reproducible measurement of left ventricular volume and ejection fraction by contrast echocardiography. A comparison with magnetic resonant imaging. J Am Coll Cardiol 2004; 44: 1030-5.
]]> 16. Waggoner AD, Williams GA, Gaffron D, et al. Potential utility of left heart contrast agents in diagnosis of myocardial rupture by 2-dimensional echocardiography. J Am Soc Echocardiogr 1999; 12: 272-274.17. Thanigaraj S, Perez JE. Diagnosis of cardiac rupture with the use of contrast-enhanced echocardiography. J Am Soc Echocardiogr 2000; 13: 862-865.
18. Moreno R, Zamorano JL, Almería C, et al. Usefulness of contrast agents in the diagnosis of left ventricular pseudo aneurysm after acute myocardial infarction. Eur J Echocardiogr 2002; 3: 111-116.
19. Cheitlin MD, Arnstrong WF, Aurigemma GP, et al. ACC/AHA/ASE 2003. Guideline update for the clinical application of echocardiography. www.asecho.org.
20. Smith LAS, Cowell J, White AC, et al. Contrast agent increases Doppler velocities and improves reproducibility of aortic valve area measurements in patients with aortic stenosis. J Am Soc Echocardiogr 2004; 17: 247-52.
21. Kaul S, Ito H. Microvasculature in acute myocardial ischemia: Part I. Evolving concepts in pathophysiology, diagnosis and treatment. Circulation 2004; 109: 146-149.
22. Kaul S, Ito H. Microvasculature in acute myocardial ischemia: Part II. Evolving concepts in pathophysiology, diagnosis and treatment. Circulation 2004; 109: 310-315.
23. Pérez de Isla L, Rodrigo JL, Almería C, et al. Myocardial contrast echocardiography in coronary artery disease. Eur J Echocardiography 2004 (Suppl 2): S11-S16.
24. Karap O, Lepper W, Vanoverschelde JL et al. Serial evaluation of perfusion defects in patients with a first acute myocardial infarction referred for primary PTCA using intravenous myocardial contrast echocardiography. Eur Heart J 2001; 22: 1485-95.
25. Sabia PJ, Powers ER, Jayaweera AR et al. Functional significance of collateral blood flow in patients with recent acute myocardial infarction. A study using myocardial contrast echocardiography. Circulation 1992; 85: 2080-9.
]]> 26. Sabia PJ, Powers ER, Ragosta M, et al. An association between collateral blood flow and myocardial viability in patients with recent myocardial infarction. N Engl J Med 1992; 327: 1825-31.27. Pérez David EP, García Fernández MA. Assessment of myocardial functional recovery in reperfused AMI: The clinical impact of visual and quantitative analysis in MCE. Eur J Echocardiography 2004 (Suppl. 2): S24-S37.
28. Ito H, Maruyama A, Iwakura K, Takiuchi S, et al. Clinical implications of the «no reflow» phenomenon. A predictor of complications and left ventricular remodeling in reperfused anterior wall myocardial infarction. Circulation 1996; 93: 223-8.
29. Sakuma T, Hayashi Y, Sumi K, Imazu M, et al. Prediction of short- and intermediate-term prognoses of patients with acute myocardial infarction using myocardial contrast echocardiography one day after recanalization. J Am Coll Cardiol 1998; 32: 890-7.
30. Bologneses L, Charraba N, Parodi G, Santero GM, et al. Impact of microvascular dysfunction on left ventricular remodeling and long-term clinical outcome after primary coronary angioplasty for acute myocardial infarction. Circulation 2004; 109: 1121-6.
31. Porter TR, Li S, Ester R, Delignoul U. The clinical implications of no reflow demonstrated with intravenous perfluorocarbon containing microbubbles following restoration of Thrombolysis in Myocardial Infarction (TIMI) 3 flow in patients with acute myocardial infarction. Am J Cardiol 1998; 82: 1173-1177.
32. Wei K, Ragosta M, Thorpe J, et al. Non-invasive quantification of coronary blood flow reserve in humans using myocardial contrast echocardiography. Circulation 2001; 103: 2560-2565.
33. Kaul S, Señor R, Dittrich H et al. Detection of coronary artery disease with myocardial contrast echocardiography: comparison with 99mTe-sestamibi single-photon emission computed tomography. Circulation 1997; 96: 785-92.
34. Simón S, Zoghbi WA, Xie F, et al. Real-time assessment of myocardial perfusion and wall motion during bicycle and treadmill exercise echocardiography: Comparison with single photon emission computed tomography. J Am Coll Cardiol 2001; 37: 741-7.
35. De Filippi CR, Wilet DL, Irani WN, et al. Comparison of myocardial contrast echocardiography and low-dose dobutamine stress echocardiography in predicting recovery of left ventricular function after coronary revascularization in chronic ischemic heart disease. Circulation 1995; 92: 2863-8.
]]> 36. Nagueh SF, Vaduganathan P, Ali N, et al. Identification of hibernating myocardium: comparative accuracy of myocardial contrast echocardiography, rest-redistribution thallium-201 tomography and dobutamine echocardiography. J Am Coll Cardiol 1997; 29: 985-93.37. Ito H, Tomooka T, Saka N, et al. Lack of myocardial perfusion immediately alter successful thrombolysis. A predictor of poor recovery of left ventricular function in anterior myocardial infarction. Circulation 1992; 85: 2080-9.
38. Simon S, Frangogiannis NG, Aggeli CJ, et al. Microvascular structural correlates of myocardial contrast echocardiography in patients with coronary artery disease and left ventricular dysfunction. Implications for the assessment of myocardial hibernation. Circulation 2002; 106; 950-6.
39. Galiuto L. Iliceto S. Myocardial contrast echocardiography in the evaluation of viable myocardium alter acute myocardial infarction. Am J Cardiol 1998; 81: 29G-32G.
40. Senior R, Swinburn J, Lahiri A. Enhanced prediction of myocardial viability by contrast echocardiography in dobutamine nonresponsive myocardium early after acute myocardial infarction. Circulation 2001; 104: 11-333.
41. Sigwart U. Non-surgical myocardial reduction for hypertrophic obstructive cardiomiopathy. Lancet 1995; 346: 211-4.
42. Lakkis NM, Nagueh SF, Duna JK, et al. Nonsurgical septal reduction therapy for hypertrophic obstructive cardiomyopathy: one-year follow-up. J Am Coll Cardiol 2000; 36: 852-5.
43. Nagueh SF, Lakkis NM, He ZX, et al. Role of myocardial contrast echocardiography during nonsurgical septal reduction therapy for hypertrophic obstructive cardiomyopathy. J Am Coll Cardiol 1998; 32: 225-9.
44. Korcarz CE, Stein JH. Noninvasive assessment of coronary flow reserve by echocardiography: technical considerations. J Am Soc Echocardiogr 2004; 17: 704-707.
45. Takeuchi M, Ogawa K, Wake R, et al. Measurement of coronary flow velocity reserve in the posterior descending coronary artery by contrast-enhanced transthoracic Doppler echocardiography. J Am Soc Echocardiogr 2004; 17: 21-7.
]]> 46. Dokainish H, Zoghbi WA, Lakkis NM, et al. Optimal noninvasive assessment of left ventricular filling pressures. A comparison of tissue Doppler echocardiography and B-type natriuretic peptide in patients with pulmonary artery catheters. Circulation 2004; 109: 2432-2439.47. Makaryus AN, Zubrow ME, Gillam LD, et al. Contrast echocardiography improves the diagnostic yield of transthoracic studies performed in the intensive care setting by novice sonographers. J Am Soc Echocardiogr 2005; 18: 475-80.
48. Reilly JP, Tunick PA, Timmermans RJ, et al. Contrast echocardiography clarifies uninterpretable wall motion in intensive care unit patients. J Am Coll Cardiol 2000; 35: 485-90.
49. Kornbluth M, Liang DH, Brown P, Gessford E, et al. Contrast echocardiography is superior to tissue harmonics for assessment of left ventricular function in mechanically ventilated patients. Am Heart J 2000; 140: 291-6.
50. Yong Y, Wu D, Fernández V, et al. Diagnostic accuracy and cost-effectiveness of contrast echocardiography on evaluation of cardiac function in technically very difficult patients in the intensive care unit. Am J Cardiol 2002; 89: 711-8.
51. Hundley WG, Kizilbash AM, Afridi I, et al. Effect of contrast enhancement on transthoracic echocardiographic assessment of left ventricular regional wall motion. Am J Cardiol 1999; 84: 1365-8.
52. Cosyns B, EJ Haddad P, Lignian H, et al. Contrast harmonic imaging improves the evaluation of left ventricular function in ventilated patients: comparison with transesophageal echocardiography. Eur J Echocardiogr 2004; 5: 118-22.
53. Yu EHC, Sloggett CE, Iwanochko RM, et al. Feasibility and accuracy of left ventricular volume and ejection fraction determination by fundamental, tissue harmonic, and intravenous contrast imaging in difficult-to-image patients. J Am Soc Echocardiogr 2000; 13: 216-24.
54. Costa JM, Tsutsui JM, Nozawa E et al. Contrast echocardiography can save nondiagnostic exams in mechanically ventilated patients. Echocardiography 2005; 22: 389-94.
55. Shoemaker WC. Use and abuse of the balloon tip pulmonary artery (Swan-Ganz) catheter: are patients getting their money’s worth? Critical Care Medicine 1990; 18: 1294-6.
]]>