Predicción de las curvas de ruptura para la remoción de plomo (II) en disolución acuosa sobre carbón activado en una columna empacada
Prediction of breakthrough curves for the removal of lead (II) in aqueous solution onto activated carbon in a packed column
Valencia Ríos J. S.*1, Castellar Ortega G. C.2
1Laboratorio de Catálisis Heterogénea. Facultad de Ciencias. Universidad Nacional de Colombia. Carrera 30 No. 45-03, Edificio 451, Departamento de Química. Bogotá, D. C., Colombia.
*Autor de correspondencia: teléfono: 57 + 1 + 3165000, correo electrónico: jsvalenciar@unal.edu.co. (J. Valencia)
]]> 2Grupo de Investigación en Química Ambiental. Universidad Autónoma del Caribe. Calle 90 No. 46-112, Bloque H, Centro de Investigaciones. Barranquilla, Colombia.
(Recibido el 23 de abril de 2012. Aceptado el 12 de febrero de 2013)
Resumen
La remoción de iones Pb(II) a partir de una disolución acuosa sobre carbón activado granular se investigó a 27°C bajo condiciones dinámicas en un lecho empacado. En este trabajo se evaluó el efecto de la altura del lecho adsorbente (1-10 cm), el flujo volumétrico (1-5 cm3 min-1) y la concentración inicial (9,8 y 24,9 mg dm-3), sobre el tiempo de ruptura y la capacidad de adsorción, a un pH inicial de 4,0. Los resultados muestran que el rendimiento de la columna mejora cuando se incrementa la altura del lecho de carbón activado y disminuye el flujo volumétrico y la concentración inicial. Los datos experimentales de las curvas de ruptura se ajustaron a los modelos BDST (Bed Depth Service Time), Clark y Wolborska. El modelo BDST proporciona el mejor ajuste para describir el comportamiento dinámico en todas las condiciones de operación estudiadas. El modelo de Clark para relaciones de C/Co entre 0,05 y 0,5 y el modelo de Wolborska para C/Co < 0,2 describen de manera satisfactoria el rendimiento de la columna.
Palabras clave: Carbón activado, plomo, isotermas de adsorción, columna de lecho fijo, curvas de ruptura
Abstract
The removal of ions Pb(II) from an aqueous solution of granular activated carbon was investigated at 27°C under dynamic conditions in a packed bed. This study evaluated the effect of the adsorbent bed height (1-10 cm), the volumetric flow (1-5 cm3 min-1) and the initial concentration (9,8 and 24,9 mg dm-3), on the breakthrough time and the adsorption capacity at an initial pH of 4. The results show that the improved performance of the column increases when the height of the bed of activated carbon increases decreasing the volumetric flow and the initial concentration. The experimental data of breakthrough curves were fitted to BDST (Bed Depth Service Time) models, Clark and Wolborska. BDST model provides the best fit to describe the dynamic behavior at all operating conditions studied. Clark model for C/Co relations between 0,05 and 0,5 and Wolborska model for C/Co< 0,2 satisfactorily describe the performance of the column.
]]> Keywords: Activated carbon, lead, adsorption isotherms, fixed bed column, breakthrough curves
Introducción
La importancia del control de la contaminación por metales pesados ha aumentado perceptiblemente en las últimas décadas debido a su alta toxicidad e impacto en la salud humana y el ambiente. Ante ello, se hacen enormes esfuerzos en la disminución de la concentración de metales pesados en las aguas residuales de los efluentes en razón de obligaciones éticas así como para satisfacer los niveles rigurosamente bajos permitidos en la descarga, tal como se ha fijado por los controles de contaminación y las autoridades reguladoras en varios países. Uno de los metales, entre la lista de aquellos potencialmente tóxicos, es el plomo [1].
La presencia de plomo en el agua potable incluso a bajas concentraciones puede causar enfermedades tales como anemia, hepatitis y síndrome nefrótico [2]. El plomo es no biodegradable y puede acumularse en los tejidos vivos, con lo que se concentra en toda la cadena alimentaria y puede ser fácilmente absorbido por el cuerpo humano [3]. Incluso en cantidades pequeñas puede causar daños fisiológicos o neurológicos graves. Es en general un veneno metabólico y un inhibidor de enzimas, también causa retardo mental y daño cerebral semipermanente en niños pequeños [4].
Las industrias que participan en el procesamiento de baterías ácidas de plomo, pulpa de papel, petroquímicas, refinerías, impresión, pigmentos, material fotográfico, fabricación de explosivos, cerámica, vidrio, pintura, la galvanoplastia, el recubrimiento de metales y la manufactura de tetraetilo de plomo, son la mayor fuente de contaminación con plomo [4].
Existen distintas alternativas para tratar el problema del plomo en los efluentes acuosos como son el ajuste del pH con hidróxidos, la coagulación- sedimentación, la ósmosis inversa, el intercambio iónico y, por supuesto, la remoción con adsorbentes, siendo esta una práctica muy extendida, ya sea como estrategia de control o como parte de un conjunto de actividades de remediación del daño ambiental causado por tales sustancias.
El estudio de la capacidad de adsorción del carbón activado, frente a numerosos adsorbibles orgánicos e inorgánicos, presentes en medio acuoso, tiene gran interés científico y tecnológico. En primer lugar, el carbón activado es un sólido poroso versátil, relativamente estable, con alta área superficial y con una estructura de microporos que no constituyen marcadas barreras de difusión aun bajo condiciones granulares compactas [5]; en segundo lugar, el carbón activado es un material renovable en la medida en que se obtiene a partir de materias primas vegetales (residuos agrícolas, madera, algas, semillas, cortezas), hulla, lignitos, turba y residuos poliméricos (cauchos, plásticos, textiles); finalmente, las estructuras tipo grafeno del carbón activado poseen grupos funcionales, que en virtud del método de activación o del tratamiento químico (oxidativo o reductivo) confieren al adsorbente características fisicoquímicas excepcionales que luego afectan los mecanismos de adsorción [6 - 8].
Los estudios de adsorción en disolución mediante experimentos por lotes (discontinuos) proporcionan una medida de la eficacia de la adsorción en la eliminación de adsorbibles específicos, así como la capacidad máxima de adsorción. Tales experimentos consisten en colocar una cantidad determinada de adsorbente en contacto con la disolución que contiene la sustancia que se va a remover, manteniéndola en suspensión mediante agitación el tiempo necesario para alcanzar el equilibrio. Los estudios de adsorción en una columna de lecho fijo, a diferencia de los experimentos por lotes, no funcionan bajo condiciones de equilibrio debido a que continuamente ingresa a la columna una disolución de alimentación, donde se establece un proceso de transferencia de masa permanente entre una fase móvil que contiene el adsorbible y la fase sólida del lecho adsorbente. Los procesos industriales generalmente se trabajan bajo condiciones continuas, por lo tanto este tipo de estudios proporciona la aplicación más práctica en el tratamiento de aguas residuales.
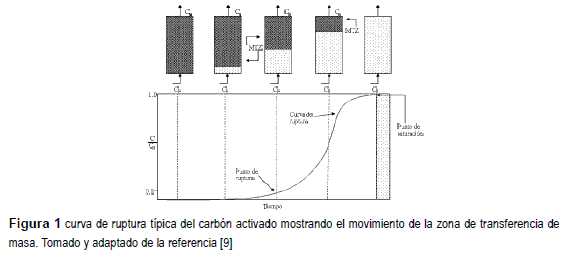
]]> En la figura 1 se muestra el esquema de una columna empacada con un material adsorbente en contacto con un líquido que contiene un soluto (adsorbible) de concentración Co. Inicialmente la parte inferior del adsorbente remueve rápidamente el soluto, así que el fluido que sale de la columna está prácticamente libre de adsorbible. Como el volumen de líquido que atraviesa la columna aumenta, la zona de transferencia de masa (MTZ) comienza a desplazarse y la concentración del adsorbible a la salida aumenta con el tiempo. Se denomina punto de ruptura (qb) al valor máximo en la concentración del adsorbible que se puede permitir a la salida de la columna, y al tiempo empleado para alcanzar esta concentración específica se le llama tiempo de ruptura (tb) para cada una de las condiciones de operación de la columna. La curva que resulta de graficar la relación C/Co en función del tiempo se conoce como curva de ruptura. En este estudio el criterio de "tiempo de ruptura" se adopta como el lapso que transcurre cuando la concentración del adsorbible llegue al 10% de la concentración inicial. Cuando la zona de transferencia de masa sale de la columna, el lecho está completamente saturado y la concentración a la salida es la misma de la entrada [9].La cantidad de soluto adsorbido por gramo de adsorbente en el punto de ruptura, qb (mg g-1) puede obtenerse a partir de la siguiente ecuación.
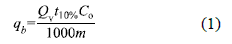
donde t10% es el tiempo de servicio (min) obtenido cuando la concentración de soluto a la salida de la columna es el 10% de la concentración inicial o de entrada, Co es la concentración inicial o de entrada a la columna (mg dm-3), Qv es el flujo volumétrico (cm3 min-1), m es la masa de adsorbente [9] y el valor de 1000 corresponde a un factor de conversión. El criterio más importante en el diseño de una columna de adsorción es la predicción de la curva de ruptura o la forma del frente de onda de adsorción, lo cual determina la longitud del lecho, la vida útil y su tiempo de regeneración.
Esta investigación tuvo como objeto estudiar el efecto de varias condiciones experimentales como: la concentración de alimentación (Co), el flujo volumétrico (Qv) y la altura del lecho (Z), sobre la capacidad de adsorción en columna, manteniendo la temperatura y pH constantes, para la remoción de iones plomo sobre carbón activado granular. De igual manera, los resultados obtenidos se compararon con varios modelos de predicción del tiempo de servicio de la columna. Algunos de estos modelos se discuten a continuación.
Modelo del tiempo de servicio de la altura de un lecho (BDST) [10]. Este modelo supone que la difusión intraparticular y la resistencia de masa externa son insignificantes y que la cinética de adsorción está controlada por la reacción superficial entre el soluto en la disolución y el adsorbente que no ha sido usado [10]. La ecuación inicial propuesta por Bohart y Adams está dada por la expresión:
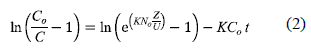
En esta relación 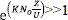 , por lo tanto
, por lo tanto 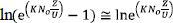 ; esta es la razón por la cual Hutchins [11] propuso la siguiente relación lineal entre la altura del lecho de la columna (Z) y el tiempo de servicio (t):
; esta es la razón por la cual Hutchins [11] propuso la siguiente relación lineal entre la altura del lecho de la columna (Z) y el tiempo de servicio (t):
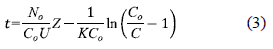
La ecuación 3 se conoce con el nombre de tiempo de servicio de una altura de lecho (BDST) y representa una línea recta que puede expresarse de una manera simplificada como:

donde

y
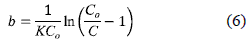
La capacidad dinámica del lecho No, puede evaluarse a partir de la pendiente de la gráfica (a) y la constante de velocidad de adsorción, K puede calcularse a partir de la ordenada al origen (b).
Modelo de Clark [12]. Clark utilizó el coeficiente de transferencia de masa en combinación con la isoterma de Freundlich para definir una nueva relación para la curva de ruptura:
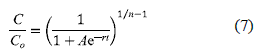

Graficando ln[(Co/C)n-1 - 1] contra t, los valores de r y A pueden determinarse a partir de la pendiente y la ordenada al origen de la línea recta [13].
Modelo de Wolborska [14]. Wolborska deduce la siguiente relación para describir la distribución de la concentración en un lecho fijo, para el rango de baja concentración de la curva de ruptura,
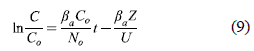
donde βα es el coeficiente cinético de transferencia de masa externo (min-1) y los otros símbolos tienen su significado habitual. Los valores de βαy No pueden determinarse a partir de la gráfica de ln (C/Co) en función de t para un Z y Qv determinados.
Metodología experimental
Adsorbible
Todos los reactivos usados en la preparación de las disoluciones fueron de grado analítico. La disolución "stock" de plomo (1.000 mg dm-3) se preparó disolviendo la cantidad requerida de Pb(NO3)2 en agua desionizada. A partir de esta disolución se hicieron diluciones a 9,8 y 24,9 mg dm-3, ajustándole el pH a un valor de 4,0 ± 0,2 con ácido nítrico diluido con el objeto de garantizar que la especie química adsorbida fuesen iones Pb(II).
]]> AdsorbenteSe seleccionó un carbón activado granular (GAC) comercial marca Norit®, empleado industrialmente en el tratamiento de aguas residuales para la remoción de sustancias orgánicas y metales pesados. Previo a su uso el adsorbente se lavó con agua destilada y luego se secó a 100°C por 12 horas. Luego se utilizó sin tratamientos posteriores.
Caracterización del carbón activado
La evaluación de las características texturales del carbón activado, se realizó a partir de isotermas de adsorción-desorción de nitrógeno a 77 K. Para tal efecto, se utilizó un sortómetro Micromeritics Gemini III 2375, empleando 0,1207 g de muestra. Las isotermas se tomaron con ochenta (80) puntos de adsorción y veinte (20) puntos de desorción. La desgasificación del adsorbente tuvo lugar a 250°C. El área superficial se obtuvo mediante el modelo de BET; de igual manera, el volumen total de poro. El contenido de humedad, materia volátil, cenizas y carbono fijo, se determinaron de acuerdo con la metodología establecida en la norma ASTM D 3.173-75. El contenido de carbono, nitrógeno, hidrógeno y oxígeno (por diferencia) se determinaron de acuerdo con la metodología establecida en la norma ASTM 5.373, y azufre total por la norma ASTM D 4.239 (método B). En gran medida estos análisis se realizaron en el laboratorio de Investigaciones en Combustibles y Energía de la Universidad Nacional de Colombia y otros fueron realizados por laboratorios externos.
Estudio dinámico en columna
El arreglo experimental utilizado se muestra en la figura 2. Consistió en un depósito de almacenamiento que contiene la disolución de Pb(NO3)2 que alimentó a la columna de vidrio Pyrex® de 0,9 cm de diámetro interno empacada con carbón activado granular; el área de flujo se mantuvo constante para todas las condiciones de operación de la columna. Para un caudal determinado (1, 3 y 5 cm3 min-1), a diferentes alturas del lecho (1, 5 y 10 cm) y concentraciones iniciales de Pb(II) (9,8 y 24,9 mg dm-3); en intervalos regulares de tiempo, usando una jeringa con una aguja hipodérmica, se tomaron alícuotas del fluido a la salida del lecho de carbón activado, con el propósito de determinar el contenido de plomo en el efluente. La medida de la concentración de Pb(II) se realizó mediante un espectrofotómetro de absorción atómica (AA Spectrometer, marca Thermo) a 217 nm. La disolución después de pasar por la columna se descargó en un tanque colector. Los flujos volumétricos se regularon con la ayuda de una bomba peristáltica.
Resultados y discusión
Caracterización del carbón activado
]]> Las propiedades fisicoquímicas tales como área superficial específica, volumen total de poro, material volátil, cenizas, contenido de carbono y otras propiedades se muestran en la tabla 1.Aunque el área superficial del carbón activado empleado en este estudio puede considerarse baja con relación a las características genéricas de este tipo de adsorbentes, la capacidad de adsorción de los materiales no solo puede interpretarse en términos de sus propiedades físicas, sino que también influye su química de superficie [15], el cual juega un papel importante en su rendimiento como adsorbente [16]. La influencia de la química superficial de los carbones activados en las propiedades de adsorción es objeto de investigación debido a que los grupos funcionales presentes en la superficie le confieren selectividad [6, 8, 17]. La presencia de heteroátomos principalmente oxígeno (tabla 1), que forma grupos funcionales orgánicos tales como ácidos carboxilicos (también en la forma de su anhídrido cíclico), lactonas, lactoles y grupos hidroxílicos de carácter fenólico, son los responsables de las propiedades ácidas del carbón activado [18].
Estos grupos funcionales específicos son esenciales en la adsorción de metales pesados debido a su marcada cualidad (como ligandos) en la formación de entidades de coordinación [19, 20]. Pero de otra parte, la capacidad de adsorción del carbón activado también recibe contribuciones de la adsorción física, que es dependiente del área superficial, de la presencia de microporosidad, de fenómenos de oclusión y de procesos de intercambio iónico en los cuales la naturaleza de la especie de plomo juega un papel importante [21]. En términos de la teoría ácido base, el Pb(II) es considerado un ácido blando de Lewis que puede unirse con grupos funcionales que contienen azufre (tabla 1), que se comportan como bases blandas de Lewis. Por lo tanto, los grupos funcionales S=O, que están presentes en el adsorbente, muestran una alta coordinación con metales pesados como el plomo [22]. De otra parte, no existe mucha evidencia sobre el efecto, en la capacidad de adsorción, del contenido de cenizas del carbón; en perspectiva, los efectos de estos componentes dependen de la carga, de la especiación y de las características de textura de los óxidos que configuran las cenizas del carbón. La posible acción de la humedad es un aspecto más difícil de evaluar como quiera que el adsorbente se carga a la columna bajo condiciones anhidras; sin embargo, existen esfuerzos y expectativas, por parte del grupo de trabajo, de evaluar mediante métodos isopiésticos las correspondientes actividades de agua y su posible incidencia en el proceso de adsorción bajo condiciones dinámicas.
Estudio dinámico en columna
Capacidad de adsorción en columna
Para este estudio la columna empacada con carbón activado granular estará agotada cuando la concentración del efluente alcance un 10% del valor de la concentración inicial, es decir, C/Co= 0,1. La capacidad de adsorción de Pb(II) de la columna expresada en mg de Pb(II) removido por gramo de adsorbente, se calculó empleando la ecuación 1. Un resumen de todos los cálculos realizados a diferentes condiciones de operación como la altura del lecho, el flujo volumétrico y la concentración de alimentación, se muestra en la tabla 2.
A partir de un estudio por lotes realizado por el grupo de trabajo empleando el mismo adsorbente, y bajo las mismas condiciones de temperatura y pH, se obtuvo que la capacidad máxima de adsorción de iones Pb(II) fue de 35,7 mg g-1. Comparando este resultado con el valor de mayor capacidad reportado por el estudio en columna (0,50 mg g-1), a una altura del lecho de 10 cm, flujo volumétrico de 1 cm3 min-1 y concentración inicial de 24,9 mg dm-3; se observa una reducción significativa en la capacidad de adsorción del CAG. Igual comportamiento ha sido reportado por otros autores [1, 9, 23, 24].
En un proceso por lote el carbón activado permanece más tiempo en contacto con la disolución, esta situación permite que se alcance una condición de equilibrio; pero además, la agitación permanente proporciona una mejor interacción entre los sitios activos del adsorbente y los iones de Pb(II), lo cual favorece la velocidad de transferencia de masa y, por lo tanto, su retención.
]]> Efecto de la altura del lechoLa remoción de metales en una columna de lecho fijo, depende, entre otros factores, de la cantidad de adsorbente utilizado, o lo que es lo mismo, de la altura de relleno con que se trabaja. Por ello se analizó el efecto que la cantidad de carbón activado (altura del lecho) tiene en el proceso de adsorción de Pb(II), para lo cual se realizaron experimentos con tres cantidades de carbón activado equivalentes a tres alturas, 1, 5 y 10 cm. Los resultados a diferentes condiciones de operación de la columna de muestran en la figura 3.
Para una concentración inicial de 9,8 mg dm-3 y un flujo volumétrico de 1 cm3 min-1 el tiempo de ruptura aumentó desde 4,0 a 130,5 minutos cuando se incrementa la altura de 1 a 10 cm. Un comportamiento similar se registra para otras condiciones de operación estudiadas. Esto indica que, al aumentar la altura del lecho, se incrementa el tiempo de ruptura y, por lo cual, la cantidad de Pb(II) removido.
Cuando la altura del lecho se reduce predomina el fenómeno de dispersión axial en la transferencia de masa, por lo tanto los iones metálicos no tienen suficiente tiempo para difundirse en toda la masa de adsorbente. Por otro lado, al aumentar la altura del lecho también se incrementa el área superficial del adsorbente, disponiéndose de más sitios de unión para la adsorción; en consecuencia, la capacidad de adsorción del lecho en el punto de ruptura se incrementa [9].
Efecto del flujo volumétrico
La figura 4 muestra el comportamiento de la columna cuando se modifica el flujo volumétrico. Para una concentración inicial de 9,8 mg dm-3 y una altura del lecho de 10 cm el tiempo de ruptura cambia de 8,7 a 130,5 minutos cuando el flujo volumétrico varía de 5 a 1 cm3 min-1; una tendencia similar se observa para las otras condiciones de operación de la columna. Esto indica que el tiempo de ruptura y, por ello, la capacidad de adsorción del carbón activado aumenta cuando se disminuye el flujo volumétrico. Igual comportamiento ha sido reportado por otros autores [9, 23, 24, 25].
Desde el punto de vista de operación de la columna los mejores resultados se obtienen a un flujo de 1 cm3 min-1 ya que los iones metálicos tienen suficiente tiempo para difundirse dentro del carbón activado mejorando su capacidad de adsorción.
Efecto de la concentración inicial de Pb(II)
]]> Las curvas de ruptura obtenidas variando la concentración inicial de Pb(II) a diferentes condiciones de proceso se muestran en la figura 5. El tiempo de ruptura para una columna de 10 cm de altura del lecho y un flujo volumétrico de 1 cm3 min-1 fue de 60,4 minutos a una concentración inicial de 24,9 mg dm-3; mientras que, a 9,8 mg dm-3 fue de 130,5 minutos. Un comportamiento similar se observa bajo otras condiciones de operación de la columna. Estos resultados demuestran que un incremento en la concentración inicial modifica la velocidad de adsorción e incrementa la capacidad de adsorción del lecho [9].La fuerza motriz para la adsorción es la diferencia de concentración entre el soluto en el adsorbente y el soluto en la disolución, un gradiente de concentración bajo causa una transporte lento debido a una disminución del coeficiente de difusión, por lo tanto se emplea un tiempo mayor para saturar los sitios activos del carbón activado. El aumento de la concentración inicial ocasiona un incremento en la fuerza motriz del proceso de adsorción, lo cual explica porqué el valor más alto de capacidad de adsorción (0,50 mg g-1) se obtiene a 24,9 mg dm-3, pero el tiempo de ruptura más prolongado se logró a 9,8 mg dm-3.
Estos resultados experimentales han sido ajustados a cada uno de los modelos desarrollados en la introducción con el objeto de describir el comportamiento de la columna y determinar los parámetros cinéticos. A continuación se describe su aplicación y los resultados obtenidos para cada uno de los modelos.
Aplicación de modelos
Modelo BDST
Las figuras 6a y 6b muestran la representación lineal del modelo BDST para la remoción de Pb(II) en un lecho fijo de carbón activado a diferentes relaciones de C/Co (0,1, 0,2, 0,4, y 0,6), concentraciones iniciales de 9,8 y 24,9 mg dm-3, velocidad de flujo lineal de 1,6 cm min-1 (flujo volumétrico de 1,0 cm3 min-1) a las diferentes alturas del lecho estudiadas.
De los valores de la pendiente e intercepto de cada una de las líneas de isoremoción se calcularon los parámetros del modelo; los resultados se muestran en la tabla 3. Se observa un ajuste satisfactorio de los datos experimentales (R2 > 0,98).
]]> Para el tiempo de ruptura escogido (C/Co) = 0,1), Co=24,9 mg dm-3 y U= 1,6 cm min-1, los valores de la capacidad dinámica del lecho y de la constante de velocidad fueron 259 mg dm-3 y 0,016 dm3 min-1 mg-1 respectivamente. Reemplazando estos valores en la ecuación 3 se obtiene la expresión:
De igual manera, reemplazando los valores correspondientes de No y K para las condiciones de proceso Co = 9,8 mg dm-3, U = 1,6 cm min-1, No = 221 mg dm-3 y K = 0,016 dm3 min-1mg-1 se obtiene la ecuación:
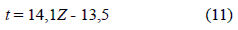
En la tabla 4 se comparan los valores del tiempo de ruptura obtenidos experimentalmente y los calculados a partir de las ecuaciones 10 y 11. El modelo BDST se ajusta muy bien a los resultados experimentales, principalmente cuando aumenta la altura del lecho y disminuye el flujo volumétrico. Bajo estas condiciones el tiempo de residencia de la disolución en la comuna es menor que su tiempo de ruptura permitiendo que la difusión intraparticular y la resistencia de masa externa no sean significativas. La figura 7 muestra las curvas de ruptura experimentales y las obtenidas por el modelo BDST.
Los parámetros No y K (tabla 3) pueden ser utilizados para el diseño de columnas de adsorción con propósitos prácticos. Según el enfoque del modelo estos valores pueden ser ajustados para el diseño de columnas que utilicen condiciones diferentes de velocidad lineal y concentración inicial. En el primero de los casos, solo será suficiente con multiplicar el valor de la pendiente original (α) por la relación entre la velocidad de flujo lineal original (U) y la nueva (Un). Con respecto al valor de la ordenada al origen (b), se asume que no se afecta significativamente por un cambio en la velocidad de flujo y por lo tanto, no es necesario ajustarla. En consecuencia,

donde αn corresponde a la pendiente para un nuevo valor de velocidad lineal (Un).
]]> Y en segundo lugar, es posible predecir la ecuación para una nueva concentración inicial (C*o), ajustando los valores originales, tanto de la pendiente (α) como de la ordenada al origen (b) como se muestra a continuación diferenciándolas con un asterisco: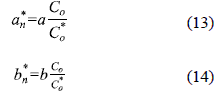
Empleando las ecuaciones 12, 13 y 14 se predijo el tiempo de ruptura para un nuevo flujo lineal y concentración inicial usando las constantes conocidas del modelo BDST; los resultados se muestran en las tablas 5 y 6 para diferentes condiciones de operación de la columna. El tiempo de ruptura calculado a partir del modelo se acerca de manera satisfactoria a los valores obtenidos experimentalmente, cuando aumenta la altura del lecho.
Modelo de Wolborska
Los datos experimentales fueron ajustados a la ecuación 9, para diferentes Z, Qv, Co y valores de C/Co menores que 0,2. Para todas las curvas de ruptura (R2> 0,72). El coeficiente cinético de transferencia de masa (βα) y la capacidad del lecho (No) se determinaron a partir de la pendiente y el intercepto al graficar ln(C/Co) contra t. La tabla 7 muestra los resultados obtenidos junto con el coeficiente de correlación correspondiente (R2) y la figura 8 las curvas de ruptura experimentales y teóricas bajo diferentes condiciones de operación de la columna.
Al incrementar la velocidad de flujo lineal (U) desde 1,6 hasta 7,8 cm min-1 se aumenta la turbulencia al pasar la disolución a través del lecho con carbón activado; ello trae como consecuencia una reducción de la película de la capa límite que rodea a las partículas del adsorbente, incrementando el coeficiente cinético de transferencia de masa (βα), tal como lo muestran los resultados resumidos en la tabla 7. Como era de esperarse, la capacidad máxima de adsorción (No) mejora al aumentar la altura del lecho (Z) y disminuye la velocidad de flujo lineal (U), como lo predice la ecuación 9. Sin embargo, los valores de βα no muestran una tendencia específica con respecto a la variación de Z. Esta situación refleja el efecto solo de la transferencia de masa en la fase líquida y la dispersión axial en los valores del coeficiente cinético [25].
]]> Aunque el modelo de Wolborska proporciona una metodología sencilla en la evaluación de las pruebas de adsorción en columna, su validez está limitada solo a relaciones de C/Co bajas, tal como se establece en los supuestos para la solución del sistema de ecuaciones diferenciales que soportan el modelo [26].Modelo de Clark
Un estudio de equilibrio de adsorción realizado por el equipo de trabajo, muestra que el modelo de isoterma de Freundlich es válido para la remoción de Pb(II) sobre carbón activado granular con una constante de Freundlich de n = 3,125. Este valor se utilizó en el modelo de Clark para calcular los otros parámetros característicos. Los datos experimentales del tiempo de ruptura se ajustan de manera satisfactoria al modelo para relaciones de C/Co entre 0,05 y 0,5 con respecto a Qv, Z y Co. Los valores de r y A se determinaron a partir de la pendiente y la ordenada al origen al graficar ln [(C/Co)n-1 - 1] contra t de acuerdo con la ecuación 8. Los parámetros de la ecuación de Clark y el coeficiente de correlación (R2) para diferentes concentraciones iniciales, flujos volumétricos y alturas del lecho se muestran en la tabla 8.
Cuando la velocidad de flujo lineal (U) aumenta desde 1,6 hasta 7,8 cm min-1 manteniendo constante la concentración inicial y la altura del lecho se observa que el valor de r se incrementa en virtud de su relación con el coeficiente de transferencia de masa externo [25]. Esto es bueno, pero no a expensas de un aumento de la velocidad superficial porque implica que el adsorbente tiene menos tiempo para responder y será menos eficiente la operación, como lo indica la disminución del tiempo de ruptura.
Por otro lado, este modelo se fundamenta en el desarrollo de ecuaciones de transferencia de masa combinadas con el modelo de isoterma de Freundlich [12], aplicado a estudios por lotes donde se alcanza una condición de equilibrio, pero se sabe que una columna empacada no siempre funciona bajo estas condiciones [1].
La figura 9 muestra las curvas de ruptura experimental y teórica obtenidas bajo diferentes condiciones de proceso.
Conclusiones
]]> La metodología experimental desarrollada en esta investigación consistió en determinar la capacidad de adsorción de un carbón activado comercial marca Norit® en la remoción de iones Pb(II) en disolución acuosa bajo condiciones de flujo continuo a diferentes alturas del lecho, flujos volumétricos y concentración inicial con el propósito de examinar el efecto de estas variables de operación sobre el tiempo de ruptura y la capacidad de adsorción. Además, se probaron varios modelos matemáticos en la predicción del tiempo de servicio de la columna. Ante lo anterior, este estudio permite formular las siguientes conclusiones:La máxima capacidad de adsorción de la columna alcanzada fue de 0,50 mg g-1 a una altura del lecho de 10 cm, un flujo volumétrico de 1 cm3 min-1 y una concentración de alimentación de 24,9 mg dm-3.
Las curvas de ruptura obtenidas a diferentes condiciones de operación de la columna muestran que tanto el tiempo de ruptura como la capacidad de adsorción del carbón activado aumentan con un incremento en la altura del lecho, disminuyen cuando el flujo volumétrico aumenta, y el tiempo de ruptura disminuye y la capacidad de adsorción aumenta cuando se incrementa la concentración inicial de iones Pb(II).
Los modelos aplicados dieron buenas aproximaciones al comportamiento experimental, pero el modelo BDST se ajustó muy bien para casi todos los valores de altura, flujo volumétrico y concentración. El modelo de Clark solo se puede aplicar para relaciones de C/Co entre 0,05 y 0,5 y el modelo de Wolborska para valores menores que 0,2.
Agradecimientos
Los autores de este artículo agradecen la colaboración del Laboratorio de Combustibles y Energía de la Universidad Nacional de Colombia, el Laboratorio de Biotecnología de Microalgas de la Universidad del Atlántico y el Laboratorio de Suelos de la Universidad del Magdalena. Los autores declaran que no existe conflicto de intereses que pongan en riesgo la validez de los resultados.
References
1. G. Jyotsna, K. Krishna, R. Chitra, K. Vinod. "Removal of lead (II) by adsorption using treated granular activated carbon: Batch and column studies". J. Hazard. Mater. Vol. 125. 2005. pp. 211-220. [ Links ]
2. L. Waihung, C. Hong, L. Kim, B. Shu. "A comparative investigation on the biosorption of lead by filamentous fungal biomass". Chemosphere. Vol. 39. 1999. pp. 2723-2736. [ Links ]
3. K. Wong, C. Lee, K. Low, M. Haron. "Removal of Cu(II) and Pb(II) by tartaric acid modified rice husk from aqueous solutions". Chemosphere. Vol. 50. 2003. pp 23-28. [ Links ]
4. P. Dwivedi, J. Sahu, C. Mohanty, B. Mohan, B. Meikap. "Column performance of granular activated carbon packed bed for Pb(II) removal". J. Hazard. Mater. Vol. 156. 2008. pp. 596-603. [ Links ]
5. P. Suhas, M. Carrott, R. Carrott. "Lignin-from natural adsorbent to activated carbon: A review". Bioresource Technol. Vol. 98. 2007. pp. 2301-2312. [ Links ]
6. S. Liu, X. Chen, X. Chen, Z. Liu, H. Wang. "Activated carbon with excellent chromium (VI) adsorption performance prepared by acid-base surface modification". J. Hazard. Mater. Vol. 141. 2007. pp. 315-319. [ Links ]
7. L. Wachowski, J. Sobczak, M. Hofman. "Speciation of functional groups formed on the surface of ammoxidised carbonaceous materials by XPS method". Appl. Surf. Sci. Vol. 253. 2007. pp. 4456-4461. [ Links ]
8. J. Díaz, L. Carballo, J. Figueiredo. "Thermal treatments of activated carbon catalysts under N2O". Carbon. Vol. 45. 2007. pp. 212-214. [ Links ]
9. V. Taty, H. Fauduet, C. Porte, Y. Ho. "Removal of lead (II) ions from synthetic and real effluents using immobilized Pinus sylvestris sawdust: Adsorption on a fixed-bed column". J. Hazard. Mater. Vol. B123. 2005. pp. 135-144. [ Links ]
10. G. Bohart, E. Adams. "Some aspects of the behavior of charcoal with respect to chlorine". J. Am. Chem. Soc. Vol. 42. 1920. pp. 523-544. [ Links ]
11. R. Hutchins. "New method simplifies design of activated carbon systems". Am. J. Chem. Eng. Vol. 80. 1973. pp. 133-138. [ Links ]
12. R. Clark. "Evaluating the cost and performance of field-scale granular activated carbon systems". Environ. Sci. Technol. Vol. 21. 1987. pp. 573-580. [ Links ]
13. O. Hamdaoui. "Removal of cooper (II) from aqueous phase by Purolite C100-MB cation exchange resin in fixed bed columns: Modeling". J. Hazard. Mater. Vol. 161. 2009. pp. 737-746. [ Links ]
14. A. Wolborska. "Adsorption on activated carbon of p-nitrophenol form aqueous solution". Water Res. Vol. 23. 1989. pp. 85-91. [ Links ]
15. J. Orfao, A. Silva, J. Pereira, S. Barata, I. Fonseca, P. Faria, M. Pereira. "Adsorption of a reactive dye on chemically modified activated carbons-influence of pH". J. Colloid Interface Sci. Vol. 296. 2006. pp. 480-489. [ Links ]
16. R. Bansal, J. Donnet, F. Stoeckli. Activated Carbon. Ed. Marcel Dekker. New York. 1988. pp. 482. [ Links ]
17. L. Wachowski, J. Sobczak, M. Hoffman. "Speciation of functional groups formed on the surface of ammoxidised carbonaceous materials by XPS method". Appl. Surf. Sci. Vol. 253. 2007. pp. 44564461. [ Links ]
18. A. Contescu, C. Contescu, K. Putyera, J. Schwarz. "Surface acidity of carbons characterized by their continuos pK distribution and Boehm titration". Carbon. Vol. 35. 1997. pp. 83-94. [ Links ]
19. L. Monser, N. Adhoum. "Modified activated carbon for the removal of copper, zinc, chromium and cyanide from wastewater". Sep. Purif. Technol. Vol. 26. 2002. pp. 137-146. [ Links ]
20. Y. Kikuchi, Q. Quian, M. Machida, H. Tatsumoto. "Effect of ZnO loading to activated carbon on Pb(II) adsorption from aqueous solution". Carbon. Vol. 44. 2006. pp. 195-202. [ Links ]
21. G. Castellar, A. García. "Remoción de Pb2+ en disolución acuosa sobre carbón activado en polvo: Estudio por lote". Prospectiva. Vol. 9. 2011. pp. 59-68. [ Links ]
22. M. Madhava, G. Chandra, K. Seshaiah, N. Choudary, M. Wang. "Activated carbon from Ceiba pentandra hulls, an agricultural waste, as an adsorbent in the removal of lead and zinc from aqueous solutions". Waste Manage. Vol. 28. 2008. pp. 849-858. [ Links ]
23. M. Mondal. "Removal of Pb(II) ions from aqueous solution using activated tea waste: Adsorption on a fixed-bed column". J. Environ. Manage. Vol. 90. 2009. pp. 3266-3271. [ Links ]
24. C. Dwivedi, J. Sahu, C. Mohanty, B. Raj. Mohan, B. Meikap. "Column performance of granular activated carbon packed bed for Pb(II) removal". J. Hazard. Mater. Vol. 156. 2008. pp. 596-603. [ Links ]
25. V. Srivastava, B. Prasad, I. Mishra, I. Mall, M. Swamy. "Prediction of breakthrough curves for sorptive removal of phenol by bagasse fly ash packed bed". Ind. Eng. Chem. Res. Vol. 47. 2008. pp. 1603-1613. [ Links ]
26. W. Zhang, L. Dong, H. Yan, H. Li, Z. Jiang, X. Kan, H. Yang, A. Li, R. Cheng. "Removal of methylene blue from aqueous solutions by straw based adsorbent in a fixed-bed column". Chem. Eng. J. Vol. 173. 2011. pp. 429-436. [ Links ]
]]>