Therapeutic approach to hepatitis for virus C
Víctor Idrovo C. MD. (1)
(1) Gastroenterólogo, Hepatólogo clínico y de trasplante hepático. Hospital Universitario Fundación Santa Fé, Bogotá, Colombia.
Fecha recibido: 02-12-04 / Fecha aceptado: 22-02-06
RESUMEN
La hepatitis C (VHC) es producida por un virus RNA perteneciente a la familia de los flavivirus, y fue identificado en 1989. Es responsable del desarrollo de hepatitis aguda la cual se autolimita en un 20 a 30% de casos, pero hasta en 70 a 80% evoluciona a infección crónica, con riesgo de cirrosis y hepatocarcinoma después de varias décadas de infección. La progresión a cirrosis es frecuentemente silenciosa hasta que se presentan las complicaciones de una enfermedad hepática avanzada, como la hipertensión portal, la insuficiencia hepática y el hepatocarcinoma. Las alternativas terapéuticas contra la hepatitis C han mejorado significativamente en los últimos años, lográndose respuestas virológicas sostenidas cercanas al 60% si se logra una adecuada adherencia al tratamiento. A continuación se presenta una revisión general y concisa sobre la hepatitis C con el fin de entender mejor la epidemiología, historia natural, diagnóstico, pronóstico y tratamiento de esta infección.
Palabras Clave
Hepatitis, PCR (reacción en cadena de polimerasa) cualitativa, carga viral, genotipo, biopsia hepática, respuesta virológica sostenida, interferón pegilado, ribavirina, adherencia.
ABSTRACT
]]> Hepatitis C (HCV) is caused by a small RNA virus that belongs to the flaviviridae family that was identified in 1989. HCV produces acute hepatitis, which is self-limited in approximately 20 to 30% of cases. However, it will progress to chronic disease in 70 to 80%, with the potential risk of developing cirrhosis and hepatocellular carcinoma (HCC) after several decades of infection. Progression to cirrhosis is usually silent until complications of advanced disease develop, such as portal hypertension, liver insufficiency, and HCC. Treatment options for HCV have improved significantly in recent years, with sustained virologic responses that reach up to 60% if optimize adherence to therapy is achieved. The following article about HCV is a general and concise review about the epidemiology, natural history, diagnosis, prognosis, and treatment options for this viral infection.Key Words
Hepatitis, qualitative PCR (polimerase chain reaction), viral load, genotype, liver biopsy, sustained virologic response, pegylated interferon, ribavirin, adherence.
PROBLEMÁTICA DE LA HEPATITIS C
Proyecciones hasta el 2008 muestran que las complicaciones derivadas de la hepatitis crónica por VHC irán en aumento así:
1. Necesidad de trasplante: 528%
2. Descompensación hepática: 279%
3. Muertes asociadas al hígado: 223%
4. Hepatocarcinoma: 68%
]]> 5. Cirrosis: 61%.HISTORIA NATURAL DEL VHC
La historia natural de la enfermedad demuestra que del 100% de los infectados agudamente, un 15 a 30% erradican la infección espontáneamente, mientras un 70 a 85% desarrollan infección crónica (más de seis meses). De estos infectados crónicos, sólo un 25% desarrollan infección severa con riesgo de cirrosis con descompensación hepática y riesgo de desarrollo de hepatocarcinoma, por lo cual generalmente fallecen.
Se han identificado factores de riesgo que favorecen una progresión más rápida de la hepatitis por VHC, como son:
1. Edad mayor de 40 años
2. Sexo masculino
3. Ingesta de licor, no importa la cantidad
4. Coinfección con VIH
5. Sobrecarga de hierro
6. Presencia de esteatosis.
]]> En quiénes se justifica investigar VHC (Grupos de riesgo)1. Transfundidos o receptores de trasplante de órganos antes de 1993
2. Drogadictos intravenosos así haya sido esporádicamente
3. Niños de madres VHC positivas
4. Parejas de infectados por VHC
5. Accidentes en trabajadores de salud
6. Infección por VIH, hemofílicos, pacientes en hemodiálisis
7. Elevaciones inexplicables de aminotransferasas.
Por qué se justifica tratar la hepatitis por VHC
La hepatitis por VHC tiene indicaciones muy claras que justifican el tratamiento, ya que es una de las mayores causas de morbimortalidad, y actualmente es la indicación más importante de trasplante hepático en el mundo.
]]> Tratada tempranamente se puede evitar la progresión a cirrosis con descompensación hepática y el desarrollo de hepatocarcinoma. Además, se puede mejorar la calidad de vida de estos individuos que sin duda está disminuida por esta enfermedad.Qué pacientes con VHC deben ser tratados
Sin duda, todo paciente con hepatitis crónica por VHC debe ser investigado para definir si debe recibir tratamiento. Se debe tener en cuenta la disminución en la calidad de vida del infectado, así como la presencia de alteraciones orgánicas de tipo hepático o extrahepático que ameriten un tratamiento. No obstante, el mejor determinante de la necesidad de tratamiento es el estudio histopatológico mediante biopsia hepática. A mayor grado de actividad inflamatoria y en especial a mayor estadio de fibrosis, mayor será la indicación de tratamiento. Es así como, mediante la clasificación de METAVIR, se puede definir qué pacientes pueden permanecer en observación porque su hepatitis es leve y no comprometerá sus vidas, o cuales están en riesgo de progresión de la enfermedad y deben ser tratados. La clasificación de METAVIR se divide en:
1. Normal
2. Fibrosis portal
3. Fibrosis con septos escasos
4. Fibrosis con septos numerosos
5. Cirrosis.
Normalmente, individuos con METAVIR 0 y 1 no deben ser tratados, mientras los METAVIR 2, 3 y 4 (cirróticos compensados) deben recibir tratamiento. Cirróticos descompensados no deben ser tratados y deben ser evaluados para trasplante hepático.
Cuáles son los predictores de respuesta al tratamiento más importantes
]]> Debido a que la respuesta al tratamiento para hepatitis C es limitada se han identificado factores predictores de respuesta al tratamiento que ayudan a predecir quiénes se van a beneficiar más del mismo y pueden lograr una curación definitiva. En general, los dos predictores de respuesta al tratamiento más importante en su orden son:1. El genotipo
2. La carga viral.
El VHC tiene una diversidad genómica que permite subclasificarlo en 6 genotipos y varios subtipos mediante técnicas de biología molecular. En Latinoamérica, al igual que en USA y en Europa predomina el genotipo 1, seguido de los genotipos 2 y 3. Los infectados con el genotipo 1 son más resistentes al tratamiento, y fallan más a la terapia actual, la cual se debe dar por un período de 48 semanas. No es así en los genotipos 2 y 3, los cuales tienen respuestas muy favorables al tratamiento, incluso por un período de sólo 24 semanas. En Colombia y en Latinoamérica en general, predomina el genotipo 1 hasta en un 70% de los infectados.
La carga viral antes del tratamiento, determinada por técnicas de biología molecular (ej. PCR cuantitativo), es otro predictor importante de respuesta al tratamiento. Si la carga viral está muy elevada (más de 800,000 UI/ml mediante técnica de PCR amplicor monitor), la respuesta al tratamiento va a ser menor que si el nivel es inferior a 800,000 UI/ml. También, la determinación de la carga viral a la semana 12 de tratamiento, para evaluar la respuesta viral temprana, será un predictor de respuesta, específicamente en pacientes con genotipo 1. Un descenso a la semana 12 mayor de 2 log (ej. antes del tratamiento tenía 800,000 UI/ml, y a la semana 12 descendió a menos de 8,000 UI/ml), indica respuesta favorable en genotipo 1 para continuar el tratamiento hasta la semana 48. Si el descenso no es mayor de 2 log en genotipo 1, se puede descontinuar el tratamiento. En pacientes con genotipos 2 ó 3, la respuesta viral temprana a la semana 12 no es importante, ya que independiente de ésta, la mayoría responderá al tratamiento.
Evolución histórica en el tratamiento para VHC
En las últimas dos décadas se ha avanzado bastante en el tratamiento de la hepatitis por VHC. Prácticamente la respuesta al tratamiento se ha incrementado desde un 16% de los tratados en los inicios del tratamiento con monoterapia con interferón standard no pegilado, a un 40% con la terapia combinada de interferón estándar y ribavirina, y actualmente respuestas hasta cerca de un 60 a 70% con la terapia combinada de interferón alfa pegilado y ribavirina.
Tratamiento actual para la Hepatitis por VHC
Actualmente el tratamiento consiste en la combinación de un inmunomodulador (Interferón pegilado alfa) y un antiviral (ribavirina).
El interferón pegilado alfa consiste en una molécula de interferón estándar que se venía usando tradicionalmente en el tratamiento de la hepatitis C, adherido a una molécula de polietilenglicol (PEG). Esta molécula de PEG favorece un aumento de la vida media del interferón mediante el retardo de la depuración del medicamento y mediante la protección que le confiere al interferón contra enzimas proteolíticas endógenas. De esta manera, el interferón pegilado mantendrá una presión constante sobre el virus, mejorando su efectividad.
]]> Existen dos interferones pegilados aprobados para su uso en hepatitis por VHC:1. Interferón pegilado alfa 2a que se usa en dosis única de 180 microgramos semanales por vía subcutánea sin necesidad de ajuste al peso.
2. Interferón pegilado alfa 2b que se usa en dosis ajustada al peso, 1,5 microgramos por kilo de peso, semanal por vía subcutánea. El perfil de seguridad, los efectos secundarios y la efectividad son prácticamente idénticos, aunque aún no se han hecho estudios cabeza a cabeza para comparar los dos medicamentos.
La ribavirina se formula a una dosis aproximada de 1000 a 1200 mg diarios por vía oral en genotipo 1, y 800 mg diarios en genotipos 2 y 3, también teniendo un buen perfil de seguridad y una efectividad significativa al darla combinada con el interferón pegilado. La ribavirina como monoterapia no es útil en el tratamiento de la hepatitis por VHC.
Se ha establecido la terapia combinada de un interferón pegilado más ribavirina por un período de 48 semanas para genotipo 1 y de 24 semanas para genotipos 2 y 3. Con este esquema se logran obtener respuestas sostenidas cercanas a 50% en genotipo 1 y hasta un 80% en genotipos 2 y 3. Se entiende por respuesta sostenida la no detección de viremia por técnica cualitativa de biología molecular (PCR menor de 50 UI/ml) 24 semanas después de finalizado el tratamiento. Este resultado es indicativo de curación de la infección por VHC.
Es importante anotar que aproximadamente un 10% de los pacientes no toleran el tratamiento o presentan efectos secundarios y por lo tanto lo descontinúan prematuramente sin obtener la respuesta esperada. Para los interferones pegilados, los principales efectos adversos que llevan a no completar el tratamiento son la neutropenia, la trombocitopenia, la depresión, o la exacerbación de fenómenos autoinmunes. Para la ribavirina, la anemia constituye el principal efecto secundario que puede limitar la terapia completa.
Si se logra una buena adherencia al tratamiento (organizar grupos de apoyo permanente), y se manejan los efectos adversos (ej. estimulantes de granulocitos, eritropoyetina, antidepresivos, manejo de hipotiroidismo, etc.), se podrá tener una mayor respuesta sostenida y habrá mayor posibilidad de curación para estos pacientes, especialmente en los que tienen genotipo 1. La meta es cumplir al menos 80% del tiempo de tratamiento programado y 80% de las dosis programadas (regla 80-80).
Grupos especiales de infección por VHC
1. Hepatitis C aguda: Rara vez se diagnostica porque usualmente es asintomática. No obstante, si se detecta un caso agudo, la monoterapia con interferón es excelente, con una respuesta sostenida que se acerca a un 98%.
2. Transaminasas normales: Generalmente tienen una enfermedad leve que no requiere tratamiento y es de buen pronóstico. Sin embargo, hasta un 15% pueden tener enfermedad histológica importante con progresión de fibrosis que indica la necesidad de tratamiento. Estos casos se deben individualizar, y la biopsia hepática se recomienda para establecer la severidad histológica de la enfermedad.
]]> 3. Coinfección con VIH: Debido a las terapias HAART contra VIH, los coinfectados con VHC están teniendo un buen control para su VIH mientras la hepatitis C progresa rápidamente a descompensación hepática, cirrosis y riesgo de hepatocarcinoma. Se recomienda tratar a los coinfectados con interferón pegilado y ribavirina, siempre y cuando tengan unos CD4 mayores de 200-250 y una carga viral para VIH baja o no detectable.4. Trasplantados de hígado: La reinfección postrasplante hepático por VHC es universal, y a veces progresa en forma rápida a descompensación hepática, comprometiendo la vida del paciente o siendo necesario retrasplantar. No está claro el momento de tratar a estos pacientes, ya que algunos grupos están a favor de tratar tempranamente después del trasplante, con un riesgo alto de producir rechazo del injerto. Otros prefieren esperar al desarrollo de infección crónica con hepatitis recidivante, haciendo un seguimiento mediante biopsia hepática seriada, y si hay recaída de la enfermedad, se iniciará tratamiento.
Futuro en el tratamiento de hepatitis por VHC
Aún se requiere de mejores terapias que aumenten la respuesta en pacientes infectados con el VHC. Actualmente hay estudios en curso con inhibidores específicos de enzimas necesarias para mantener la replicación viral: proteasas, helicasas, RNA polimerasa. Es probable que en un futuro no muy lejano se disponga de estas terapias, que en combinación con la ya disponibles podrán aumentar el porcentaje de individuos curados de esta infección.
También se está investigando en el desarrollo de vacunas que puedan prevenir la infección por VHC, pero hasta la fecha no está disponible y la posibilidad de tenerla aún es difícil debido a la capacidad del VHC de mutar constantemente cuando está bajo presión inmunológica, desarrollando lo que es conocido como cuasiespecies que evaden la inmunidad del individuo infectado.
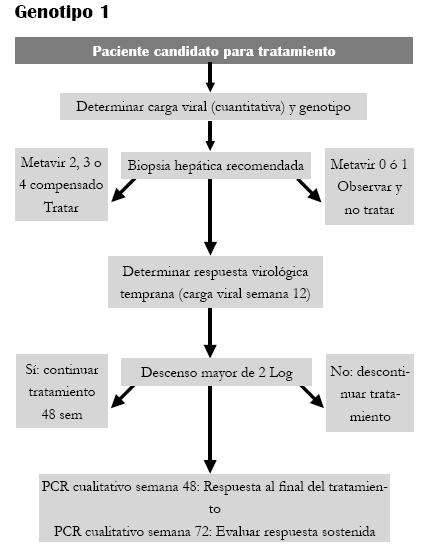
Algoritmos para el manejo de la hepatitis por VHC propuestos por Strader y col, guías de la AASLD, 2004
Genotipo 1 (Ver Fig. 1)
Dosis: Peg IFN Alfa 2a: 180 mcg QW, Peg IFN Alfa 2b: 1.5 mcg/kg de peso QW
Ribavirina: 1000 a 1200 mg QD para genotipo 1.
]]> Genotipos 2 y 3 (Ver fig. 2)Dosis: Peg IFN Alfa 2a: 180 mcg QW, Peg IFN Alfa 2b: 1.5 mcg/kg de peso QW
Ribavirina: 800 mg QD para genotipos 2 y 3.
Referencias
1. Asociación Colombiana de Hepatología. Consenso Colombiano de Hepatitis C, 2004. Revista Colombiana de Gastroenterología, en publicación, 2004. [ Links ]
2. Foster GR, Goldin RD. Management of Chronic Viral Hepatitis, Ed. Dunitz, UK 2002. [ Links ]
3. National Institutes of Health Consensus Development Conference Statement: Management of Hepatitis C, Hepatology 2002; 36(suppl 1): S3-S20. [ Links ]
4. Poynard T. Hepatitis B and C, Management and Treatment, Ed. Dunitz, UK, 2002. [ Links ]
5. Strader DB, Wright T, Thomas DL, et al. Diagnosis, management, and treatment of Hepatitis C, AASLD Practice Guidelines, Hepatology 2004; 39: 1147-1171. [ Links ] ]]>